NOx(主要指NO和NO2)是大气主要污染物之一、有效去除大气中的NOx是环境保护的重要课题。
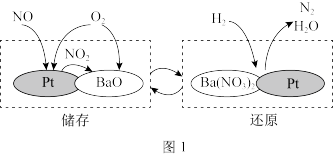
(1)NSR储存还原时,NO的储存和还原在不同时段交替进行,如图1所示。
①NO储存转化为Ba(NO3)2过程中,参加反应的NO和O2的物质的量之比为___________ 。
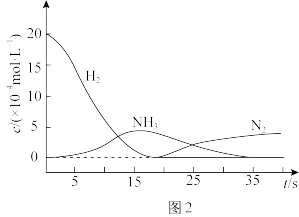
②H2还原Ba(NO3)2的过程分两步进行,图2表示该过程相关物质浓度随时间的变化关系。第一步反应的化学方程式为___________ 。
(2)NaClO溶液能有效去除NO。25℃时,NO的去除率随pH的变化如图3所示(用盐酸调节pH);pH=4时,NO的去除率随温度的变化如图4所示。
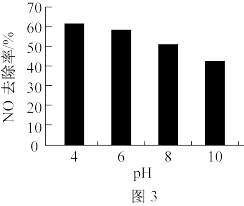

①25℃时,随着pH降低,NO脱除率增大的原因是___________ 。
②pH=4时,60~80℃间NO脱除率下降的原因是___________ 。
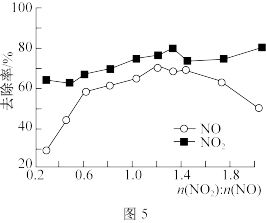
(3)一定条件下,将一定浓度NOx(NO2和NO的混合气体)通入Ca(OH)2悬浊液中,改变n(NO2)︰n(NO)的值,NOx的去除率如图5所示。
已知:a.NOx的去除率=1-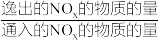 ×100%
×100%
b.NO与Ca(OH)2不反应
①当n(NO2)︰n(NO)在0.3~0.5之间,NO与NO2吸收转化为Ca(NO2)2反应的离子方程式为___________ 。
②当n(NO2)︰n(NO)大于1.4时,NO2的去除率升高,但NO的去除率却降低。其可能的原因是___________ 。
(1)NSR储存还原时,NO的储存和还原在不同时段交替进行,如图1所示。
①NO储存转化为Ba(NO3)2过程中,参加反应的NO和O2的物质的量之比为
②H2还原Ba(NO3)2的过程分两步进行,图2表示该过程相关物质浓度随时间的变化关系。第一步反应的化学方程式为
(2)NaClO溶液能有效去除NO。25℃时,NO的去除率随pH的变化如图3所示(用盐酸调节pH);pH=4时,NO的去除率随温度的变化如图4所示。




①25℃时,随着pH降低,NO脱除率增大的原因是
②pH=4时,60~80℃间NO脱除率下降的原因是
(3)一定条件下,将一定浓度NOx(NO2和NO的混合气体)通入Ca(OH)2悬浊液中,改变n(NO2)︰n(NO)的值,NOx的去除率如图5所示。

已知:a.NOx的去除率=1-
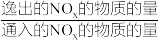 ×100%
×100%b.NO与Ca(OH)2不反应
①当n(NO2)︰n(NO)在0.3~0.5之间,NO与NO2吸收转化为Ca(NO2)2反应的离子方程式为
②当n(NO2)︰n(NO)大于1.4时,NO2的去除率升高,但NO的去除率却降低。其可能的原因是
更新时间:2023-05-30 14:41:24
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】铁元素在地壳中含量居于第四位。铁是目前产量最大,使用最广泛的金属。我国目前发现最早的人工冶铁制品是河南三门峡出土的西周晚期的玉柄铁剑。
(1)在钢铁厂的生产中,炽热的铁水或钢水注入模具之前必须进行充分的干燥处理,不得留有水,请用化学方程式解释___________ 。
(2)电子工业中常用FeCl3溶液作为“腐蚀液”腐蚀覆铜板,请用离子方程式解释该现象:___________ 。
(3)高铁酸钠(Na2FeO4)是一种新型绿色消毒剂,其一种制备原理如下:_______ClO- ___________
___________ ___________=___________
___________=___________ ___________
___________ ___________
___________ ,请将方程式补充完整并配平该方程式
,请将方程式补充完整并配平该方程式__________ 。
(4) 很不稳定,露置在空气中容易被氧化,该反应的化学方程式为
很不稳定,露置在空气中容易被氧化,该反应的化学方程式为___________ ,现象为___________ 。
(5)向一个金属铝的易拉罐内充满CO2,然后向罐内注入足量NaOH溶液,立即用胶布严封罐口,过一段时间后,罐壁内凹而瘪,再过一段时间后,瘪了的罐壁重新鼓起,请用离子方程式解释罐子重新鼓起的现象:___________ 。
(1)在钢铁厂的生产中,炽热的铁水或钢水注入模具之前必须进行充分的干燥处理,不得留有水,请用化学方程式解释
(2)电子工业中常用FeCl3溶液作为“腐蚀液”腐蚀覆铜板,请用离子方程式解释该现象:
(3)高铁酸钠(Na2FeO4)是一种新型绿色消毒剂,其一种制备原理如下:_______ClO-
 ___________
___________ ___________=___________
___________=___________ ___________
___________ ___________
___________ ,请将方程式补充完整并配平该方程式
,请将方程式补充完整并配平该方程式(4)
 很不稳定,露置在空气中容易被氧化,该反应的化学方程式为
很不稳定,露置在空气中容易被氧化,该反应的化学方程式为(5)向一个金属铝的易拉罐内充满CO2,然后向罐内注入足量NaOH溶液,立即用胶布严封罐口,过一段时间后,罐壁内凹而瘪,再过一段时间后,瘪了的罐壁重新鼓起,请用离子方程式解释罐子重新鼓起的现象:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】现有以下物质:①NaOH溶液;②液氯;③Ba(OH)2固体,④熔融KHSO4;⑤Fe(OH)3胶体:⑥水银;⑦CO2;⑧CH3COOH;⑨蔗糖;⑩NaHCO3;
Ⅰ.(1)以上物质中属于混合物的是___________ (填序号),以上物质中属于电解质的是___________ (填序号);以上纯净物中能导电的是___________ (填序号)。以上物质中是非电解质的是___________ (填序号)。
(2)写出⑩在水溶液中的电离方程式___________ 。
Ⅱ.将③Ba(OH)2固体配制成溶液,某小组实验室探究Ba(OH)2溶液与稀盐酸反应的实质。向0.2 mol/L Ba(OH)2溶液中滴加0.1 mol/L盐酸,测定导电率的变化如图所示,回答下列问题:
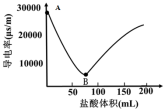
(3)该Ba(OH)2在水中导电率高,写出Ba(OH)2的电离方程式为___________ 。
(4)A—B段,发生的离子反应方程式是___________ 。
(5)B点恰好完全反应,此时溶液中存在的微粒有H2O、___________ 。
(6)下列化学反应的实质与Ba(OH)2溶液和稀盐酸反应的实质相同的是___________ 。
A.Ba(OH)2和H2SO4 B.NaOH 和H2SO4 C.Ba(OH)2与HNO3
Ⅰ.(1)以上物质中属于混合物的是
(2)写出⑩在水溶液中的电离方程式
Ⅱ.将③Ba(OH)2固体配制成溶液,某小组实验室探究Ba(OH)2溶液与稀盐酸反应的实质。向0.2 mol/L Ba(OH)2溶液中滴加0.1 mol/L盐酸,测定导电率的变化如图所示,回答下列问题:

(3)该Ba(OH)2在水中导电率高,写出Ba(OH)2的电离方程式为
(4)A—B段,发生的离子反应方程式是
(5)B点恰好完全反应,此时溶液中存在的微粒有H2O、
(6)下列化学反应的实质与Ba(OH)2溶液和稀盐酸反应的实质相同的是
A.Ba(OH)2和H2SO4 B.NaOH 和H2SO4 C.Ba(OH)2与HNO3
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】CuSO4溶液与Ba(OH)2溶液混合:_______
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】目前新能源技术被不断利用,高铁电池技术就是科研机构着力研究的一个方向。
(1)高铁酸钾—锌电池(碱性介质)是一种典型的高铁电池,则该种电池负极材料是___________ 。
(2)工业上常采用NaClO氧化法生产高铁酸钾(K2FeO4),K2FeO4在碱性环境中稳定,在中性和酸性条件下不稳定。反应原理为:
Ⅰ.在碱性条件下,利用NaClO氧化Fe(NO3)3制得Na2FeO4:3NaClO+2Fe(NO3)3+10NaOH=2Na2FeO4+3NaCl+6NaNO3+5H2O
Ⅱ.Na2FeO4与KOH反应生成K2FeO4,主要的生产流程如下:
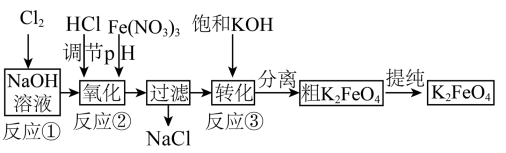
①写出反应①的离子方程式___________ 。
②请写出生产流程中“转化”(反应③)的化学方程式___________ 。
③该反应是在低温下进行的,说明此温度下Ksp(K2FeO4)___________ Ksp(Na2FeO4)(填“>”“<”或“=”)。
④“提纯”K2FeO4中采用重结晶、洗涤、低温烘干的方法,则洗涤剂最好选用___________ 溶液。
a.H2O B.CH3COONa、异丙醇 C.NH4Cl、异丙醇 D.Fe(NO3)3、异丙醇
(3)已知K2FeO4在水溶液中可以发生:4 +10H2O
+10H2O 4Fe(OH)3+8OH-+3O2↑,则K2FeO4可以在水处理中的作用是
4Fe(OH)3+8OH-+3O2↑,则K2FeO4可以在水处理中的作用是___________ 。
(4) 在水溶液中的存在形态图如图所示。
在水溶液中的存在形态图如图所示。
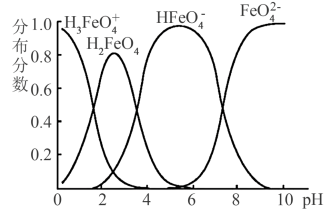
①若向pH=10的这种溶液中加硫酸至pH=2,HFeO 的分布分数的变化情况是
的分布分数的变化情况是___________ 。
②若向pH=6的这种溶液中滴加KOH溶液,则溶液中含铁元素的微粒中,___________ 转化为___________ 。(填化学式)
(1)高铁酸钾—锌电池(碱性介质)是一种典型的高铁电池,则该种电池负极材料是
(2)工业上常采用NaClO氧化法生产高铁酸钾(K2FeO4),K2FeO4在碱性环境中稳定,在中性和酸性条件下不稳定。反应原理为:
Ⅰ.在碱性条件下,利用NaClO氧化Fe(NO3)3制得Na2FeO4:3NaClO+2Fe(NO3)3+10NaOH=2Na2FeO4+3NaCl+6NaNO3+5H2O
Ⅱ.Na2FeO4与KOH反应生成K2FeO4,主要的生产流程如下:

①写出反应①的离子方程式
②请写出生产流程中“转化”(反应③)的化学方程式
③该反应是在低温下进行的,说明此温度下Ksp(K2FeO4)
④“提纯”K2FeO4中采用重结晶、洗涤、低温烘干的方法,则洗涤剂最好选用
a.H2O B.CH3COONa、异丙醇 C.NH4Cl、异丙醇 D.Fe(NO3)3、异丙醇
(3)已知K2FeO4在水溶液中可以发生:4
 +10H2O
+10H2O 4Fe(OH)3+8OH-+3O2↑,则K2FeO4可以在水处理中的作用是
4Fe(OH)3+8OH-+3O2↑,则K2FeO4可以在水处理中的作用是(4)
 在水溶液中的存在形态图如图所示。
在水溶液中的存在形态图如图所示。
①若向pH=10的这种溶液中加硫酸至pH=2,HFeO
 的分布分数的变化情况是
的分布分数的变化情况是②若向pH=6的这种溶液中滴加KOH溶液,则溶液中含铁元素的微粒中,
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】臭氧也可用于处理NO。O3氧化NO结合水洗可产生HNO3和O2,写出该反应的化学方程式_______ ,每生成1mol的HNO3转移_______ mol电子
您最近一年使用:0次
【推荐3】氮元素可以形成多种化合物,如NH3、N2H4、NO、HNO3等。
(1)汽车尾气中含NO和CO,为减轻污染,某市为汽车加装了“三效催化净化器”,可将尾气中的CO、NO转化为可参与大气循环的无毒混合气体,反应的化学方程式为___________________________________ 。
(2)工业上以惰性材料为电极采用电解法处理汽车尾气中的NO,将NO转化成NH4NO3,用硝酸铵溶液作电解质溶液。当两极转移的电子数目相等时,阳极、阴极上产生含氮物质的物质的量之比为______________ (不考虑水解)。
(3) N2H4可作为火箭燃料,其在氧气中燃烧生成一种无毒气体和水。当有16 g N2H4燃烧时,转移电子的数目约为_________________ 个。
(4)利用氨气可除去工厂烟气中的氮氧化物。写出氨气与氮氧化物(用NOx表示)反应的化学方程式:___________________________________ 。同温同压下,3.5 L NH3恰好与3.0 L NO和NO2的混合气完全反应,最终转化为N2,则原混合气中NO和NO2的体积之比是_____________ 。
(1)汽车尾气中含NO和CO,为减轻污染,某市为汽车加装了“三效催化净化器”,可将尾气中的CO、NO转化为可参与大气循环的无毒混合气体,反应的化学方程式为
(2)工业上以惰性材料为电极采用电解法处理汽车尾气中的NO,将NO转化成NH4NO3,用硝酸铵溶液作电解质溶液。当两极转移的电子数目相等时,阳极、阴极上产生含氮物质的物质的量之比为
(3) N2H4可作为火箭燃料,其在氧气中燃烧生成一种无毒气体和水。当有16 g N2H4燃烧时,转移电子的数目约为
(4)利用氨气可除去工厂烟气中的氮氧化物。写出氨气与氮氧化物(用NOx表示)反应的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】NaCl是一种化工原料,可以制备一系列物质,如图所示。

(1)下列说法不正确的是___________(填字母)。
(2)Cl2与Ca(OH)2反应的化学方程式为___________ 。
(3)84消毒液(含次氯酸钠)不能与洁厕剂(含盐酸)混合使用,否则可能产生使人中毒的气体,请解释其原因___________ (用化学反应方程式表示)。
(4)纯净的氢气在氯气中燃烧的现象是___________ 。
(5)实验室常用浓盐酸和MnO2加热制备氯气,请写出该反应的离子方程式___________ 。

(1)下列说法不正确的是___________(填字母)。
| A.Na2CO3的热稳定性比NaHCO3强 |
| B.侯氏制碱法可以制得Na2CO3 |
| C.图示转化反应都是氧化还原反应 |
| D.焰色试验中需用硫酸洗净铁丝,并灼烧至与原来的火焰颜色相同为止 |
(2)Cl2与Ca(OH)2反应的化学方程式为
(3)84消毒液(含次氯酸钠)不能与洁厕剂(含盐酸)混合使用,否则可能产生使人中毒的气体,请解释其原因
(4)纯净的氢气在氯气中燃烧的现象是
(5)实验室常用浓盐酸和MnO2加热制备氯气,请写出该反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】按要求用合适的化学用语回答下列问题:
(1)写出含有8个质子、10个中子的原子化学符号___________ 。
(2)相同质量的D2O和H2O中质子数之比是___________ 。
(3)第ⅦA族上下相邻的两种元素X、Y(X在上),X元素所在周期含m,Y元素所在周期含n种元素,若X的原子序数为x,则Y的原子序数为___________ 。
(4)金属Li与氧气加热生成物质的化学式___________ 。
(5)向NaHSO4溶液中滴加Ba(OH)2溶液至溶液呈中性的离子方程式:___________ 。
(6)“洁厕灵”和“84消毒液”混合发生氯气中毒的离子方程式:___________ 。
(7)标况下,VL NH3溶于1L水中所形成的氨水的密度为dg/cm3,该溶液的物质的量浓度为___________ 。
(8)—种固体管道疏通剂的主要成分是NaOH和Al粉,试解释其疏通原理(用化学方程式回答):___________ 。
(1)写出含有8个质子、10个中子的原子化学符号
(2)相同质量的D2O和H2O中质子数之比是
(3)第ⅦA族上下相邻的两种元素X、Y(X在上),X元素所在周期含m,Y元素所在周期含n种元素,若X的原子序数为x,则Y的原子序数为
(4)金属Li与氧气加热生成物质的化学式
(5)向NaHSO4溶液中滴加Ba(OH)2溶液至溶液呈中性的离子方程式:
(6)“洁厕灵”和“84消毒液”混合发生氯气中毒的离子方程式:
(7)标况下,VL NH3溶于1L水中所形成的氨水的密度为dg/cm3,该溶液的物质的量浓度为
(8)—种固体管道疏通剂的主要成分是NaOH和Al粉,试解释其疏通原理(用化学方程式回答):
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】地震是一种危害极大的自然灾害,会造成大量的人员伤亡和财产损失。在地震后的灾区常需要大量的消毒剂、漂白剂、清洁剂。请回答下列相关问题:
(1)过碳酸钠是一种多用途的新型固态漂白剂,化学式可表示为 ,它具有
,它具有 和
和 的双重性质。下列物质能使过碳酸钠失效的是
的双重性质。下列物质能使过碳酸钠失效的是___________ (填选项编号)。
A.稀硫酸 B. C.
C. 溶液
溶液
(2)过氧化氢是日常生活中常用的消毒剂。有过氧化氢参与的某反应: ,已知该反应中
,已知该反应中 只发生了如下过程
只发生了如下过程 。请用双线桥法标出该反应电子转移的方向和数目
。请用双线桥法标出该反应电子转移的方向和数目___________ 。
(3)二氧化氯( )是一种消毒杀菌效率高、二次污染小的水处理剂。实验室可以通过以下反应制得:
)是一种消毒杀菌效率高、二次污染小的水处理剂。实验室可以通过以下反应制得: (X表示某种物质,
(X表示某种物质, 是一种有机酸)。请回答下列问题:
是一种有机酸)。请回答下列问题:
①X的化学式为___________ 。
②从物质分类的角度看,上述反应体系涉及的物质属于盐类的有___________ 。
③氧化剂与还原剂物质的量之比为___________ 。
(4)曾有报道,在清洗卫生间时,因混合使用“洁厕灵”(主要成分是稀盐酸)与“84消毒液”(主要成分是 )而发生氯气中毒事件。试写出可能发生反应的化学方程式
)而发生氯气中毒事件。试写出可能发生反应的化学方程式___________ 。
(1)过碳酸钠是一种多用途的新型固态漂白剂,化学式可表示为
 ,它具有
,它具有 和
和 的双重性质。下列物质能使过碳酸钠失效的是
的双重性质。下列物质能使过碳酸钠失效的是A.稀硫酸 B.
 C.
C. 溶液
溶液(2)过氧化氢是日常生活中常用的消毒剂。有过氧化氢参与的某反应:
 ,已知该反应中
,已知该反应中 只发生了如下过程
只发生了如下过程 。请用双线桥法标出该反应电子转移的方向和数目
。请用双线桥法标出该反应电子转移的方向和数目(3)二氧化氯(
 )是一种消毒杀菌效率高、二次污染小的水处理剂。实验室可以通过以下反应制得:
)是一种消毒杀菌效率高、二次污染小的水处理剂。实验室可以通过以下反应制得: (X表示某种物质,
(X表示某种物质, 是一种有机酸)。请回答下列问题:
是一种有机酸)。请回答下列问题:①X的化学式为
②从物质分类的角度看,上述反应体系涉及的物质属于盐类的有
③氧化剂与还原剂物质的量之比为
(4)曾有报道,在清洗卫生间时,因混合使用“洁厕灵”(主要成分是稀盐酸)与“84消毒液”(主要成分是
 )而发生氯气中毒事件。试写出可能发生反应的化学方程式
)而发生氯气中毒事件。试写出可能发生反应的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】汽车尾气净化装置“催化转化器”是防止尾气(含一氧化碳、氮氧化物等气体) 污染的有效方法,能使尾气中的一氧化碳和氮氧化物发生反应生成可参与大气生态循环的无毒气体。
(1)汽车尾气中易造成光化学烟雾的物质是____ (写名称)。
(2)写出催化转化器中,一氧化碳和一氧化氮反应的化学方程式为__ , 并分析标出电子转移的方向及数目_____
(3)下列措施中有利于控制城市空气污染的是__ (填字母)。
a.推广电动汽车 b.加快煤炭开采和使用 c.开发和使用氢能
(4)采用NaOH溶液可以吸收废气中的氮氧化物,反应的化学方程式如下:
NO + NO2 + 2NaOH= 2NaNO2 + H2O
2NO2 + 2NaOH= NaNO2 + NaNO3 + H2O
若反应中消耗了10 L0.1 mol ·L-1的NaOH溶液,则参加反应的气体在标准状况下的体积为____ 。
(1)汽车尾气中易造成光化学烟雾的物质是
(2)写出催化转化器中,一氧化碳和一氧化氮反应的化学方程式为
(3)下列措施中有利于控制城市空气污染的是
a.推广电动汽车 b.加快煤炭开采和使用 c.开发和使用氢能
(4)采用NaOH溶液可以吸收废气中的氮氧化物,反应的化学方程式如下:
NO + NO2 + 2NaOH= 2NaNO2 + H2O
2NO2 + 2NaOH= NaNO2 + NaNO3 + H2O
若反应中消耗了10 L0.1 mol ·L-1的NaOH溶液,则参加反应的气体在标准状况下的体积为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】“绿水青山就是金山银山”。近年来,绿色发展、生态保护成为中国展示给世界的一张新“名片”,减少废气的排放是环境保护的重要内容之一、
(1)氮氧化物是形成光化学烟雾的主要元凶,利用碱液吸收法可以有效地吸收氮氧化物,发生的反应有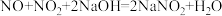 、
、 。若某混合气体中含amolNO和bmolNO2,用NaOH溶液吸收时,要使气体完全被吸收,则a与b需满足的关系为
。若某混合气体中含amolNO和bmolNO2,用NaOH溶液吸收时,要使气体完全被吸收,则a与b需满足的关系为___________ ,气体完全被吸收后测得溶液中NaNO2和NaNO3的物质的量之比为4∶1,则混合气体中NO的体积分数为___________ 。
(2)煤燃烧时排放的烟气中含有SO2和NOx,用NaClO2溶液作为吸收剂可同时对烟气进行脱硫、脱硝。将含有SO2和NOx的烟气通入盛有NaClO2和NaOH溶液的反应器中,反应一段时间后,测得溶液中离子浓度的有关数据如下表所示(其他极微量离子忽略不计):
①SO2和NaClO2溶液反应的离子方程式为___________ 。
②表中y=___________ 。
(3)工业生产硫酸也会产生SO2。硫铁矿(FeS2)煅烧的化学方程式为___________ ;当有11.2L(标准状况) SO2气体生成时,反应中转移的电子数为___________ NA。
(1)氮氧化物是形成光化学烟雾的主要元凶,利用碱液吸收法可以有效地吸收氮氧化物,发生的反应有
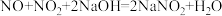 、
、 。若某混合气体中含amolNO和bmolNO2,用NaOH溶液吸收时,要使气体完全被吸收,则a与b需满足的关系为
。若某混合气体中含amolNO和bmolNO2,用NaOH溶液吸收时,要使气体完全被吸收,则a与b需满足的关系为(2)煤燃烧时排放的烟气中含有SO2和NOx,用NaClO2溶液作为吸收剂可同时对烟气进行脱硫、脱硝。将含有SO2和NOx的烟气通入盛有NaClO2和NaOH溶液的反应器中,反应一段时间后,测得溶液中离子浓度的有关数据如下表所示(其他极微量离子忽略不计):
| 离子 | Na+ | SO | NO | H+ | Cl- |
| 浓度/(mol/L) | 3.0×10-3 | y | 8.8×10-4 | 3.8×10-4 | 1.0×10-3 |
①SO2和NaClO2溶液反应的离子方程式为
②表中y=
(3)工业生产硫酸也会产生SO2。硫铁矿(FeS2)煅烧的化学方程式为
您最近一年使用:0次

 通入
通入 溶液中:
溶液中: 通入
通入 中:
中: 和
和 制氨气:
制氨气: 中,固体由黑色变红色:
中,固体由黑色变红色: 管道是否漏气,若漏气则有白烟生成:
管道是否漏气,若漏气则有白烟生成:

