下列物质中:①MgCl2 ②金刚石 ③NaCl ④H2O ⑤Na2O2 ⑥O2 ⑦H2SO4 ⑧CO2 ⑨NH4Cl ⑩Ne。
(1)属于强电解质的_ ,属于弱电解质的_ ,属于非电解质的__ ,溶于水能导电的___ ;
(2)只含离子键的是____ ,只含共价键的是___ ,既含离子键又含共价键的是___ ,不存在化学键的是___ ,属于离子化合物的是___ ,属于共价化合物的是___ 。
(1)属于强电解质的
(2)只含离子键的是
更新时间:2021-04-22 21:27:38
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】科学研究中观察到的宏观现象能反映微观本质。回答下列问题:
(1)次磷酸分子式为H3PO2,与足量NaOH溶液反应生成NaH2PO2,次磷酸为_______ 元弱酸,次磷酸溶液中微粒有_______ ,次磷酸的电离方程式为_________ 。
(2)在一定温度下,有等物质的量浓度的盐酸、硫酸、醋酸三种酸,c(H+)由大到小的顺序是________ ;当体积相同时,三种酸中和NaOH的能力由大到小的顺序是_______ 。
(3)25℃时,部分物质的电离平衡常数如表所示:
①当温度升高时,电离平衡常数K值_______ (填“增大”“减小”或“不变”)。
②向NaClO溶液中通入少量二氧化碳气体,发生反应的离子方程式为_______ ,结合所给数据说明生成该产物的理由:________ 。
③把足量醋酸滴入Na2SO3溶液中,反应的离子方程式为_______ 。
(1)次磷酸分子式为H3PO2,与足量NaOH溶液反应生成NaH2PO2,次磷酸为
(2)在一定温度下,有等物质的量浓度的盐酸、硫酸、醋酸三种酸,c(H+)由大到小的顺序是
(3)25℃时,部分物质的电离平衡常数如表所示:
| 化学式 | CH3COOH | H2CO3 | HClO | H2SO3 |
| 电离平衡常数 | Ka=1.75×10-5 | Ka1=4.5×10-7、 Ka2=4.7×10-11 | Ka=3.0×10-8 | K1=1.54×10-2、 K2=1.02×10-7 |
②向NaClO溶液中通入少量二氧化碳气体,发生反应的离子方程式为
③把足量醋酸滴入Na2SO3溶液中,反应的离子方程式为
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐2】下列物质中:①NaCl;②NaOH;③NH3·H2O;④CH3COOH溶液;⑤BaSO4;⑥H2O;⑦HCl;⑧H2SO4;⑨CO2;⑩酒精溶液(均填写编号回答)
(1)pH相等的②的溶液和③的溶液等体积加水稀释相同倍数后,pH大的是______ .
(2)有pH均为2的④、⑦、⑧三种物质的溶液,物质的量浓度大到小的顺序为______ ,若分别用这三种酸中和含等物质的量NaOH的溶液,所需酸溶液的体积分别为a、b、c,则a、b、c的大小关系是__________ .
(3)某温度时,1mol·L-1的醋酸溶液电离平衡常数为1.0×10-8,达平衡时,溶液中氢离子浓度是______________ .
(1)pH相等的②的溶液和③的溶液等体积加水稀释相同倍数后,pH大的是
(2)有pH均为2的④、⑦、⑧三种物质的溶液,物质的量浓度大到小的顺序为
(3)某温度时,1mol·L-1的醋酸溶液电离平衡常数为1.0×10-8,达平衡时,溶液中氢离子浓度是
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐3】判断下列说法是否正确,并说明理由。
(1)强电解质溶液的导电能力一定比弱电解质溶液的强___________ 。
(2)中和等体积、等物质的量浓度的盐酸和醋酸,盐酸所需氢氧化钠的物质的量多于醋酸___________ 。
(3)将NaOH溶液和氨水各稀释一倍,两者的 均减少到原来的
均减少到原来的
___________ 。
(4)如果盐酸中溶质的浓度是醋酸中溶质浓度的2倍,则盐酸中的 也是醋酸的2倍
也是醋酸的2倍___________ 。
(5)物质的量浓度相同的磷酸钠溶液和磷酸中所含 的浓度相同
的浓度相同___________ 。
(1)强电解质溶液的导电能力一定比弱电解质溶液的强
(2)中和等体积、等物质的量浓度的盐酸和醋酸,盐酸所需氢氧化钠的物质的量多于醋酸
(3)将NaOH溶液和氨水各稀释一倍,两者的
 均减少到原来的
均减少到原来的
(4)如果盐酸中溶质的浓度是醋酸中溶质浓度的2倍,则盐酸中的
 也是醋酸的2倍
也是醋酸的2倍(5)物质的量浓度相同的磷酸钠溶液和磷酸中所含
 的浓度相同
的浓度相同
您最近半年使用:0次
填空题
|
适中
(0.65)
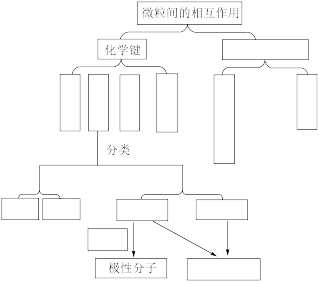
【推荐1】微粒间的相互作用包括多种类型,微粒通过这些作用可以形成具有不同空间结构的分子或物质。本章学习了微粒间的相互作用及与其相关的许多知识,如共价键、 键、
键、 键、极性键、非极性键、离子键、配位键、金属键、范德华力、氢键、分子空间结构、极性分子、非极性分子等,请通过图示的方式表示它们之间的相互关系,以加深对所学内容的理解
键、极性键、非极性键、离子键、配位键、金属键、范德华力、氢键、分子空间结构、极性分子、非极性分子等,请通过图示的方式表示它们之间的相互关系,以加深对所学内容的理解___________ 。
 键、
键、 键、极性键、非极性键、离子键、配位键、金属键、范德华力、氢键、分子空间结构、极性分子、非极性分子等,请通过图示的方式表示它们之间的相互关系,以加深对所学内容的理解
键、极性键、非极性键、离子键、配位键、金属键、范德华力、氢键、分子空间结构、极性分子、非极性分子等,请通过图示的方式表示它们之间的相互关系,以加深对所学内容的理解
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】Ⅰ.根据下列6种符号回答问题:
①1H ②2H ③3H ④14C ⑤14N ⑥16O
(1)互为同位素的是____________ 。(填序号,下同)
(2)质量数相等的是______________ ,中子数相等的是_________ 。
Ⅱ.现有6种物质: ①MgCl2②HCl ③SO2 ④ K2CO3⑤ CaO ⑥ NaOH
请根据下列标准,对上述物质进行分类(填序号):
(1)属于共价化合物是_____________ 。
(2)只含离子键的化合物是_________ 。
(3)含共价键的离子化合物是______ 。
①1H ②2H ③3H ④14C ⑤14N ⑥16O
(1)互为同位素的是
(2)质量数相等的是
Ⅱ.现有6种物质: ①MgCl2②HCl ③SO2 ④ K2CO3⑤ CaO ⑥ NaOH
请根据下列标准,对上述物质进行分类(填序号):
(1)属于共价化合物是
(2)只含离子键的化合物是
(3)含共价键的离子化合物是
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】(1)比较结合 H+能力的相对强弱:H2O_____ NH3 (填“>”、“<”或“=”);用一个离子 方程式说明 H3O+和 NH4+给出 H+能力的相对强弱_____ 。
(2)NaOCN 是离子化合物,各原子均满足 8 电子稳定结构。写出 NaOCN 的电子式_____ 。
(3)乙酸汽化时,测定气体的相对分子质量,有数据表明其摩尔质量变为 120g·mol-1,从结构上 分析其可能的原因是_____
(2)NaOCN 是离子化合物,各原子均满足 8 电子稳定结构。写出 NaOCN 的电子式
(3)乙酸汽化时,测定气体的相对分子质量,有数据表明其摩尔质量变为 120g·mol-1,从结构上 分析其可能的原因是
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】H2O2、KCl、Na2SO4、Na2O2、HCl、O2中只含离子键的是___ ,只含极性键的是___ ,只含非极性键的是___ ,既含离子键又含极性键的是___ ,既含离子键又含非极性键的是___ ,既极性键含又含非极性键的是________ 。
您最近半年使用:0次



