已知不同温度或压强下,反应物的转化率α(或百分含量)与时间的关系曲线,推断温度的高低及反应的热效应或压强的大小及气体物质间的化学计量数的关系。[以反应aA(g)+bB(g)=cC(g)中反应物A的转化率αA为例说明]
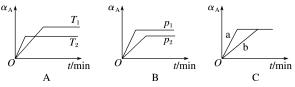
(1)根据图A、B、C回答下列问题:
①图A中T2___________ (填“>”“<”或“=”,下同)T1;图B中p1___________ p2;图C若为催化剂引起的变化,则___________ (填“a”或“b”)使用了催化剂。
②该反应为___________ 热反应;反应中的系数a+b___________ (填“>”“<”或“=”)c。
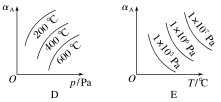
(2)根据图D判断该反应是___________ 热反应;反应中的化学计量数存在如下关系:a+b___________ (填“>”“<”或“=”)c。
(3)①若图A、B纵坐标表示A的百分含量,则该反应为___________ 热反应;反应中的化学计量数存在如下关系:a+b___________ (填“>”“<”或“=”)c。
②若图E纵坐标表示A的百分含量,则由图E可判断该反应是___________ 热反应;反应中的化学计量数存在如下关系:a+b___________ (填“>”“<”或“=”)c。


(1)根据图A、B、C回答下列问题:
①图A中T2
②该反应为
(2)根据图D判断该反应是
(3)①若图A、B纵坐标表示A的百分含量,则该反应为
②若图E纵坐标表示A的百分含量,则由图E可判断该反应是
2021高三·全国·专题练习 查看更多[2]
(已下线)小题30 化学平衡常规图像——备战2021年高考化学经典小题考前必刷(全国通用)(已下线)第2章能力提升测评卷-【帮课堂】2022-2023学年高二化学同步精品讲义(沪科版2020选择性必修第一册)
更新时间:2021-05-05 20:19:48
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】氨催化分解既可防治氨气污染,又能得到氢能源,得到广泛研究。
(1)已知:
①4NH3(g)+3O2(g) 2N2(g)+6H2O(g) △H=-1266.6kJ·mol-1,
2N2(g)+6H2O(g) △H=-1266.6kJ·mol-1,
②H2(g)+1/2O2(g)===H2O(l) △H2=-285.8 kJ·mol-1
③H2O(l)===H2O(g) △H3=+44.0kJ·mol-1
反应①在任何温度下都能自发进行的原因为___________ ;NH3分解为N2和H2的热化学方程式______________________ 。
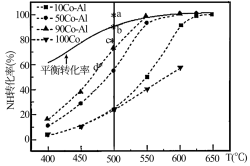
(2)在Co-Al催化剂体系中,压强P0下氨气以一定流速通过反应器,在相同时间下测转化率。得到不同催化剂下氨气转化率随温度变化曲线如下图。使反应的活化能最小的催化剂为___________ 。同一催化剂下,温度高时NH3的转化率接近平衡转化率的原因___________ 。如果增大氨气浓度(其它条件不变),则b点对应的点可能为___________ 。(填“a”、“c”或“d”)
(3)T℃时,体积为2L的密闭容器中加入1.0molNH3和0.2molH2,30min达到平衡时,N2体积分数为20%,则T℃时平衡常数K=___________ ,NH3转化率为___________ ;达到平衡后再加入1.0molNH3和0.2molH2,此时体系中v正___________ v逆(填“>“<”或“=”)。
(1)已知:
①4NH3(g)+3O2(g)
 2N2(g)+6H2O(g) △H=-1266.6kJ·mol-1,
2N2(g)+6H2O(g) △H=-1266.6kJ·mol-1,②H2(g)+1/2O2(g)===H2O(l) △H2=-285.8 kJ·mol-1
③H2O(l)===H2O(g) △H3=+44.0kJ·mol-1
反应①在任何温度下都能自发进行的原因为
(2)在Co-Al催化剂体系中,压强P0下氨气以一定流速通过反应器,在相同时间下测转化率。得到不同催化剂下氨气转化率随温度变化曲线如下图。使反应的活化能最小的催化剂为

(3)T℃时,体积为2L的密闭容器中加入1.0molNH3和0.2molH2,30min达到平衡时,N2体积分数为20%,则T℃时平衡常数K=
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】反应:aA(g)+bB(g) cC(g)(ΔH<0)在等容条件下进行。改变其他反应条件,在Ⅰ、Ⅱ、Ⅲ阶段体系中各物质浓度随时间变化的曲线如图所示:
cC(g)(ΔH<0)在等容条件下进行。改变其他反应条件,在Ⅰ、Ⅱ、Ⅲ阶段体系中各物质浓度随时间变化的曲线如图所示:
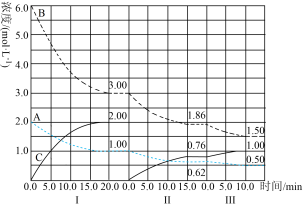
回答下列问题:
(1)反应的化学方程式中,a∶b∶c为___ ;
(2)B的平衡转化率αⅠ(B)、αⅡ(B)、αⅢ(B)中最小的是___ ;
(3)由第一次平衡到第二次平衡,平衡移动的方向是___ ,采取的措施是___ 。
 cC(g)(ΔH<0)在等容条件下进行。改变其他反应条件,在Ⅰ、Ⅱ、Ⅲ阶段体系中各物质浓度随时间变化的曲线如图所示:
cC(g)(ΔH<0)在等容条件下进行。改变其他反应条件,在Ⅰ、Ⅱ、Ⅲ阶段体系中各物质浓度随时间变化的曲线如图所示:
回答下列问题:
(1)反应的化学方程式中,a∶b∶c为
(2)B的平衡转化率αⅠ(B)、αⅡ(B)、αⅢ(B)中最小的是
(3)由第一次平衡到第二次平衡,平衡移动的方向是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】反应aA(g)+bB(g) cC(g)(△H<0)在等容条件下进行。改变其他反应条件,在I、II、III阶段体系中各物质浓度随时间变化的曲线如下图所示:
cC(g)(△H<0)在等容条件下进行。改变其他反应条件,在I、II、III阶段体系中各物质浓度随时间变化的曲线如下图所示:
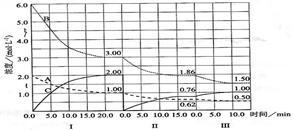
回答问题:
(1)反应的化学方程式中,a:b:c为________ ;
(2)A的平均反应速率vI(A)、vII(A)、vIII(A)从大到小排列次序为_________ ;
(3) B的平衡转化率aI(B)、aII(B)、aIII(B)中最小的是________ ,其值是_________ ;
(4)由第一次平衡到第二次平衡,平衡移动的方向是________________ ,采取的措施是_________________________________ ;
(5)比较第II阶段反应温度(T1)和第III阶段反应速度(T3)的高低:T2__ T3(填“>、=、<”)判断的理由是________________________________________ ;
(6)达到第三次平衡后,将容器的体积扩大一倍,假定10min后达到新的平衡,请在下图中用曲线表示IV阶段体系中各物质的浓度随时间变化的趋势(曲线上必须标出A、B、C).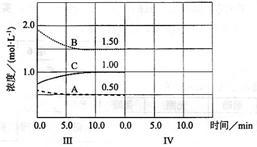
 cC(g)(△H<0)在等容条件下进行。改变其他反应条件,在I、II、III阶段体系中各物质浓度随时间变化的曲线如下图所示:
cC(g)(△H<0)在等容条件下进行。改变其他反应条件,在I、II、III阶段体系中各物质浓度随时间变化的曲线如下图所示:
回答问题:
(1)反应的化学方程式中,a:b:c为
(2)A的平均反应速率vI(A)、vII(A)、vIII(A)从大到小排列次序为
(3) B的平衡转化率aI(B)、aII(B)、aIII(B)中最小的是
(4)由第一次平衡到第二次平衡,平衡移动的方向是
(5)比较第II阶段反应温度(T1)和第III阶段反应速度(T3)的高低:T2
(6)达到第三次平衡后,将容器的体积扩大一倍,假定10min后达到新的平衡,请在下图中用曲线表示IV阶段体系中各物质的浓度随时间变化的趋势(曲线上必须标出A、B、C).

您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】研究含氮物质之间的转化,对防治污染具有重大意义。回答下列问题:
(1)已知:①
②
一定条件下,向体积为 的恒容密闭容器中通入
的恒容密闭容器中通入 和
和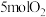 发生上述反应。经过t秒达到平衡状态,测得平衡时容器中
发生上述反应。经过t秒达到平衡状态,测得平衡时容器中 为
为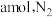 为
为 ,则
,则
________ (用含字母的代数式表示)。理论上参与反应①和②的 之比为
之比为______ 时,生成的 在混合气体中的含量最高。
在混合气体中的含量最高。
(2)在一定温度下,向容积不同的恒容密闭容器中分别通入 和
和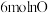 ,发生反应
,发生反应 。反应相同时间,某时刻测得各容器中
。反应相同时间,某时刻测得各容器中 的转化率与容器体积的关系如图所示。
的转化率与容器体积的关系如图所示。
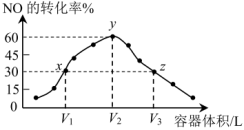
①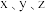 三点对应速率常数
三点对应速率常数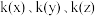 ,三者间的大小关系为
,三者间的大小关系为__ ,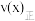
__ 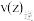 。
。
②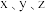 三点中已达到平衡状态的点为
三点中已达到平衡状态的点为___ ,z点比y点转化率低的原因是____ 。
(3)在一恒容密闭容器中充入 和
和 发生反应
发生反应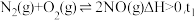 时达到平衡状态I,在
时达到平衡状态I,在 时改变某一条件,
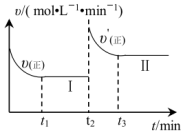
时改变某一条件, 时重新达到平衡状态II,正反应速率随时间的变化如图所示。
时重新达到平衡状态II,正反应速率随时间的变化如图所示。 时改变的条件可能为
时改变的条件可能为_____ (答2条)。
(1)已知:①

②

一定条件下,向体积为
 的恒容密闭容器中通入
的恒容密闭容器中通入 和
和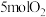 发生上述反应。经过t秒达到平衡状态,测得平衡时容器中
发生上述反应。经过t秒达到平衡状态,测得平衡时容器中 为
为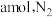 为
为 ,则
,则
 之比为
之比为 在混合气体中的含量最高。
在混合气体中的含量最高。(2)在一定温度下,向容积不同的恒容密闭容器中分别通入
 和
和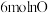 ,发生反应
,发生反应 。反应相同时间,某时刻测得各容器中
。反应相同时间,某时刻测得各容器中 的转化率与容器体积的关系如图所示。
的转化率与容器体积的关系如图所示。
①
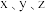 三点对应速率常数
三点对应速率常数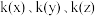 ,三者间的大小关系为
,三者间的大小关系为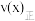
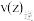 。
。②
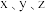 三点中已达到平衡状态的点为
三点中已达到平衡状态的点为(3)在一恒容密闭容器中充入
 和
和 发生反应
发生反应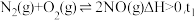 时达到平衡状态I,在
时达到平衡状态I,在 时改变某一条件,
时改变某一条件, 时重新达到平衡状态II,正反应速率随时间的变化如图所示。
时重新达到平衡状态II,正反应速率随时间的变化如图所示。 时改变的条件可能为
时改变的条件可能为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】氢气是一种理想的绿色能源.利用生物质发酵得到的乙醇制取氢气,具有良好的应用前景.乙醇水蒸气重整制氢的部分反应过程如图所示:

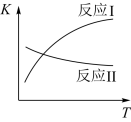
已知:反应I和反应II的平衡常数随温度变化曲线如图所示。
(1)反应I中,1molCH3CH2OH(g)参与反应后的热量变化是256kJ。
①反应II的△H___ 0(填“<”“=”或“>”)。
②反应I的热化学方程式是____ 。
(2)反应II,在进气比[n(CO):n(H2O)]不同时,测得相应的CO的平衡转化率见下图(各点对应的反应温度可能相同,也可能不同)。

①图中D、E两点对应的反应温度分别为TD和TE.判断:TD______ TE(填“<”“=”或“>”)。
②经分析,A、E和G三点对应的反应温度相同,其原因是A、E和G三点对应的______ 相同.
③当不同的进气比达到相同的CO平衡转化率时,对应的反应温度和进气比的关系是______ 。
(3)反应III,在经CO2饱和处理的KHCO3电解液中,电解活化CO2制备乙醇的原理如图所示。
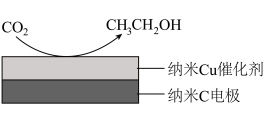
①电解活化CO2制备乙醇化学方程式是_____ 。
②从电解后溶液中分离出乙醇的操作方法是_____ 。

已知:反应I和反应II的平衡常数随温度变化曲线如图所示。

(1)反应I中,1molCH3CH2OH(g)参与反应后的热量变化是256kJ。
①反应II的△H
②反应I的热化学方程式是
(2)反应II,在进气比[n(CO):n(H2O)]不同时,测得相应的CO的平衡转化率见下图(各点对应的反应温度可能相同,也可能不同)。

①图中D、E两点对应的反应温度分别为TD和TE.判断:TD
②经分析,A、E和G三点对应的反应温度相同,其原因是A、E和G三点对应的
③当不同的进气比达到相同的CO平衡转化率时,对应的反应温度和进气比的关系是
(3)反应III,在经CO2饱和处理的KHCO3电解液中,电解活化CO2制备乙醇的原理如图所示。

①电解活化CO2制备乙醇化学方程式是
②从电解后溶液中分离出乙醇的操作方法是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】某温度时,在2L的密闭容器中,A、B、C三种气体的物质的量随时间的变化曲线如图所示。由图中数据分析
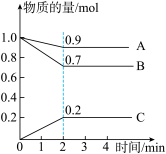
(1)该反应的反应物是_______ 。
(2)该反应_______ (填“是”或“不是”)可逆反应,原因是______________ 。写出该反应的化学方程式:_______ 。
(3)反应开始至2min时,用C表示的平均反应速率为_______ 。

(1)该反应的反应物是
(2)该反应
(3)反应开始至2min时,用C表示的平均反应速率为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】某密闭容器中充入等物质的量的气体A和B,一定温度下发生反应: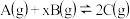 ,达到平衡后,只改变反应的一个条件,测得容器中物质的浓度、反应速率随时间变化的关系如图所示。请回答下列问题:
,达到平衡后,只改变反应的一个条件,测得容器中物质的浓度、反应速率随时间变化的关系如图所示。请回答下列问题:

 反应方程式中的
反应方程式中的
_______ ,30min时改变的反应条件是_______ 。
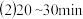 时反应的平衡常数
时反应的平衡常数_______ 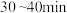 时反应的平衡常数
时反应的平衡常数 填:
填: 、
、 或
或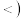 。
。
 该反应的正反应为
该反应的正反应为________  填:“放热”或“吸热”
填:“放热”或“吸热” 反应。
反应。
 反应过程中B的转化率最大的时间段是
反应过程中B的转化率最大的时间段是____________ 。
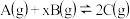 ,达到平衡后,只改变反应的一个条件,测得容器中物质的浓度、反应速率随时间变化的关系如图所示。请回答下列问题:
,达到平衡后,只改变反应的一个条件,测得容器中物质的浓度、反应速率随时间变化的关系如图所示。请回答下列问题:
 反应方程式中的
反应方程式中的
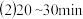 时反应的平衡常数
时反应的平衡常数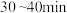 时反应的平衡常数
时反应的平衡常数 填:
填: 、
、 或
或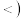 。
。 该反应的正反应为
该反应的正反应为 填:“放热”或“吸热”
填:“放热”或“吸热” 反应。
反应。 反应过程中B的转化率最大的时间段是
反应过程中B的转化率最大的时间段是
您最近一年使用:0次


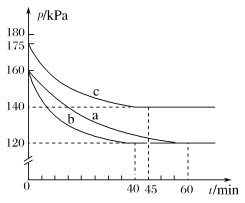
 AX5(g)在容积为10 L的密闭容器中进行。起始时AX3和X2均为0.2 mol。反应在不同条件下进行,反应体系总压强随时间的变化如图所示。
AX5(g)在容积为10 L的密闭容器中进行。起始时AX3和X2均为0.2 mol。反应在不同条件下进行,反应体系总压强随时间的变化如图所示。