反应:aA(g)+bB(g) cC(g)(ΔH<0)在等容条件下进行。改变其他反应条件,在Ⅰ、Ⅱ、Ⅲ阶段体系中各物质浓度随时间变化的曲线如图所示:
cC(g)(ΔH<0)在等容条件下进行。改变其他反应条件,在Ⅰ、Ⅱ、Ⅲ阶段体系中各物质浓度随时间变化的曲线如图所示:
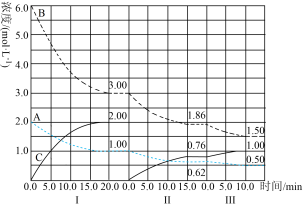
回答下列问题:
(1)反应的化学方程式中,a∶b∶c为___ ;
(2)B的平衡转化率αⅠ(B)、αⅡ(B)、αⅢ(B)中最小的是___ ;
(3)由第一次平衡到第二次平衡,平衡移动的方向是___ ,采取的措施是___ 。
 cC(g)(ΔH<0)在等容条件下进行。改变其他反应条件,在Ⅰ、Ⅱ、Ⅲ阶段体系中各物质浓度随时间变化的曲线如图所示:
cC(g)(ΔH<0)在等容条件下进行。改变其他反应条件,在Ⅰ、Ⅱ、Ⅲ阶段体系中各物质浓度随时间变化的曲线如图所示:
回答下列问题:
(1)反应的化学方程式中,a∶b∶c为
(2)B的平衡转化率αⅠ(B)、αⅡ(B)、αⅢ(B)中最小的是
(3)由第一次平衡到第二次平衡,平衡移动的方向是
更新时间:2019-11-03 21:36:56
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】25℃时,50mL0.10mol·L-1醋酸中存在下述平衡:CH3COOH⇌CH3COO-+H+,请回答以下问题:
(1)加入少量冰醋酸,平衡将___________ (填“向左”“向右”或“不”) 移动,溶液中c(H+)将___________ (填“增大”“减小”或“不变”);
(2)加入一定量蒸馏水,平衡将___________ (填“向左”“向右”或“不”) 移动,溶液中c(H+)将___________ (填“增大”“减小”或“不变”),c(OH-)将___________ (填“增大”“减小”或“不变”);
(3)加入20mL0.10mol·L-1NaCl溶液,平衡将___________ (填“向左”“向右”或“不”) 移动,溶液中c(H+)将___________ (填“增大”“减小”或“不变”)。
(1)加入少量冰醋酸,平衡将
(2)加入一定量蒸馏水,平衡将
(3)加入20mL0.10mol·L-1NaCl溶液,平衡将
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】密闭容器中发生如下反应:A(g)+3B(g) 2C(g) ΔH<0,根据下列速率﹣时间图像,回答下列问题。
2C(g) ΔH<0,根据下列速率﹣时间图像,回答下列问题。
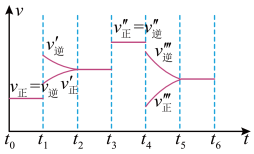
(1)下列时刻所改变的外界条件是:t1_________ ,t3_________ ,t4_________ ;
(2)物质A的体积分数最大的时间段是_________ ;
(3)反应速率最大的时间段是_________ ;
(4)t0~t1、t3~t4、t5~t6时间段的平衡常数K0、K3、K5的关系_________ 。
 2C(g) ΔH<0,根据下列速率﹣时间图像,回答下列问题。
2C(g) ΔH<0,根据下列速率﹣时间图像,回答下列问题。
(1)下列时刻所改变的外界条件是:t1
(2)物质A的体积分数最大的时间段是
(3)反应速率最大的时间段是
(4)t0~t1、t3~t4、t5~t6时间段的平衡常数K0、K3、K5的关系
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】在一容积为2 L的密闭容器内加入0.2 mol N2和0.6 mol H2,在一定条件下发生如下反应:N2(g)+3H2(g) 2NH3 ΔH<0。反应中NH3的物质的量浓度的变化情况如图所示:
2NH3 ΔH<0。反应中NH3的物质的量浓度的变化情况如图所示:
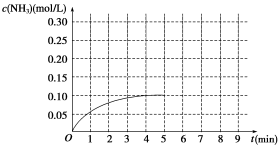
(1)根据图示,计算从反应开始到第4分钟达到平衡时,平均反应速率υ(N2)为__________ 。
(2)达到平衡后,第5分钟末,若保持其它条件不变,只改变反应温度,则NH3的物质的量浓度不可能为_____________ 。
a.0.20 mol/L b.0.12 mol/L c.0.10 mol/L d.0.08 mol/L
(3)达到平衡后,第5分钟末,若保持其它条件不变,只把容器的体积缩小,新平衡时NH3的浓度恰好为原来的2倍,则新体积_____ (选填“大于”、“等于”、“小于”)二分之一倍的原体积,化学平衡常数________ (选填“增大”、“减小”或“不变”)。
(4)在第5分钟末将容器的体积缩小一半,若在第8分钟末达到新的平衡(此时NH3的浓度约为0.25 mol/L)
 2NH3 ΔH<0。反应中NH3的物质的量浓度的变化情况如图所示:
2NH3 ΔH<0。反应中NH3的物质的量浓度的变化情况如图所示:
(1)根据图示,计算从反应开始到第4分钟达到平衡时,平均反应速率υ(N2)为
(2)达到平衡后,第5分钟末,若保持其它条件不变,只改变反应温度,则NH3的物质的量浓度不可能为
a.0.20 mol/L b.0.12 mol/L c.0.10 mol/L d.0.08 mol/L
(3)达到平衡后,第5分钟末,若保持其它条件不变,只把容器的体积缩小,新平衡时NH3的浓度恰好为原来的2倍,则新体积
(4)在第5分钟末将容器的体积缩小一半,若在第8分钟末达到新的平衡(此时NH3的浓度约为0.25 mol/L)
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】(1)如图表示在密闭容器中反应:2SO2+O2⇌2SO3 ∆H=-Q kJ/mol。到平衡时,由于条件改变而引起反应速度和化学平衡的变化情况,a→b 过程中改变的条件可能是_____ ;b→c过程中改变的条件可能是_____ ;若增大压强时,将反应速度变化情况画在c~d处_____ 。
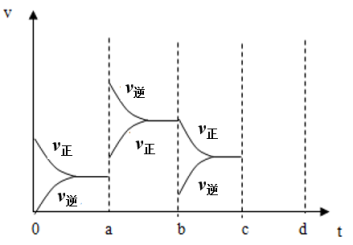
(2)可逆反应 mA(g)+nB(g)⇌pC(g)达到平衡后,升高温度,B 的转化率变大;当减小压强,C 的体积分数减小。
①用“>”、“=”或“<”填空:该反应的 Δ H_____ 0,m+n_____ p。
②用“增大”“减小”或“不变”填空(其他条件不变):恒容下加入 B,则 A 的转化率_____ ;升高温度,则平衡时 B、C 的浓度之比 c(B)/c(C)将_____ ;加入催化剂,平衡时气体混合物的总物质的量_____ 。

(2)可逆反应 mA(g)+nB(g)⇌pC(g)达到平衡后,升高温度,B 的转化率变大;当减小压强,C 的体积分数减小。
①用“>”、“=”或“<”填空:该反应的 Δ H
②用“增大”“减小”或“不变”填空(其他条件不变):恒容下加入 B,则 A 的转化率
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】定条件下,发生反应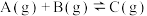
 ,达到平衡后根据下列图像判断:
,达到平衡后根据下列图像判断:
A.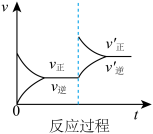 B.
B.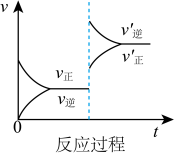 C.
C.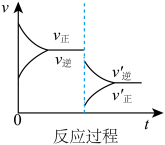 D.
D.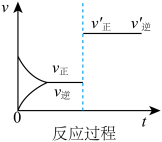 E.
E.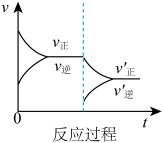
(1)表示升高温度,达到新平衡的是_______ (填“A”、“B”、“C”、“D”或“E”,下同),新平衡中C的质量分数_______ (填“增大”、“减小”或“不变”,下同)。
(2)表示降低压强,达到新平衡的是_______ ,A的转化率_______ 。
(3)表示减少C的浓度,达到新平衡的是_______ 。
(4)增加A的浓度,达到平衡后A的转化率_______ 。
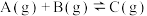
 ,达到平衡后根据下列图像判断:
,达到平衡后根据下列图像判断:A.
 B.
B. C.
C. D.
D. E.
E.
(1)表示升高温度,达到新平衡的是
(2)表示降低压强,达到新平衡的是
(3)表示减少C的浓度,达到新平衡的是
(4)增加A的浓度,达到平衡后A的转化率
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】氢能是一种极具发展潜力的清洁能源。以太阳能为热源,热化学硫碘循环分解水是一种高效、无污染的制氢方法。其反应过程如下图所示:
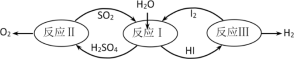
(1)反应Ⅰ的化学方程式是______________________________________
(2)已知反应Ⅱ:2H2SO4(l)=2SO2(g)+O2(g)+2H2O(g) △H=+550 kJ·mol-1
它由两步反应组成:i.H2SO4(l)=SO3(g)+H2O(g) △H=+177 kJ·mol-1
ii.SO3(g)分解。
则SO3(g)分解的热化学方程式为____________________ 。
(3)L(L1、L2)、X可分别代表压强或温度其中之一。如图表示L一定时,ii中SO3(g)的质量分数随X的变化关系。
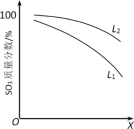
①X代表的物理量是__________ 。
②判断L1、L2的大小关系:L1_______ L2,并简述理由:______________ 。

(1)反应Ⅰ的化学方程式是
(2)已知反应Ⅱ:2H2SO4(l)=2SO2(g)+O2(g)+2H2O(g) △H=+550 kJ·mol-1
它由两步反应组成:i.H2SO4(l)=SO3(g)+H2O(g) △H=+177 kJ·mol-1
ii.SO3(g)分解。
则SO3(g)分解的热化学方程式为
(3)L(L1、L2)、X可分别代表压强或温度其中之一。如图表示L一定时,ii中SO3(g)的质量分数随X的变化关系。

①X代表的物理量是
②判断L1、L2的大小关系:L1
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】一定条件下,在体积为5 L的密闭容器中,A、B、C三种气体的物质的量n(mol)随时间t(min)的变化如图1所示。已知达平衡后,降低温度,A的体积分数将减小。
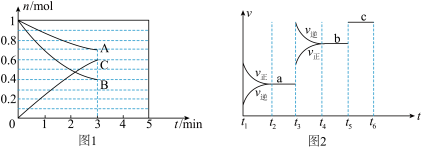
(1)该反应的化学方程式为__________________ ,此反应平衡常数的表达式为K=________ 。
(2)从开始到最初达到平衡,C的平均反应速率v(C)=________________ 。3min时,A的转化率=________ %。该反应的
________ 0。(填“ ”、“
”、“ ”或“
”或“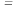 ”)
”)
(3)对于该反应改变某些条件,化学反应速率及化学平衡状态可能会发生变化,请回答:
①恒温恒容充入惰性气体,平衡______ 移动(填“正向”、“逆向”或“不”,下同)
②恒温恒压充入惰性气体,平衡______ 移动,化学反应速率_______ (填“加快”或“减慢”)
③升高温度,平衡______ 移动。
(4)该反应的反应速率v随时间t的关系如图2所示:
①根据图2判断,在t3时刻改变的外界条件是_______ ,t5时刻改变的外界条件是_______ 。
②a、b、c三个阶段中,C的体积分数最大的是________ ,
③a、b、c三个阶段的平衡常数分别用K1、K2、K3表示则:K1、K2、K3之间的关系为___________ (用“ ”、“
”、“ ”或“
”或“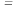 ”连接)。
”连接)。

(1)该反应的化学方程式为
(2)从开始到最初达到平衡,C的平均反应速率v(C)=

 ”、“
”、“ ”或“
”或“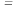 ”)
”)(3)对于该反应改变某些条件,化学反应速率及化学平衡状态可能会发生变化,请回答:
①恒温恒容充入惰性气体,平衡
②恒温恒压充入惰性气体,平衡
③升高温度,平衡
(4)该反应的反应速率v随时间t的关系如图2所示:
①根据图2判断,在t3时刻改变的外界条件是
②a、b、c三个阶段中,C的体积分数最大的是
③a、b、c三个阶段的平衡常数分别用K1、K2、K3表示则:K1、K2、K3之间的关系为
 ”、“
”、“ ”或“
”或“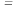 ”连接)。
”连接)。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】(1)对于反应:2NO(g)+O2(g) 2NO2(g),在其他条件相同时,分别测得NO的平衡转化率在不同压强(p1、p2)下随温度变化的曲线(如图)。
2NO2(g),在其他条件相同时,分别测得NO的平衡转化率在不同压强(p1、p2)下随温度变化的曲线(如图)。

①比较p1、p2的大小关系:__ 。
②随温度降低,该反应平衡常数变化的趋势是__ (填“增大”或“减小”)。
(2)在容积为1.00L的容器中,通入一定量的N2O4,发生反应N2O4(g) 2NO2(g),随温度升高,混合气体的颜色变深。
2NO2(g),随温度升高,混合气体的颜色变深。
回答下列问题:
①反应的ΔH__ (填“>”或“<”)0;100℃时,体系中各物质浓度随时间变化如图所示。在0~60s时段,反应速率v(NO2)为__ ;反应的平衡常数K为_ 。
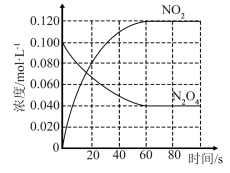
②100℃时达平衡后,改变反应温度为T,c(N2O4)以0.0020mol·L-1·s-1的平均速率降低,10s后又达到平衡,则T__ (填“大于”或“小于”)100℃。
 2NO2(g),在其他条件相同时,分别测得NO的平衡转化率在不同压强(p1、p2)下随温度变化的曲线(如图)。
2NO2(g),在其他条件相同时,分别测得NO的平衡转化率在不同压强(p1、p2)下随温度变化的曲线(如图)。
①比较p1、p2的大小关系:
②随温度降低,该反应平衡常数变化的趋势是
(2)在容积为1.00L的容器中,通入一定量的N2O4,发生反应N2O4(g)
 2NO2(g),随温度升高,混合气体的颜色变深。
2NO2(g),随温度升高,混合气体的颜色变深。回答下列问题:
①反应的ΔH

②100℃时达平衡后,改变反应温度为T,c(N2O4)以0.0020mol·L-1·s-1的平均速率降低,10s后又达到平衡,则T
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】向某体积固定的密闭容器中加入0.3molA、0.1molC和一定量(未知)的B三种气体,一定条件下发生反应,各物质浓度随时间变化如下图所示。已知在反应过程中混合气体的总的物质的量没有变化。请回答:
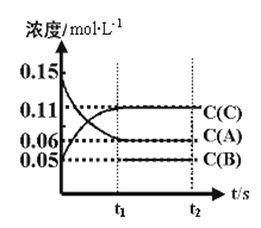
(1)若t1=15s时,则t0-t1阶段以C物质浓度变化表示的反应速率V(C)=________________ mol/(L•s)。已知t0 时刻A的浓度为0.15mol/L
(2)t1 s时,反应是否达平衡状态?________ (填“是”或“否”),t2 s时,V正________ V逆(填“>”“<”或“=”)。
(3)写出反应的化学方程式:_________________________________

(1)若t1=15s时,则t0-t1阶段以C物质浓度变化表示的反应速率V(C)=
(2)t1 s时,反应是否达平衡状态?
(3)写出反应的化学方程式:
您最近一年使用:0次



