黄铜是由铜和锌组成的合金,在黄铜中加入镍可显著提高黄铜在大气中和海水中的耐蚀性。回答下列问题:
(1)基态29Cu的核外电子排布式为_______ 。
(2)CuSO4溶液里逐滴滴入过量氨水,形成深蓝色溶液。深蓝色的溶液是因为生成了一种配离子,其中配位原子是_______ 。
(1)基态29Cu的核外电子排布式为
(2)CuSO4溶液里逐滴滴入过量氨水,形成深蓝色溶液。深蓝色的溶液是因为生成了一种配离子,其中配位原子是
更新时间:2021-05-08 12:57:17
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】2022年央视春晚的舞蹈剧《只此青绿》灵感来自北宋卷轴画《千里江山图》,该卷长11.91米,颜色绚丽,由石绿、雌黄、赭石、砗磲、朱砂等颜料绘制而成。颜料中经常含有铜、锌、钛、铁等元素。
(1)写出Zn所在元素周期表中的分区是_______ 区;基态Ti原子的价电子排布式_______ ;基态 核外电子的空间运动状态有
核外电子的空间运动状态有_______ 种,基态铁原子处在最高能层的电子的电子云形状为_______ 。
(2) 、
、 、
、 的键角由大到小的顺序为
的键角由大到小的顺序为_______ 。
(3)一种新研发出的铁磁性材料M的分子结构如图所示。
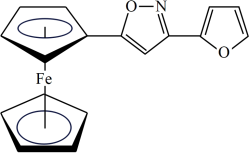
①M分子中C、N、O三种元素的电负性由大到小的顺序为_______ 。
②M分子中 共提供6个杂化轨道,则铁原子可能的杂化方式为
共提供6个杂化轨道,则铁原子可能的杂化方式为_______ (填序号)。
A. B.
B. C.
C. D.
D.
(1)写出Zn所在元素周期表中的分区是
 核外电子的空间运动状态有
核外电子的空间运动状态有(2)
 、
、 、
、 的键角由大到小的顺序为
的键角由大到小的顺序为(3)一种新研发出的铁磁性材料M的分子结构如图所示。

①M分子中C、N、O三种元素的电负性由大到小的顺序为
②M分子中
 共提供6个杂化轨道,则铁原子可能的杂化方式为
共提供6个杂化轨道,则铁原子可能的杂化方式为A.
 B.
B. C.
C. D.
D.
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】硼(B)及其化合物在化学中有重要的地位。请回答下列问题:
(1)Ga与B同主族,Ga的基态原子核外电子排布式为_______ ,第一电离能由大到小的顺序是_______ 。
(2)硼酸(H3BO3)是白色片状晶体(层状结构如图),有滑腻感,在冷水中溶解度很小,加热时溶解度增大。
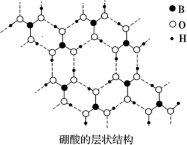
①硼酸中B原子的杂化轨道类型为_______ 。
②硼酸晶体中存在的作用力有范德华力和_______ 。
③加热时,硼酸的溶解度增大,主要原因是_______ 。
④硼酸是一元弱酸,在水中电离时,硼酸结合水电离出的OH-而呈酸性。写出硼酸的电离方程式:_______ 。
(3)硼氢化钠(NaBH4)是有机化学中的一种常用还原剂,在热水中水解生成硼酸钠和氢气,用化学方程式表示其反应原理:_______ 。[BH4]-的空间构型是_______ 。
(4)B3N3H6可用来制造具有耐油、耐高温性能的特殊材料。写出它的一种等电子体物质的分子式:_______ 。
(5)硼化镁晶体在39 K时呈超导性。在硼化镁晶体中,镁原子和硼原子是分层排布的,如图是该晶体微观结构的透视图,图中的硼原子和镁原子投影在同一平面上。则硼化镁的化学式为_______ 。

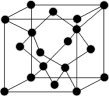
(6)金刚石的晶胞如图。立方氮化硼的结构与金刚石相似,已知晶胞边长为361.5 pm,则立方氮化硼的密度是_______ g· cm-3。(只要求列算式,不必计算出数值,阿伏加德罗常数用NA表示)。
(1)Ga与B同主族,Ga的基态原子核外电子排布式为
(2)硼酸(H3BO3)是白色片状晶体(层状结构如图),有滑腻感,在冷水中溶解度很小,加热时溶解度增大。

①硼酸中B原子的杂化轨道类型为
②硼酸晶体中存在的作用力有范德华力和
③加热时,硼酸的溶解度增大,主要原因是
④硼酸是一元弱酸,在水中电离时,硼酸结合水电离出的OH-而呈酸性。写出硼酸的电离方程式:
(3)硼氢化钠(NaBH4)是有机化学中的一种常用还原剂,在热水中水解生成硼酸钠和氢气,用化学方程式表示其反应原理:
(4)B3N3H6可用来制造具有耐油、耐高温性能的特殊材料。写出它的一种等电子体物质的分子式:
(5)硼化镁晶体在39 K时呈超导性。在硼化镁晶体中,镁原子和硼原子是分层排布的,如图是该晶体微观结构的透视图,图中的硼原子和镁原子投影在同一平面上。则硼化镁的化学式为

(6)金刚石的晶胞如图。立方氮化硼的结构与金刚石相似,已知晶胞边长为361.5 pm,则立方氮化硼的密度是

您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】工厂烟气(主要污染物NO)直接排放会造成空气污染,需处理后才能排放。“纳米零价铁— ”体系可将烟气中难溶的NO氧化为可溶的
”体系可将烟气中难溶的NO氧化为可溶的 。
。
(1)制备纳米零价铁将 溶液与碱性
溶液与碱性 溶液混合可生成纳米零价铁、
溶液混合可生成纳米零价铁、 和
和 等。
等。
 中
中 电子排布式为
电子排布式为___________ 。
(2)NO的氧化:在一定温度下,将 溶液和HCl溶液雾化后与烟气按一定比例混合,以一定流速通过装有纳米零价铁的反应装置,可将烟气中的NO氧化。
溶液和HCl溶液雾化后与烟气按一定比例混合,以一定流速通过装有纳米零价铁的反应装置,可将烟气中的NO氧化。
①X催化 分解产生HO·,HO·将NO氧化为
分解产生HO·,HO·将NO氧化为 的机理如图所示,则Y的化学式为
的机理如图所示,则Y的化学式为___________ ,纳米零价铁的作用是___________ 。___________ 。
③ 与Y反应可实现X再生,同时产生
与Y反应可实现X再生,同时产生 ,写出
,写出 的电子式
的电子式___________ ,此时 作为
作为___________ 剂。
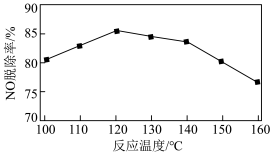
④NO脱除率随温度的变化如下图所示。温度高于120℃时,NO脱除率随温度升高呈现下降趋势的主要原因是___________ 。 表示),可大致分为2个过程,反应原理如下图所示。
表示),可大致分为2个过程,反应原理如下图所示。___________ 。
 ”体系可将烟气中难溶的NO氧化为可溶的
”体系可将烟气中难溶的NO氧化为可溶的 。
。(1)制备纳米零价铁将
 溶液与碱性
溶液与碱性 溶液混合可生成纳米零价铁、
溶液混合可生成纳米零价铁、 和
和 等。
等。 中
中 电子排布式为
电子排布式为(2)NO的氧化:在一定温度下,将
 溶液和HCl溶液雾化后与烟气按一定比例混合,以一定流速通过装有纳米零价铁的反应装置,可将烟气中的NO氧化。
溶液和HCl溶液雾化后与烟气按一定比例混合,以一定流速通过装有纳米零价铁的反应装置,可将烟气中的NO氧化。①X催化
 分解产生HO·,HO·将NO氧化为
分解产生HO·,HO·将NO氧化为 的机理如图所示,则Y的化学式为
的机理如图所示,则Y的化学式为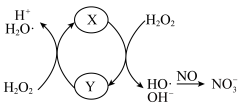
③
 与Y反应可实现X再生,同时产生
与Y反应可实现X再生,同时产生 ,写出
,写出 的电子式
的电子式 作为
作为④NO脱除率随温度的变化如下图所示。温度高于120℃时,NO脱除率随温度升高呈现下降趋势的主要原因是
 表示),可大致分为2个过程,反应原理如下图所示。
表示),可大致分为2个过程,反应原理如下图所示。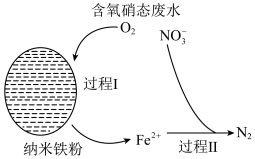
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】现有两种配合物晶体[Co(NH3)6]Cl3和[Co(NH3)5Cl]Cl2,一种为橙黄色,另一种为紫红色。
(1)请写出两种晶体在水中的电离方程式_______ 。
(2)请设计实验方案将这两种配合物区别开来_______ 。
照相底片的定影液中银的回收过程如下:
步骤1:将曝光后的照相底片用定影液(Na2S2O3)浸泡,使未曝光的AgBr转化成配合物溶解,该反应AgBr和Na2S2O3的物质的量之比为1∶2。
步骤2:在步骤1的废定影液中加Na2S使配合物转化为黑色沉淀,并使定影液再生。
步骤3:过滤,将黑色沉淀灼烧回收银。
(3)下列说法不正确的是_______ 。

(1)请写出两种晶体在水中的电离方程式
(2)请设计实验方案将这两种配合物区别开来
照相底片的定影液中银的回收过程如下:
步骤1:将曝光后的照相底片用定影液(Na2S2O3)浸泡,使未曝光的AgBr转化成配合物溶解,该反应AgBr和Na2S2O3的物质的量之比为1∶2。
步骤2:在步骤1的废定影液中加Na2S使配合物转化为黑色沉淀,并使定影液再生。
步骤3:过滤,将黑色沉淀灼烧回收银。
(3)下列说法不正确的是

| A.步骤1中配合物的内外界离子数之比为1∶2 |
| B.步骤2中黑色沉淀为Ag2S |
| C.步骤3灼烧时要进行尾气吸收 |
| D.如图所示NaBr晶胞中有4个Br- |
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】完成下列问题
(1)据科技日报网报道,南开大学科研团队借助镍和苯基硼酸共催化剂,首次实现烯丙醇高效、绿色合成。烯丙醇的结构简式为 。请回答下列问题:
。请回答下列问题:
①基态镍原子的价电子排布式为_______ 。
② ,烯丙醇分子中碳原子的杂化类型为
,烯丙醇分子中碳原子的杂化类型为_______ 。
③某种含Cu2+的化合物可催化烯丙醇制备丙醛的反应:HOCH2CH=CH2→CH3CH2CHO,在烯丙醇分子中σ键和π键的个数比为_______ 。
(2) 具有对称的空间构型,若其中两个NH3被两个Cl-取代,能得到两种不同结构的产物,则
具有对称的空间构型,若其中两个NH3被两个Cl-取代,能得到两种不同结构的产物,则 中的配位数为
中的配位数为_______ ,配离子的空间构型为_______ 。
(3)铜是重要的过渡元素,能形成多种配合物,如Cu2+与乙二胺可形成如图所示配离子。
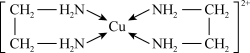
①Cu2+与乙二胺所形成的配离子内部不含有的化学键类型是_______ (填字母序号)。
a.配位键 b.极性键 c.离子键 d.非极性键
②乙二胺和三甲胺 均属于胺。但乙二胺比三甲胺的沸点高很多,原因是
均属于胺。但乙二胺比三甲胺的沸点高很多,原因是_______ 。
(1)据科技日报网报道,南开大学科研团队借助镍和苯基硼酸共催化剂,首次实现烯丙醇高效、绿色合成。烯丙醇的结构简式为
 。请回答下列问题:
。请回答下列问题:①基态镍原子的价电子排布式为
②
 ,烯丙醇分子中碳原子的杂化类型为
,烯丙醇分子中碳原子的杂化类型为③某种含Cu2+的化合物可催化烯丙醇制备丙醛的反应:HOCH2CH=CH2→CH3CH2CHO,在烯丙醇分子中σ键和π键的个数比为
(2)
 具有对称的空间构型,若其中两个NH3被两个Cl-取代,能得到两种不同结构的产物,则
具有对称的空间构型,若其中两个NH3被两个Cl-取代,能得到两种不同结构的产物,则 中的配位数为
中的配位数为(3)铜是重要的过渡元素,能形成多种配合物,如Cu2+与乙二胺可形成如图所示配离子。

①Cu2+与乙二胺所形成的配离子内部不含有的化学键类型是
a.配位键 b.极性键 c.离子键 d.非极性键
②乙二胺和三甲胺
 均属于胺。但乙二胺比三甲胺的沸点高很多,原因是
均属于胺。但乙二胺比三甲胺的沸点高很多,原因是
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐3】大量研究证明:稀土离子对植物确有促进生根发芽、增加叶绿素含量、增强光合强度、改善植物对大量营养元素吸收的作用,从而促进作物干物质的积累,使其产量和质量得到提高与改进。目前有关稀土元素植物光合作用机理的研究取得了一些新进展。我国科学家通过研究提出其一-种机理是,稀土离子替代镁离子而配位到叶绿素(见图1)的卟啉环上,形成叶绿素a-稀土配合物。已合成了错叶绿素a(Pr-Chla)(见图2),并证明Pr-Chla具有双层夹心结构。Pr(III)夹于两个卟啉环之间,与上下卟啉环上共8个N原子配位,Pr-N键平均键长为0.242nm。
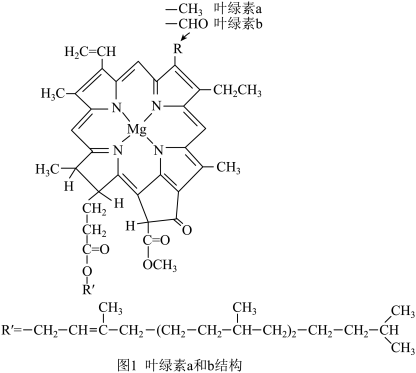
一些元素的离子半径如上表所示。有专家提出上述夹心物形成除它们的激发态能量与叶绿素配体三重态能量相当,能量转移效率较高因素外,还与元素的离子势(即离子吸引电子的能力)相关,离子势与离子电荷成正比,与离子半径成反比。请根据本题所给信息和上表中数据,回答下列问题:
(1)专家首先选择元素Pr3+替代Mg2+,且获得了成功,请简述首选Pr3+的原因:_______ 。
(2)植物体内有大量钙元素,钙和镁同族,简述Ca2+是否容易形成钙叶绿素a(CaChla)?____ 。

| 元素名称、离子 | 镁、Mg2+ | 镧、La3+ | 铈、Ce3+ | 镨、Pr3+ | 钐、Sm3+ | 钙、Ca2+ |
| 离子半径/(pm) | 66 | 106.1 | 103.4. | 101.3 | 96.4 | 99 |
一些元素的离子半径如上表所示。有专家提出上述夹心物形成除它们的激发态能量与叶绿素配体三重态能量相当,能量转移效率较高因素外,还与元素的离子势(即离子吸引电子的能力)相关,离子势与离子电荷成正比,与离子半径成反比。请根据本题所给信息和上表中数据,回答下列问题:
(1)专家首先选择元素Pr3+替代Mg2+,且获得了成功,请简述首选Pr3+的原因:
(2)植物体内有大量钙元素,钙和镁同族,简述Ca2+是否容易形成钙叶绿素a(CaChla)?
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】锌是一种重要的过渡金属,锌及其化合物有着广泛的应用。
(1)指出锌在周期表中的_______ 区。
(2)葡萄糖酸锌[CH2OH(CHOH)4COO]2Zn是目前市场上流行的补锌剂。写出Zn2+基态电子排布式_______ ;葡萄糖分子中碳原子的杂化方式有_______ 。
(3)Zn2+能与NH3形成配离子[Zn(NH3)4]2+。配位体:NH3分子属于_______ (填“极性分子”或“非极性分子”);在[Zn(NH3)4]2+中,Zn2+位于正四面体中心,NH3位于正四面体的顶点,试在图甲中表示[Zn(NH3)4]2+中Zn2+与NH3之间的化学键_____________ 。_______ ;该化合物晶体的熔点比干冰高得多,原因是_______ 。
(1)指出锌在周期表中的
(2)葡萄糖酸锌[CH2OH(CHOH)4COO]2Zn是目前市场上流行的补锌剂。写出Zn2+基态电子排布式
(3)Zn2+能与NH3形成配离子[Zn(NH3)4]2+。配位体:NH3分子属于

您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】2020年,比亚迪宣布推出基于磷酸铁锂技术的“刀片电池”,刀片电池能量密度大,安全性高。电池的正极活性材料是 。请回答下列问题
。请回答下列问题
(1)铁元素位于周期表第四周期第___________ 族;基态 的最外层电子排布式为
的最外层电子排布式为___________ 。
(2)正极材料 的阴离子
的阴离子 的空间结构为
的空间结构为___________ ,请写出一个与 为等电子体的分子
为等电子体的分子___________ 。
(3) 原子或离子外围有较多能量相近的空轨道,能与
原子或离子外围有较多能量相近的空轨道,能与 等形成配合物。
等形成配合物。
① 与
与 形成配位键时,提供孤电子对的原子是
形成配位键时,提供孤电子对的原子是___________ ,1mol[Fe(SCN)6]3-的 键数目为
键数目为___________ 。
②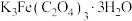 为可溶于水的晶体,某同学欲检验该晶体中
为可溶于水的晶体,某同学欲检验该晶体中 元素的价态,取少量晶体放入试管中,加蒸馏水使其充分溶解,再向试管中滴入几滴
元素的价态,取少量晶体放入试管中,加蒸馏水使其充分溶解,再向试管中滴入几滴 溶液。
溶液。
已知:i.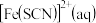 为血红色:
为血红色:
ii. 时,
时,
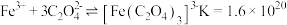
上述实验方案___________ (填“可行”或“不可行”),并解释其原因___________ 。
 。请回答下列问题
。请回答下列问题(1)铁元素位于周期表第四周期第
 的最外层电子排布式为
的最外层电子排布式为(2)正极材料
 的阴离子
的阴离子 的空间结构为
的空间结构为 为等电子体的分子
为等电子体的分子(3)
 原子或离子外围有较多能量相近的空轨道,能与
原子或离子外围有较多能量相近的空轨道,能与 等形成配合物。
等形成配合物。①
 与
与 形成配位键时,提供孤电子对的原子是
形成配位键时,提供孤电子对的原子是 键数目为
键数目为②
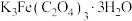 为可溶于水的晶体,某同学欲检验该晶体中
为可溶于水的晶体,某同学欲检验该晶体中 元素的价态,取少量晶体放入试管中,加蒸馏水使其充分溶解,再向试管中滴入几滴
元素的价态,取少量晶体放入试管中,加蒸馏水使其充分溶解,再向试管中滴入几滴 溶液。
溶液。已知:i.
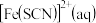 为血红色:
为血红色:ii.
 时,
时,
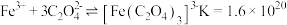
上述实验方案
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】CuCl和CuCl2都是重要的化工原料,常用作催化剂、颜料、防腐剂和消毒剂等。
已知:①CuCl可以由CuCl2用适当的还原剂如SO2,SnCl2等还原制得:
2Cu2++2Cl-+SO2+2H2O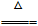 2CuCl↓+4H++SO
2CuCl↓+4H++SO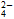
2CuCl2+SnCl2===2CuCl↓+SnCl4
②CuCl2溶液与乙二胺(H2N—CH2—CH2—NH2)可形成配离子:

请回答下列问题:
(1)基态Cu原子的核外电子排布式为________ ;H、N、O三种元素的电负性由大到小的顺序是________ 。
(2)SO2分子的空间构型为________ ;与SnCl4互为等电子体的一种离子的化学式为________ 。
(3)乙二胺分子中氮原子轨道的杂化类型为________ 。乙二胺和三甲胺[N(CH3)3]均属于胺,但乙二胺比三甲胺的沸点高得多,原因是_________________________________ 。
(4)②中所形成的配离子中含有的化学键类型有______ (填字母)。
A.配位键 B.极性键
C.离子键 D.非极性键
已知:①CuCl可以由CuCl2用适当的还原剂如SO2,SnCl2等还原制得:
2Cu2++2Cl-+SO2+2H2O
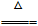 2CuCl↓+4H++SO
2CuCl↓+4H++SO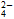
2CuCl2+SnCl2===2CuCl↓+SnCl4
②CuCl2溶液与乙二胺(H2N—CH2—CH2—NH2)可形成配离子:

请回答下列问题:
(1)基态Cu原子的核外电子排布式为
(2)SO2分子的空间构型为
(3)乙二胺分子中氮原子轨道的杂化类型为
(4)②中所形成的配离子中含有的化学键类型有
A.配位键 B.极性键
C.离子键 D.非极性键
您最近半年使用:0次



