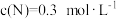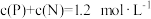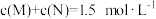在密闭容器中进行反应:N2 + 3H2 (g)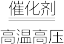 2NH3 (g),当反应达到限度时,下列说法正确的是
2NH3 (g),当反应达到限度时,下列说法正确的是
 2NH3 (g),当反应达到限度时,下列说法正确的是
2NH3 (g),当反应达到限度时,下列说法正确的是| A.N2、H2 完全转化为 NH3 | B.此时反应已停止 |
| C.氮气、氢气、氨气的浓度不变 | D.氮气、氢气、氨气的浓度相等 |
更新时间:2021-05-10 15:47:55
|
相似题推荐
单选题
|
较易
(0.85)
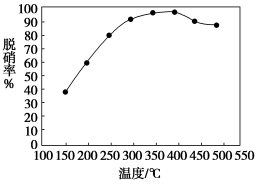
【推荐1】NOx是生成光化学烟雾、破坏臭氧层和形成酸雨的前驱气体之一。烟道气中氮氧化物可采用氯气催化脱硝,下图是相同流速不同温度下的脱硝率,反应方程式可表示为2NH3(g)+NO(g)+NO2(g) 2N2(g)+3H2O(g)。下列说法不正确的是
2N2(g)+3H2O(g)。下列说法不正确的是
 2N2(g)+3H2O(g)。下列说法不正确的是
2N2(g)+3H2O(g)。下列说法不正确的是
| A.脱硝的适宜温度约400 ℃左右 |
| B.平衡时,其他条件不变,升高温度该反应的平衡常数减小 |
| C.其他条件不变,使用高效催化剂,脱硝率增大 |
| D.单位时间内消耗NO和N2的物质的量比为1:2时,反应达到平衡 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】一定条件下,在体积一定的密闭容器中加入1molCO2和4molH2发生反应:CO2+4H2 CH4+2H2O。下列关于该反应的说法正确的是( )
CH4+2H2O。下列关于该反应的说法正确的是( )
 CH4+2H2O。下列关于该反应的说法正确的是( )
CH4+2H2O。下列关于该反应的说法正确的是( )| A.降低温度能加快反应速率 |
| B.反应达到平衡时,v(正)=v(逆)=0 |
| C.增大压强可以加快反应速率 |
| D.达到化学反应限度时,将生成1molCH4 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐1】工业制硫酸中的一步重要反应是二氧化硫在400~600℃下的催化氧化:2SO2+O2 2SO3。如果反应在密闭容器中进行,下列有关的叙述不正确的是
2SO3。如果反应在密闭容器中进行,下列有关的叙述不正确的是
 2SO3。如果反应在密闭容器中进行,下列有关的叙述不正确的是
2SO3。如果反应在密闭容器中进行,下列有关的叙述不正确的是| A.使用催化剂是为了加快反应速率 |
| B.在上述条件下,SO2、O2、SO3将共存于反应体系之中 |
| C.当生成O2的速率与生成SO3的速率相等时达到了平衡 |
| D.SO2是酸性氧化物 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】氯气与水反应的化学方程式为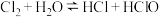 ,可用于自来水消毒。下列关于该反应的说法正确的是
,可用于自来水消毒。下列关于该反应的说法正确的是
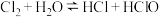 ,可用于自来水消毒。下列关于该反应的说法正确的是
,可用于自来水消毒。下列关于该反应的说法正确的是| A.升高温度能减慢反应速率 | B.增大 的浓度能加快反应速率 的浓度能加快反应速率 |
| C.增大压强,对该反应的速率没有影响 | D.达到化学平衡时, 能100%转化 能100%转化 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐3】下列实验内容能达到相应实验目的的是
| 选项 | 实验内容 | 实验目的 |
| A | 向1mL  ,溶液中加入5mL ,溶液中加入5mL  溶液,充分反应后,加入2mL苯,充分振荡、静置,分液后将水层分装于两支小试管中,向其中一支小试管中滴加5~6滴15%的 溶液,充分反应后,加入2mL苯,充分振荡、静置,分液后将水层分装于两支小试管中,向其中一支小试管中滴加5~6滴15%的 溶液,观察并比较两支试管中溶液的颜色 溶液,观察并比较两支试管中溶液的颜色 | 证明 与 与 之间的反应属于可逆反应 之间的反应属于可逆反应 |
| B | 室温时,将等体积、等物质的量浓度的 、 、 ,溶液分别加入等体积的30%的 ,溶液分别加入等体积的30%的 溶液中,观察并比较两支试管中气泡产生的快慢 溶液中,观察并比较两支试管中气泡产生的快慢 | 探究 、 、 催化效果的优劣 催化效果的优劣 |
| C | 取两支试管,分别加入5mL4%、5mL12%的 溶液,向其中一支试管中加入少量 溶液,向其中一支试管中加入少量 粉末,观察并比较两支试管中气泡产生的快慢 粉末,观察并比较两支试管中气泡产生的快慢 | 探究浓度对反应速率的影响 |
| D | 将相同体积相同浓度的稀硫酸分别加入两支试管中,再向两支试管中分别加入不同体积、等浓度的 溶液,将两支试管分别放入盛有等温等量的热水的烧杯中,观察并比较两支试管中出现浑浊现象的快慢 溶液,将两支试管分别放入盛有等温等量的热水的烧杯中,观察并比较两支试管中出现浑浊现象的快慢 | 探究浓度对反应速率的影响 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】一定条件下,将一定量的N2和H2的混合气体充入某恒容密闭容器中,一段时间后,下列叙述能说明该反应达到平衡状态的是
| A.容器中N2、H2、NH3共存 | B.N2、H2、NH3的物质的量之比为1∶3∶2 |
| C.容器中的压强不随时间变化 | D.N2、NH3浓度相等 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】在一定温度下,可逆反应2A(g)+3B(g) 2C(g)达到平衡的标志是( )
2C(g)达到平衡的标志是( )
 2C(g)达到平衡的标志是( )
2C(g)达到平衡的标志是( )| A.A的生成速率与C的分解速率相等 |
| B.单位时间生成2n mol A,同时生成3n mol B |
| C.A、B、C的浓度不再变化 |
| D.A、B、C的分子数之比为2∶3∶2 |
您最近一年使用:0次

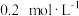 、
、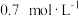 、
、 ,可逆反应
,可逆反应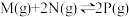 达到平衡时,下列数据合理的是
达到平衡时,下列数据合理的是