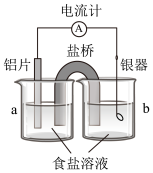
原电池是将化学能转化为电能的装置。
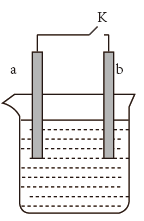
(1)a为铜片,b为铁片,烧杯中是稀硫酸溶液。
①当开关K断开时产生的现象为___________ 。
A.a不断溶解
B.b不断溶解
C.a上产生气泡
D.b上产生气泡
E.溶液逐渐变蓝
②闭合开关K,反应一段时间后断开开关K,经过一段时间后,下列叙述不正确的是___________ 。
A.溶液中H+浓度减小 B.正极附近 浓度逐渐增大
浓度逐渐增大
C.溶液中含有FeSO4 D.溶液中 浓度基本不变
浓度基本不变
(2)FeCl3常用于腐蚀印刷电路铜板,若将此反应设计成原电池,请写出该原电池正极电极反应为___________ 。
(3)下图为氢氧燃料电池的结构示意图,电解质溶液为NaOH溶液,电极材料为疏松多孔的石墨棒。请回答下列问题:
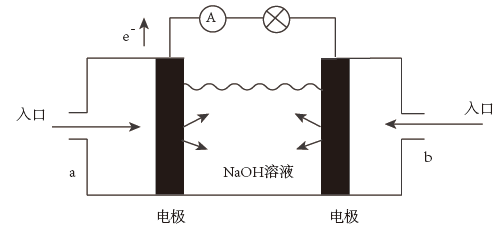
①a极通入的物质为___________ ,电解质溶液中的 移向
移向___________ 极(选填“负”或“正”)。
②写出此氢氧燃料电池工作时,负极的电极反应式:___________ 。
③当消耗氢气11.2L(标准状况下)时,假设电池的能量转化效率为80%,则导线中转移的电子的物质的量为___________ mol。

(1)a为铜片,b为铁片,烧杯中是稀硫酸溶液。
①当开关K断开时产生的现象为
A.a不断溶解
B.b不断溶解
C.a上产生气泡
D.b上产生气泡
E.溶液逐渐变蓝
②闭合开关K,反应一段时间后断开开关K,经过一段时间后,下列叙述不正确的是
A.溶液中H+浓度减小 B.正极附近
 浓度逐渐增大
浓度逐渐增大C.溶液中含有FeSO4 D.溶液中
 浓度基本不变
浓度基本不变(2)FeCl3常用于腐蚀印刷电路铜板,若将此反应设计成原电池,请写出该原电池正极电极反应为
(3)下图为氢氧燃料电池的结构示意图,电解质溶液为NaOH溶液,电极材料为疏松多孔的石墨棒。请回答下列问题:

①a极通入的物质为
 移向
移向②写出此氢氧燃料电池工作时,负极的电极反应式:
③当消耗氢气11.2L(标准状况下)时,假设电池的能量转化效率为80%,则导线中转移的电子的物质的量为
20-21高一下·山西吕梁·期中 查看更多[2]
更新时间:2021-05-11 17:17:52
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】化学反应与能量,是学习和研究化学原理的重要内容。
(1)铁、铜、铝是生活中使用广泛的金属,氯化铁溶液常用于腐蚀印刷电路铜板,若将此反应设计成原电池,则负极所用电极材料为___________ ,正极反应式为___________ 。
(2)将氢气与氧气的反应设计成燃料电池,其能量利用率更高,装置如图所示(a、b为多孔炭棒),其中___________ (填A或B)处电极入口通氢气,其电极反应式为___________ 。工作一段时间后正极区溶液的pH值___________ (填变大、减小或不变)。当消耗标况下氢气33.6L时,假设能量转化率为90%,则导线中转移电子的物质的量为___________ mol。
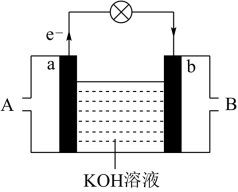
(1)铁、铜、铝是生活中使用广泛的金属,氯化铁溶液常用于腐蚀印刷电路铜板,若将此反应设计成原电池,则负极所用电极材料为
(2)将氢气与氧气的反应设计成燃料电池,其能量利用率更高,装置如图所示(a、b为多孔炭棒),其中

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】如图,请回答下列问题:

(1)若在原电池中,a电极有气泡产生,b电极逐渐变细,则该原电池的正极是_____ (填写字母“a”或“b”),外电路中电流流动的方向是_______ (填写字母“a→b”或“b→a”),b电极发生的反应类型是_______ (填“氧化反应”或“还原反应”) 。
。
(2)当电极a为Zn、电极b为Ag、电解质溶液为CuSO4时,正极的电极反应式为____ 。当a极溶解的质量为6.5g时,有____ mol电子通过导线。

(1)若在原电池中,a电极有气泡产生,b电极逐渐变细,则该原电池的正极是
 。
。(2)当电极a为Zn、电极b为Ag、电解质溶液为CuSO4时,正极的电极反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
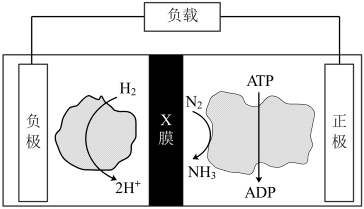
【推荐3】(1)氨气是合成众多含氮物质的原料,利用H2-N2-生物燃料电池,科学家以固氮酶为正极催化剂、氢化酶为负极催化剂,X交换膜为隔膜,在室温条件下合成NH3的同时还获得电能。其工作原理图如下,则X膜为______ 交换膜,正极的电极反应式为______ 。
(2)O2辅助的Al—CO2电池工作原理如图所示。该电池电容量大,能有效利用CO2,电池反应产物Al2(C2O4)3是重要的化工原料。电池的负极反应式:_________ ,电池的正极反应式:__________ ,反应过程中O2的作用是___________ ,该电池的总反应式:____________________ 。
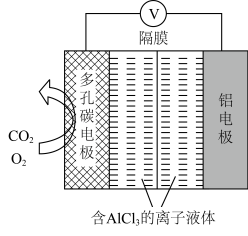

(2)O2辅助的Al—CO2电池工作原理如图所示。该电池电容量大,能有效利用CO2,电池反应产物Al2(C2O4)3是重要的化工原料。电池的负极反应式:

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】某化学兴趣小组为了探索铝电极在原电池中的作用,设计并进行了以下一系列实验,实验结果记录如下:
试根据上表中的实验现象回答下列问题:
(1)实验1、2中,Al电极的作用是否相同?___________ (填“相同”或“不同”)。
(2)在实验3中,铝作___________ 极,其电极反应式为___________ ;该电池总反应方程式为___________ 。
(3)实验4中的铝作___________ 极,试解释原因:___________ 。
| 编号 | 电极材料 | 电解质溶液 | 电流计指针偏转方向 |
| 1 | Mg、Al | 稀盐酸 | 偏向Al |
| 2 | Al、Cu | 稀盐酸 | 偏向Cu |
| 3 | Al、石墨 | 稀盐酸 | 偏向石墨 |
| 4 | Mg、Al | NaOH溶液 | 偏向Mg |
(1)实验1、2中,Al电极的作用是否相同?
(2)在实验3中,铝作
(3)实验4中的铝作
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】新型高效的甲烷燃料电池采用铂为电极材料,两电极上分别通入 和
和 ,电解质溶液为KOH溶液。某研究小组以甲烷燃料电池(装置甲)为电源,模拟氯碱工业生产原理,装置如图所示。
,电解质溶液为KOH溶液。某研究小组以甲烷燃料电池(装置甲)为电源,模拟氯碱工业生产原理,装置如图所示。
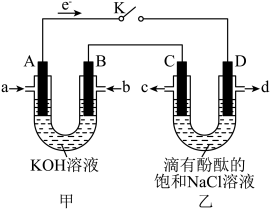
请回答以下问题:
(1)B、D的电极名称分别是___________ 、___________ 。
(2)C极可以选用的材料是___________(填标号)。
(3)该装置工作一段时间后,观察到C极和D极的不同现象是___________ 。
(4)气体b应为___________ (填“ ”或“
”或“ ”),A极发生的电极反应为
”),A极发生的电极反应为___________ 。
(5)装置甲、乙中的电解质溶液足量,当电路中通过0.4mol电子时,气体a、b的总物质的量与气体c、d的总物质的量之比为___________ 。
(6)若以装置甲为电源,要在铁器上镀铜,则铁器应连接___________ (填“A”或“B”)极。
 和
和 ,电解质溶液为KOH溶液。某研究小组以甲烷燃料电池(装置甲)为电源,模拟氯碱工业生产原理,装置如图所示。
,电解质溶液为KOH溶液。某研究小组以甲烷燃料电池(装置甲)为电源,模拟氯碱工业生产原理,装置如图所示。
请回答以下问题:
(1)B、D的电极名称分别是
(2)C极可以选用的材料是___________(填标号)。
| A.铁棒 | B.银棒 | C.石墨棒 | D.铜棒 |
(4)气体b应为
 ”或“
”或“ ”),A极发生的电极反应为
”),A极发生的电极反应为(5)装置甲、乙中的电解质溶液足量,当电路中通过0.4mol电子时,气体a、b的总物质的量与气体c、d的总物质的量之比为
(6)若以装置甲为电源,要在铁器上镀铜,则铁器应连接
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】最近科学家研发了可充电“全氢电池”,其工作原理如图所示,

(1)吸附层a中发生反应的方程式是____________________________
(2)电池的总反应方程式是____________________________
(3)请在图中标出 的移动方向
的移动方向 _______________________ 。
(4)下列说法正确的是_____________________________ (选序号)。
a. 可循环利用,基本不需要补充
可循环利用,基本不需要补充
b.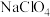 的作用是传导离子和参与电极反应
的作用是传导离子和参与电极反应
c“全氢电池”工作时将化学能转化为电能
d.该电池充电时,吸附层b接电源正极

(1)吸附层a中发生反应的方程式是
(2)电池的总反应方程式是
(3)请在图中标出
 的移动方向
的移动方向 (4)下列说法正确的是
a.
 可循环利用,基本不需要补充
可循环利用,基本不需要补充b.
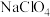 的作用是传导离子和参与电极反应
的作用是传导离子和参与电极反应c“全氢电池”工作时将化学能转化为电能
d.该电池充电时,吸附层b接电源正极
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】回答下列问题:
(1)pH=3的醋酸和pH=ll的氢氧化钠溶液等体积混合后,混合溶液中c(Na+)____ c(CH3COO-)(填“>”或“<”)。
(2)将NaHCO3溶液跟A12(SO4)3溶液混合,相关反应的离子方程式是_________ 。
(3)—定温度下,在一个固定容积的密闭容器中,可逆反应A(g)+2B(g)⇌4C(g)△H>0,达到平衡时,c(A)=2mol•L-1,c(B)=7mol•L-1,c(C)=4mol•L-1。试确定B的起始浓度c(B)的取值范围是________________ 。若改变条件重新达到平衡后体系中C的质量分数增大,其采取的措施是________________ 。
(4)以丙烷为燃料制作新型燃料电池,电池的一极通入O2和CO2,另一极通入丙烷,电解质是熔融碳酸盐,电池负极的电极反应式为___________ ;放电时,CO32−移向电池的___ (填“正”或“负”)极。
(1)pH=3的醋酸和pH=ll的氢氧化钠溶液等体积混合后,混合溶液中c(Na+)
(2)将NaHCO3溶液跟A12(SO4)3溶液混合,相关反应的离子方程式是
(3)—定温度下,在一个固定容积的密闭容器中,可逆反应A(g)+2B(g)⇌4C(g)△H>0,达到平衡时,c(A)=2mol•L-1,c(B)=7mol•L-1,c(C)=4mol•L-1。试确定B的起始浓度c(B)的取值范围是
(4)以丙烷为燃料制作新型燃料电池,电池的一极通入O2和CO2,另一极通入丙烷,电解质是熔融碳酸盐,电池负极的电极反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】(1)如图为氢-氧燃料电池装置示意图。其中A为KOH,C为多孔惰性电极。
①在该电池工作时,a是_______ 极;b电极的电极反应式是____________ 。
②若将进口a的燃料换成CH4,则a电极的电极方程式为______________ 。
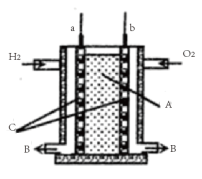
(2)如图为氯碱工业电解饱和氯化钠溶液的装置示意图。
①电解时,电解池总反应的离子反应方程式为___________ 。
②逸出的气体D是___________ ;流出的物质G是___________ 。
③该电解池中离子交换膜属于______________ (填“阳离子交换膜”或“阴离子交换膜”)。

①在该电池工作时,a是
②若将进口a的燃料换成CH4,则a电极的电极方程式为
(2)如图为氯碱工业电解饱和氯化钠溶液的装置示意图。

①电解时,电解池总反应的离子反应方程式为
②逸出的气体D是
③该电解池中离子交换膜属于
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】电化学原理在能量转换、金属冶炼等方面应用广泛。
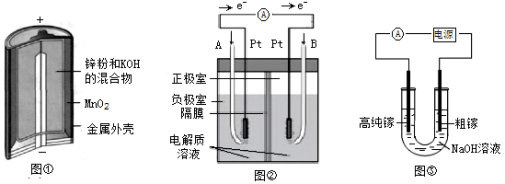
(1)图①是碱性锌锰电池,在负极发生反应的物质是__________ (填“Zn”或“MnO2”),正极发生_________ 反应(填“氧化”或“还原”)。
(2)图②是碱性电解质的氢氧燃料电池,B极通入的气体为________ ,A极发生的电极反应式____________________________________________ 。
(3)电解法可以提纯粗镓,具体原理如图③所示:
①粗镓与电源___________ 极相连(填“正”或“负”)。
②镓在阳极溶解生成的Ga3+与NaOH溶液反应生成GaO2-,GaO2-在阴极放电的电极反应式______________________________________________________ 。
(4)由下列物质冶炼相应金属,须采用电解法的是________ (选填字母序号)。
a.NaCl b.Fe2O3 c.Cu2S d.Al2O3

(1)图①是碱性锌锰电池,在负极发生反应的物质是
(2)图②是碱性电解质的氢氧燃料电池,B极通入的气体为
(3)电解法可以提纯粗镓,具体原理如图③所示:
①粗镓与电源
②镓在阳极溶解生成的Ga3+与NaOH溶液反应生成GaO2-,GaO2-在阴极放电的电极反应式
(4)由下列物质冶炼相应金属,须采用电解法的是
a.NaCl b.Fe2O3 c.Cu2S d.Al2O3
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】化学在生产生活中有广泛的应用,请用所学的知识填空:
(1)氢氧燃料电池具有启动快、效率高等优点,其能量密度高于铅蓄电池。若电解液为 KOH 溶液,则氢氧燃料电池的负极反应式为______ 。
(2)泡沫灭火器内盛有 Al2(SO4)3、NaHCO3溶液,写出其反应的离子方程式______ 。
(3)金属铍(Be)是高效率的火箭燃料,燃烧时放出巨大的能量,已知 1 g 铍完全燃烧放出的热量为 62. 70 kJ,则表示铍的燃烧热的热化学方程式为: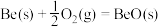 ∆H=
∆H=______ kJ·mol-1.
(4)FeCl3溶液蚀刻铜箔制造电路板的工艺中,废液处理和资源回收的最后一步是在常温下调节溶液 pH=5,此时 c(Fe3+)=______ mol·L-1(已知:Ksp[Fe(OH)3]= 4.0×10-38)。
(1)氢氧燃料电池具有启动快、效率高等优点,其能量密度高于铅蓄电池。若电解液为 KOH 溶液,则氢氧燃料电池的负极反应式为
(2)泡沫灭火器内盛有 Al2(SO4)3、NaHCO3溶液,写出其反应的离子方程式
(3)金属铍(Be)是高效率的火箭燃料,燃烧时放出巨大的能量,已知 1 g 铍完全燃烧放出的热量为 62. 70 kJ,则表示铍的燃烧热的热化学方程式为:
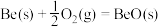 ∆H=
∆H=(4)FeCl3溶液蚀刻铜箔制造电路板的工艺中,废液处理和资源回收的最后一步是在常温下调节溶液 pH=5,此时 c(Fe3+)=
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】氢气是一种新型的绿色能源,又是一种重要的化工原料。
①氢气燃烧热值高。实验测得,在常温常压下,1 mol H2完全燃烧生成液态水,放出285.8 kJ热量,则H2燃烧的热化学方程式正确的是________ 。
A.H2(g)+ O2(g)═H2O(g)△H=+285.8kJ/mol
O2(g)═H2O(g)△H=+285.8kJ/mol
B. H2(g)+ O2(g)═H2O(l)△H=﹣285.8kJ/mol
O2(g)═H2O(l)△H=﹣285.8kJ/mol
C. H2(g)+ O2(g)═H2O(l)△H=+285.8kJ/mol
O2(g)═H2O(l)△H=+285.8kJ/mol
D. H2+ O2═H2O△H=﹣285.8 kJ/mol
O2═H2O△H=﹣285.8 kJ/mol
②氢氧燃料电池能量转化率高,具有广阔的发展前景。氢氧燃料电池中,发生还原反应的物质是______ (填“氢气”或“氧气”)。
③氢气是合成氨的重要原料,合成氨反应的热化方程式如下:
N2(g)+3H2(g)⇌2NH3(g) △H=﹣92.4 kJ/mol
反应达到平衡后,升高温度则反应速率_______ (填“增大”或“减小”);平衡将向____________ (填“正反应方向”或“逆反应方向”)移动。
①氢气燃烧热值高。实验测得,在常温常压下,1 mol H2完全燃烧生成液态水,放出285.8 kJ热量,则H2燃烧的热化学方程式正确的是
A.H2(g)+
 O2(g)═H2O(g)△H=+285.8kJ/mol
O2(g)═H2O(g)△H=+285.8kJ/molB. H2(g)+
 O2(g)═H2O(l)△H=﹣285.8kJ/mol
O2(g)═H2O(l)△H=﹣285.8kJ/molC. H2(g)+
 O2(g)═H2O(l)△H=+285.8kJ/mol
O2(g)═H2O(l)△H=+285.8kJ/molD. H2+
 O2═H2O△H=﹣285.8 kJ/mol
O2═H2O△H=﹣285.8 kJ/mol②氢氧燃料电池能量转化率高,具有广阔的发展前景。氢氧燃料电池中,发生还原反应的物质是
③氢气是合成氨的重要原料,合成氨反应的热化方程式如下:
N2(g)+3H2(g)⇌2NH3(g) △H=﹣92.4 kJ/mol
反应达到平衡后,升高温度则反应速率
您最近一年使用:0次