2020年世界环境日的宣传主题为“关爱自然。刻不容慢”。防治大气污染、水体污染等是世界各国保护环境的最重要课题。
(1)氮的氧化物是造成大气污染的主要物质,研究氮氧化物的反应机理更有助于消除大气污染。
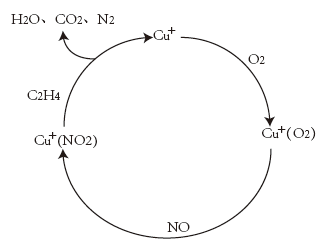
C2H4催化还原NO是重要的烟气脱硝技术,研究发现在Cu+上可能发生的反应过程如图。写出该脱硝过程的总反应的化学方程式:___________ 。
(2)烟气中的氮氧化物经O3预处理后用CaSO3水悬浮液吸收,可减少烟气中氮氧化物的含量。
①室温下,固定进入反应器的NO的物质的量,改变加入O3的物质的量,反应一段时间后体系中n(NO)和n(NO2)随反应前n(O3):n(NO)的变化见下图。
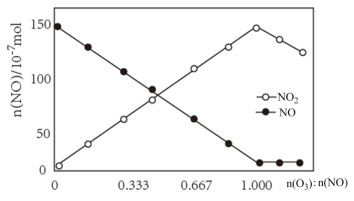
当n(O3):n(NO)≤1时,发生反应的化学方程式为___________ ;
当n(O3):n(NO)>1时,反应后NO2的物质的量减少,其原因是___________ ;
②当用CaSO3水悬浮液吸收经O3预处理的烟气时,清液(弱碱性)中SO 将NO2转化为NO
将NO2转化为NO ,其离子方程式为
,其离子方程式为___________ 。
(3)可综合利用上述吸收烟气后的溶液处理含NH 废水,每产生1 mol无污染气体转移电子数为
废水,每产生1 mol无污染气体转移电子数为_______ 。
(1)氮的氧化物是造成大气污染的主要物质,研究氮氧化物的反应机理更有助于消除大气污染。

C2H4催化还原NO是重要的烟气脱硝技术,研究发现在Cu+上可能发生的反应过程如图。写出该脱硝过程的总反应的化学方程式:
(2)烟气中的氮氧化物经O3预处理后用CaSO3水悬浮液吸收,可减少烟气中氮氧化物的含量。
①室温下,固定进入反应器的NO的物质的量,改变加入O3的物质的量,反应一段时间后体系中n(NO)和n(NO2)随反应前n(O3):n(NO)的变化见下图。

当n(O3):n(NO)≤1时,发生反应的化学方程式为
当n(O3):n(NO)>1时,反应后NO2的物质的量减少,其原因是
②当用CaSO3水悬浮液吸收经O3预处理的烟气时,清液(弱碱性)中SO
 将NO2转化为NO
将NO2转化为NO ,其离子方程式为
,其离子方程式为(3)可综合利用上述吸收烟气后的溶液处理含NH
 废水,每产生1 mol无污染气体转移电子数为
废水,每产生1 mol无污染气体转移电子数为
更新时间:2021-05-12 14:38:16
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】氮氧化物(NO、NO2)、SO2是大气污染物。回答下列问题:
(1)以上污染物会造成的环境问题有_______ (写一种即可)。
(2)如图包含气体发生装置和收集装置(部分装置的夹持仪器已省略),实验室以Cu与浓HNO3反应制备并收集NO2,应选择的装置是_______ (填字母)。

(3)SCR脱硝技术已成为使用广泛和成熟的烟气净化技术,脱硝效率高达90%以上。值,化反应机理如图所示,写出该反应发生的化学方程式:_______
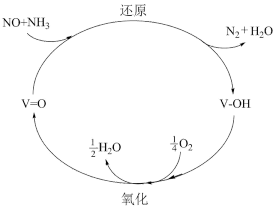
(4)目前,NaClO溶液广泛地应用于脱硫脱硝。某课外小组同学设计了如图喷淋吸收塔装置(如图)。设计该装置的优点是_______ 脱硝(NO)反应的离子方程式为_______ 。

(5)某兴趣小组用Fe2(SO4);溶液吸收含SO2的尾气(SO2的体积分数约10%,其余为空气),实验装置如图所示:

①装置A中用Fe2(SO4);溶液吸收SO2反应的离子方程式:_______ 。
②反应后,若要检验SO2是否过量,可用试剂为_______ 。
③若实验测得反应后的装置A中不含有SO2,为测定其中所含FeSO4的物质的量浓度,现进行如下实验:取20.00mL装置A中溶液,向其中逐滴加入0.1000mol·L-1Ce(SO4)2溶液,发生反应Fe2++Ce4+=Ce3++Fe3+,当反应恰好完全时,共消耗Ce(SO4)2溶液18.00mL。请通过计算确定FeSO4的物质的量浓度_______ 。
(1)以上污染物会造成的环境问题有
(2)如图包含气体发生装置和收集装置(部分装置的夹持仪器已省略),实验室以Cu与浓HNO3反应制备并收集NO2,应选择的装置是

(3)SCR脱硝技术已成为使用广泛和成熟的烟气净化技术,脱硝效率高达90%以上。值,化反应机理如图所示,写出该反应发生的化学方程式:

(4)目前,NaClO溶液广泛地应用于脱硫脱硝。某课外小组同学设计了如图喷淋吸收塔装置(如图)。设计该装置的优点是

(5)某兴趣小组用Fe2(SO4);溶液吸收含SO2的尾气(SO2的体积分数约10%,其余为空气),实验装置如图所示:

①装置A中用Fe2(SO4);溶液吸收SO2反应的离子方程式:
②反应后,若要检验SO2是否过量,可用试剂为
③若实验测得反应后的装置A中不含有SO2,为测定其中所含FeSO4的物质的量浓度,现进行如下实验:取20.00mL装置A中溶液,向其中逐滴加入0.1000mol·L-1Ce(SO4)2溶液,发生反应Fe2++Ce4+=Ce3++Fe3+,当反应恰好完全时,共消耗Ce(SO4)2溶液18.00mL。请通过计算确定FeSO4的物质的量浓度
您最近一年使用:0次
填空题
|
适中
(0.65)
真题
名校
【推荐2】普通纸张的主要成分是纤维素,在早期的纸张生产中,常采用纸表面涂覆明矾的工艺,以填补其表面的微孔,防止墨迹扩散,请回答下列问题:
(1)人们发现纸张会发生酸性腐蚀而变脆、破损,严重威胁纸质文物的保存。经分析检验,发现酸性腐蚀主要与造纸中涂覆明矾的工艺有关,其中的化学原理是______ ;为了防止纸张的酸性腐蚀,可在纸浆中加入碳酸钙等添加剂,该工艺原理的化学方程式为______ 。
(2)为了保护这些纸质文物,有人建议采取下列措施。
①喷洒碱性溶液,如稀氢氧化钠溶液或氨水等,这样操作产生的主要问题是______ 。
②喷洒 ,
, 可以与水反应生成氧化锌和乙烷。用化学(离子)方程式表示生成氧化锌的方法
可以与水反应生成氧化锌和乙烷。用化学(离子)方程式表示生成氧化锌的方法______ 。
(3)现代造纸工艺常用钛白粉( ) 替代明矾,钛白粉的一种工业制法是以钛铁矿(主要成分
) 替代明矾,钛白粉的一种工业制法是以钛铁矿(主要成分 ),为原料按下过程进行的,请完成下列化学方程式:
),为原料按下过程进行的,请完成下列化学方程式:
①___FeTiO3+___C+___Cl2 ___TiCl4+___FeCl3+___CO,
___TiCl4+___FeCl3+___CO,______
②___TiCl4+___O2 ___TiO2+___Cl2,
___TiO2+___Cl2,______ 。
(1)人们发现纸张会发生酸性腐蚀而变脆、破损,严重威胁纸质文物的保存。经分析检验,发现酸性腐蚀主要与造纸中涂覆明矾的工艺有关,其中的化学原理是
(2)为了保护这些纸质文物,有人建议采取下列措施。
①喷洒碱性溶液,如稀氢氧化钠溶液或氨水等,这样操作产生的主要问题是
②喷洒
 ,
, 可以与水反应生成氧化锌和乙烷。用化学(离子)方程式表示生成氧化锌的方法
可以与水反应生成氧化锌和乙烷。用化学(离子)方程式表示生成氧化锌的方法(3)现代造纸工艺常用钛白粉(
 ) 替代明矾,钛白粉的一种工业制法是以钛铁矿(主要成分
) 替代明矾,钛白粉的一种工业制法是以钛铁矿(主要成分 ),为原料按下过程进行的,请完成下列化学方程式:
),为原料按下过程进行的,请完成下列化学方程式:①___FeTiO3+___C+___Cl2
 ___TiCl4+___FeCl3+___CO,
___TiCl4+___FeCl3+___CO,②___TiCl4+___O2
 ___TiO2+___Cl2,
___TiO2+___Cl2,
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】利用如图可以从不同角度研究含硫物质的性质及其转化关系。
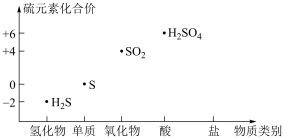
回答下列问题:
(1)H2S与SO2反应的化学方程式为____ ,反应中H2S体现____ (填“氧化性”或“还原性”)。
(2)加热时,浓硫酸与木炭反应的化学方程式为____ ,下列试剂不能用于验证生成物中含有SO2的是____ (填标号)。
a.品红溶液b.酸性KMnO4溶液c.澄清石灰水
(3)SO2的过度排放会引起酸雨,酸雨是指pH<____ 的雨水,其中NOx的排放也会导致酸雨的形成,写出NO2与水反应的化学方程式____ 。
(4)实验室可用碱液吸收法对NOx进行尾气处理,写出NO2与氢氧化钠溶液反应的离子方程式____ 。

回答下列问题:
(1)H2S与SO2反应的化学方程式为
(2)加热时,浓硫酸与木炭反应的化学方程式为
a.品红溶液b.酸性KMnO4溶液c.澄清石灰水
(3)SO2的过度排放会引起酸雨,酸雨是指pH<
(4)实验室可用碱液吸收法对NOx进行尾气处理,写出NO2与氢氧化钠溶液反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】烟气的“脱硫”“脱硝”是环境治理的热点问题,为消除燃煤烟气中的 及
及 ,研究专家提出了若干“脱硫”“脱硝”的方法。回答下列问题:
,研究专家提出了若干“脱硫”“脱硝”的方法。回答下列问题:
(1) 催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术,将烟气中
催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术,将烟气中 转化为无污染气体。当
转化为无污染气体。当 与NO的物质的量之比为1:1时,每转化1mol该氮氧化物混合气体,需要消耗
与NO的物质的量之比为1:1时,每转化1mol该氮氧化物混合气体,需要消耗 的体积(STP)为
的体积(STP)为_____________ L。
(2)利用氨水可以吸收 、
、 ,原理如图1所示:
,原理如图1所示:

①I中发生反应的化学方程式为____________________________________________________ 。
②减压蒸发是通过减小压强,使溶液沸点降低而进行蒸发的方法。该流程中采用减压蒸发的原因是____________ 。
(3)以NaClO溶液作为吸收剂进行一体化“脱硫”“脱硝”,控制溶液 ,将烟气中的
,将烟气中的 、NO转化为
、NO转化为 、
、 。一定时间内,温度对脱除率的影响曲线如图2所示。
。一定时间内,温度对脱除率的影响曲线如图2所示。
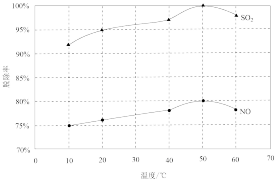
①脱除率 高于NO的可能原因是
高于NO的可能原因是_____________ (写出一种即可)。
②若烟气中 与NO的体积比为2:1,则50℃时,NaClO溶液吸收烟气后的溶液中
与NO的体积比为2:1,则50℃时,NaClO溶液吸收烟气后的溶液中 与
与 的物质的量之比
的物质的量之比
_____________ 。
 及
及 ,研究专家提出了若干“脱硫”“脱硝”的方法。回答下列问题:
,研究专家提出了若干“脱硫”“脱硝”的方法。回答下列问题:(1)
 催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术,将烟气中
催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术,将烟气中 转化为无污染气体。当
转化为无污染气体。当 与NO的物质的量之比为1:1时,每转化1mol该氮氧化物混合气体,需要消耗
与NO的物质的量之比为1:1时,每转化1mol该氮氧化物混合气体,需要消耗 的体积(STP)为
的体积(STP)为(2)利用氨水可以吸收
 、
、 ,原理如图1所示:
,原理如图1所示:
①I中发生反应的化学方程式为
②减压蒸发是通过减小压强,使溶液沸点降低而进行蒸发的方法。该流程中采用减压蒸发的原因是
(3)以NaClO溶液作为吸收剂进行一体化“脱硫”“脱硝”,控制溶液
 ,将烟气中的
,将烟气中的 、NO转化为
、NO转化为 、
、 。一定时间内,温度对脱除率的影响曲线如图2所示。
。一定时间内,温度对脱除率的影响曲线如图2所示。
①脱除率
 高于NO的可能原因是
高于NO的可能原因是②若烟气中
 与NO的体积比为2:1,则50℃时,NaClO溶液吸收烟气后的溶液中
与NO的体积比为2:1,则50℃时,NaClO溶液吸收烟气后的溶液中 与
与 的物质的量之比
的物质的量之比
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】 是一种重要的杀菌消毒剂,也常用来漂白织物等。回答下列问题:
是一种重要的杀菌消毒剂,也常用来漂白织物等。回答下列问题:
(1) 中Cl的化合价为
中Cl的化合价为_________________ 。
(2)可用 还原硫酸酸化的
还原硫酸酸化的 制备
制备 ,产物还有
,产物还有 ,该反应的化学方程式为
,该反应的化学方程式为______________________ 。
(3)有效氯含量可用来衡量含氯消毒剂的消毒能力,其定义是每克含氯消毒剂的氧化能力相当于多少克 的氧化能力。
的氧化能力。 的有效氯含量为
的有效氯含量为_______________ (计算结果保留两位小数)。
 是一种重要的杀菌消毒剂,也常用来漂白织物等。回答下列问题:
是一种重要的杀菌消毒剂,也常用来漂白织物等。回答下列问题:(1)
 中Cl的化合价为
中Cl的化合价为(2)可用
 还原硫酸酸化的
还原硫酸酸化的 制备
制备 ,产物还有
,产物还有 ,该反应的化学方程式为
,该反应的化学方程式为(3)有效氯含量可用来衡量含氯消毒剂的消毒能力,其定义是每克含氯消毒剂的氧化能力相当于多少克
 的氧化能力。
的氧化能力。 的有效氯含量为
的有效氯含量为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】Cl2是一种重要的化工原料,结合氯气的相关知识解决下列问题。
(1)工业上将氯气通入消石灰中制取漂白粉,写出该反应的化学方程式__________ 。
(2)漂白粉的有效成分是(填化学式)_________ 。
(3)氯水与二氧化硫均具有漂白性,若将两者按适当比例混合则漂白性很差,用离子方程式表示其原因____ 。
(4)实验室可以用KMnO4与浓盐酸在常温下制备Cl2。高锰酸钾溶液常用于物质的定性检验与定量分析。某化学兴趣小组在实验室里用0.1mol/LKMnO4溶液与300ml0.2mol/L的KI溶液恰好反应,生成等物质的量的I2和KIO3,则消耗KMnO4的体积为________ ml。(已知MnO4-在此条件下被还原为Mn2+)
(1)工业上将氯气通入消石灰中制取漂白粉,写出该反应的化学方程式
(2)漂白粉的有效成分是(填化学式)
(3)氯水与二氧化硫均具有漂白性,若将两者按适当比例混合则漂白性很差,用离子方程式表示其原因
(4)实验室可以用KMnO4与浓盐酸在常温下制备Cl2。高锰酸钾溶液常用于物质的定性检验与定量分析。某化学兴趣小组在实验室里用0.1mol/LKMnO4溶液与300ml0.2mol/L的KI溶液恰好反应,生成等物质的量的I2和KIO3,则消耗KMnO4的体积为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】解决汽车尾气污染,效果最好的办法是在汽车发动机和排气管之间装一个净化装置,该装置与抽烟用的过滤嘴非常相似,其外形是一个椭圆形的筒,筒内有许多规则的蜂窝状细孔,在孔壁上涂有用特殊工艺制备的催化剂,当汽车尾气经过这些小孔时,尾气中的 和
和 在催化剂作用下发生氧化还原反应,生成两种无害的物质,然后排到大气中。
在催化剂作用下发生氧化还原反应,生成两种无害的物质,然后排到大气中。
试回答下列问题:
(1)写出在催化剂作用下一氧化碳和一氧化氮反应的化学方程式:___________ 。
(2)请你判断该反应在无催化剂的作用下能否发生?___________ (填“能”或“否”)。
(3)催化剂对该反应的作用是___________ 。
 和
和 在催化剂作用下发生氧化还原反应,生成两种无害的物质,然后排到大气中。
在催化剂作用下发生氧化还原反应,生成两种无害的物质,然后排到大气中。试回答下列问题:
(1)写出在催化剂作用下一氧化碳和一氧化氮反应的化学方程式:
(2)请你判断该反应在无催化剂的作用下能否发生?
(3)催化剂对该反应的作用是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】氮的氧化物是主要的大气污染物,必须脱除才能排放。
(1)臭氧与空气中的氮氧化物,以及汽油、柴油等化石燃料的不完全燃烧所残留的_____ (填字母)在紫外线照射下容易产生光化学烟雾。
a.惰性气体 b.碳氢化合物 c.二氧化碳
(2)汽车排气管内的催化剂能将CO和NO2转化为无害气体,发生的反应方程式为_____ 。
(3)工业上在催化剂作用下用NH3还原废气中NOx生成N2和H2O达到脱除目的,但当温度高于400℃时,NOx脱除率下降,原因可能是_____ 。
(4)工业上氮的氧化物通常是用碱性溶液吸收。
①用Na2CO3溶液吸收硝酸工业尾气中的NO2,生成等物质的量的两种钠盐(一种为NaNO2)及一种气体,反应的离子方程式为_____ 。
②NaOH溶液浓度越大黏稠度越高,用不同浓度的NaOH溶液吸收NO2(混有NO)含量不同的工业尾气,氮氧化物的吸收率随NaOH溶液浓度的变化如题图所示,曲线II表示NO的物质的量______ (填:“大于”、“小于”、“等于”)NO2物质的量。当NaOH溶液浓度高于0.5mol·L-1后,氮氧化物的吸收率随NaOH溶液浓度的升高而降低的原因是_____ 。

(1)臭氧与空气中的氮氧化物,以及汽油、柴油等化石燃料的不完全燃烧所残留的
a.惰性气体 b.碳氢化合物 c.二氧化碳
(2)汽车排气管内的催化剂能将CO和NO2转化为无害气体,发生的反应方程式为
(3)工业上在催化剂作用下用NH3还原废气中NOx生成N2和H2O达到脱除目的,但当温度高于400℃时,NOx脱除率下降,原因可能是
(4)工业上氮的氧化物通常是用碱性溶液吸收。
①用Na2CO3溶液吸收硝酸工业尾气中的NO2,生成等物质的量的两种钠盐(一种为NaNO2)及一种气体,反应的离子方程式为
②NaOH溶液浓度越大黏稠度越高,用不同浓度的NaOH溶液吸收NO2(混有NO)含量不同的工业尾气,氮氧化物的吸收率随NaOH溶液浓度的变化如题图所示,曲线II表示NO的物质的量

您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】I.自然界中氮循环如图所示。

(1)固氮是将游离态氮转化为化合态氮的过程,过程①是_______ 固氮,反应过程中_______ 能转化成_______ 能。过程②是人工固氮,人工固氮的意义有_______ 。过程③中氮元素由_______ 态转化为_______ 态。
(2)在细菌的作用下铵态氮( )与亚硝态氮(
)与亚硝态氮( )可以转化为氮气,所涉及的离子方程式为:
)可以转化为氮气,所涉及的离子方程式为: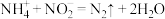 ,反应中,每生成
,反应中,每生成 氮气时,转移电子的物质的量为
氮气时,转移电子的物质的量为_______ 。
(3)实验室检验铵盐中的 时,可取少量铵盐样品于试管中,加入强碱浓溶液,加热,若产生的气体能使
时,可取少量铵盐样品于试管中,加入强碱浓溶液,加热,若产生的气体能使_______ ,说明有 。
。
Ⅱ.工业制硝酸时尾气中含有的NO、NO2可用溶液吸收。发生的反应有:
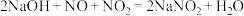

用不同浓度溶液吸收NO2含量不同的尾气(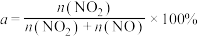 ),氮氧化物吸收率与浓度间的关系如图所示:
),氮氧化物吸收率与浓度间的关系如图所示:

(4)随 溶液浓度的增大,氮氧化物吸收率的变化情况是
溶液浓度的增大,氮氧化物吸收率的变化情况是_______ 。
(5)当 小于50%时,加入H2O2能提升氮氧化物的吸收率,原因是
小于50%时,加入H2O2能提升氮氧化物的吸收率,原因是_______ 。
(6)某小组同学建议用废氨水对含NO、NO2的废气进行吸收,请简述用废氨水吸收NOx的优点_______ 。

(1)固氮是将游离态氮转化为化合态氮的过程,过程①是
(2)在细菌的作用下铵态氮(
 )与亚硝态氮(
)与亚硝态氮( )可以转化为氮气,所涉及的离子方程式为:
)可以转化为氮气,所涉及的离子方程式为: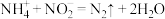 ,反应中,每生成
,反应中,每生成 氮气时,转移电子的物质的量为
氮气时,转移电子的物质的量为(3)实验室检验铵盐中的
 时,可取少量铵盐样品于试管中,加入强碱浓溶液,加热,若产生的气体能使
时,可取少量铵盐样品于试管中,加入强碱浓溶液,加热,若产生的气体能使 。
。Ⅱ.工业制硝酸时尾气中含有的NO、NO2可用溶液吸收。发生的反应有:
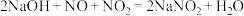

用不同浓度溶液吸收NO2含量不同的尾气(
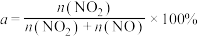 ),氮氧化物吸收率与浓度间的关系如图所示:
),氮氧化物吸收率与浓度间的关系如图所示:
(4)随
 溶液浓度的增大,氮氧化物吸收率的变化情况是
溶液浓度的增大,氮氧化物吸收率的变化情况是(5)当
 小于50%时,加入H2O2能提升氮氧化物的吸收率,原因是
小于50%时,加入H2O2能提升氮氧化物的吸收率,原因是(6)某小组同学建议用废氨水对含NO、NO2的废气进行吸收,请简述用废氨水吸收NOx的优点
您最近一年使用:0次



