用TiOSO4溶液生产纳米TiO2的工艺流程如下:
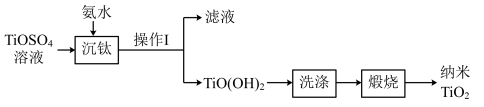
下列说法错误的是

下列说法错误的是
| A.在实验室中进行“操作I”,需要的玻璃仪器有烧杯、玻璃棒、漏斗 |
B.“沉钛”时反应的离子方程式为:TiO2++2NH3·H2O=TiO(OH)2↓+2NH |
| C.回收“滤液”中的(NH4)2SO4,应采用蒸发结晶法 |
| D.纳米TiO2形成分散系时,具有较好的散射能力 |
2021·山东日照·三模 查看更多[7]
山东省日照市2021届高三下学期第三次模拟考试化学试题福建省厦门外国语学校2021届高三5月高考适应性考试化学试题(已下线)2021年秋季高三开学摸底考化学试卷02(江苏专用)陕西省西安市铁一中学2022届高三第二次月考化学试题广东省深圳外国语学校2022届高三上学期第一次月考化学试题(已下线)备战2022年高考化学精准检测卷【全国卷】14湖南省汨罗市第二中学2021-2022学年高三下学期4月月考化学试题
更新时间:2021-05-14 17:54:50
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】下列离子方程式书写正确的是
A.将稀盐酸滴在石灰石上: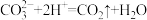 |
B.稀盐酸与铁粉反应: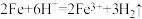 |
C.氢氧化钡溶液与稀硫酸反应: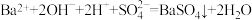 |
D.用盐酸除铁锈: |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列离子方程式正确的是
A.用KIO3氧化酸性溶液中的KI: 5I-+ IO +3H2O = 3I2 + 6OH- +3H2O = 3I2 + 6OH- |
B.用稀硝酸洗涤试管内壁的银镜: Ag +2H++ NO = Ag++ NO↑+ H2O = Ag++ NO↑+ H2O |
C.NaHS溶液水解:HS-+H2O H3O++S2- H3O++S2- |
D.将 溶液加入到石灰乳中得到氢氧化镁: 溶液加入到石灰乳中得到氢氧化镁: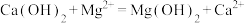 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列是部分矿物资源铝土矿(主要含有氧化铝、氧化铁)和黄铜矿(主要成分CuFeS2)的利用及产品生产流程,有关说法不正确的是
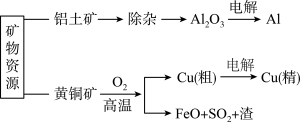

| A.除杂过程中铝元素的存在形式的变化可以如下:Al2O3→AlO2-→Al(OH)3→Al2O3 |
| B.Al和Cu(精)均在电解槽的阴极获得 |
C.粗铜炼制过程中反应2CuFeS2+O2 Cu2S+2FeS+SO2,每转移1.2mol电子,则有0.2mol硫被氧化 Cu2S+2FeS+SO2,每转移1.2mol电子,则有0.2mol硫被氧化 |
| D.若电解法分别制铝和铜的过程中转移电子数相等,理论上获得的铝和铜的物质的量之比为3:2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】除去下列物质中的杂质(括号内为杂质),所选用的试剂及操作方法均正确的一组是
| 选项 | 待提纯的物质 | 选用的试剂 | 操作的方法 |
| A | KNO3(NaCl) | 水 | 溶解、过滤、蒸发结晶 |
| B | Cu(CuO) | 稀盐酸 | 溶解、过滤、洗涤、干燥 |
| C | FeSO4溶液 (CuSO4) | 氢氧化钠溶液 | 过滤 |
| D | CO2(H2) | 氧气 | 点燃 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】碘(紫黑色固体,微溶于水)及其化合物广泛用于医药、染料等方面。 的一种制备方法如图所示。
的一种制备方法如图所示。
下列说法正确的是
 的一种制备方法如图所示。
的一种制备方法如图所示。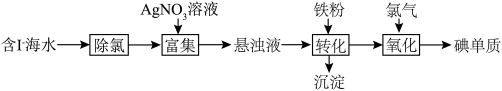

下列说法正确的是
| A.“富集”过程中发生氧化还原反应 | B.“悬浊液”静置后得到白色沉淀 |
| C.“沉淀”的组成主要是银和铁 | D.“氧化”过程通入足量 提高碘单质产量 提高碘单质产量 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】K2FeO4具有强氧化性,酸性条件下,其氧化性强于Cl2、KMnO4,其制备的流程如下: 生成。下列说法正确的是
生成。下列说法正确的是

 生成。下列说法正确的是
生成。下列说法正确的是| A.K2FeO4中铁元素的化合价是+8 |
B.“转化1”发生反应的离子方程式为:2Fe3++3ClO-+5H2O=2 +3Cl-+10H+ +3Cl-+10H+ |
| C.“转化2” 能进行的原因是该条件下K2FeO4的溶解度比Na2FeO4小 |
D.所得滤液含有大量的Na+、H+、 、Cl- 、Cl- |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】铁、镍及其化合物有广泛的用途。某矿渣的主要成分为NiFe2O4(铁酸镍)、NiO、FeO、CaO、SiO2等,以下是从该矿渣中回收NiSO4的工艺流程:
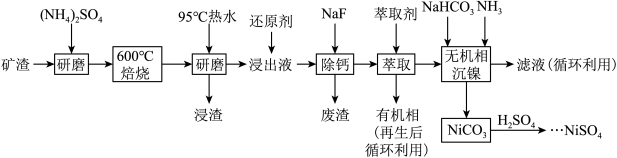
已知:①(NH4)2SO4在350℃以上会分解生成NH3和H2SO4;NiFe2O4在焙烧过程中生成NiSO4、Fe2(SO4)3;
②Ksp(CaF2)=4.0×10-11。
则下列说法错误的是

已知:①(NH4)2SO4在350℃以上会分解生成NH3和H2SO4;NiFe2O4在焙烧过程中生成NiSO4、Fe2(SO4)3;
②Ksp(CaF2)=4.0×10-11。
则下列说法错误的是
| A.(NH4)2SO4的作用是将金属元素转化为可溶性硫酸盐,便于浸出 |
| B.“浸渣”的成分为Fe(OH)3和SiO2 |
C.沉镍过程中的离子方程式:Ni2++HCO +NH3=NiCO3↓+NH +NH3=NiCO3↓+NH |
| D.“浸出液”中c(Ca2+)=1.0×10-3mol•L-1,当除钙率达到99%时,溶液中c(F-)=2.0×10-3mol•L-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】实验室模拟“侯氏制碱法”制取 ,反应原理为
,反应原理为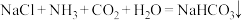
 (
( 极易溶于水)。下列说法正确的是
极易溶于水)。下列说法正确的是
 ,反应原理为
,反应原理为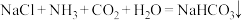
 (
( 极易溶于水)。下列说法正确的是
极易溶于水)。下列说法正确的是
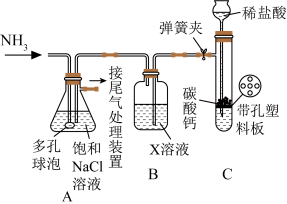
| A.装置A中使用“多孔球泡”的作用是防止倒吸 |
B.装置B中X溶液为饱和 溶液,主要作用是吸收混合气中的HCl 溶液,主要作用是吸收混合气中的HCl |
C.装置C中发生反应的离子方程式为 |
D.利用锥形瓶中所得物质制备 固体,还需经历过滤、洗涤、干燥及焙烧等过程 固体,还需经历过滤、洗涤、干燥及焙烧等过程 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
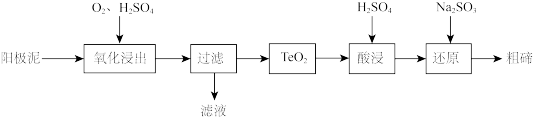
【推荐2】从粗铜精炼的阳极泥(主要含有 )中提取粗碲的一种工艺流程如图:(已知
)中提取粗碲的一种工艺流程如图:(已知 微溶于水,易溶于强酸和强碱)下列有关说法正确的是( )
微溶于水,易溶于强酸和强碱)下列有关说法正确的是( )
 )中提取粗碲的一种工艺流程如图:(已知
)中提取粗碲的一种工艺流程如图:(已知 微溶于水,易溶于强酸和强碱)下列有关说法正确的是( )
微溶于水,易溶于强酸和强碱)下列有关说法正确的是( )
| A.“氧化浸出”时为使碲元素沉淀充分,应加入过量的硫酸 |
| B.“过滤”用到的玻璃仪器:分液漏斗、烧杯、玻璃棒 |
C.“还原”时发生的离子方程式为 |
D.判断粗碲洗净的方法:取最后一次洗涤液,加入 溶液,没有白色沉淀生成 溶液,没有白色沉淀生成 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】氢化钙(CaH2)固体是一种储氢材料,遇水反应生成氢氧化钙和氢气,是登山运动员常用的能源提供剂。某化学兴趣小组设计制取氢化钙的装置如下(固定装置已略去)。下列说法不正确的是
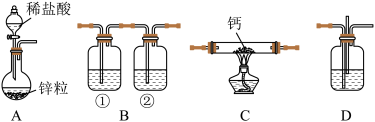

| A.装置A:制取H2,离子方程式为Zn+2H+=Zn2++H2↑ |
| B.装置B:用于除去H2中杂质,①中盛有NaOH溶液,②中盛有浓硫酸 |
| C.装置C:制取CaH2,先点燃C处酒精灯,后打开A中分液漏斗的活塞 |
| D.装置D:竖直导管的作用是平衡压强,观察H2流速以调节反应的进行 |
您最近一年使用:0次


 等离子。下列说法正确的是
等离子。下列说法正确的是

