氮氧化物和硫氧化物污染已成为一个世界性的环境问题,但只要合理利用也是重要的资源,NH3还原法可将NO还原为N2进行脱除。
已知:①4NH3(g)+3O2(g)=2N2(g)+6H2O(g) ΔH1=−1530kJ·mol−1
②N2(g)+O2(g)=2NO(g) ΔH2=+180kJ·mol−1
写出NH3还原NO的热化学方程式:_______ 。
已知:①4NH3(g)+3O2(g)=2N2(g)+6H2O(g) ΔH1=−1530kJ·mol−1
②N2(g)+O2(g)=2NO(g) ΔH2=+180kJ·mol−1
写出NH3还原NO的热化学方程式:
2021高三·全国·专题练习 查看更多[1]
(已下线)难点1 反应热的相关计算-2021年高考化学专练【热点·重点·难点】
更新时间:2021-05-17 19:53:07
|
相似题推荐
计算题
|
较易
(0.85)
解题方法
【推荐1】为了合理利用化学能,确保安全生产,化工设计需要充分考虑化学反应的焓变,并采取相应措施。化学反应的焓变通常用实验进行测定,也可进行理论推算。
(1)实验测得 甲醇在氧气中充分燃烧生成二氧化碳气体和液态水时释放出
甲醇在氧气中充分燃烧生成二氧化碳气体和液态水时释放出 的热量,试写出甲醇燃烧的热化学方程式:
的热量,试写出甲醇燃烧的热化学方程式:__________ 。
(2)由气态基态原子形成 化学键释放的最低能量叫键能。从化学键的角度分析,化学反应的过程就是反应物的化学键被破坏和生成物的化学键的形成过程。在化学反应过程中,拆开化学键需要消耗能量,形成化学键又会释放能量。
化学键释放的最低能量叫键能。从化学键的角度分析,化学反应的过程就是反应物的化学键被破坏和生成物的化学键的形成过程。在化学反应过程中,拆开化学键需要消耗能量,形成化学键又会释放能量。
已知反应: 。试根据表中所列键能数据估算
。试根据表中所列键能数据估算 的值为
的值为__________ 。
(3)依据盖斯定律可以对某些难以通过实验直接测定的化学反应的焓变进行推算。已知:25℃、 时:
时:
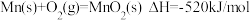


 与
与 反应生成无水
反应生成无水 的热化方程式是:
的热化方程式是:___________ 。
(1)实验测得
 甲醇在氧气中充分燃烧生成二氧化碳气体和液态水时释放出
甲醇在氧气中充分燃烧生成二氧化碳气体和液态水时释放出 的热量,试写出甲醇燃烧的热化学方程式:
的热量,试写出甲醇燃烧的热化学方程式:(2)由气态基态原子形成
 化学键释放的最低能量叫键能。从化学键的角度分析,化学反应的过程就是反应物的化学键被破坏和生成物的化学键的形成过程。在化学反应过程中,拆开化学键需要消耗能量,形成化学键又会释放能量。
化学键释放的最低能量叫键能。从化学键的角度分析,化学反应的过程就是反应物的化学键被破坏和生成物的化学键的形成过程。在化学反应过程中,拆开化学键需要消耗能量,形成化学键又会释放能量。| 化学键 | H-H | N-H | N≡N |
| 键能/(kJ·mol-1) | 436 | 391 | 945 |
已知反应:
 。试根据表中所列键能数据估算
。试根据表中所列键能数据估算 的值为
的值为(3)依据盖斯定律可以对某些难以通过实验直接测定的化学反应的焓变进行推算。已知:25℃、
 时:
时: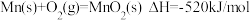


 与
与 反应生成无水
反应生成无水 的热化方程式是:
的热化方程式是:
您最近一年使用:0次
【推荐2】氮及其化合物是科学家们一直在探究的问题,它们在工农业生产和生命活动中起着重要的作用。回答下列问题。已知H—H键的键能为a kJ·mol-1,N—H键的键能为b kJ·mol-1,N≡N键的键能是c kJ·mol-1,则反应NH3(g)⇌ N2(g)+
N2(g)+  H2(g)的ΔH=
H2(g)的ΔH=_______ kJ·mol-1,若在某温度下其平衡常数为K,则N2(g)+3H2(g)⇌2NH3(g)的平衡常数K1=_______ (用K表示)。
 N2(g)+
N2(g)+  H2(g)的ΔH=
H2(g)的ΔH=
您最近一年使用:0次
【推荐3】第十三届全国人大第一次会议的政府工作报告中,对大气污染物的治理提出了更高要求。治理NO2污染的一种方法是将其转化成N2。
已知:①2H2(g)+O2(g)=2H2O(g) ΔH=-483.6kJ/mol
②N2(g)+2O2(g)=2NO2(g) ΔH=+133.0kJ/mol
(1)反应①属于___ (填“吸热”或“放热”)反应。
(2)反应①消耗1molO2(g)时,热量变化是____ kJ。
(3)反应②的热量变化为133.0kJ时,需消耗N2(g)的质量是___ g。
(4)治理NO2的反应:4H2(g)+2NO2(g)=N2(g)+4H2O(g) ΔH=______ kJ/mol。
已知:①2H2(g)+O2(g)=2H2O(g) ΔH=-483.6kJ/mol
②N2(g)+2O2(g)=2NO2(g) ΔH=+133.0kJ/mol
(1)反应①属于
(2)反应①消耗1molO2(g)时,热量变化是
(3)反应②的热量变化为133.0kJ时,需消耗N2(g)的质量是
(4)治理NO2的反应:4H2(g)+2NO2(g)=N2(g)+4H2O(g) ΔH=
您最近一年使用:0次
【推荐1】回答下列问题:
(1)已知:①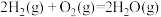 ∆H1=-483.6kJ/mol
∆H1=-483.6kJ/mol
②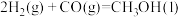 ∆H2=-128.3kJ/mol
∆H2=-128.3kJ/mol
③ ∆H3=+206.1kJ/mol
∆H3=+206.1kJ/mol
属于吸热反应的是__________ (填序号)。
写出由甲烷和氧气合成液态甲醇的热化学方程式:_____________ 。
(2)通过化学键的键能计算。已知:
则合成氨反应N2(g)+3H2(g) 2NH3(g) △H=a kJ/mol,a为
2NH3(g) △H=a kJ/mol,a为______ 。
(3)已知:1 mol H2O(g)转化为1 mol H2O(l)时放出44.0 kJ的热量。写出H2O(g)转化为1 mol H2O(l)热化学方程式:_______________ 。H2O(l)的稳定性_________ 填(“大于”“小于”)H2O(g)
(1)已知:①
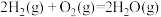 ∆H1=-483.6kJ/mol
∆H1=-483.6kJ/mol ②
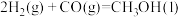 ∆H2=-128.3kJ/mol
∆H2=-128.3kJ/mol ③
 ∆H3=+206.1kJ/mol
∆H3=+206.1kJ/mol 属于吸热反应的是
写出由甲烷和氧气合成液态甲醇的热化学方程式:
(2)通过化学键的键能计算。已知:
化学键 | H—H | N—H | N≡N |
键能(kJ/mol ) | 436 | 391 | 945 |
 2NH3(g) △H=a kJ/mol,a为
2NH3(g) △H=a kJ/mol,a为(3)已知:1 mol H2O(g)转化为1 mol H2O(l)时放出44.0 kJ的热量。写出H2O(g)转化为1 mol H2O(l)热化学方程式:
您最近一年使用:0次
计算题
|
较易
(0.85)
【推荐2】已知一氧化碳与水蒸气的反应为
CO(g)+H2O(g) CO2(g)+H2(g)
CO2(g)+H2(g)
在密闭容器中,将1.0mol CO与3.6mol H2O混合加热到434℃,在434℃的平衡常数K1=9,
我们跟踪测定H2O的物质的量浓度,
如图所示:
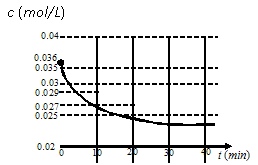
则0~20min的反应速率是 从434℃升温至800℃,800℃的平衡常数K2=1,则正反应为_____________(填“放热反应”或“吸热反应”或“不能确定”)。
求800℃平衡时CO转化为CO2的转化率(写出必要的计算过程)。
CO(g)+H2O(g)
 CO2(g)+H2(g)
CO2(g)+H2(g)在密闭容器中,将1.0mol CO与3.6mol H2O混合加热到434℃,在434℃的平衡常数K1=9,
我们跟踪测定H2O的物质的量浓度,
如图所示:

则0~20min的反应速率是 从434℃升温至800℃,800℃的平衡常数K2=1,则正反应为_____________(填“放热反应”或“吸热反应”或“不能确定”)。
求800℃平衡时CO转化为CO2的转化率(写出必要的计算过程)。
您最近一年使用:0次
计算题
|
较易
(0.85)
解题方法
【推荐1】采用科学技术减少氮氧化物等物质的排放可促进社会主义生态文明建设。
用CH4催化还原氮氧化物的相关热化学方程式如下:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(1)∆H=-662kJ•mol-1
②CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(l)∆H=-1248kJ•mol-1
反应CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(l)∆H=_____ kJ•mol-1
用CH4催化还原氮氧化物的相关热化学方程式如下:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(1)∆H=-662kJ•mol-1
②CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(l)∆H=-1248kJ•mol-1
反应CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(l)∆H=
您最近一年使用:0次
计算题
|
较易
(0.85)
解题方法
【推荐2】按要求写出下列反应的热化学方程式。
(1)以CO2和NH3为原料可合成尿素[CO(NH2)2]。已知:
①2NH3(g)+CO2(g) =NH2COONH4(s) ΔH1=-159.47 kJ·mol-1
②NH2COONH4(s) =CO(NH2)2(s)+H2O(g) ΔH2=+116.49 kJ·mol-1
③H2O(l)=H2O(g) ΔH3=+44.0 kJ·mol-1
则NH3和CO2合成尿素和液态水的热化学方程式为________ 。
(2)已知25 ℃、101 kPa时:
①2SO2(g) +O2(g) 2SO3(g) ΔH1=-197 kJ·mol-1
2SO3(g) ΔH1=-197 kJ·mol-1
②H2O(g) =H2O(l) ΔH2=-44 kJ·mol-1
③2SO2(g) +O2(g) +2H2O(g) =2H2SO4(l) ΔH3=-545 kJ·mol-1
则SO3(g)与H2O(l)反应的热化学方程式为_____ 。
(3)工业上利用甲烷催化还原NOx可减少氮氧化物的排放。已知:
①CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) ΔH1=-574 kJ·mol-1
②CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) ΔH2=-1160 kJ·mol-1
甲烷直接将NO2还原为N2的热化学方程式为__________ 。
(4)通常人们把拆开1 mol某化学键所吸收的能量看成该化学键的键能。键能的大小可以衡量化学键的强弱,也可用于估算化学反应的反应热(ΔH),化学反应的ΔH等于反应中断裂旧化学键的键能之和与反应中形成新化学键的键能之和的差。已知:
工业上通过氢气在氯气中充分燃烧制取HCl气体,该反应的热化学方程式为_____ 。
(1)以CO2和NH3为原料可合成尿素[CO(NH2)2]。已知:
①2NH3(g)+CO2(g) =NH2COONH4(s) ΔH1=-159.47 kJ·mol-1
②NH2COONH4(s) =CO(NH2)2(s)+H2O(g) ΔH2=+116.49 kJ·mol-1
③H2O(l)=H2O(g) ΔH3=+44.0 kJ·mol-1
则NH3和CO2合成尿素和液态水的热化学方程式为
(2)已知25 ℃、101 kPa时:
①2SO2(g) +O2(g)
 2SO3(g) ΔH1=-197 kJ·mol-1
2SO3(g) ΔH1=-197 kJ·mol-1②H2O(g) =H2O(l) ΔH2=-44 kJ·mol-1
③2SO2(g) +O2(g) +2H2O(g) =2H2SO4(l) ΔH3=-545 kJ·mol-1
则SO3(g)与H2O(l)反应的热化学方程式为
(3)工业上利用甲烷催化还原NOx可减少氮氧化物的排放。已知:
①CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) ΔH1=-574 kJ·mol-1
②CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) ΔH2=-1160 kJ·mol-1
甲烷直接将NO2还原为N2的热化学方程式为
(4)通常人们把拆开1 mol某化学键所吸收的能量看成该化学键的键能。键能的大小可以衡量化学键的强弱,也可用于估算化学反应的反应热(ΔH),化学反应的ΔH等于反应中断裂旧化学键的键能之和与反应中形成新化学键的键能之和的差。已知:
| 化学键 | H—H | H—Cl | Cl—Cl |
| 键能/(kJ·mol-1) | 436 | 431 | 242 |
工业上通过氢气在氯气中充分燃烧制取HCl气体,该反应的热化学方程式为
您最近一年使用:0次
计算题
|
较易
(0.85)
解题方法
【推荐3】下图是2SO2(g) + O2(g) = 2SO3(g)反应过程中的能量变化, 已知1mol SO2(g)完全氧化为1mol SO3的ΔH= —99kJ·mol-1,请回答下列问题:

(1)图中A、C分别表的物质是__________________ 、________________ ,E的大小对该反应的焓变有无影响?___________ (填“有”或“无”)(该反应通常用V2O5作催化剂,加V2O5会使图中B点降低。);
(2)图中△H =_____________ kJ·mol-1;
(3)已知:S(s) + O2(g) = SO2(g) ΔH=-296 kJ·mol-1,计算由3 mol S(s)与氧气反应生成3 molSO3(g)的△H =______________ 。

(1)图中A、C分别表的物质是
(2)图中△H =
(3)已知:S(s) + O2(g) = SO2(g) ΔH=-296 kJ·mol-1,计算由3 mol S(s)与氧气反应生成3 molSO3(g)的△H =
您最近一年使用:0次



 的
的
 。
。 催化重整反应为
催化重整反应为 。
。


 在催化剂作用下发生反应:
在催化剂作用下发生反应:

 的
的 为
为 的相关热化学方程式如下:
的相关热化学方程式如下:

 的
的

