某工厂的废水中含有大量的FeSO4和较多的Cu2+。为了减少污染并变废为宝,工厂计划从该废水中回收FeSO4和金属Cu。请根据以下流程图,回答下列问题。
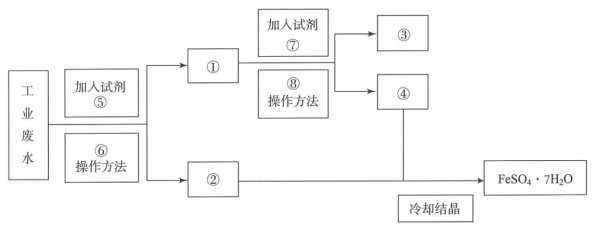
(1)填写下列标号所代表的物质(主要成分化学物质的化学式):①_______ ②_______ ③_______ ④_______ ⑤_______ ⑦_______
(2)写出加入试剂⑤与工业废水反应的离子方程式:_______

(1)填写下列标号所代表的物质(主要成分化学物质的化学式):①
(2)写出加入试剂⑤与工业废水反应的离子方程式:
更新时间:2021-05-10 16:46:15
|
相似题推荐
解答题-无机推断题
|
容易
(0.94)
解题方法
【推荐1】某溶液中可能含有下列离子:Na+、 、
、 、Cl-,分别进行如下实验,请根据要求填空:
、Cl-,分别进行如下实验,请根据要求填空:
(1)取少量溶液于试管中,加入过量氢氧化钡溶液,无沉淀生成,一定不存在的离子是_______ 。
(2)另取少量原溶液于试管中,加入稀硝酸和硝酸银溶液,有白色沉淀生成,则说明一定存在的离子是_______ 。
(3)通过上述实验,还无法确定的离子是___ ,要想鉴别这种离子,可以选用的方法是____ 。
 、
、 、Cl-,分别进行如下实验,请根据要求填空:
、Cl-,分别进行如下实验,请根据要求填空:(1)取少量溶液于试管中,加入过量氢氧化钡溶液,无沉淀生成,一定不存在的离子是
(2)另取少量原溶液于试管中,加入稀硝酸和硝酸银溶液,有白色沉淀生成,则说明一定存在的离子是
(3)通过上述实验,还无法确定的离子是
您最近一年使用:0次
解答题-实验探究题
|
容易
(0.94)
名校
解题方法
【推荐2】某废水中可能含有下列离子中的若干种: 、
、 、
、 、
、 、
、 、
、 、
、 、
、 、
、 。现进行如下实验:
。现进行如下实验:
①取少量溶液,加入KSCN溶液,无明显变化。
②另取溶液加入少量盐酸,有无色气体生成,该无色气体遇空气变成红棕色。
③向②中所得溶液中加入 溶液,有白色沉淀生成。
溶液,有白色沉淀生成。
④另取②中所得溶液加入过量浓氨水,仅有红褐色沉淀生成,过滤,在所得溶液中加入盐酸至酸性时,再加入氢氧化钠溶液,有蓝色沉淀生成。
请回答下列问题:
(1)该废水一定含有的离子是_______ ;
(2)实验②中加入盐酸生成无色气体的离子方程式是_______ ;
(3)过滤除去④中的蓝色沉淀,调整溶液的pH为10.7左右时,加入铝粉,反应产生氨气和氮气的体积比为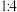 ,其离子方程式为
,其离子方程式为 (未配平)。若除去
(未配平)。若除去 ,消耗铝
,消耗铝_______ g。
 、
、 、
、 、
、 、
、 、
、 、
、 、
、 、
、 。现进行如下实验:
。现进行如下实验:①取少量溶液,加入KSCN溶液,无明显变化。
②另取溶液加入少量盐酸,有无色气体生成,该无色气体遇空气变成红棕色。
③向②中所得溶液中加入
 溶液,有白色沉淀生成。
溶液,有白色沉淀生成。④另取②中所得溶液加入过量浓氨水,仅有红褐色沉淀生成,过滤,在所得溶液中加入盐酸至酸性时,再加入氢氧化钠溶液,有蓝色沉淀生成。
请回答下列问题:
(1)该废水一定含有的离子是
(2)实验②中加入盐酸生成无色气体的离子方程式是
(3)过滤除去④中的蓝色沉淀,调整溶液的pH为10.7左右时,加入铝粉,反应产生氨气和氮气的体积比为
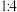 ,其离子方程式为
,其离子方程式为 (未配平)。若除去
(未配平)。若除去 ,消耗铝
,消耗铝
您最近一年使用:0次
解答题-无机推断题
|
容易
(0.94)
名校
解题方法
【推荐3】某溶液中只含有Ba2+ Mg2+ Ag+三种阳离子,现用适量的NaOH溶液、稀盐酸和Na2SO4溶液将这三种离子逐一沉淀分离,其流程如图所示:
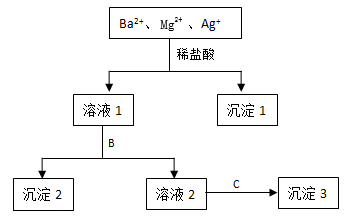
(1)沉淀1的化学式为_________ ,生成该沉淀的离子方程式为______________ 。
(2)若试剂B为Na2SO4溶液,则沉淀2化学式为______________ 。
(3)若试剂B为NaOH溶液,则生成沉淀2的离子方程式为______________ 。
(4)如果原溶液中Ba2+ Mg2+ Ag+的浓度均为0.1 mol·L-1,且溶液中含有的阴离子只有NO3-,则溶液中NO3- 浓度为_______ mol·L-1。

(1)沉淀1的化学式为
(2)若试剂B为Na2SO4溶液,则沉淀2化学式为
(3)若试剂B为NaOH溶液,则生成沉淀2的离子方程式为
(4)如果原溶液中Ba2+ Mg2+ Ag+的浓度均为0.1 mol·L-1,且溶液中含有的阴离子只有NO3-,则溶液中NO3- 浓度为
您最近一年使用:0次
解答题-工业流程题
|
容易
(0.94)
解题方法
【推荐1】一种用铝土矿和硫铁矿烧渣(配料中含Al2O3、Fe2O3、FeO及SiO2等)为原料制备无机高分子絮凝剂聚合碱式氯化铝铁的流程如下:
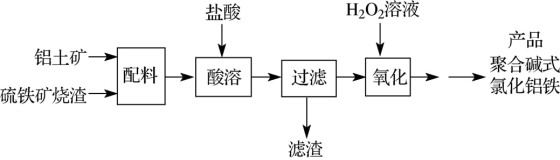
(1)“酸溶”时Fe2O3被溶解的化学方程式为_________ 。
(2)过滤操作所需的玻璃仪器除了烧杯、玻璃棒,还有_________ 。
(3)滤渣的成分为_________ (填化学式)。
(4)“氧化”反应的离子方程式为_________ 。

(1)“酸溶”时Fe2O3被溶解的化学方程式为
(2)过滤操作所需的玻璃仪器除了烧杯、玻璃棒,还有
(3)滤渣的成分为
(4)“氧化”反应的离子方程式为
您最近一年使用:0次
解答题-工业流程题
|
容易
(0.94)
名校
解题方法
【推荐2】铁红可用于油漆、油墨、橡胶等工业中,可作为玻璃、宝石、金属的抛光剂等。某课外活动小组用废铁渣(含Fe和少量Fe2O3)制取铁红,所设计的流程如下:
(1)苏打中的化学键类型为___________ ;沉淀的化学式为___________ ;“滤液”中主要溶质的化学式为___________ 。
(2)要检测“酸溶”后,溶液中是否含有Fe3+所用的试剂是___________ (名称);若溶液中检测不到Fe3+的原因是___________ 。
(3)“酸溶”时,Fe2O3与稀硫酸反应的离子方程式为___________ 。
(4)实验室过滤所需的玻璃仪器(填名称)有___________ 。
(5)煅烧的化学方程式为___________ 。
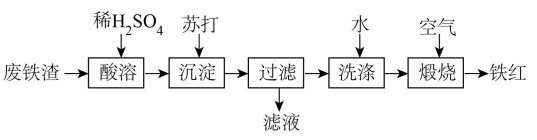
(1)苏打中的化学键类型为
(2)要检测“酸溶”后,溶液中是否含有Fe3+所用的试剂是
(3)“酸溶”时,Fe2O3与稀硫酸反应的离子方程式为
(4)实验室过滤所需的玻璃仪器(填名称)有
(5)煅烧的化学方程式为
您最近一年使用:0次
解答题-工业流程题
|
容易
(0.94)
解题方法
【推荐1】某化学兴趣小组模拟侯氏制碱法制备NaHCO3,进一步处理得到Na2CO3和NH4Cl,实验流程如图:

向母液中加入NaCl粉末,存在NaCl(s)+NH4Cl(aq)→NaCl(aq)+NH4Cl(s)过程。为使NH4Cl沉淀充分析出并分离,根据NaCl和NH4Cl溶解度曲线,需采用的操作为___________ 、___________ 、___________ 、洗涤、干燥。


向母液中加入NaCl粉末,存在NaCl(s)+NH4Cl(aq)→NaCl(aq)+NH4Cl(s)过程。为使NH4Cl沉淀充分析出并分离,根据NaCl和NH4Cl溶解度曲线,需采用的操作为

您最近一年使用:0次
解答题-实验探究题
|
容易
(0.94)
解题方法
【推荐2】某化学研究性学习小组为了解从工业溴中提纯溴的方法,查阅了有关资料,Br2的沸点为59℃。微溶于水,有毒性和强腐蚀性和强挥发性。他们参观生产过程后,绘制了如图装置简图。
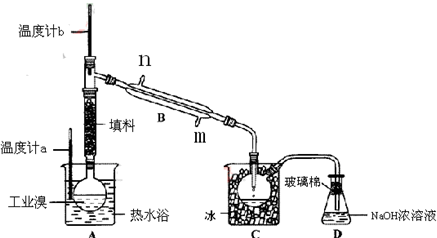
请你参与分析讨论:
(1)图中仪器B的名称:_____ ,冷却水从_____ 进,_____ 出。
(2)烧杯A的作用_____________ ,C中冰的作用是_____ 。

请你参与分析讨论:
(1)图中仪器B的名称:
(2)烧杯A的作用
您最近一年使用:0次
解答题-工业流程题
|
容易
(0.94)
解题方法
【推荐1】一种用铝土矿和硫铁矿烧渣(配料中含Al2O3、Fe2O3、FeO及SiO2等)为原料制备无机高分子絮凝剂聚合碱式氯化铝铁的流程如下:

(1)“酸溶”时Fe2O3被溶解的化学方程式为_________ 。
(2)过滤操作所需的玻璃仪器除了烧杯、玻璃棒,还有_________ 。
(3)滤渣的成分为_________ (填化学式)。
(4)“氧化”反应的离子方程式为_________ 。

(1)“酸溶”时Fe2O3被溶解的化学方程式为
(2)过滤操作所需的玻璃仪器除了烧杯、玻璃棒,还有
(3)滤渣的成分为
(4)“氧化”反应的离子方程式为
您最近一年使用:0次
解答题-实验探究题
|
容易
(0.94)
【推荐2】实验室模拟工业从海藻中提取碘的流程如图:
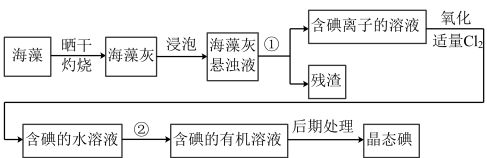
(1)选择合适实验操作名称填入流程图中:①_____ ,②_____ 。
A.溶解 B.过滤 C.萃取 D.分液
从“含碘的有机溶液”中回收溶剂,并得到碘单质,可选用如图装置完成。
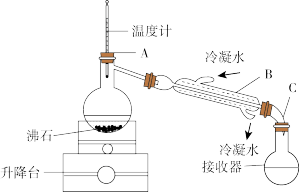
(2)装置中间部分是“冷凝管”,该装置中有一处明显的错误是_____ 。
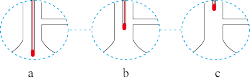
(3)装置A中,温度计所处的正确位置是_____ 。(选填编号)

(1)选择合适实验操作名称填入流程图中:①
A.溶解 B.过滤 C.萃取 D.分液
从“含碘的有机溶液”中回收溶剂,并得到碘单质,可选用如图装置完成。

(2)装置中间部分是“冷凝管”,该装置中有一处明显的错误是
(3)装置A中,温度计所处的正确位置是

您最近一年使用:0次

 产生废液X进行回收处理,流程如图所示。
产生废液X进行回收处理,流程如图所示。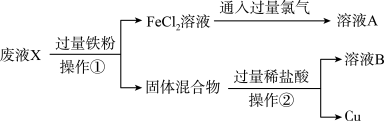
 反应外,还可能发生
反应外,还可能发生
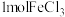 与Cu完全反应,转移电子数约为
与Cu完全反应,转移电子数约为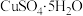 )是一种重要化工原料,某研究小组以生锈的铜屑为原料[主要成分是Cu,含有少量的油污、CuO、
)是一种重要化工原料,某研究小组以生锈的铜屑为原料[主要成分是Cu,含有少量的油污、CuO、 、
、 ]制备胆矾。流程如下。
]制备胆矾。流程如下。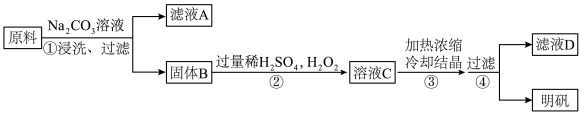
 溶解固体B,将生成
溶解固体B,将生成 存在下Cu溶于稀
存在下Cu溶于稀

