乙二酸(H2C2O4)俗称草酸,在实验研究和化学工业中应用广泛。
(1) 室温下,测得 0.1 mol·L−1 H2C2O4溶液的pH = 1.3,写出草酸的电离方程式_______ 。
(2)草酸溶液中各粒子的物质的量分数随溶液pH变化关系如下图所示:
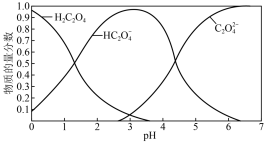
向草酸溶液中滴加KOH溶液至pH = 3时发生的主要反应的离子方程式是_______ 。
(3)工业上利用硫酸亚铁与草酸反应制备草酸亚铁晶体,其离子方程式为:Fe2++H2C2O4 + xH2O⇌FeC2O4 xH2O↓ + 2H+
xH2O↓ + 2H+
①制备时需添加氨水以提高FeC2O4·xH2O的产率,从化学平衡移动原理角度解释原因:________________ 。
②测定草酸亚铁晶体(FeC2O4·xH2O)的x值,实验如下:
称取0.5400 g草酸亚铁晶体溶于一定浓度的硫酸中,用KMnO4酸性溶液滴定。到达滴定终点时,消耗0.1000 mol·L-1的KMnO4酸性溶液18.00 mL。
已知:滴定过程中铁、碳元素被氧化为Fe3+、CO2,锰元素被还原为Mn2+
则滴定实验应选用______ (填写酸式或碱式)滴定管,通过计算FeC2O4·xH2O中x的值。(FeC2O4的摩尔质量是144 g·mol-1)__________ 。(写出计算过程)
(1) 室温下,测得 0.1 mol·L−1 H2C2O4溶液的pH = 1.3,写出草酸的电离方程式
(2)草酸溶液中各粒子的物质的量分数随溶液pH变化关系如下图所示:

向草酸溶液中滴加KOH溶液至pH = 3时发生的主要反应的离子方程式是
(3)工业上利用硫酸亚铁与草酸反应制备草酸亚铁晶体,其离子方程式为:Fe2++H2C2O4 + xH2O⇌FeC2O4
 xH2O↓ + 2H+
xH2O↓ + 2H+①制备时需添加氨水以提高FeC2O4·xH2O的产率,从化学平衡移动原理角度解释原因:
②测定草酸亚铁晶体(FeC2O4·xH2O)的x值,实验如下:
称取0.5400 g草酸亚铁晶体溶于一定浓度的硫酸中,用KMnO4酸性溶液滴定。到达滴定终点时,消耗0.1000 mol·L-1的KMnO4酸性溶液18.00 mL。
已知:滴定过程中铁、碳元素被氧化为Fe3+、CO2,锰元素被还原为Mn2+
则滴定实验应选用
更新时间:2021-05-23 06:51:35
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】三氯乙醛(CCl3CHO)用于制造农药和杀虫剂,某小组设计如图所示装置制备三氯乙醛。
回答下列问题:
(1)实验中D装置在80~90℃水浴条件下进行反应,写出D装置中制备三氯乙醛的化学方程式:___________ 。
(2)D装置中可能发生副反应,若缺少B装置,D装置中有机副产物___________ (写名称)的量会增加,可采用___________ 的方法分离提纯三氯乙醛。
(3)从提升产率的角度,说明C装置的作用:___________ 。
(4)E装置中盛装的试剂为___________ 。
(5)测定产品纯度:称取0.70g产品配成溶液,向待测液中加入适量KOH溶液,再加入20.00mL 0.2mol/L碘标准溶液,待反应 ;
; 进行完全。再加盐酸调节溶液的pH,加入淀粉作指示剂,立即用0.1mol/L
进行完全。再加盐酸调节溶液的pH,加入淀粉作指示剂,立即用0.1mol/L  溶液滴定至终点,发生反应
溶液滴定至终点,发生反应 。进行三次平行实验,测得平均消耗
。进行三次平行实验,测得平均消耗 溶液10.00mL。
溶液10.00mL。
①取用碘标准溶液的仪器为___________ (填“酸式”或“碱式”)滴定管。
②实验测得产品的纯度为___________ 。
③若取用 溶液的滴定管,滴定前仰视读数,滴定后俯视读数,则测定结果将
溶液的滴定管,滴定前仰视读数,滴定后俯视读数,则测定结果将___________ (填“偏大”“偏小”或“不变”)。

| 物质 |  |  |  |  |
| 相对分子质量 | 46 | 147.5 | 163.5 | 64.5 |
| 熔点/℃ | -114.1 | -57.5 | 58 | -140.8 |
| 沸点/℃ | 78.5 | 97.8 | 198 | 12.3 |
| 溶解性 | 与水互溶 | 可溶于水、乙醇 | 可溶于水、乙醇、三氯乙醛 | 微溶于水,可溶于乙醇 |
(1)实验中D装置在80~90℃水浴条件下进行反应,写出D装置中制备三氯乙醛的化学方程式:
(2)D装置中可能发生副反应,若缺少B装置,D装置中有机副产物
(3)从提升产率的角度,说明C装置的作用:
(4)E装置中盛装的试剂为
(5)测定产品纯度:称取0.70g产品配成溶液,向待测液中加入适量KOH溶液,再加入20.00mL 0.2mol/L碘标准溶液,待反应
 ;
; 进行完全。再加盐酸调节溶液的pH,加入淀粉作指示剂,立即用0.1mol/L
进行完全。再加盐酸调节溶液的pH,加入淀粉作指示剂,立即用0.1mol/L  溶液滴定至终点,发生反应
溶液滴定至终点,发生反应 。进行三次平行实验,测得平均消耗
。进行三次平行实验,测得平均消耗 溶液10.00mL。
溶液10.00mL。①取用碘标准溶液的仪器为
②实验测得产品的纯度为
③若取用
 溶液的滴定管,滴定前仰视读数,滴定后俯视读数,则测定结果将
溶液的滴定管,滴定前仰视读数,滴定后俯视读数,则测定结果将
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】无水碱式氯化铜[Cu2(OH)3Cl]为绿色或墨绿色结晶性粉末,难溶于水,溶于稀酸和氨水,在空气中十分稳定。
Ⅰ模拟制备碱式氯化铜晶体
向精制的CuCl2溶液中通入NH3和HCl,调节溶液pH至5.0~5.5,控制反应温度为70~80℃,实验装置如图所示(部分夹持装置已省略)。
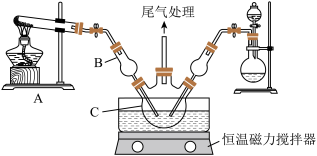
(1)仪器B为球型干燥管,其主要的作用是_____ 。装置C中的反应混合溶液pH过高或过低将导致产率降低,原因是_________ 。
(2)下列说法错误的是_____ 。
A.可通过观察装置C中的气泡速率,调节控制通入NH3和HCl的速率
B.可用pH计不断测定装置C中溶液的pH,以达到实验要求
C.可用右图装置吸收尾气,防止污染空气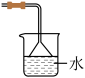
D.为了加快干燥速率,可选用加热烘干
(3)如图装置(活塞K处于打开状态),经过一系列操作获得较干燥的碱式氯化铜。请选择合适的编号,按正确的操作顺序补充完整.
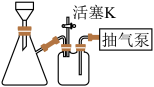
将反应产物冷却至40℃左右,倒入烧杯中→将滤纸放入布氏漏斗内,用蒸馏水润湿,打开抽气泵→( ) →( ) →( ) →( ) →用滤液淋洗烧杯,至所有晶体被收集到布氏漏斗中抽滤→( ) →( ) →( ) →确认抽干,开大活塞K,关抽气泵。
a.用倾析法转移溶液
b.加入洗涤剂
c.开大活塞K
d.微开活塞K
e.关活塞K
f.微关活塞K
g.待溶液快流尽时转移固体混合物
Ⅱ无水碱式氯化铜含量的测定
(4)上述操作后得到的固体经提纯得产品无水碱式氯化铜。称取产品加硝酸溶解,并加水定容至200mL,得到待测液。
采用银量法测定氯,用NH4SCN标准溶液滴定过量的AgNO3,发生反应Ag++SCN-=AgSCN↓,实验示意图如下。

(聚乙烯醇的作用是阻止AgCl与AgSCN的转化)
①滴定时,可选用NH4Fe(SO4)2作为指示剂,到达滴定终点的现象为_____ 。
②重复实验操作三次,消耗NH4SCN溶液体积平均为12.50mL。则称取的样品中n(Cl−)为_____ mol。
Ⅰ模拟制备碱式氯化铜晶体
向精制的CuCl2溶液中通入NH3和HCl,调节溶液pH至5.0~5.5,控制反应温度为70~80℃,实验装置如图所示(部分夹持装置已省略)。

(1)仪器B为球型干燥管,其主要的作用是
(2)下列说法错误的是
A.可通过观察装置C中的气泡速率,调节控制通入NH3和HCl的速率
B.可用pH计不断测定装置C中溶液的pH,以达到实验要求
C.可用右图装置吸收尾气,防止污染空气

D.为了加快干燥速率,可选用加热烘干
(3)如图装置(活塞K处于打开状态),经过一系列操作获得较干燥的碱式氯化铜。请选择合适的编号,按正确的操作顺序补充完整.

将反应产物冷却至40℃左右,倒入烧杯中→将滤纸放入布氏漏斗内,用蒸馏水润湿,打开抽气泵→
a.用倾析法转移溶液
b.加入洗涤剂
c.开大活塞K
d.微开活塞K
e.关活塞K
f.微关活塞K
g.待溶液快流尽时转移固体混合物
Ⅱ无水碱式氯化铜含量的测定
(4)上述操作后得到的固体经提纯得产品无水碱式氯化铜。称取产品加硝酸溶解,并加水定容至200mL,得到待测液。
采用银量法测定氯,用NH4SCN标准溶液滴定过量的AgNO3,发生反应Ag++SCN-=AgSCN↓,实验示意图如下。

(聚乙烯醇的作用是阻止AgCl与AgSCN的转化)
①滴定时,可选用NH4Fe(SO4)2作为指示剂,到达滴定终点的现象为
②重复实验操作三次,消耗NH4SCN溶液体积平均为12.50mL。则称取的样品中n(Cl−)为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】 是白色固体,难溶于水,可用于制备补血剂。
是白色固体,难溶于水,可用于制备补血剂。
Ⅰ. 的制取步骤和装置图如下(夹持仪器略):
的制取步骤和装置图如下(夹持仪器略):
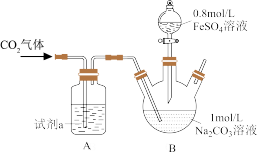
①先向 中的
中的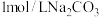 溶液通入一段时间
溶液通入一段时间 至其
至其 为7;
为7;
②然后滴加一定量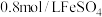 溶液,产生白色沉淀;
溶液,产生白色沉淀;
③过滤、洗涤、干燥,得到 固体。
固体。
(1)通入 溶液的
溶液的 用大理石与盐酸反应制得后,先经过
用大理石与盐酸反应制得后,先经过 装置再进入
装置再进入 中,
中, 装置的作用是
装置的作用是_______ ,试剂a是_______ 。
(2)写出装置 中制取
中制取 的离子方程式:
的离子方程式:_______ 。若向 溶液中直接滴入
溶液中直接滴入 溶液,产生的沉淀可能有
溶液,产生的沉淀可能有_______ 。
Ⅱ. 溶于乳酸能制得可溶性乳酸亚铁(
溶于乳酸能制得可溶性乳酸亚铁( )补血剂。
)补血剂。
(3)验证乳酸亚铁补血剂中亚铁离子未被氧化的试剂是_______ 。
Ⅲ.两位同学分别用不同的方案进行乳酸亚铁补血剂中铁元素含量测定:
(4)甲同学通过 滴定法测定样品中
滴定法测定样品中 的含量计算样品纯度。在操作均正确的前提下,所得纯度总是大于
的含量计算样品纯度。在操作均正确的前提下,所得纯度总是大于 ,其原因可能是
,其原因可能是_______ 。
(5)乙同学经查阅资料后改用碘量法测定铁元素的含量。称取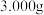 样品,灼烧完全灰化,加足量盐酸溶解,取所有可溶物配成
样品,灼烧完全灰化,加足量盐酸溶解,取所有可溶物配成 溶液。吸取
溶液。吸取 该溶液加入过量
该溶液加入过量 溶液充分反应,然后加入几滴淀粉溶液,用
溶液充分反应,然后加入几滴淀粉溶液,用 硫代硫酸钠溶液滴定(已知:
硫代硫酸钠溶液滴定(已知: ),当
),当_______ ,即为滴定终点;平行滴定3次,硫代硫酸钠溶液的平均用量为 ,则样品纯度为
,则样品纯度为_______ 
 是白色固体,难溶于水,可用于制备补血剂。
是白色固体,难溶于水,可用于制备补血剂。Ⅰ.
 的制取步骤和装置图如下(夹持仪器略):
的制取步骤和装置图如下(夹持仪器略):
①先向
 中的
中的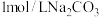 溶液通入一段时间
溶液通入一段时间 至其
至其 为7;
为7;②然后滴加一定量
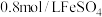 溶液,产生白色沉淀;
溶液,产生白色沉淀;③过滤、洗涤、干燥,得到
 固体。
固体。(1)通入
 溶液的
溶液的 用大理石与盐酸反应制得后,先经过
用大理石与盐酸反应制得后,先经过 装置再进入
装置再进入 中,
中, 装置的作用是
装置的作用是(2)写出装置
 中制取
中制取 的离子方程式:
的离子方程式: 溶液中直接滴入
溶液中直接滴入 溶液,产生的沉淀可能有
溶液,产生的沉淀可能有Ⅱ.
 溶于乳酸能制得可溶性乳酸亚铁(
溶于乳酸能制得可溶性乳酸亚铁( )补血剂。
)补血剂。(3)验证乳酸亚铁补血剂中亚铁离子未被氧化的试剂是
Ⅲ.两位同学分别用不同的方案进行乳酸亚铁补血剂中铁元素含量测定:
(4)甲同学通过
 滴定法测定样品中
滴定法测定样品中 的含量计算样品纯度。在操作均正确的前提下,所得纯度总是大于
的含量计算样品纯度。在操作均正确的前提下,所得纯度总是大于 ,其原因可能是
,其原因可能是(5)乙同学经查阅资料后改用碘量法测定铁元素的含量。称取
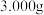 样品,灼烧完全灰化,加足量盐酸溶解,取所有可溶物配成
样品,灼烧完全灰化,加足量盐酸溶解,取所有可溶物配成 溶液。吸取
溶液。吸取 该溶液加入过量
该溶液加入过量 溶液充分反应,然后加入几滴淀粉溶液,用
溶液充分反应,然后加入几滴淀粉溶液,用 硫代硫酸钠溶液滴定(已知:
硫代硫酸钠溶液滴定(已知: ),当
),当 ,则样品纯度为
,则样品纯度为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】次磷酸(H3PO2)是一种精细磷化工产品,具有较强还原性。回答下列问题:
(1)H3PO2是一种一元中强酸,写出其电离方程式__________ 。
(2)H3PO2及NaH2PO2均可将溶液中的Ag+还原为银,从而可用于化学镀银。
①H3PO2中,P元素的化合价为__________ 。
②利用(H3PO2)进行化学镀银反应中,氧化剂与还原剂的物质的量之比为4︰1,则氧化产物为:____ (填化学式)。
③NaH2PO2为______ (填“正盐”或“酸式盐”),其溶液显_______ (填“弱酸性”、“中性”或“弱碱性”)。
(3)H3PO2的工业制法:将白磷(P4)与Ba(OH)2溶液反应生成PH3气体和Ba(H2PO2)2,后者再与H2SO4反应。写出白磷与Ba(OH)2溶液反应的化学方程式__________ 。
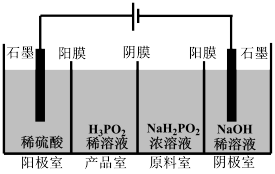
(4)H3PO2也可用电渗析法制备,“四室电渗析法”工作原理如图所示(阳膜和阴膜分别只允许阳离子、阴离子通过):
①写出阳极的电极反应式__________ 。
②分析产品室可得到H3PO2的原因__________ 。
(1)H3PO2是一种一元中强酸,写出其电离方程式
(2)H3PO2及NaH2PO2均可将溶液中的Ag+还原为银,从而可用于化学镀银。
①H3PO2中,P元素的化合价为
②利用(H3PO2)进行化学镀银反应中,氧化剂与还原剂的物质的量之比为4︰1,则氧化产物为:
③NaH2PO2为
(3)H3PO2的工业制法:将白磷(P4)与Ba(OH)2溶液反应生成PH3气体和Ba(H2PO2)2,后者再与H2SO4反应。写出白磷与Ba(OH)2溶液反应的化学方程式
(4)H3PO2也可用电渗析法制备,“四室电渗析法”工作原理如图所示(阳膜和阴膜分别只允许阳离子、阴离子通过):

①写出阳极的电极反应式
②分析产品室可得到H3PO2的原因
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】(1)结合表中给出的电离平衡常数回答下列问题:
①上述四种酸中,酸性最弱、最强的酸分别是_______ 、_______ (用化学式表示)。
②下列能使醋酸溶液中CH3COOH的电离程度增大,而电离平衡常数不变的操作是____ (填序号)。
A.升高温度 B.加水稀释 C.加少量的CH3COONa固体
D.加少量冰醋酸 E.加氢氧化钠固体
③依上表数据判断醋酸和次氯酸钠溶液能否反应,如果不能反应说出理由,如果能发生反应请写出相应的离子方程式___________________________________ 。
(2) 某学习小组利用酸性KMnO4和H2C2O4反应来探究“外界条件对化学反应速率的影响”。 实验时,先分别量取KMnO4酸性溶液、H2C2O4溶液,然后倒入大试管中迅速振荡混合均匀,开始计时,通过测定褪色所需时间来判断反应的快慢。
①已知草酸H2C2O4是一种二元弱酸,写出草酸的电离方程式__________ 、___________ 。酸性KMnO4溶液和H2C2O4溶液反应的离子方程式为:_____________________________
某同学设计了如下实验
②探究浓度对化学反应速率影响的组合实验编号是__________ ,可探究温度对化学反应速率影响的实验编号是__________ 。
③实验a测得混合后溶液褪色的时间为40 s,忽略混合前后体积的微小变化,则这段时间内的平均反应速率v(KMnO4)=______ mol·L-1·min-1。
④在实验中,草酸(H2C2O4)溶液与KMnO4酸性溶液反应时,褪色总是先慢后快,其可能的原因是___________________________________
| 酸或碱 | CH3COOH | HNO2 | HCN | HClO |
| 电离平衡常数(Ka或Kb) | 1.8×10-5 | 4.6×10-4 | 5×10-10 | 3×10-8 |
①上述四种酸中,酸性最弱、最强的酸分别是
②下列能使醋酸溶液中CH3COOH的电离程度增大,而电离平衡常数不变的操作是
A.升高温度 B.加水稀释 C.加少量的CH3COONa固体
D.加少量冰醋酸 E.加氢氧化钠固体
③依上表数据判断醋酸和次氯酸钠溶液能否反应,如果不能反应说出理由,如果能发生反应请写出相应的离子方程式
(2) 某学习小组利用酸性KMnO4和H2C2O4反应来探究“外界条件对化学反应速率的影响”。 实验时,先分别量取KMnO4酸性溶液、H2C2O4溶液,然后倒入大试管中迅速振荡混合均匀,开始计时,通过测定褪色所需时间来判断反应的快慢。
①已知草酸H2C2O4是一种二元弱酸,写出草酸的电离方程式
某同学设计了如下实验
| 实验编号 | H2C2O4溶液 | KMnO4溶液 | 温度/℃ | ||
| 浓度(mol/L) | 体积(mL) | 浓度(mol/L) | 体积(mL) | ||
| a | 0.10 | 2.0 | 0.010 | 4.0 | 25 |
| b | 0.20 | 2.0 | 0.010 | 4.0 | 25 |
| c | 0.20 | 2.0 | 0.010 | 4.0 | 50 |
②探究浓度对化学反应速率影响的组合实验编号是
③实验a测得混合后溶液褪色的时间为40 s,忽略混合前后体积的微小变化,则这段时间内的平均反应速率v(KMnO4)=
④在实验中,草酸(H2C2O4)溶液与KMnO4酸性溶液反应时,褪色总是先慢后快,其可能的原因是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】已知X、Y、Z是阳离子,K是阴离子,M、N是分子.它们都由短周期元素组成,且具有以下结构特征和性质:
①它们的核外电子总数都相同;
②N溶于M中,滴入酚酞,溶液变红;
③Y和K都由A.B两元素组成,Y核内质子数比K多2个;
④X和N都由A、C两元素组成,X和Y核内质子总数相等;
⑤X和K的浓溶液在加热条件下生成M和N;
⑥Z为单核离子,向含有Z的溶液中加入少量含K的溶液,有白色沉淀J生成,再加入过量的含K或Y的溶液,沉淀J消失.
回答下列问题:
(1)Y的化学式为________________ ;N的电子式为____________ ;
(2)试比较M和N的稳定性:M_____ N(填“>”或“<”).
(3)写出Z和N的水溶液反应的离子方程式:_____________ ;
(4)从电离的角度看白色沉淀J能溶于过量的含K或Y的溶液其原因是(用离子方程式表示):______
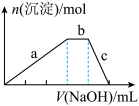
(5)上述六种微粒中的两种可与硫酸根形成一种含三种离子的盐,向该盐的浓溶液中逐滴加入0.1mol/L的NaOH溶液,出现了如图中a、b、c三个阶段的图象,①写出b阶段的离子方程式:___________ .
②根据图象判断该盐的化学式为____________ .
①它们的核外电子总数都相同;
②N溶于M中,滴入酚酞,溶液变红;
③Y和K都由A.B两元素组成,Y核内质子数比K多2个;
④X和N都由A、C两元素组成,X和Y核内质子总数相等;
⑤X和K的浓溶液在加热条件下生成M和N;
⑥Z为单核离子,向含有Z的溶液中加入少量含K的溶液,有白色沉淀J生成,再加入过量的含K或Y的溶液,沉淀J消失.
回答下列问题:
(1)Y的化学式为
(2)试比较M和N的稳定性:M
(3)写出Z和N的水溶液反应的离子方程式:
(4)从电离的角度看白色沉淀J能溶于过量的含K或Y的溶液其原因是(用离子方程式表示):
(5)上述六种微粒中的两种可与硫酸根形成一种含三种离子的盐,向该盐的浓溶液中逐滴加入0.1mol/L的NaOH溶液,出现了如图中a、b、c三个阶段的图象,①写出b阶段的离子方程式:
②根据图象判断该盐的化学式为

您最近一年使用:0次



