无水碱式氯化铜[Cu2(OH)3Cl]为绿色或墨绿色结晶性粉末,难溶于水,溶于稀酸和氨水,在空气中十分稳定。
Ⅰ模拟制备碱式氯化铜晶体
向精制的CuCl2溶液中通入NH3和HCl,调节溶液pH至5.0~5.5,控制反应温度为70~80℃,实验装置如图所示(部分夹持装置已省略)。
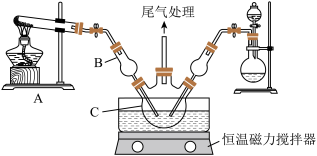
(1)仪器B为球型干燥管,其主要的作用是_____ 。装置C中的反应混合溶液pH过高或过低将导致产率降低,原因是_________ 。
(2)下列说法错误的是_____ 。
A.可通过观察装置C中的气泡速率,调节控制通入NH3和HCl的速率
B.可用pH计不断测定装置C中溶液的pH,以达到实验要求
C.可用右图装置吸收尾气,防止污染空气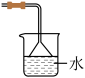
D.为了加快干燥速率,可选用加热烘干
(3)如图装置(活塞K处于打开状态),经过一系列操作获得较干燥的碱式氯化铜。请选择合适的编号,按正确的操作顺序补充完整.
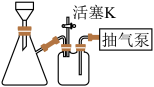
将反应产物冷却至40℃左右,倒入烧杯中→将滤纸放入布氏漏斗内,用蒸馏水润湿,打开抽气泵→( ) →( ) →( ) →( ) →用滤液淋洗烧杯,至所有晶体被收集到布氏漏斗中抽滤→( ) →( ) →( ) →确认抽干,开大活塞K,关抽气泵。
a.用倾析法转移溶液
b.加入洗涤剂
c.开大活塞K
d.微开活塞K
e.关活塞K
f.微关活塞K
g.待溶液快流尽时转移固体混合物
Ⅱ无水碱式氯化铜含量的测定
(4)上述操作后得到的固体经提纯得产品无水碱式氯化铜。称取产品加硝酸溶解,并加水定容至200mL,得到待测液。
采用银量法测定氯,用NH4SCN标准溶液滴定过量的AgNO3,发生反应Ag++SCN-=AgSCN↓,实验示意图如下。

(聚乙烯醇的作用是阻止AgCl与AgSCN的转化)
①滴定时,可选用NH4Fe(SO4)2作为指示剂,到达滴定终点的现象为_____ 。
②重复实验操作三次,消耗NH4SCN溶液体积平均为12.50mL。则称取的样品中n(Cl−)为_____ mol。
Ⅰ模拟制备碱式氯化铜晶体
向精制的CuCl2溶液中通入NH3和HCl,调节溶液pH至5.0~5.5,控制反应温度为70~80℃,实验装置如图所示(部分夹持装置已省略)。

(1)仪器B为球型干燥管,其主要的作用是
(2)下列说法错误的是
A.可通过观察装置C中的气泡速率,调节控制通入NH3和HCl的速率
B.可用pH计不断测定装置C中溶液的pH,以达到实验要求
C.可用右图装置吸收尾气,防止污染空气

D.为了加快干燥速率,可选用加热烘干
(3)如图装置(活塞K处于打开状态),经过一系列操作获得较干燥的碱式氯化铜。请选择合适的编号,按正确的操作顺序补充完整.

将反应产物冷却至40℃左右,倒入烧杯中→将滤纸放入布氏漏斗内,用蒸馏水润湿,打开抽气泵→
a.用倾析法转移溶液
b.加入洗涤剂
c.开大活塞K
d.微开活塞K
e.关活塞K
f.微关活塞K
g.待溶液快流尽时转移固体混合物
Ⅱ无水碱式氯化铜含量的测定
(4)上述操作后得到的固体经提纯得产品无水碱式氯化铜。称取产品加硝酸溶解,并加水定容至200mL,得到待测液。
采用银量法测定氯,用NH4SCN标准溶液滴定过量的AgNO3,发生反应Ag++SCN-=AgSCN↓,实验示意图如下。

(聚乙烯醇的作用是阻止AgCl与AgSCN的转化)
①滴定时,可选用NH4Fe(SO4)2作为指示剂,到达滴定终点的现象为
②重复实验操作三次,消耗NH4SCN溶液体积平均为12.50mL。则称取的样品中n(Cl−)为
2020·浙江·模拟预测 查看更多[2]
更新时间:2020-12-16 15:31:09
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
【推荐1】侯德榜是我国著名科学家,1933年出版《纯碱制造》一书,创立了中国自己的制碱工艺。其纯碱制造原理如下图所示:
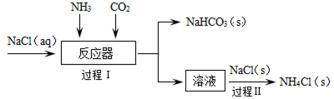
(1)由NaHCO3制备纯碱的化学方程式是_________________ 。
(2)过程Ⅰ通入NH3和CO2的顺序是__________________ 。
(3)过程Ⅱ析出NH4Cl(s)的原因是_____________ 。
(4)充分利用副产品NH4Cl生产NH3和HCl。直接加热分解NH4Cl,NH3和HCl的产率往往很低,原因是________________ 。
(5)采用MgO循环分解NH4Cl。加热,在300℃以下获得NH3;继续加热至350℃~600℃获得HCl气体。利用下列装置(加热及加持装置略)可测量NH3和HCl的产率。
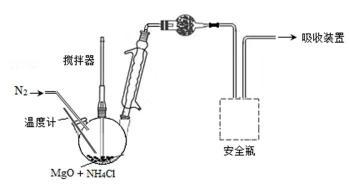
① 低于300℃时,干燥管盛装的干燥剂是_________ 。NH3吸收完全后,更换干燥剂和吸收装置中的吸收液。
② 产生NH3的化学反应方程式是_________________ 。
③ 在350℃~600℃,上图虚线框内应选择的安全瓶是________ 。
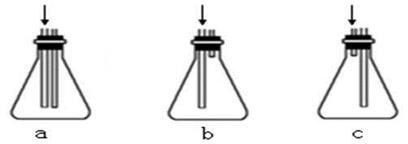
④ MgO可以循环分解NH4Cl制得NH3和HCl的原因是____________ (结合化学方程式解释)。

(1)由NaHCO3制备纯碱的化学方程式是
(2)过程Ⅰ通入NH3和CO2的顺序是
(3)过程Ⅱ析出NH4Cl(s)的原因是
(4)充分利用副产品NH4Cl生产NH3和HCl。直接加热分解NH4Cl,NH3和HCl的产率往往很低,原因是
(5)采用MgO循环分解NH4Cl。加热,在300℃以下获得NH3;继续加热至350℃~600℃获得HCl气体。利用下列装置(加热及加持装置略)可测量NH3和HCl的产率。

① 低于300℃时,干燥管盛装的干燥剂是
② 产生NH3的化学反应方程式是
③ 在350℃~600℃,上图虚线框内应选择的安全瓶是

④ MgO可以循环分解NH4Cl制得NH3和HCl的原因是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】工业上从海水中获得纯净氯化钠溶液经过下列流程生产焦亚硫酸钠( ,能溶于水,在空气中容易被氧化),回答下列问题:
,能溶于水,在空气中容易被氧化),回答下列问题:
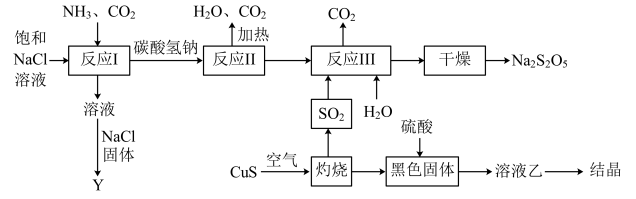
(1)反应I中应该先通入_______ ,反应I的离子方程式_______ 。
(2)Y的主要成分是_______ 。
(3)从溶液乙中结晶的具体操作是_______ 。
(4)该流程中,_______ 可以循环使用。
(5)灼烧的化学方程式为_______ 。
(6)已知 与稀硫酸反应生成
与稀硫酸反应生成 ,其离子方程式为
,其离子方程式为_______ 。焦亚硫酸钠常用作食物的抗氧化剂,在空气中容易被氧化而变质。要检验焦亚硫酸钠是否变质,具体的实验操作为_______ 。
 ,能溶于水,在空气中容易被氧化),回答下列问题:
,能溶于水,在空气中容易被氧化),回答下列问题:
(1)反应I中应该先通入
(2)Y的主要成分是
(3)从溶液乙中结晶的具体操作是
(4)该流程中,
(5)灼烧的化学方程式为
(6)已知
 与稀硫酸反应生成
与稀硫酸反应生成 ,其离子方程式为
,其离子方程式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐3】氨既是一种重要的化工产品,又是一种重要的化工原料。下图为合成氨以及氨氧化制硝酸的流程示意:
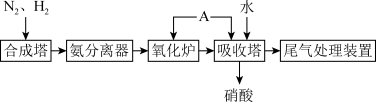
(1)氨分离器中压强约为15MPa,温度约为-20℃,分离氨应用了氨_______ 的性质,从氨分离器中又回到合成塔中的物质是_______ 。
(2)请写出氧化炉内发生反应的化学方程式并用单线桥标出电子转移的方向和数目_______ 。
(3)向吸收塔中通入过量A是_______ ,作用是_______ 。
(4)硝酸可氧化绝大多数金属,而工业上盛装大量浓硝酸可用铝制容器,原因是_______ 。

(1)氨分离器中压强约为15MPa,温度约为-20℃,分离氨应用了氨
(2)请写出氧化炉内发生反应的化学方程式并用单线桥标出电子转移的方向和数目
(3)向吸收塔中通入过量A是
(4)硝酸可氧化绝大多数金属,而工业上盛装大量浓硝酸可用铝制容器,原因是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】二氧化氯是国际公认的高效消毒灭菌剂。二氧化氯漂白液中常含有ClO2和Cl2两种主要成分。
某同学为测定某二氧化氯漂白液中ClO2的浓度,进行如下实验:
【实验Ⅰ】需要480mL0.10mol/L的Na2S2O3溶液,步骤如下:
①将容量瓶塞盖好,充分摇匀
②将烧杯中的溶液小心的注入容量瓶中:。
③继续向容量瓶中加水至距刻度线1~2cm处,改用胶头滴管加水至刻度线;
④用蒸馏水洗涤烧杯内壁和玻璃棒2~3次;并将每次洗涤的洛液转入容量瓶中,振荡;
⑤用天平准确称取一定质量的Na2S2O3·5H2O固体,放入烧杯,用适量蒸馏水溶解。
回答下列问题:
(1)上述实验步骤的正确顺序为______ 。
(2)配制溶液过程中需称量Na2S2O3·5H2O固体的质量为______ 。
(3)容量瓶是配制溶液所用的主要仪器。容量瓶上需标有______ (填序号)。
①温度②浓度③容量④压强⑤刻度线
(4)下列关于容量瓶操作的说法中,正确的是______(填序号)。
(5)配制溶液过程中,若定容时俯视刻度线,则配制的溶液浓度______ (填偏大、偏小或无影响)。
【实验Ⅱ】测定二氧化氯漂白液中ClO2浓度,步骤如下:
①量取5mL二氧化氯漂白液于锥形瓶中,加蒸馏水稀释到25mL再向其中加入过量KI溶液,二氧化氯漂白液中的两种成分分别发生反应:2ClO2+2KI=2KClO2+I2、Cl2+2KI=2KCl+I2
②加入淀粉作指示剂,向其中逐滴加入0.10mol/L的Na2S2O3溶液至反应恰好完全进行,过程中发生的反应为:2Na2S2O3+I2=Na2S4O6+2NaI
③加入稀硫酸调节溶液pH=3,发生反应:KClO2+4KI+2H2SO4=KCl+2K2SO4+2I2+2H2O
④再逐滴加入0.10mo/L的Na2S2O3溶液,反应恰好完全进行时,该步消耗Na2S2O3溶液20mL。
回答下列问题:
(6)用双线桥标出反应中电子转移的方向和数目______ :2ClO2+2KI=2KClO2+I2
(7)该二氧化氡漂白液中ClO2的物质的量浓度为______ 。
某同学为测定某二氧化氯漂白液中ClO2的浓度,进行如下实验:
【实验Ⅰ】需要480mL0.10mol/L的Na2S2O3溶液,步骤如下:
①将容量瓶塞盖好,充分摇匀
②将烧杯中的溶液小心的注入容量瓶中:。
③继续向容量瓶中加水至距刻度线1~2cm处,改用胶头滴管加水至刻度线;
④用蒸馏水洗涤烧杯内壁和玻璃棒2~3次;并将每次洗涤的洛液转入容量瓶中,振荡;
⑤用天平准确称取一定质量的Na2S2O3·5H2O固体,放入烧杯,用适量蒸馏水溶解。
回答下列问题:
(1)上述实验步骤的正确顺序为
(2)配制溶液过程中需称量Na2S2O3·5H2O固体的质量为
(3)容量瓶是配制溶液所用的主要仪器。容量瓶上需标有
①温度②浓度③容量④压强⑤刻度线
(4)下列关于容量瓶操作的说法中,正确的是______(填序号)。
| A.查漏时,应将活塞旋转180°再次检验是否漏水 |
| B.容量瓶洗涤后需要烘干后再使用 |
| C.定容时,馒慢将蒸馏水倒至凹液面最低处与刻度线相平 |
| D.定容摇匀后,若发现液面变低,应补加蒸馏水至刻度线 |
(5)配制溶液过程中,若定容时俯视刻度线,则配制的溶液浓度
【实验Ⅱ】测定二氧化氯漂白液中ClO2浓度,步骤如下:
①量取5mL二氧化氯漂白液于锥形瓶中,加蒸馏水稀释到25mL再向其中加入过量KI溶液,二氧化氯漂白液中的两种成分分别发生反应:2ClO2+2KI=2KClO2+I2、Cl2+2KI=2KCl+I2
②加入淀粉作指示剂,向其中逐滴加入0.10mol/L的Na2S2O3溶液至反应恰好完全进行,过程中发生的反应为:2Na2S2O3+I2=Na2S4O6+2NaI
③加入稀硫酸调节溶液pH=3,发生反应:KClO2+4KI+2H2SO4=KCl+2K2SO4+2I2+2H2O
④再逐滴加入0.10mo/L的Na2S2O3溶液,反应恰好完全进行时,该步消耗Na2S2O3溶液20mL。
回答下列问题:
(6)用双线桥标出反应中电子转移的方向和数目
(7)该二氧化氡漂白液中ClO2的物质的量浓度为
您最近一年使用:0次
【推荐2】Na2S可用于制造硫化染料、沉淀水体中的重金属等。
(1)Na2S溶液中S2-水解的离子方程式为_________ 。
(2)室温时,几种重金属离子的硫化物的溶度积常数如下表:
①向物质的量浓度相同的Fe2+、Pb2+、Cu2+、Hg2+的混合稀溶液中,逐滴加入Na2S稀溶液,首先沉淀的离子是____ 。
②用Na2S溶液沉淀废水中Pb2+,为使Pb2+沉淀完全[c(Pb2+)≤1×10-6mol/L],则应满足溶液中c(S2-)≥_____ mol/L。
③反应Cu2+(aq)+FeS(s) Fe2+(aq)+CuS(s)的平衡常数K=
Fe2+(aq)+CuS(s)的平衡常数K=_______ 。
(3)测定某Na2S和NaHS混合样品中两者含量的实验步骤如下:
步骤1.准确称取一定量样品于烧杯中,加入少量蒸馏水溶解,转移至500mL容量瓶中定容。
步骤2.准确移取25.00mL上述溶液于锥形瓶中,加入茜素黄GG-百时香酚蓝混合指示剂,用0.2500mol/L盐酸标准溶液滴定(Na2S+HCl=NaHS+NaCl)至终点,消耗盐酸24.00mL;向其中再加入5mL中性甲醛(NaHS+HCHO+H2O→NaOH+HSCH2OH)和3滴酚酞指示剂,继续用0.2500mol/L盐酸标准溶液滴定(NaOH+HCl=NaCl+H2O)至终点,又消耗盐酸34.00mL。
计算原混合物中Na2S与NaHS的物质的量之比(写出计算过程)___________ 。
(1)Na2S溶液中S2-水解的离子方程式为
(2)室温时,几种重金属离子的硫化物的溶度积常数如下表:
| 金属硫化物 | FeS | PbS | CuS | HgS |
| Ksp | 6.3×10-18 | 1.0×10-28 | 6.3×10-36 | 1.6×10-52 |
①向物质的量浓度相同的Fe2+、Pb2+、Cu2+、Hg2+的混合稀溶液中,逐滴加入Na2S稀溶液,首先沉淀的离子是
②用Na2S溶液沉淀废水中Pb2+,为使Pb2+沉淀完全[c(Pb2+)≤1×10-6mol/L],则应满足溶液中c(S2-)≥
③反应Cu2+(aq)+FeS(s)
 Fe2+(aq)+CuS(s)的平衡常数K=
Fe2+(aq)+CuS(s)的平衡常数K=(3)测定某Na2S和NaHS混合样品中两者含量的实验步骤如下:
步骤1.准确称取一定量样品于烧杯中,加入少量蒸馏水溶解,转移至500mL容量瓶中定容。
步骤2.准确移取25.00mL上述溶液于锥形瓶中,加入茜素黄GG-百时香酚蓝混合指示剂,用0.2500mol/L盐酸标准溶液滴定(Na2S+HCl=NaHS+NaCl)至终点,消耗盐酸24.00mL;向其中再加入5mL中性甲醛(NaHS+HCHO+H2O→NaOH+HSCH2OH)和3滴酚酞指示剂,继续用0.2500mol/L盐酸标准溶液滴定(NaOH+HCl=NaCl+H2O)至终点,又消耗盐酸34.00mL。
计算原混合物中Na2S与NaHS的物质的量之比(写出计算过程)
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】化学反应常伴随热效应。某些反应(如中和反应)的热量变化,其数值Q可通过量热装置测量反应前后体系温度变化后计算获得。
实验步骤I:盐酸浓度的测定
移取 待测液,加入酚酞做指示剂,用
待测液,加入酚酞做指示剂,用 溶液滴定至终点,消耗
溶液滴定至终点,消耗 溶液
溶液 。
。
(1)对于一支洁净的滴定管使用前两步操作为:___________ ;___________ 。
(2)用 溶液进行滴定操作时,用到的玻璃仪器有
溶液进行滴定操作时,用到的玻璃仪器有___________ (写名称)。
(3)判断滴定终点的操作及现象为___________ 。
(4)该盐酸浓度为___________  。
。
(5)在上述实验过程中,出现了以下操作(其他操作正确),其中会造成测定结果(待测液浓度值)偏高的有___________ (填序号,下同)。
A.量取标准液的碱式滴定管未润洗
B.锥形瓶水洗后直接装待测液
C.酸式滴定管水洗后未用待测液润洗
D.滴定到达终点时,俯视读出滴定管读数
E.滴定前碱式滴定管尖嘴部分有气泡,滴定后气泡消失
实验步骤Ⅱ:热量的测定
(6)取上述 溶液和盐酸各
溶液和盐酸各 进行反应,测得反应前后体系的温度值(℃)分别为
进行反应,测得反应前后体系的温度值(℃)分别为 、
、 ,则该酸碱中和反应生成
,则该酸碱中和反应生成 水时放出的热量为
水时放出的热量为___________ kJ(近似认为稀溶液的比热容和密度与水相同,已知 )。
)。
(7)若将盐酸换成等浓度的乙酸进行相同的热量测定实验,则测得的热量数据将___________ (填“变大”、“变小”或“不变”)。
实验步骤I:盐酸浓度的测定
移取
 待测液,加入酚酞做指示剂,用
待测液,加入酚酞做指示剂,用 溶液滴定至终点,消耗
溶液滴定至终点,消耗 溶液
溶液 。
。(1)对于一支洁净的滴定管使用前两步操作为:
(2)用
 溶液进行滴定操作时,用到的玻璃仪器有
溶液进行滴定操作时,用到的玻璃仪器有(3)判断滴定终点的操作及现象为
(4)该盐酸浓度为
 。
。(5)在上述实验过程中,出现了以下操作(其他操作正确),其中会造成测定结果(待测液浓度值)偏高的有
A.量取标准液的碱式滴定管未润洗
B.锥形瓶水洗后直接装待测液
C.酸式滴定管水洗后未用待测液润洗
D.滴定到达终点时,俯视读出滴定管读数
E.滴定前碱式滴定管尖嘴部分有气泡,滴定后气泡消失
实验步骤Ⅱ:热量的测定
(6)取上述
 溶液和盐酸各
溶液和盐酸各 进行反应,测得反应前后体系的温度值(℃)分别为
进行反应,测得反应前后体系的温度值(℃)分别为 、
、 ,则该酸碱中和反应生成
,则该酸碱中和反应生成 水时放出的热量为
水时放出的热量为 )。
)。(7)若将盐酸换成等浓度的乙酸进行相同的热量测定实验,则测得的热量数据将
您最近一年使用:0次
【推荐1】锗是一种重要的战略资源,在半导体、航空航天测控等领域都有着广泛的应用。下图是以一种锗矿 主要成分为
主要成分为 、
、 、
、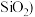 为原料制备锗的工艺流程:
为原料制备锗的工艺流程:
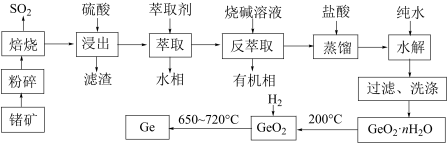
已知:
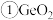 为两性氧化物。
为两性氧化物。
 “萃取”时用的萃取剂在本实验条件下对
“萃取”时用的萃取剂在本实验条件下对 有很好的选择性。
有很好的选择性。
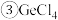 的熔、沸点分别为
的熔、沸点分别为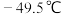 、
、 ,极易水解放热。
,极易水解放热。
 “蒸馏”过程中发生的反应为
“蒸馏”过程中发生的反应为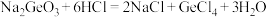 。
。
(1)锗在元素周期表中的位置为第_________ 周期第________ 族。
(2)“粉碎”的目的是_______________________ 。
(3)“焙烧”过程中 发生反应的化学方程式为
发生反应的化学方程式为________________ 。
(4)“滤渣”的成分为________________  填化学式
填化学式 ,“水相”中的阳离子除了
,“水相”中的阳离子除了 和
和 外,还有
外,还有__________________  填离子符号
填离子符号 。
。
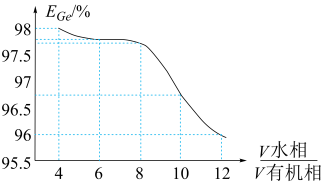
(5)“萃取”时,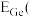 锗的萃取率
锗的萃取率 与
与 水相与有机相的体积比
水相与有机相的体积比 的关系如图所示,从生产成本的角度考虑,最适宜的
的关系如图所示,从生产成本的角度考虑,最适宜的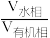 为
为______________  填序号
填序号 。
。
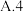
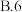

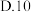
(6)“水解”时反应的化学方程式为_________________ ,该步实验操作必须在冰盐浴中进行的原因除了有利于水解反应正向进行外,还有______________ 。
(7)假设流程中每步都没有锗元素损失,若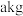 锗
锗  含锗
含锗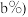 经提纯得到
经提纯得到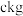 的锗,则杂质元素的脱除率为
的锗,则杂质元素的脱除率为_____________  用含a、b、c的式子表示
用含a、b、c的式子表示 。
。 已知:杂质元素的脱除率
已知:杂质元素的脱除率
 主要成分为
主要成分为 、
、 、
、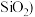 为原料制备锗的工艺流程:
为原料制备锗的工艺流程:
已知:
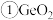 为两性氧化物。
为两性氧化物。 “萃取”时用的萃取剂在本实验条件下对
“萃取”时用的萃取剂在本实验条件下对 有很好的选择性。
有很好的选择性。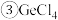 的熔、沸点分别为
的熔、沸点分别为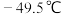 、
、 ,极易水解放热。
,极易水解放热。 “蒸馏”过程中发生的反应为
“蒸馏”过程中发生的反应为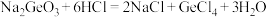 。
。(1)锗在元素周期表中的位置为第
(2)“粉碎”的目的是
(3)“焙烧”过程中
 发生反应的化学方程式为
发生反应的化学方程式为(4)“滤渣”的成分为
 填化学式
填化学式 ,“水相”中的阳离子除了
,“水相”中的阳离子除了 和
和 外,还有
外,还有 填离子符号
填离子符号 。
。(5)“萃取”时,
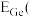 锗的萃取率
锗的萃取率 与
与 水相与有机相的体积比
水相与有机相的体积比 的关系如图所示,从生产成本的角度考虑,最适宜的
的关系如图所示,从生产成本的角度考虑,最适宜的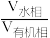 为
为 填序号
填序号 。
。
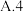
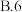

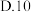
(6)“水解”时反应的化学方程式为
(7)假设流程中每步都没有锗元素损失,若
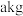 锗
锗  含锗
含锗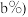 经提纯得到
经提纯得到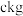 的锗,则杂质元素的脱除率为
的锗,则杂质元素的脱除率为 用含a、b、c的式子表示
用含a、b、c的式子表示 。
。 已知:杂质元素的脱除率
已知:杂质元素的脱除率
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】在周期表中,锗和硅位于同主族。四氯化锗(GeCl4)是光导纤维的掺杂剂,其熔点为-49.5℃, 沸点为83.1℃;易水解,对上呼吸道及皮肤有刺激作用。实验室制备四氯化锗的原理是:Ge+2Cl2=GeCl4。某课题组同学拟选择下列装置设计实验制备四氯化锗(部分加热装置和夹持装置省略)。回答下列问题:
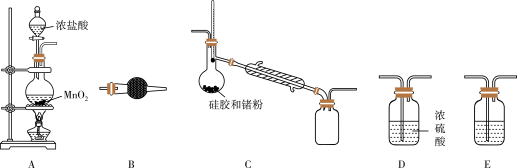
(1)写出A装置中发生反应的化学方程式_______________ 。
(2)若气体从左到右流动,则装置连接顺序为A、_______________ 。
(3)C装置中用于冷凝四氯化锗蒸气的仪器名称是_______________ ,B装置中的试剂是_______________ 。
(4)E装置中的试剂是_______________ ,其作用是_______________ 。
(5)下列有关说法正确的是_______________ 。
①实验中,先通入氯气,后加热C中烧瓶
②C装置中温度计的温度控制在49℃左右
③观察到D瓶有气泡和液面上有黄绿色气体
④C装置中硅胶的主要作用可能是干燥产品
(6)四氯化锗遇水蒸气产生一种强酸和一种弱酸。实验室用足量NaOH溶液吸收尾气中少量四氯化锗气体,写出该反应的化学方程式:__________________ 。
(7)实验中消耗m g 纯锗粉制得a g GeCl4,则锗的利用率为_______________ (用含 m、a 的代数式表示)。

(1)写出A装置中发生反应的化学方程式
(2)若气体从左到右流动,则装置连接顺序为A、
(3)C装置中用于冷凝四氯化锗蒸气的仪器名称是
(4)E装置中的试剂是
(5)下列有关说法正确的是
①实验中,先通入氯气,后加热C中烧瓶
②C装置中温度计的温度控制在49℃左右
③观察到D瓶有气泡和液面上有黄绿色气体
④C装置中硅胶的主要作用可能是干燥产品
(6)四氯化锗遇水蒸气产生一种强酸和一种弱酸。实验室用足量NaOH溶液吸收尾气中少量四氯化锗气体,写出该反应的化学方程式:
(7)实验中消耗m g 纯锗粉制得a g GeCl4,则锗的利用率为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】铝是重要的金属材料,铝土矿(主要成分是Al2O3和少量的SiO2、Fe2O3杂质)是工业上制取铝的原料。实验室模拟工业上以铝土矿为原料制取Al2(SO4)3和铵明矾晶体[NH4Al(SO4)2·12H2O]的工艺流程如图所示:
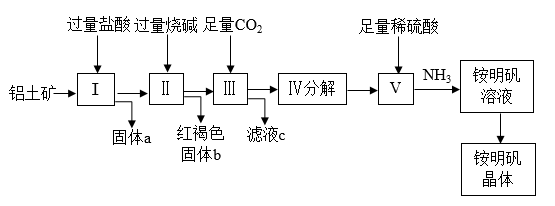
请回答下列问题:
(1)固体a的化学式为______ 。
(2)Ⅲ中通入足量CO2气体发生反应的离子方程式为_______ 。
(3)从铵明矾溶液中获得铵明矾晶体的实验操作依次为(填操作名称)_____ 、冷却结晶、过滤洗涤。
(4)日常生活中常用滤液c的溶质来_______ (任写一点);
(5)向铵明矾NH4Al(SO4)2中加氢氧化钡使硫酸根离子完全沉淀的离子方程式为______ 。

请回答下列问题:
(1)固体a的化学式为
(2)Ⅲ中通入足量CO2气体发生反应的离子方程式为
(3)从铵明矾溶液中获得铵明矾晶体的实验操作依次为(填操作名称)
(4)日常生活中常用滤液c的溶质来
(5)向铵明矾NH4Al(SO4)2中加氢氧化钡使硫酸根离子完全沉淀的离子方程式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】氯化亚铜(CuCl)是一种重要的化工产品,常用作催化剂、杀菌剂、媒染剂、脱色剂等,它难溶于水和乙醇,可溶于浓HCl与氨水形成的混合物,实验室用酸性蚀刻液(含 、
、 、
、 、
、 )和碱性蚀刻液[含
)和碱性蚀刻液[含 、
、 、
、 ]来制备CuCl,实验过程的流程如下:
]来制备CuCl,实验过程的流程如下:

(1)步骤Ⅳ需要控制pH为1~2、80℃下进行,合适的加热方式是_______ 。
(2)步骤Ⅱ过滤得到 固体,下列说法正确的是_______。
固体,下列说法正确的是_______。
(3)步骤Ⅴ为了得到较为纯净的硫酸铜晶体,根据下表中物质的溶解度(单位为g)随温度的变化,写出步骤Ⅴ得到硫酸铜晶体的操作:_______ 。
(4)写出还原过程中发生主要反应的离子方程式:_______ 。
(5)CuCl的定量分析,称取样品0.25g置于预先放入玻璃珠和过量 溶液的锥形瓶中,不断摇动,待样品全部溶解后,加入50mL水,邻菲罗啉指示剂2滴,立即用
溶液的锥形瓶中,不断摇动,待样品全部溶解后,加入50mL水,邻菲罗啉指示剂2滴,立即用 的硫酸铈标准液滴定至绿色出现为终点,消耗标准液20.00mL,发生的反应为
的硫酸铈标准液滴定至绿色出现为终点,消耗标准液20.00mL,发生的反应为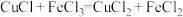 ,
,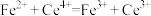 ,则样品的CuCl的质量分数为
,则样品的CuCl的质量分数为_______ 。
 、
、 、
、 、
、 )和碱性蚀刻液[含
)和碱性蚀刻液[含 、
、 、
、 ]来制备CuCl,实验过程的流程如下:
]来制备CuCl,实验过程的流程如下:
(1)步骤Ⅳ需要控制pH为1~2、80℃下进行,合适的加热方式是
(2)步骤Ⅱ过滤得到
 固体,下列说法正确的是_______。
固体,下列说法正确的是_______。| A.为加快过滤速度,得到较干燥的固体,可进行抽滤 |
| B.宜用酸溶液洗涤沉淀 |
| C.在布氏漏斗中放入滤纸后,直接用倾析法转移溶液和沉淀,再打开水龙头抽滤 |
| D.在抽滤装置中洗涤晶体时,为减少晶体的损失,应使洗涤剂快速通过滤纸 |
温度 物质 | 0℃ | 20℃ | 40℃ | 60℃ | 80℃ | 100℃ |
| 氯化铜 | 75 | 80 | 85 | 90 | 100 | 108 |
| 硫酸铜 | 12 | 18 | 30 | 50 | 60 | 87 |
(5)CuCl的定量分析,称取样品0.25g置于预先放入玻璃珠和过量
 溶液的锥形瓶中,不断摇动,待样品全部溶解后,加入50mL水,邻菲罗啉指示剂2滴,立即用
溶液的锥形瓶中,不断摇动,待样品全部溶解后,加入50mL水,邻菲罗啉指示剂2滴,立即用 的硫酸铈标准液滴定至绿色出现为终点,消耗标准液20.00mL,发生的反应为
的硫酸铈标准液滴定至绿色出现为终点,消耗标准液20.00mL,发生的反应为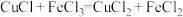 ,
,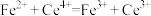 ,则样品的CuCl的质量分数为
,则样品的CuCl的质量分数为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】乙酰苯胺作为一种常用药,具有解热镇痛的效果。实验室制备乙酰苯胺时,可以用苯胺与乙酸酐加热来制取,该反应放热:
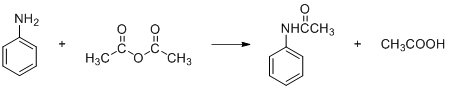
实验步骤
①取5.00mL苯胺,倒入100mL锥形瓶中,加入20mL水,在旋摇下分批加入6.00mL乙酸酐,搅拌均匀。若有结块现象产生,用玻璃棒将块状物研碎,再充分搅拌;
②反应完全后,及时把反应混合物转移到烧杯中,冷却后,抽滤,洗涤,得粗乙酰苯胺固体;
③将粗产品转移至150mL烧杯中,加入适量水配制成80℃的饱和溶液,再加入过量20%的水。稍冷后,加半匙活性炭,搅拌下将溶液煮沸3~5min,_______,冷却结晶,抽滤、洗涤、晾干得乙酰苯胺纯品6.2g。
请回答:
(1)反应温度过高会导致苯胺挥发,下列操作可控制反应温度,防止反应温度升高过快的是_______ 。
A.加20mL水 B.旋摇下分批加入6.0mL乙酸酐 C.玻璃棒将块状物研碎 D.充分搅拌
(2)在步骤②中对粗产品进行洗涤需要用到以下操作:
a.加入洗涤剂至浸没固体;b.洗涤剂缓慢通过;c.关小水龙头;d.开大水龙头;e.重复2~3次。
请对以上操作做出正确的排序_______ 。
(3)横线处的操作步骤是_______ 。
(4)下列说法不正确的是_______ 。
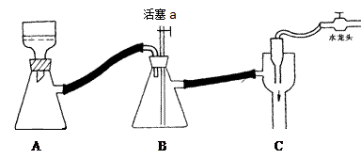
A.步骤③加入过量20%水的目的是防止加热煮沸时,溶剂减少使产品析出导致产率降低
B.冷却时,室温冷却比冰水浴冷却更易得到大颗粒晶体便于抽滤
C.抽滤用如上图装置,为防止倒吸,结束时可先关闭水龙头,后打开活塞a
D.产品可放在表面皿上用热水浴烘干,烘干后可通过测量产品熔点判断产品纯度
(5)该实验的产率是_______ 。

| 密度(g/mL) | 相对分子质量 | 颜色、状态 | 溶解性 | |
| 苯胺 | 1.04 | 93 | 无色油状液体 | 微溶于水, 易溶于乙醇、乙醚 |
| 乙酸酐 | 1.08 | 102 | 无色透明液体 | 遇水缓慢反应生成乙酸 |
| 乙酰苯胺 | 135 | 无色片状晶体, 熔点114℃ | 不溶于冷水,可溶于热 水、乙醇、乙醚 |
①取5.00mL苯胺,倒入100mL锥形瓶中,加入20mL水,在旋摇下分批加入6.00mL乙酸酐,搅拌均匀。若有结块现象产生,用玻璃棒将块状物研碎,再充分搅拌;
②反应完全后,及时把反应混合物转移到烧杯中,冷却后,抽滤,洗涤,得粗乙酰苯胺固体;
③将粗产品转移至150mL烧杯中,加入适量水配制成80℃的饱和溶液,再加入过量20%的水。稍冷后,加半匙活性炭,搅拌下将溶液煮沸3~5min,_______,冷却结晶,抽滤、洗涤、晾干得乙酰苯胺纯品6.2g。
请回答:
(1)反应温度过高会导致苯胺挥发,下列操作可控制反应温度,防止反应温度升高过快的是
A.加20mL水 B.旋摇下分批加入6.0mL乙酸酐 C.玻璃棒将块状物研碎 D.充分搅拌
(2)在步骤②中对粗产品进行洗涤需要用到以下操作:
a.加入洗涤剂至浸没固体;b.洗涤剂缓慢通过;c.关小水龙头;d.开大水龙头;e.重复2~3次。
请对以上操作做出正确的排序
(3)横线处的操作步骤是
(4)下列说法不正确的是

A.步骤③加入过量20%水的目的是防止加热煮沸时,溶剂减少使产品析出导致产率降低
B.冷却时,室温冷却比冰水浴冷却更易得到大颗粒晶体便于抽滤
C.抽滤用如上图装置,为防止倒吸,结束时可先关闭水龙头,后打开活塞a
D.产品可放在表面皿上用热水浴烘干,烘干后可通过测量产品熔点判断产品纯度
(5)该实验的产率是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】甲基橙[ ]是一种常见的酸碱指示剂。实验室通过将对氨基苯磺酸与NaOH作用生成易溶于水的盐,再与
]是一种常见的酸碱指示剂。实验室通过将对氨基苯磺酸与NaOH作用生成易溶于水的盐,再与 重氨化,然后与N,N-二甲基苯胺偶联得到粗产品甲基橙。反应原理如下:
重氨化,然后与N,N-二甲基苯胺偶联得到粗产品甲基橙。反应原理如下:
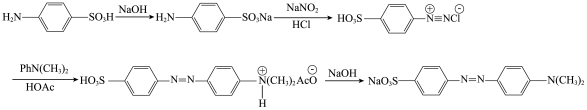
实验过程为

(1)实验过程中为缩短制备时间、加快制备速率,采取的措施有_______ (任写两项)。
(2)淀粉-KI试纸用于检验生成重氮盐时 是否过量。若
是否过量。若 过量,可观察到的现象有
过量,可观察到的现象有_______ ,反应的化学方程式为_______ 。
(3)①选择合适仪器并组装抽滤装置,安装顺序为_______ (填序号)。

②抽滤也称减压过滤,下列说法不正确的是_______ (填序号)。
A.抽滤的原理是利用抽气泵使抽滤瓶中的压强降低,以达到固液分离的目的
B.抽滤的优点是过滤速度快,可得到较干燥的沉淀
C.过滤完之后,先关抽气泵,后去除抽滤瓶接管
③抽滤后,收集晶体,依次用少量水、乙醇、乙醚洗涤,最后压干。用乙醇、乙醚洗涤的目的是_______ ,防止产品变质。
(4)采用_______ 的方法提纯甲基橙粗产品,获得甲基橙精产品。
(5)滴定实验中一般要选择合适的指示剂,下列滴定中能选择甲基橙作指示剂且滴定终点颜色变化正确的是_______ (填序号)。
 ]是一种常见的酸碱指示剂。实验室通过将对氨基苯磺酸与NaOH作用生成易溶于水的盐,再与
]是一种常见的酸碱指示剂。实验室通过将对氨基苯磺酸与NaOH作用生成易溶于水的盐,再与 重氨化,然后与N,N-二甲基苯胺偶联得到粗产品甲基橙。反应原理如下:
重氨化,然后与N,N-二甲基苯胺偶联得到粗产品甲基橙。反应原理如下:
实验过程为

(1)实验过程中为缩短制备时间、加快制备速率,采取的措施有
(2)淀粉-KI试纸用于检验生成重氮盐时
 是否过量。若
是否过量。若 过量,可观察到的现象有
过量,可观察到的现象有(3)①选择合适仪器并组装抽滤装置,安装顺序为

②抽滤也称减压过滤,下列说法不正确的是
A.抽滤的原理是利用抽气泵使抽滤瓶中的压强降低,以达到固液分离的目的
B.抽滤的优点是过滤速度快,可得到较干燥的沉淀
C.过滤完之后,先关抽气泵,后去除抽滤瓶接管
③抽滤后,收集晶体,依次用少量水、乙醇、乙醚洗涤,最后压干。用乙醇、乙醚洗涤的目的是
(4)采用
(5)滴定实验中一般要选择合适的指示剂,下列滴定中能选择甲基橙作指示剂且滴定终点颜色变化正确的是
| 选项 | 滴定管中的溶液 | 锥形瓶中的溶液 | 滴定终点颜色变化 |
| A | NaOH溶液 |  溶液 溶液 | 红色→橙色 |
| B | 盐酸 | 氨水 | 黄色→橙色 |
| C | NaOH溶液 | 盐酸 | 黄色→橙色 |
| D | 酸性 溶液 溶液 |  溶液 溶液 | 红色→橙色 |
您最近一年使用:0次



