铁酸H2FeO4是一种多功能、高效无毒的新型绿色水处理剂,投入水中会迅速发生反应。
(1)H2FeO4中Fe的化合价为________ 。
(2)已知:常温下高铁酸为紫黑色固体,将H2FeO4投入水中,有气体生成,同时有红褐色沉淀产生,则H2FeO4与水反应的化学方程式为________ 。
(3)在工业上制备H2FeO4的方法有多种。
Ⅰ.干法制备的反应原理如下:2FeSO4+6Na2O2=aNa2FeO4+bM↑+2Na2O+2Na2SO4
①b=________ 。
②每生成1molM,该反应转移电子的物质的量为________ mol。
Ⅱ.湿法制备的工艺流程如下;
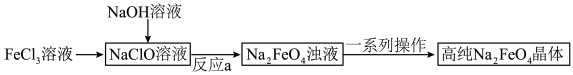
已知:H2FeO4在强碱性溶液中的溶解度较小,高温易分解。
③反应a中,生成物除了H2FeO4外,另一种盐的化学式为________ 。
④一系列操作包括过滤、________ 、________ 。
(1)H2FeO4中Fe的化合价为
(2)已知:常温下高铁酸为紫黑色固体,将H2FeO4投入水中,有气体生成,同时有红褐色沉淀产生,则H2FeO4与水反应的化学方程式为
(3)在工业上制备H2FeO4的方法有多种。
Ⅰ.干法制备的反应原理如下:2FeSO4+6Na2O2=aNa2FeO4+bM↑+2Na2O+2Na2SO4
①b=
②每生成1molM,该反应转移电子的物质的量为
Ⅱ.湿法制备的工艺流程如下;
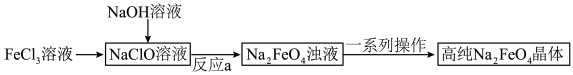
已知:H2FeO4在强碱性溶液中的溶解度较小,高温易分解。
③反应a中,生成物除了H2FeO4外,另一种盐的化学式为
④一系列操作包括过滤、
更新时间:2021-05-24 14:39:06
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】根据反应 8NH3 + 3Cl2 = N2 + 6NH4Cl,回答下列问题:
①用双线桥法标出该反应中电子转移的方向和数目:_____ .
②该反应中_____ 元素被还原,_____ 元素被氧化.
③氧化剂和还原剂的物质的量之比为_____ .
④在该反应中,若有 3mol 电子发生转移,在标准状况下,可生成N2的体积为_____ L.
①用双线桥法标出该反应中电子转移的方向和数目:
②该反应中
③氧化剂和还原剂的物质的量之比为
④在该反应中,若有 3mol 电子发生转移,在标准状况下,可生成N2的体积为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】NH3、NO、NO2都是常见重要的无机物,是工农业生产、环境保护、生命科学等方面的研究热点。
(1)写出氨在催化剂条件下与氧气反应生成NO的化学方程式_____ 。
(2)氮氧化物不仅能形成酸雨,还会对环境产生的危害是形成_____ 。
(3)实验室可用Cu与浓硝酸制取少量NO2,该反应的离子方程式是_____ 。
(4)为了消除NO对环境的污染,根据氧化还原反应原理,可选用NH3使NO转化为两种无毒气体(其中之一是水蒸气),该反应需要催化剂参加,其化学方程式为_____ 。
(5)一定质量的Cu与适量浓硝酸恰好完全反应,生成标准状况下NO2和NO气体均为2240mL。向反应后的溶液中加入NaOH溶液使Cu2+刚好完全沉淀,则生成Cu(OH)2沉淀的质量为_____ 克。
(1)写出氨在催化剂条件下与氧气反应生成NO的化学方程式
(2)氮氧化物不仅能形成酸雨,还会对环境产生的危害是形成
(3)实验室可用Cu与浓硝酸制取少量NO2,该反应的离子方程式是
(4)为了消除NO对环境的污染,根据氧化还原反应原理,可选用NH3使NO转化为两种无毒气体(其中之一是水蒸气),该反应需要催化剂参加,其化学方程式为
(5)一定质量的Cu与适量浓硝酸恰好完全反应,生成标准状况下NO2和NO气体均为2240mL。向反应后的溶液中加入NaOH溶液使Cu2+刚好完全沉淀,则生成Cu(OH)2沉淀的质量为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】氢能是一种洁净的可再生能源。回答下列问题:
(1) 是常见储氢材料,已知其由
是常见储氢材料,已知其由 和
和 构成,
构成, 释放氢气的原理为
释放氢气的原理为 。
。
①根据元素周期律,判断下列说法正确的是___________ 。(填序号)
A.碱性: B.与水反应的剧烈程度:
B.与水反应的剧烈程度:
C.氧化性: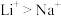 D.密度:
D.密度:
②上述反应中涉及的物质含有共价键的单质是___________ (填化学式,下同),写出氢化锂( )的电子式
)的电子式___________ 。
③若该反应中释放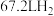 (标况下),则转移的电子数为
(标况下),则转移的电子数为___________ 个。
(2)金属锂也是一种重要的储氢材料,吸氢和放氢原理如下: ,
,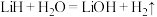
①用锂吸收 (标准状况)
(标准状况) ,生成的
,生成的 与
与 作用,放出的
作用,放出的 用作电池燃料,若能量转化率为80%,则导线中通过电子的物质的量为
用作电池燃料,若能量转化率为80%,则导线中通过电子的物质的量为___________  。
。
②写出 用作燃料电池的反应物,熔融碳酸盐作离子导体的负极反应式
用作燃料电池的反应物,熔融碳酸盐作离子导体的负极反应式___________ 。
(1)
 是常见储氢材料,已知其由
是常见储氢材料,已知其由 和
和 构成,
构成, 释放氢气的原理为
释放氢气的原理为 。
。①根据元素周期律,判断下列说法正确的是
A.碱性:
 B.与水反应的剧烈程度:
B.与水反应的剧烈程度:
C.氧化性:
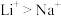 D.密度:
D.密度:
②上述反应中涉及的物质含有共价键的单质是
 )的电子式
)的电子式③若该反应中释放
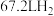 (标况下),则转移的电子数为
(标况下),则转移的电子数为(2)金属锂也是一种重要的储氢材料,吸氢和放氢原理如下:
 ,
,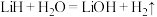
①用锂吸收
 (标准状况)
(标准状况) ,生成的
,生成的 与
与 作用,放出的
作用,放出的 用作电池燃料,若能量转化率为80%,则导线中通过电子的物质的量为
用作电池燃料,若能量转化率为80%,则导线中通过电子的物质的量为 。
。②写出
 用作燃料电池的反应物,熔融碳酸盐作离子导体的负极反应式
用作燃料电池的反应物,熔融碳酸盐作离子导体的负极反应式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】Ⅰ.NaNO2 因外观和食盐相似,又有咸味,容易使人误食中毒。已知 NaNO2能发生反应:2NaNO2+4HI=2NO↑+I2+2NaI+2H2O。
(1)上述反应中氧化剂是_____ 。
(2)根据上述反应,鉴别 NaNO2 和 NaCl。可选用的物质有①水、②碘化钾淀粉试纸③淀粉、④白酒、⑤食醋,你认为必须选用的物质有_____ (填序号)。
(3)请配平以下化学方程式:______
 Al+
Al+ NaNO3+
NaNO3+ NaOH=
NaOH= NaAlO2+
NaAlO2+ N2↑+
N2↑+ H2O
H2O
若反应过程中转移 5 mol 电子,则生成标准状况下 N2 的体积为_____ L。
Ⅱ.“钢是虎,钒是翼,钢含钒犹如虎添翼”,钒是“现代工业的味精”。钒对稀酸是稳定的,但室温下能溶解于浓硝酸中生成 VO2+。
(4)请写出金属钒与浓硝酸反应的离子方程式:_____ 。
(5)V2O5 是两性氧化物,与强碱反应生成钒酸盐(阴离子为 VO43-),溶于强酸生成含钒氧离子(VO2+)的盐。请写出 V2O5 分别与烧碱溶液和稀硫酸反应生成的盐的化学式:_____ 、_____ 。
(1)上述反应中氧化剂是
(2)根据上述反应,鉴别 NaNO2 和 NaCl。可选用的物质有①水、②碘化钾淀粉试纸③淀粉、④白酒、⑤食醋,你认为必须选用的物质有
(3)请配平以下化学方程式:
 Al+
Al+ NaNO3+
NaNO3+ NaOH=
NaOH= NaAlO2+
NaAlO2+ N2↑+
N2↑+ H2O
H2O若反应过程中转移 5 mol 电子,则生成标准状况下 N2 的体积为
Ⅱ.“钢是虎,钒是翼,钢含钒犹如虎添翼”,钒是“现代工业的味精”。钒对稀酸是稳定的,但室温下能溶解于浓硝酸中生成 VO2+。
(4)请写出金属钒与浓硝酸反应的离子方程式:
(5)V2O5 是两性氧化物,与强碱反应生成钒酸盐(阴离子为 VO43-),溶于强酸生成含钒氧离子(VO2+)的盐。请写出 V2O5 分别与烧碱溶液和稀硫酸反应生成的盐的化学式:
您最近一年使用:0次
【推荐2】化学工业为疫情防控提供了强有力的物质支撑。氯的许多化合物既是重要化工原料,又是高效、广谱的灭菌消毒剂。回答下列问题:
(1)Cl2O为淡棕黄色气体,是次氯酸的酸酐,可由新制的HgO和Cl2反应来制备,该反应为歧化反应(氧化剂和还原剂为同一种物质的反应)。上述制备Cl2O的化学方程式为____ 。
(2)ClO2常温下为黄色气体,易溶于水,其水溶液是一种广谱杀菌剂。一种有效成分为NaClO2、NaHSO4、NaHCO3的“二氧化氯泡腾片”,能快速溶于水,溢出大量气泡,得到ClO2溶液。上述过程中,生成ClO2的反应属于歧化反应,每生成1 mol ClO2消耗NaClO2的量为____ mol;产生“气泡”的化学方程式为____ 。
(3)FeO•Cr2O3+Na2CO3+NaNO3 Na2CrO4+Fe2O3+CO2+NaNO2,上述反应配平后FeO•Cr2O3与NaNO3的系数比为
Na2CrO4+Fe2O3+CO2+NaNO2,上述反应配平后FeO•Cr2O3与NaNO3的系数比为____ 。该步骤不能使用陶瓷容器,原因是____ 。
(1)Cl2O为淡棕黄色气体,是次氯酸的酸酐,可由新制的HgO和Cl2反应来制备,该反应为歧化反应(氧化剂和还原剂为同一种物质的反应)。上述制备Cl2O的化学方程式为
(2)ClO2常温下为黄色气体,易溶于水,其水溶液是一种广谱杀菌剂。一种有效成分为NaClO2、NaHSO4、NaHCO3的“二氧化氯泡腾片”,能快速溶于水,溢出大量气泡,得到ClO2溶液。上述过程中,生成ClO2的反应属于歧化反应,每生成1 mol ClO2消耗NaClO2的量为
(3)FeO•Cr2O3+Na2CO3+NaNO3
 Na2CrO4+Fe2O3+CO2+NaNO2,上述反应配平后FeO•Cr2O3与NaNO3的系数比为
Na2CrO4+Fe2O3+CO2+NaNO2,上述反应配平后FeO•Cr2O3与NaNO3的系数比为
您最近一年使用:0次
【推荐3】2020年春“新冠病毒”疫情肆虐,在全国抗击“新冠肺炎”的战役中使用了大量的含氯消毒剂,原料氯气的制备有多种方法。回答下列问题:
(1)用离子方程式表示实验室制取氯气的化学反应原理为:_______
该反应中氧化剂是_______ (填化学式),被氧化的元素是_______ (元素符号)。该反应中氧化剂和还原剂的物质的量之比为_______
(2)配平下列化学方程式并用单线桥法表示电子转移的方向和数目:_______
_______KClO3+_______HC1(浓)→_______KCl+_______C12↑+_______H2O
(3)有一种“地康法”制取氯气,是在氯化铜的催化作用下,在450℃用空气中氧气跟氯化氢反应制氯气。反应原理如下所示。

①分步反应I属于_______ 反应(填四种基本反应类型之一)。
②“地康法”制取氯气的总反应方程式为:_______ 。
③工业生产中常用氨气检查输送氯气的管道是否有Cl2泄漏。若Cl2有泄漏,可以观察到有大量的白烟生成(为NH4Cl固体),同时会生成一种对环境无污染的气体,试写出该反应的化学方程式:_______ 。
(1)用离子方程式表示实验室制取氯气的化学反应原理为:
该反应中氧化剂是
(2)配平下列化学方程式并用单线桥法表示电子转移的方向和数目:
_______KClO3+_______HC1(浓)→_______KCl+_______C12↑+_______H2O
(3)有一种“地康法”制取氯气,是在氯化铜的催化作用下,在450℃用空气中氧气跟氯化氢反应制氯气。反应原理如下所示。

①分步反应I属于
②“地康法”制取氯气的总反应方程式为:
③工业生产中常用氨气检查输送氯气的管道是否有Cl2泄漏。若Cl2有泄漏,可以观察到有大量的白烟生成(为NH4Cl固体),同时会生成一种对环境无污染的气体,试写出该反应的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】铝是一种应用广泛的金属,工业上用Al2O3和冰晶石(Na3AlF6)混合熔融电解制得。
①铝土矿的主要成分是Al2O3和SiO2等。从铝土矿中提炼Al2O3的流程如下:

②以萤石(CaF2)和纯碱为原料制备冰晶石的流程如下:

请回答下列问题:
(1)写出反应①的化学方程式:__________________ 。
(2)滤液Ⅰ中加入CaO生成的沉淀是_______ (填化学式),反应②的离子方程式为______________ 。
(3)写出由气体D制备冰晶石的化学方程式:__________________ 。
①铝土矿的主要成分是Al2O3和SiO2等。从铝土矿中提炼Al2O3的流程如下:

②以萤石(CaF2)和纯碱为原料制备冰晶石的流程如下:

请回答下列问题:
(1)写出反应①的化学方程式:
(2)滤液Ⅰ中加入CaO生成的沉淀是
(3)写出由气体D制备冰晶石的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】氯化磷酸三钠[(Na3PO4·12H2O)4·NaClO]的熔点为62℃,常温下较稳定,受热易分解,具有良好的灭菌、消毒、漂白作用,可广泛地用于医院、餐馆、食品加工等行业。一种以磷矿石[主要成分为Ca5(PO4)3F]为原料生产氯化磷酸三钠的工艺流程如图。

“酸浸”中反应的化学方程式是Ca5(PO4)3F+5H2SO4+5nH2O=3H3PO4+5CaSO4·nH2O↓+HF↑,该操作中使用一定浓度的硫酸,而不用盐酸、硝酸,使用硫酸的优点是___________ 。

“酸浸”中反应的化学方程式是Ca5(PO4)3F+5H2SO4+5nH2O=3H3PO4+5CaSO4·nH2O↓+HF↑,该操作中使用一定浓度的硫酸,而不用盐酸、硝酸,使用硫酸的优点是
您最近一年使用:0次




