用短线“ ”表示共用电子对,用“
”表示共用电子对,用“ ”表示未成键孤对电子的式子叫路易斯结构式.R分子的路易斯结构式可以表示为:则以下叙述错误的是
”表示未成键孤对电子的式子叫路易斯结构式.R分子的路易斯结构式可以表示为:则以下叙述错误的是

 ”表示共用电子对,用“
”表示共用电子对,用“ ”表示未成键孤对电子的式子叫路易斯结构式.R分子的路易斯结构式可以表示为:则以下叙述错误的是
”表示未成键孤对电子的式子叫路易斯结构式.R分子的路易斯结构式可以表示为:则以下叙述错误的是
| A.R为三角锥形 | B.R只能是NH3 |
| C.R不可能是SO3 | D.该分子键角小于 |
20-21高二下·陕西宝鸡·期中 查看更多[5]
陕西省宝鸡市金台区2020-2021学年高二下学期期中考试化学试题(已下线)作业04 分子的空间结构-2021年高二化学暑假作业(人教版2019)新疆新源县第二中学2020-2021学年高二下学期期末联考化学试题(已下线)第2.2.1讲 分子结构的测定和多样性 价层电子对互斥模型-2021-2022学年高二化学链接教材精准变式练(人教版2019选择性必修2)河南省南阳市六校2021-2022学年高二下学期第一次联考化学试题(B)
更新时间:2021-05-25 22:37:56
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列说法正确的是
| A. SO2的水溶液不能导电 | B. SO2的键角比SO3的键角大 |
C. 的空间构型为平面三角形 的空间构型为平面三角形 | D. 中S原子轨道杂化类型为sp3 中S原子轨道杂化类型为sp3 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列说法不正确的是( )
| A.HCHO分子中的C采用sp方式杂化,C有两个未参与杂化的2p轨道形成π键 |
| B.H2O分子的键角不是90° |
| C.甲烷是正四面体形分子,NF3是三角锥形分子 |
| D.BF3的空间构型是平面三角形 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】用价层电子对互斥理论(VSEPR)可以预测许多分子或离子的空间构型,有时也能用来推测键角大小,下列判断正确的是( )
| A.SO2、CS2、HI都是直线型的分子 |
| B.BF3键角为120°,SnBr2键角大于120° |
| C.COCl2、BF3、SO3都是平面三角型的分子 |
| D.PCl3、NH3、PCl5都是三角锥型的分子 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】5-氨基四唑硝酸盐受热迅速生成以 为主的环境友好型气体,并放出大量的热,是制造HTPB火箭推进剂的重要原料,结构简式如图,其中五元环为平面结构,下列说法正确的是
为主的环境友好型气体,并放出大量的热,是制造HTPB火箭推进剂的重要原料,结构简式如图,其中五元环为平面结构,下列说法正确的是

 为主的环境友好型气体,并放出大量的热,是制造HTPB火箭推进剂的重要原料,结构简式如图,其中五元环为平面结构,下列说法正确的是
为主的环境友好型气体,并放出大量的热,是制造HTPB火箭推进剂的重要原料,结构简式如图,其中五元环为平面结构,下列说法正确的是 
| A.基态N原子核外电子的运动状态有3种 |
| B.阴离子的空间构型为三角锥形 |
| C.该化合物中五元环上的5个原子的杂化方式都相同 |
D.该化合物因存在类似于苯分子的大 键,所以非常稳定 键,所以非常稳定 |
您最近一年使用:0次

 分子的VSEPR模型:
分子的VSEPR模型: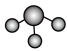
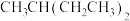 的名称:2-乙基丁烷
的名称:2-乙基丁烷


