完成下列相关反应的化学方程式或离子方程式。
(1)用NaOH溶液除去Mg中混有的杂质Al,相关化学方程式为___________ ;
(2)氯气溶于水,部分发生了反应,相关离子方程式为___________ ;
(3)Al(OH)3可用于治疗胃酸过多,相关化学方程式为___________ ;
(4)实验室用氨水和硫酸铝溶液制取氢氧化铝,离子方程式为___________ ;
(5)实验室加热NH4Cl和Ca(OH)2的混合物制取NH3的化学方程式:___________ 。
(1)用NaOH溶液除去Mg中混有的杂质Al,相关化学方程式为
(2)氯气溶于水,部分发生了反应,相关离子方程式为
(3)Al(OH)3可用于治疗胃酸过多,相关化学方程式为
(4)实验室用氨水和硫酸铝溶液制取氢氧化铝,离子方程式为
(5)实验室加热NH4Cl和Ca(OH)2的混合物制取NH3的化学方程式:
更新时间:2021-06-07 18:12:48
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】已知反应:
①SO3+H2O=H2SO4
②3NO2+H2O=2HNO3+NO
③2F2+2H2O=4HF+O2
④2Na+2H2O=2NaOH+H2↑
⑤Na2O+2HCl=2NaCl+H2O
⑥Al2O3+2NaOH=2NaAlO2+H2O
(1)上述反应不属于氧化还原反应的有___________ (填序号,下同)。H2O被氧化的是___________ ,H2O被还原的是___________ 。
(2)用双线桥法表示反应②的电子转移方向和数目:___________ 。
(3)用单线桥法表示反应③的电子转移方___________ 。
(4)写出反应④的离子方程式:___________ 。
①SO3+H2O=H2SO4
②3NO2+H2O=2HNO3+NO
③2F2+2H2O=4HF+O2
④2Na+2H2O=2NaOH+H2↑
⑤Na2O+2HCl=2NaCl+H2O
⑥Al2O3+2NaOH=2NaAlO2+H2O
(1)上述反应不属于氧化还原反应的有
(2)用双线桥法表示反应②的电子转移方向和数目:
(3)用单线桥法表示反应③的电子转移方
(4)写出反应④的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】分类是学习化学的一种重要方法,科学合理的分类对于系统掌握知识、提高学习效率、解决问题都有着重要的意义。请回答下列问题:
(1)现有以下物质:①Na2SO4固体 ②稀 硫酸 ③熔融 KCl ④KOH 溶液 ⑤CO2 ⑥铜。上述物质中能导电的是_______ (填标号,下同),属于电解质的是_______ 。写出少量的⑤通入④中发生反应的化学方程式: _______ 。
(2)请对下列过程形成的分散系进行分类:
①将植物油加入水中,充分搅拌;
②一定温度下,向蒸馏水中加入氯化钠至恰好饱和;
③将颗粒直径为20nm~30nm的氧化铜分散在塑料中制备的复合材料;
④将饱和氯化铁溶液加入沸水中加热至呈红褐色。
属于溶液的是_______ ( 填标号,下同) ;属于胶体的是_______ 。
(3)常用碘酸钠和亚硫酸氢钠反应来制备单质碘,其化学方程式为2NaIO3+5NaHSO3=3NaHSO4+2Na2SO4+I2+ H2O。
①该反应中被还原的是_______ ( 填化学式,下同) ,还原剂是_______ 。
②用单线桥法标出电子的转移方向和数目:_______ 。
(1)现有以下物质:①Na2SO4固体 ②稀 硫酸 ③熔融 KCl ④KOH 溶液 ⑤CO2 ⑥铜。上述物质中能导电的是
(2)请对下列过程形成的分散系进行分类:
①将植物油加入水中,充分搅拌;
②一定温度下,向蒸馏水中加入氯化钠至恰好饱和;
③将颗粒直径为20nm~30nm的氧化铜分散在塑料中制备的复合材料;
④将饱和氯化铁溶液加入沸水中加热至呈红褐色。
属于溶液的是
(3)常用碘酸钠和亚硫酸氢钠反应来制备单质碘,其化学方程式为2NaIO3+5NaHSO3=3NaHSO4+2Na2SO4+I2+ H2O。
①该反应中被还原的是
②用单线桥法标出电子的转移方向和数目:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】根据氮及其化合物的转化关系回答下列问题:
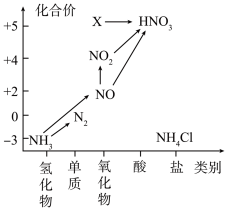
(1)X的化学式为_______ ,从化合价上看,X具有_______ 性(填“氧化”或“还原”)。
(2)实验室常用 与
与 制取氨气,该反应的化学方程式为
制取氨气,该反应的化学方程式为_______ ;下列试剂不能用于干燥 的是
的是_______ (填字母)。
A.浓硫酸 B.碱石灰 C.NaOH固体 D.无水

(1)X的化学式为
(2)实验室常用
 与
与 制取氨气,该反应的化学方程式为
制取氨气,该反应的化学方程式为 的是
的是A.浓硫酸 B.碱石灰 C.NaOH固体 D.无水

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】化学在治理空气污染方面发挥着重要的作用。
I、化石燃料的过度使用是导致酸雨的主要原因。研究表明,NOx、SO2形成酸雨时的转化关系如图所示:
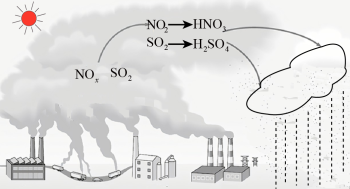
(1)HNO3的电离方程式为_______ 。
(2)SO2会被雨水吸收形成酸雨,这种酸雨在空气中久置酸性增强的原因是_______ (用化学方程式表示)。
Ⅱ、NOx、SO2等均为大气污染物,需处理后才能排放。
(3)用NaOH溶液可以吸收NOx,反应的化学方程式如下:
i.
ii.
①反应i中,每消耗0.3molNO2,转移电子数为_______ 。
②反应ii中,氧化剂和还原剂的物质的量之比为_______ 。
(4)用氨水可以吸收SO2制取铵盐。
①实验室用NH4Cl和Ca(OH)2制取NH3的化学方程式为_______ 。
②用足量氨水吸收SO2的化学方程式为_______ 。
(5)利用NaClO吸收液可在脱除烟气中NOx的同时脱除SO2。研究发现在不同的初始pH条件下,吸收液对流动烟气的脱硫效率都接近100%,而对NO的脱除率如下图所示。
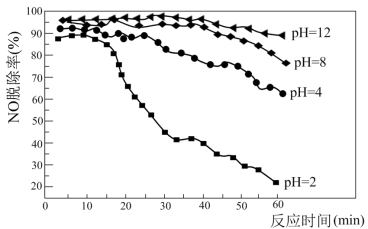
pH=2时,脱除SO2的离子方程式为_______ ;脱硝效率随反应时间的延长而逐渐降低的可能原因是_______ 。
I、化石燃料的过度使用是导致酸雨的主要原因。研究表明,NOx、SO2形成酸雨时的转化关系如图所示:

(1)HNO3的电离方程式为
(2)SO2会被雨水吸收形成酸雨,这种酸雨在空气中久置酸性增强的原因是
Ⅱ、NOx、SO2等均为大气污染物,需处理后才能排放。
(3)用NaOH溶液可以吸收NOx,反应的化学方程式如下:
i.

ii.

①反应i中,每消耗0.3molNO2,转移电子数为
②反应ii中,氧化剂和还原剂的物质的量之比为
(4)用氨水可以吸收SO2制取铵盐。
①实验室用NH4Cl和Ca(OH)2制取NH3的化学方程式为
②用足量氨水吸收SO2的化学方程式为
(5)利用NaClO吸收液可在脱除烟气中NOx的同时脱除SO2。研究发现在不同的初始pH条件下,吸收液对流动烟气的脱硫效率都接近100%,而对NO的脱除率如下图所示。

pH=2时,脱除SO2的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】下图是氮的化合物的“价类二维图”。___________ 。
(2)图中方框中的化学式为___________ ,一水合氨电离可使溶液显碱性,写出一水合氨的电离方程式:___________ 。
(3)写出 和
和 在加热催化剂条件下生成
在加热催化剂条件下生成 的化学方程式:
的化学方程式:___________ 。
(4)向盛有少量 溶液的试管中加入
溶液的试管中加入 溶液并加热,在试管口放一片湿润的红色石蕊试纸,实验现象是
溶液并加热,在试管口放一片湿润的红色石蕊试纸,实验现象是___________ 。
(5)将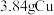 和稀硝酸充分反应,生成的气体体积为
和稀硝酸充分反应,生成的气体体积为___________ L(在标准状况下),用排水法收集该气体,将收集到的气体的试管倒立于水槽中缓缓通入___________ 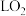 (标准状况)使
(标准状况)使 恰好完全反应。
恰好完全反应。
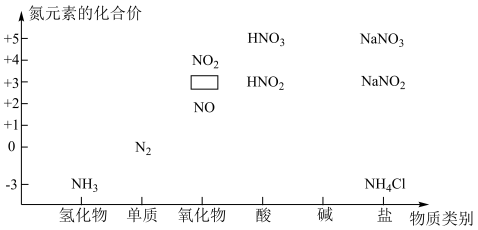
(2)图中方框中的化学式为
(3)写出
 和
和 在加热催化剂条件下生成
在加热催化剂条件下生成 的化学方程式:
的化学方程式:(4)向盛有少量
 溶液的试管中加入
溶液的试管中加入 溶液并加热,在试管口放一片湿润的红色石蕊试纸,实验现象是
溶液并加热,在试管口放一片湿润的红色石蕊试纸,实验现象是(5)将
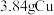 和稀硝酸充分反应,生成的气体体积为
和稀硝酸充分反应,生成的气体体积为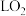 (标准状况)使
(标准状况)使 恰好完全反应。
恰好完全反应。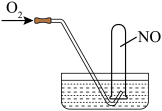
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】按要求回答问题
(1) KAl(SO4)2的电离方程式_______________________ 。
(2)向石蕊试液中通入氯气,起始时溶液变红,一段时间后溶液褪色,则使溶液变红和褪色的微粒分别是______________ 、_________________ (填微粒符号)。
(3) 实验室用质量分数为36.5%,密度为1.19g·cm-3的浓盐酸来配制100ml,2mol/L的稀盐酸,需要用量筒量取_______________ ml 该浓盐酸。
(4)化学方程式H2S+H2SO4(浓)=SO2↑+S↓+2H2O,当生成4.48L (标况) SO2时,转移的电子是__________ mol。
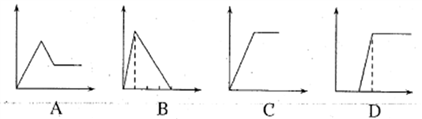
(5)下列四个图象中,横坐标表示加入物质的物质的量,纵坐标表示生成沉淀的量或产生气体的量,从A~D中选择符合各题要求的序号填人表中。
(1) KAl(SO4)2的电离方程式
(2)向石蕊试液中通入氯气,起始时溶液变红,一段时间后溶液褪色,则使溶液变红和褪色的微粒分别是
(3) 实验室用质量分数为36.5%,密度为1.19g·cm-3的浓盐酸来配制100ml,2mol/L的稀盐酸,需要用量筒量取
(4)化学方程式H2S+H2SO4(浓)=SO2↑+S↓+2H2O,当生成4.48L (标况) SO2时,转移的电子是
(5)下列四个图象中,横坐标表示加入物质的物质的量,纵坐标表示生成沉淀的量或产生气体的量,从A~D中选择符合各题要求的序号填人表中。

溶液 | 加入的物质 | 序号 |
①AlCl3溶液 | 通入过量的NH3 | |
②Na2CO3和NaOH的溶液 | 滴入过量的盐酸 | |
③NaAlO2溶液 | 滴加稀硫酸至过量 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】图是依据一定的分类标准,对某些物质与水反应情况进行分类:
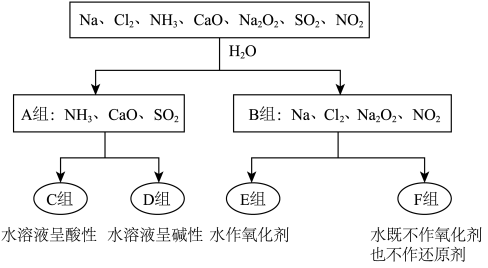
(1)根据物质与水反应的情况,分成A、B组的分类依据是____________ 。
(2)A组中的CaO经常用作食品包装袋中的干燥剂,CaO所属物质类别为______ (填序号)。
①金属氧化物 ②酸性氧化物 ③碱性氧化物 ④两性氧化物
(3)B组物质中,可用作潜水艇供氧剂的是______ (填化学式)。B组→E组反应的离子方程式为______ 。
(4)工业上常用D组中的______ (填化学式)消除C组中物质对大气的污染。
(5)实验室用 制备
制备 时,可选择上述物质中某一物质的水溶液,该过程涉及的离子反应方程式为
时,可选择上述物质中某一物质的水溶液,该过程涉及的离子反应方程式为_______ 。
(6)C组中某一物质可使酸性 溶液褪色,用离子方程式表示溶液褪色的原因
溶液褪色,用离子方程式表示溶液褪色的原因____________ 。
(7)F组中,与水反应氧化剂与还原剂物质的量之比为1:1的物质是____________ (填化学式)。

(1)根据物质与水反应的情况,分成A、B组的分类依据是
(2)A组中的CaO经常用作食品包装袋中的干燥剂,CaO所属物质类别为
①金属氧化物 ②酸性氧化物 ③碱性氧化物 ④两性氧化物
(3)B组物质中,可用作潜水艇供氧剂的是
(4)工业上常用D组中的
(5)实验室用
 制备
制备 时,可选择上述物质中某一物质的水溶液,该过程涉及的离子反应方程式为
时,可选择上述物质中某一物质的水溶液,该过程涉及的离子反应方程式为(6)C组中某一物质可使酸性
 溶液褪色,用离子方程式表示溶液褪色的原因
溶液褪色,用离子方程式表示溶液褪色的原因(7)F组中,与水反应氧化剂与还原剂物质的量之比为1:1的物质是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】(I).请按要求写出下列反应的离子方程式。
(1)铝和烧碱溶液反应___________ 。
(2)向 溶液中滴加过量浓氨水
溶液中滴加过量浓氨水___________ 。
(II).氧气是支持生命活动的一种重要物质,回答下列问题:
(3)氧气的摩尔质量为___________ 。
(4)现有0.5molO2,含氧原子物质的量为___________ ,含氧分子数为___________ 个,其体积(标准状况)为___________ ,其质量为___________ 。
(5)氧气与炭在一定条件下发生反应可以生成 CO和CO2.在标准状况下18.8 g CO与CO2的混合气体,体积为11.2 L。则:CO2和CO的物质的量之比是___________ 。
(1)铝和烧碱溶液反应
(2)向
 溶液中滴加过量浓氨水
溶液中滴加过量浓氨水(II).氧气是支持生命活动的一种重要物质,回答下列问题:
(3)氧气的摩尔质量为
(4)现有0.5molO2,含氧原子物质的量为
(5)氧气与炭在一定条件下发生反应可以生成 CO和CO2.在标准状况下18.8 g CO与CO2的混合气体,体积为11.2 L。则:CO2和CO的物质的量之比是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】回答下列问题:
(1)常用澄清石灰水检验 CO2 气体,反应的离子方程式是_____ 。
(2)请配平反应_____ KClO3+__ HCl=___ KCl + ____ Cl2↑ +____ H2O
(3)人体胃液中有胃酸(0.2%~0.4%的盐酸),起杀菌、帮助消化等作用,但胃酸的量不能过多或过少,它必须控制在一定范围内,当胃酸过多时,医生通常用“小苏打片”或“胃舒平”给病人治疗。
① 用小苏打片(NaHCO3)治疗胃酸过多的离子方程式为________ 。
② 如果病人同时患有胃溃疡,此时最好服用胃舒平[主要成分是Al(OH)3],反应的离子方程式为_______ 。
(4)Fe(OH)3胶体的制备:向沸水中逐滴加入几滴_______ 溶液,继续加热煮沸至液体呈_______ 色,停止加热,即可制得氢氧化铁胶体。其反应的化学方程式为_______ 。
(1)常用澄清石灰水检验 CO2 气体,反应的离子方程式是
(2)请配平反应
(3)人体胃液中有胃酸(0.2%~0.4%的盐酸),起杀菌、帮助消化等作用,但胃酸的量不能过多或过少,它必须控制在一定范围内,当胃酸过多时,医生通常用“小苏打片”或“胃舒平”给病人治疗。
① 用小苏打片(NaHCO3)治疗胃酸过多的离子方程式为
② 如果病人同时患有胃溃疡,此时最好服用胃舒平[主要成分是Al(OH)3],反应的离子方程式为
(4)Fe(OH)3胶体的制备:向沸水中逐滴加入几滴
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】工业上从铝土矿(主要成分是Al2O3还含有SiO2、Fe203等杂质)中提取铝可采用如图工艺流程(反应条件已经省略):

请回答下列问题:
(1)图中I、Ⅱ、Ⅲ步骤中涉及分离溶液与沉淀的实验方法是___________ (填操作名称)。
(2)Al2O3是两性氧化物,SiO2是酸性氧化物,Fe2O3是碱性氧化物,根据它们的性质,判断固体B的成分是__________ (填化学式)。
(3)Fe2O3和盐酸反应的化学方程式为______________ ,沉淀C的化学式是__________ 。
(4)如果溶液D中通入“过量CO2”,改成通入“过量HCl”可以吗? 为什么?____________________ 。

请回答下列问题:
(1)图中I、Ⅱ、Ⅲ步骤中涉及分离溶液与沉淀的实验方法是
(2)Al2O3是两性氧化物,SiO2是酸性氧化物,Fe2O3是碱性氧化物,根据它们的性质,判断固体B的成分是
(3)Fe2O3和盐酸反应的化学方程式为
(4)如果溶液D中通入“过量CO2”,改成通入“过量HCl”可以吗? 为什么?
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】简要回答下列问题
(1)氢氧化铝是典型且常用的抗酸药,具有抗酸、吸着、局部止血和保护溃疡面等作用。请用化学方程式表示其治疗胃酸过多的原理:___________ 。
(2)写出Cu在Cl2中燃烧的化学方程式:___________ 。
(3)如何用化学方法辨别溶液中是否含氯离子:___________ 。
(4)实验室浓硝酸应保存在棕色试剂瓶中并放置在阴凉处,其原因是______ (用化学方程式表示)。

(1)氢氧化铝是典型且常用的抗酸药,具有抗酸、吸着、局部止血和保护溃疡面等作用。请用化学方程式表示其治疗胃酸过多的原理:
(2)写出Cu在Cl2中燃烧的化学方程式:
(3)如何用化学方法辨别溶液中是否含氯离子:
(4)实验室浓硝酸应保存在棕色试剂瓶中并放置在阴凉处,其原因是
您最近一年使用:0次



