(1)氨易溶于水的原因是_______ ;_______ (写出两点即可)。
(2)化学上有一种见解,认为含氧酸的通式可写成(HO)mROn,如果成酸元素R相同,则n值越大,酸性越_______ (填“强”或“弱”)。以下各种含氧酸①H3RO4、②(HO)RO3、③H4RO4、④(HO)2RO2的酸性由强到弱的顺序排列为_______ (填序号)。
(3)为了减缓温室效应,科学家设计反应CO2+4H2=CH4+2H2O以减少空气中CO2的排放量。若有1 mol CH4生成,则有_______ mol σ键和_______ mol π键断裂。
(4)已知氮元素是植物生长所需的元素,常见氮肥有铵盐(NH )、尿素
)、尿素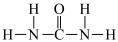 等
等
①尿素分子中四种元素的电负性由大到小顺序是_______ 。
②NH 中H-N-H键角比NH3中H-N-H键角大,原因为
中H-N-H键角比NH3中H-N-H键角大,原因为_______ 。
(5)①与H2O分子互为等电子体的阴离子为_______
②[Zn(CN)4]2-中Zn2+与CN-的C原子形成配位键。不考虑空间构型,[Zn(CN)4]2-的结构可用示意图表示为_______ 。
(6)根据对角线规则,铍(Be)与铝性质相似。对铍及其化合物的推断肯定不正确的是_______
a.常温下铍会在浓硫酸中钝化 b.氯化铍是共价化合物
c.氧化铍坚硬难熔 d.氢氧化铍是强碱
(2)化学上有一种见解,认为含氧酸的通式可写成(HO)mROn,如果成酸元素R相同,则n值越大,酸性越
(3)为了减缓温室效应,科学家设计反应CO2+4H2=CH4+2H2O以减少空气中CO2的排放量。若有1 mol CH4生成,则有
(4)已知氮元素是植物生长所需的元素,常见氮肥有铵盐(NH
 )、尿素
)、尿素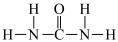 等
等①尿素分子中四种元素的电负性由大到小顺序是
②NH
 中H-N-H键角比NH3中H-N-H键角大,原因为
中H-N-H键角比NH3中H-N-H键角大,原因为(5)①与H2O分子互为等电子体的阴离子为
②[Zn(CN)4]2-中Zn2+与CN-的C原子形成配位键。不考虑空间构型,[Zn(CN)4]2-的结构可用示意图表示为
(6)根据对角线规则,铍(Be)与铝性质相似。对铍及其化合物的推断肯定不正确的是
a.常温下铍会在浓硫酸中钝化 b.氯化铍是共价化合物
c.氧化铍坚硬难熔 d.氢氧化铍是强碱
更新时间:2021-06-01 22:43:42
|
相似题推荐
解答题-无机推断题
|
较难
(0.4)
名校
解题方法
【推荐1】A、B、C、D、E是位于短周期的主族元素。已知:①热稳定性:HmD>HmC;②Cm-、E(m-1)-具有相同的电子层结构;③A与B在同一周期,在该周期所有主族元素中,A的原子半径最大,B的离子半径最小;④A与B质子数之和是D质子数的3倍。依据上述信息用相应的化学用语回答下列问题:
(1)HmDm的电子式为___________________________________ 。
(2)HmC与C元素的具有漂白性的氧化物反应的化学方程式为:_________________________ ,该反应中氧化产物与还原产物的质量之比为:____________________ 。
(3)用电子式表示C的氢化物的形成过程___________________________ ,用电子式表示A2C的形成过程_____________________________________ 。
(4)在A、B、C、E形成的单质中,符合下列转化关系的是________________ (填元素符号)。
(5)由A、B、D三种元素形成的化合物与E元素的最高价含氧酸按物质的量之比2:7反应的离
子方程式:_________________________________________________________ 。
(1)HmDm的电子式为
(2)HmC与C元素的具有漂白性的氧化物反应的化学方程式为:
(3)用电子式表示C的氢化物的形成过程
(4)在A、B、C、E形成的单质中,符合下列转化关系的是
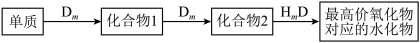
(5)由A、B、D三种元素形成的化合物与E元素的最高价含氧酸按物质的量之比2:7反应的离
子方程式:
您最近半年使用:0次
解答题-无机推断题
|
较难
(0.4)
【推荐2】X、Y、Z、M、R、Q是短周期主族元素,部分信息如下表所示:
(1)R在元素周期表中的位置是__________________ 。
(2)Y与R相比,非金属性较强的是____ (用元素符号表示),下列事实能证明这一结论的是_________ (选填字母序号)。
a.常温下Y的单质呈固态,R的单质呈气态
b.稳定性.XR>YX4
c.Y与R形成的化合物中Y呈正价
(3)根据表中数据推测,Y的原子半径的最小范围是__________________ .
(4)甲、乙是上述部分元素的最高价氧化物对应的水化物,且甲+乙→丙+水。若丙的水溶液呈碱性,则丙的化学式是____________ 或____________ .
| X | Y | Z | M | R | Q | |
| 原子半径/nm | 0.186 | 0.074 | 0.099 | 0.143 | ||
| 主要化合价 | -4,+4 | -2 | -1,+7 | +3 | ||
| 其它 | 阳离子核外无电子 | 无机非金属材料的主角 | 焰色反应呈黄色 |
(2)Y与R相比,非金属性较强的是
a.常温下Y的单质呈固态,R的单质呈气态
b.稳定性.XR>YX4
c.Y与R形成的化合物中Y呈正价
(3)根据表中数据推测,Y的原子半径的最小范围是
(4)甲、乙是上述部分元素的最高价氧化物对应的水化物,且甲+乙→丙+水。若丙的水溶液呈碱性,则丙的化学式是
您最近半年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐3】表中所列字母分别代表一种元素。
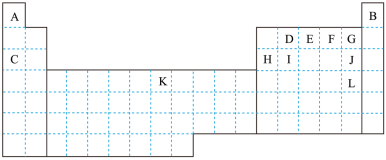
(1)G的气态氢化物比J的气态氢化物_______ (填“稳定”或“不稳定”)。
(2)在一定条件下,A与E可形成一种极易溶于水的气态化合物,其电子式为_______ ;该物质溶于水后的溶液呈_______ 性(填“酸”、“碱”或“中”)。
(3)元素C和H的最高价氧化物对应的水化物相互反应的离子方程式为:_______ 。
(4)元素G和L的原子序数相差:_______ ,它们的氢化物的水溶液酸性相对强的是:_______ (填化学式)
(5)表中A和F两种元素的原子按1:1组成的常见液态化合物的稀溶液易被催化分解,可使用的催化剂为:_______
(6)K为生产、生活中应用最广泛的金属,通常采用的冶炼方法为:_______

(1)G的气态氢化物比J的气态氢化物
(2)在一定条件下,A与E可形成一种极易溶于水的气态化合物,其电子式为
(3)元素C和H的最高价氧化物对应的水化物相互反应的离子方程式为:
(4)元素G和L的原子序数相差:
(5)表中A和F两种元素的原子按1:1组成的常见液态化合物的稀溶液易被催化分解,可使用的催化剂为:_______
| A.MnO2 | B.Na2SO4 | C.FeCl3 | D.KMnO4 |
| A.电解法 | B.热分解法 | C.热还原法 |
您最近半年使用:0次
解答题-结构与性质
|
较难
(0.4)
【推荐1】A、B、C、D为原子序数依次增大的四种元素,A2-和B+具有相同的电子层结构;C、D为同周期元素,C核外电子总数是最外层电子数的3倍;D元素最外层有一个未成对电子。回答下列问题:
(1)四种元素中电负性最大的是_______________ 。(填元素符号),其中C原子的核外电子排布式为__________________________ 。
(2)单质A有两种同素异形体,其中沸点高的是___________ (填分子式),原因是___________________ 。A 和B的氧化物所属的晶体类型分别为__________ 和___________ 。
(3)C和D反应可生成组成比为1∶3的化合物E,E的立体构型为______________ ,中心原子的杂化轨道类型为______________________ 。
(4)化合物D2A的立体构型为_____________ ,中心原子的价层电子对数为_______________ ,单质D与湿润的Na2CO3反应可制备D2A,其化学方程式为____________________________________ 。
(5)A 和B能够形成化合物F,其晶胞结构如图所示,F的化学式为_____________ ;晶胞中A原子的配位数为____________________ 。
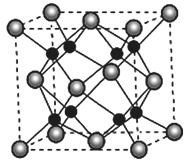
(1)四种元素中电负性最大的是
(2)单质A有两种同素异形体,其中沸点高的是
(3)C和D反应可生成组成比为1∶3的化合物E,E的立体构型为
(4)化合物D2A的立体构型为
(5)A 和B能够形成化合物F,其晶胞结构如图所示,F的化学式为

您最近半年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐2】B和Ni均为新材料的主角。回答下列问题:
(1)基态B原子的核外电子有____ 种空间运动状态;基态Ni原子核外占据最高能层电子的电子云轮廓图的形状为____ 。
(2)硼的卤化物的沸点如表所示:解释表中卤化物之间沸点差异的原因____ 。
(3)镍可做许多有机物与氢气加成的催化剂,例如吡啶(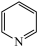 )的反应方程式为:3H2+
)的反应方程式为:3H2+
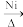
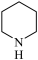 ,吡啶中大Π键可以表示为
,吡啶中大Π键可以表示为____ 。
(4)镍及其化合物常用作有机合成的催化剂,如Ni(PPh3)2,其中Ph表示苯基,PPh3表示分子,PPh3的空间构型为____ ;Ni(PPh3)2晶体中存在的化学键类型有____ (填字母)。
A.离子键 B.极性键 C.非极性键 D.金属键 E.配位键 F.氢键
(5)鉴定Ni2+的特征反应如图:

在1mol鲜红色沉淀中,含有sp2杂化原子的数目为____ 个(阿伏加德罗常数的值为NA)。丁二酮肟中,各元素电负性由大到小的顺序为____ (用元素符号表示)。
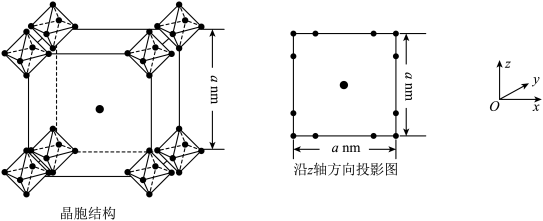
(6)硼化钙可用于新型半导体材料,一种硼化钙的晶胞结构及沿z轴方向的投影图如图所示,硼原子形成的正八面体占据顶角位置。若阿伏加德罗常数的值为NA,晶体密度ρ=____ g•cm-3。
(1)基态B原子的核外电子有
(2)硼的卤化物的沸点如表所示:解释表中卤化物之间沸点差异的原因
| 卤化物 | BF3 | BCl3 | BBr3 |
| 沸点/℃ | -100.3 | 12.5 | 90 |
(3)镍可做许多有机物与氢气加成的催化剂,例如吡啶(
 )的反应方程式为:3H2+
)的反应方程式为:3H2+
 ,吡啶中大Π键可以表示为
,吡啶中大Π键可以表示为(4)镍及其化合物常用作有机合成的催化剂,如Ni(PPh3)2,其中Ph表示苯基,PPh3表示分子,PPh3的空间构型为
A.离子键 B.极性键 C.非极性键 D.金属键 E.配位键 F.氢键
(5)鉴定Ni2+的特征反应如图:

在1mol鲜红色沉淀中,含有sp2杂化原子的数目为
(6)硼化钙可用于新型半导体材料,一种硼化钙的晶胞结构及沿z轴方向的投影图如图所示,硼原子形成的正八面体占据顶角位置。若阿伏加德罗常数的值为NA,晶体密度ρ=

您最近半年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐3】金属镍及其化合物在合成材料以及催化剂等方面应用广泛。请回答下列问题:
(1)基态Ni原子的原子结构示意图为_____ 。
(2)NiO、FeO晶体类型与晶胞与NaCl相同,则NiO晶胞结构中Ni2+的配位数为_____ ;又知Ni2+、Fe2+的离子半径分别为69pm、78pm,则NiO熔点_____ FeO(填“>”、“<”、“=”)。
(3)丁二酮肟常用于检验Ni2+:在稀氨水介质中,丁二酮肟与Ni2+反应可生成鲜红色沉淀,其结构如图甲所示,则该沉淀中Ni2+的配位数为_____ ;元素H、C、N、O、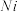 电负性由大到小的顺序为
电负性由大到小的顺序为____ 。
(4)金属镍与镧(La)形成的合金是一种良好的储氢材料,其晶胞结构示意图及晶胞参数如图乙所示。该晶体的化学式为_____ ;晶体密度为_____ g•cm-3(列出含a、b、NA计算表达式,NA表示阿伏加德罗常数的值)。

(1)基态Ni原子的原子结构示意图为
(2)NiO、FeO晶体类型与晶胞与NaCl相同,则NiO晶胞结构中Ni2+的配位数为
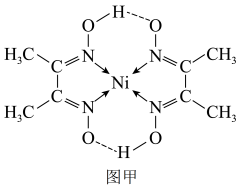
(3)丁二酮肟常用于检验Ni2+:在稀氨水介质中,丁二酮肟与Ni2+反应可生成鲜红色沉淀,其结构如图甲所示,则该沉淀中Ni2+的配位数为
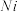 电负性由大到小的顺序为
电负性由大到小的顺序为
(4)金属镍与镧(La)形成的合金是一种良好的储氢材料,其晶胞结构示意图及晶胞参数如图乙所示。该晶体的化学式为

您最近半年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
【推荐1】我国在新材料领域研究的重大突破,为“天宫”空间站的建设提供了坚实的物质基础。“天宫”空间站使用的材料中含有B、C、N、Ni、Cu等元素。回答下列问题:
(1)下列不同状态的硼中,失去一个电子需要吸收能量最多的是____ (填标号,下同),用光谱仪可捕捉到发射光谱的是____ 。
A. B.
B.
C. D.
D.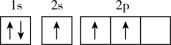
(2)已知高温下Cu2O比CuO更稳定,试从核外电子排布的角度解释:________ 。
(3)类卤素(SCN)2对应的酸有两种,理论上硫氰酸(H−S−C≡N)的沸点低于异硫氰酸(H−N=C=S)的沸点,其主要原因为______ 。
(4)写出与 互为等电子体的一种非极性分子的化学式
互为等电子体的一种非极性分子的化学式_______ 。
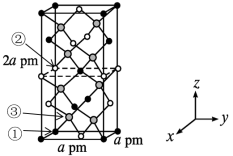
(5)一种高迁移率的新型热电材料由Cd、Sn、As三种原子构成。该晶胞结构如图所示,晶胞棱边夹角均为90°,晶胞中部分原子的坐标如表所示。
①该晶胞中粒子个数比Cd:Sn:As=________ ,找出距离Cd(0,0,0)最近的Sn原子:_______ (用坐标表示)。
②与Sn距离最近的As的数目为______ ,设该化合物的最简式量为M,该晶体的密度为_____  。(列计算式,设NA为阿伏加德罗常数的数值)
。(列计算式,设NA为阿伏加德罗常数的数值)
(1)下列不同状态的硼中,失去一个电子需要吸收能量最多的是
A.
 B.
B.
C.
 D.
D.
(2)已知高温下Cu2O比CuO更稳定,试从核外电子排布的角度解释:
(3)类卤素(SCN)2对应的酸有两种,理论上硫氰酸(H−S−C≡N)的沸点低于异硫氰酸(H−N=C=S)的沸点,其主要原因为
(4)写出与
 互为等电子体的一种非极性分子的化学式
互为等电子体的一种非极性分子的化学式(5)一种高迁移率的新型热电材料由Cd、Sn、As三种原子构成。该晶胞结构如图所示,晶胞棱边夹角均为90°,晶胞中部分原子的坐标如表所示。
| 原子 | 坐标 | ||
| x | y | z | |
| ①Cd | 0 | 0 | 0 |
| ②Sn | 0 | 0 | 1 |
| ③As | 0.25 | 0.25 | 0.25 |

①该晶胞中粒子个数比Cd:Sn:As=
②与Sn距离最近的As的数目为
 。(列计算式,设NA为阿伏加德罗常数的数值)
。(列计算式,设NA为阿伏加德罗常数的数值)
您最近半年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐2】2019年10月1日,在庆祝中华人民共和国成立70周年的阅兵仪式上,最后亮相的DF-31A洲际战略导弹是我国大国地位、国防实力的显著标志。其制作材料包含了Fe、Cr、Ni、C等多种元素。回答下列问题:
(1)基态铁原子的价电子排布式为___ 。
(2)与Cr同周期且基态原子最外层电子数相同的元素,可能位于周期表的___ 区。
(3)实验室常用KSCN溶液、苯酚(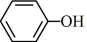 )检验Fe3+。其中N、O、S的第一电离能由大到小的顺序为
)检验Fe3+。其中N、O、S的第一电离能由大到小的顺序为___ (用元素符号表示),苯酚中碳原子的杂化轨道类型为___ 。
(4)铁元素能于CO形成Fe(CO)5。羰基铁[Fe(CO)5]可用作催化剂、汽油抗爆剂等。1mol Fe(CO)5分子中含___ molσ键,与CO互为等电子体的一种离子的化学式为___ 。
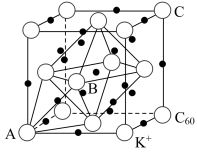
(5)碳的一种同素异形体的晶体可采取非最密堆积,然后在空隙中插入金属离子获得超导体。如图为一种超导体的面心立方晶胞,C60分子占据顶点和面心处,K+占据的是C60分子围成的___ 空隙和___ 空隙(填几何空间构型);若C60分子的坐标参数分别为A(0,0,0),B( ,0,
,0, ),C(1,1,1)等,则距离A位置最近的阳离子的原子坐标参数为
),C(1,1,1)等,则距离A位置最近的阳离子的原子坐标参数为___ 。
(6)Ni可以形成多种氧化物,其中一种NiaO晶体晶胞结构为NaCl型,由于晶体缺陷,a的值为0.88,且晶体中的Ni分别为Ni2+、Ni3+,则晶体中Ni2+与Ni3+的最简整数比为___ ,晶胞参数为428pm,则晶体密度为___ g/cm3(NA表示阿伏加 德罗常数的值,列出表达式)。
(1)基态铁原子的价电子排布式为
(2)与Cr同周期且基态原子最外层电子数相同的元素,可能位于周期表的
(3)实验室常用KSCN溶液、苯酚(
 )检验Fe3+。其中N、O、S的第一电离能由大到小的顺序为
)检验Fe3+。其中N、O、S的第一电离能由大到小的顺序为(4)铁元素能于CO形成Fe(CO)5。羰基铁[Fe(CO)5]可用作催化剂、汽油抗爆剂等。1mol Fe(CO)5分子中含
(5)碳的一种同素异形体的晶体可采取非最密堆积,然后在空隙中插入金属离子获得超导体。如图为一种超导体的面心立方晶胞,C60分子占据顶点和面心处,K+占据的是C60分子围成的
 ,0,
,0, ),C(1,1,1)等,则距离A位置最近的阳离子的原子坐标参数为
),C(1,1,1)等,则距离A位置最近的阳离子的原子坐标参数为
(6)Ni可以形成多种氧化物,其中一种NiaO晶体晶胞结构为NaCl型,由于晶体缺陷,a的值为0.88,且晶体中的Ni分别为Ni2+、Ni3+,则晶体中Ni2+与Ni3+的最简整数比为
您最近半年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐3】(1)基态Na原子中,核外电子占据的最高能层的符号是___________ ,占据该能层电子的电子排布式为______________________ 。
(2)三硫化四磷是黄绿色针状结晶,其结构如图所示。不溶于冷水,溶于叠氮酸、二硫化碳、苯等有机溶剂,在沸腾的NaOH稀溶液中会迅速水解。

①第一电离能:S___________ P(填“>”或“<”,下同),电负性:S___________ P。
②三硫化四磷分子中P原子采取___________ 杂化,与PO3-互为等电子体的化合物分子的化学式为___________ 。
(3)血红素是吡咯(C4H4N)的重要衍生物,血红素(含Fe2+)可用于治疗缺铁性贫血。吡咯和血红素的结构如图所示。

①1mol吡咯分子中所含的σ键总数为___________ 个。分子中的大π键可用 表示
表示 ,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数,则吡咯环中的大π键应表示为
,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数,则吡咯环中的大π键应表示为_______________________________________________________ 。
②血液中的O2是由血红素在人体内形成的血红蛋白来输送的,则血红蛋白中的Fe2+与O2是通过___________ 键相结合。
(4)晶体锌和镉都是体心立方结构,如图所示。

①镉晶体的配位数为___________ 。
②已知锌晶体的密度为dg·cm-3,NA代表阿伏伽德罗常数的值。锌晶体中锌离子之间最近的核间距(D)=___________ nm。
(2)三硫化四磷是黄绿色针状结晶,其结构如图所示。不溶于冷水,溶于叠氮酸、二硫化碳、苯等有机溶剂,在沸腾的NaOH稀溶液中会迅速水解。

①第一电离能:S
②三硫化四磷分子中P原子采取
(3)血红素是吡咯(C4H4N)的重要衍生物,血红素(含Fe2+)可用于治疗缺铁性贫血。吡咯和血红素的结构如图所示。

①1mol吡咯分子中所含的σ键总数为
 表示
表示 ,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数,则吡咯环中的大π键应表示为
,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数,则吡咯环中的大π键应表示为②血液中的O2是由血红素在人体内形成的血红蛋白来输送的,则血红蛋白中的Fe2+与O2是通过
(4)晶体锌和镉都是体心立方结构,如图所示。

①镉晶体的配位数为
②已知锌晶体的密度为dg·cm-3,NA代表阿伏伽德罗常数的值。锌晶体中锌离子之间最近的核间距(D)=
您最近半年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
【推荐1】锰及其化合物用途非常广泛,也是人体的重要微量元素。请回答下列问题:
(1)锰在元素周期表中的位置为_______ 。
(2)下列状态的锰原子或离子中,能用原子发射光谱捕捉以鉴别锰元素的是_______(填序号)。
(3)锰能形成多种化合物如 、
、 、
、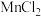 、
、 ,其中磁矩
,其中磁矩 最大的是
最大的是_______ 。(已知 ,其中n为金属离子核外的单电子数)
,其中n为金属离子核外的单电子数)
(4)锰的一种配合物的化学式为[Mn(CO)5(CH3CN)]。配体 与中心原子形成配位键时,提供孤对电子的原子是
与中心原子形成配位键时,提供孤对电子的原子是_______ 原子;该配合物中除氢以外的元素,第一电离能从小到大的顺序为_______ (用元素符号表示)。
(5)水杨醛缩邻氨基苯酚(A)又被称为“锰试剂”,可与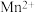 形成黄色的配合物,其同分异构体水杨醛缩邻氨基苯酚(B),沸点较高的是
形成黄色的配合物,其同分异构体水杨醛缩邻氨基苯酚(B),沸点较高的是_______ (填“A”或“B”),原因是_______ 。
A.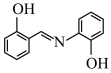 B.
B.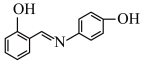
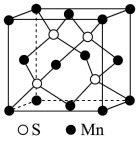
(6)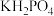 晶体具有优异的非线性光学性能。我国科学工作者制备的超大
晶体具有优异的非线性光学性能。我国科学工作者制备的超大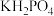 晶体已应用于大功率固体激光器,填补了国家战略空白。分别用○、●表示
晶体已应用于大功率固体激光器,填补了国家战略空白。分别用○、●表示 和
和 ,
, 晶体的四方晶胞如图(a)所示,图(b)、图(c)分别显示的是
晶体的四方晶胞如图(a)所示,图(b)、图(c)分别显示的是 、
、 在晶胞xz面、yz面上的位置:
在晶胞xz面、yz面上的位置:
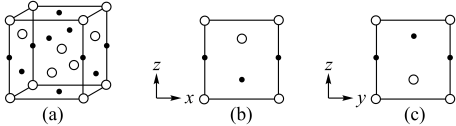
①若晶胞底边的边长均为apm、高为cpm,阿伏加德罗常数的值为NA,晶体的密度_______ 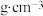 (写出表达式)。
(写出表达式)。
②晶胞在x轴方向的投影图为_______ (填标号)。
A.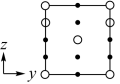 B.
B.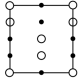 C.
C. D.
D.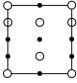
(1)锰在元素周期表中的位置为
(2)下列状态的锰原子或离子中,能用原子发射光谱捕捉以鉴别锰元素的是_______(填序号)。
A.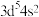 | B.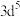 | C.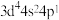 | D.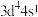 |
 、
、 、
、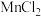 、
、 ,其中磁矩
,其中磁矩 最大的是
最大的是 ,其中n为金属离子核外的单电子数)
,其中n为金属离子核外的单电子数)(4)锰的一种配合物的化学式为[Mn(CO)5(CH3CN)]。配体
 与中心原子形成配位键时,提供孤对电子的原子是
与中心原子形成配位键时,提供孤对电子的原子是(5)水杨醛缩邻氨基苯酚(A)又被称为“锰试剂”,可与
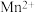 形成黄色的配合物,其同分异构体水杨醛缩邻氨基苯酚(B),沸点较高的是
形成黄色的配合物,其同分异构体水杨醛缩邻氨基苯酚(B),沸点较高的是A.
 B.
B.

(6)
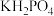 晶体具有优异的非线性光学性能。我国科学工作者制备的超大
晶体具有优异的非线性光学性能。我国科学工作者制备的超大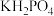 晶体已应用于大功率固体激光器,填补了国家战略空白。分别用○、●表示
晶体已应用于大功率固体激光器,填补了国家战略空白。分别用○、●表示 和
和 ,
,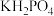 晶体的四方晶胞如图(a)所示,图(b)、图(c)分别显示的是
晶体的四方晶胞如图(a)所示,图(b)、图(c)分别显示的是 、
、 在晶胞xz面、yz面上的位置:
在晶胞xz面、yz面上的位置:
①若晶胞底边的边长均为apm、高为cpm,阿伏加德罗常数的值为NA,晶体的密度
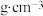 (写出表达式)。
(写出表达式)。②晶胞在x轴方向的投影图为
A.
 B.
B. C.
C. D.
D.
您最近半年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
【推荐2】回答下列问题:
(1)分子中含有两个或两个以上中心原子(离子)的配合物称为多核配合物,如图为Co(Ⅱ)双核配合物的内界。
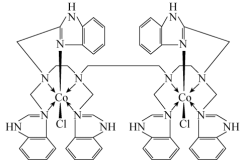
①配合物中每个中心离子的配位数为____ 。
②Co2+的最高能层电子排布式为____ 。
③下列状态的钴中,电离最外层一个电子所需能量最大的是___ (填标号)。
A.[Ar]3d74s1 B.[Ar]3d74s2 C.[Ar]3d74s14p1 D.[Ar]3d74p1
(2)碳酸亚乙酯(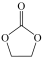 )是某锂离子电池电解液的添加剂,该物质能溶于水,请解释原因
)是某锂离子电池电解液的添加剂,该物质能溶于水,请解释原因____ 。
(3)一氧化锰在医药、冶炼上应用广泛,其立方晶胞如图所示。
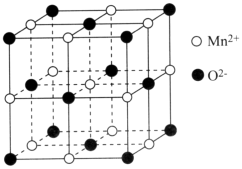
①该晶胞中由O2-形成的正八面体的空隙数为____ 。
②晶胞中距离最近的两个O2-之间的距离为apm,MnO晶体的密度为ρg·cm-3,则阿伏加德罗常数的值为____ (用含a和ρ的代数式表示)(MnO:71)。
(1)分子中含有两个或两个以上中心原子(离子)的配合物称为多核配合物,如图为Co(Ⅱ)双核配合物的内界。

①配合物中每个中心离子的配位数为
②Co2+的最高能层电子排布式为
③下列状态的钴中,电离最外层一个电子所需能量最大的是
A.[Ar]3d74s1 B.[Ar]3d74s2 C.[Ar]3d74s14p1 D.[Ar]3d74p1
(2)碳酸亚乙酯(
 )是某锂离子电池电解液的添加剂,该物质能溶于水,请解释原因
)是某锂离子电池电解液的添加剂,该物质能溶于水,请解释原因(3)一氧化锰在医药、冶炼上应用广泛,其立方晶胞如图所示。

①该晶胞中由O2-形成的正八面体的空隙数为
②晶胞中距离最近的两个O2-之间的距离为apm,MnO晶体的密度为ρg·cm-3,则阿伏加德罗常数的值为
您最近半年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐3】NH3与甲醛CH2O反应可以制备乌洛托品(六亚甲基四胺,分子结构为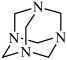 ),乌洛托品可用于有机合成、消毒、杀虫、军事燃料等用途。回答下列有关问题:
),乌洛托品可用于有机合成、消毒、杀虫、军事燃料等用途。回答下列有关问题:
(1)基态氮原子的价电子轨道表达式为___________ ,第三电离能I3(C)___________ I3(N)(填“>”或“<)。
(2)NH3的空间构型为___________ ,CH2O中C采取的杂化类型为___________ 。CH2O中碳氢键与NH3中氮氢键相比,键长较长的是___________ 。
(3)乌洛托品为___________ (填“极性”或“非极性”)分子,分子中的所有N原子呈正四面体分布,所有C原子呈___________ 几何体分布,该分子可与H+形成配位键,电子对给予体为___________ 原子。
(4)在乌洛托品晶体中,分子采取体心立方堆积,其分子配位数为___________ 。乌洛托品比金刚烷(C10H16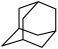 )水溶性更高,理由是
)水溶性更高,理由是___________ 。
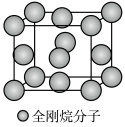
(5)金刚烷晶体采取分子密堆积、晶胞结构如图所示,若晶胞体积为Vnm3,阿伏加德罗常数为L×1023mol-1,则晶体的密度为___________ g/cm3。
 ),乌洛托品可用于有机合成、消毒、杀虫、军事燃料等用途。回答下列有关问题:
),乌洛托品可用于有机合成、消毒、杀虫、军事燃料等用途。回答下列有关问题:(1)基态氮原子的价电子轨道表达式为
(2)NH3的空间构型为
(3)乌洛托品为
(4)在乌洛托品晶体中,分子采取体心立方堆积,其分子配位数为
 )水溶性更高,理由是
)水溶性更高,理由是(5)金刚烷晶体采取分子密堆积、晶胞结构如图所示,若晶胞体积为Vnm3,阿伏加德罗常数为L×1023mol-1,则晶体的密度为

您最近半年使用:0次



