某实验小组学习了反应 的相关知识后,欲探究镁是否与
的相关知识后,欲探究镁是否与 气体反应,设计了下列实验装置图(注:石棉绒是一种耐火材料,不参与反应)。
气体反应,设计了下列实验装置图(注:石棉绒是一种耐火材料,不参与反应)。
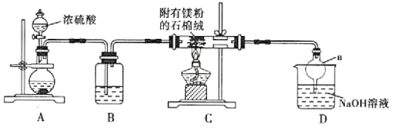
请回答下列问题:
(1)若可供选择的固体试剂有:木炭、铜片、亚硫酸钠固体。则装置A中发生反应的化学方程式为___________ 。
(2)装置B中所盛放的药品是___________ 。
(3)仪器a的名称是___________ ,其作用是___________ 。
(4)实验完毕后观察到石棉绒上有黄色物质生成,将石棉绒及其附着物投入到稀盐酸中,会产生具有臭鸡蛋气味的气态氢化物,则镁与 除了发生反应
除了发生反应 外,还发生的反应是
外,还发生的反应是___________ 。
(5)在装置C、D间插入下图所示装置,可以获得亚硫酸( )溶液。
)溶液。
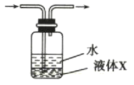
①液体X可以是下列试剂中的___________ (填序号)。
A.苯 B.汽油 C.四氯化碳 D.酒精
②向亚硫酸溶液中通入空气,溶液的pH___________ (填“增大”“减小”或“不变”),其原因是___________ (用化学方程式表示)。
 的相关知识后,欲探究镁是否与
的相关知识后,欲探究镁是否与 气体反应,设计了下列实验装置图(注:石棉绒是一种耐火材料,不参与反应)。
气体反应,设计了下列实验装置图(注:石棉绒是一种耐火材料,不参与反应)。
请回答下列问题:
(1)若可供选择的固体试剂有:木炭、铜片、亚硫酸钠固体。则装置A中发生反应的化学方程式为
(2)装置B中所盛放的药品是
(3)仪器a的名称是
(4)实验完毕后观察到石棉绒上有黄色物质生成,将石棉绒及其附着物投入到稀盐酸中,会产生具有臭鸡蛋气味的气态氢化物,则镁与
 除了发生反应
除了发生反应 外,还发生的反应是
外,还发生的反应是(5)在装置C、D间插入下图所示装置,可以获得亚硫酸(
 )溶液。
)溶液。
①液体X可以是下列试剂中的
A.苯 B.汽油 C.四氯化碳 D.酒精
②向亚硫酸溶液中通入空气,溶液的pH
更新时间:2021-06-22 13:04:52
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】如图是硫元素的常见化合价与部分物质类别的对应关系。请回答下列问题。
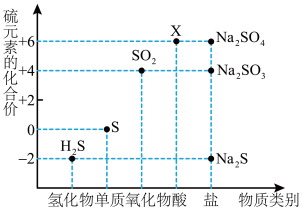
(1)X 的浓溶液与碳在一定条件下可以发生反应,体现了 X 的_______ 性。
(2)仅从硫元素化合价变化的角度分析,图中只有还原性的物质有_______ (填化学式)。
(3)将 H2S 与 SO2混合可生成淡黄色沉淀。该反应中氧化产物与还原产物的物质的量之比为_______ 。
(4)配平下列反应,并用单线桥法标出电子转移的方向和数目______ 。
Na2S+_______Na2SO3+_______H2SO4=_______Na2SO4+_______S↓+_______H2O
(5)下列关于硫及其化合物的叙述正确的是
(6)设 NA为阿伏加德罗常数的值。下列说法正确的是
为了证明铁和硫反应产物中铁的化合价,下面是某同学设计的实验过程的一部分:
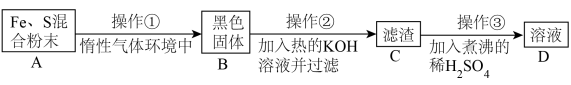
请回答以下问题:
(7)操作②的作用是_______ ,也可改用_______ 。
(8)混合粉末 A 中硫粉过量的原因是_______ 。
(9)下列溶液中通入SO2一定不会产生沉淀的是
(10)区别浓H2SO4和稀H2SO4,既简单又可靠的方法是

(1)X 的浓溶液与碳在一定条件下可以发生反应,体现了 X 的
(2)仅从硫元素化合价变化的角度分析,图中只有还原性的物质有
(3)将 H2S 与 SO2混合可生成淡黄色沉淀。该反应中氧化产物与还原产物的物质的量之比为
(4)配平下列反应,并用单线桥法标出电子转移的方向和数目
Na2S+_______Na2SO3+_______H2SO4=_______Na2SO4+_______S↓+_______H2O
(5)下列关于硫及其化合物的叙述正确的是
| A.试管内壁残留的硫可用酒精洗涤 | B.SO2的水溶液长期放置,酸性会增强 |
| C.SO2有毒,不可以做食品添加剂 | D.浓硫酸在空气中敞口放置,质量会减小 |
| A.1mol 铁单质与足量的硫单质充分反应,转移电子的数目为3NA |
| B.常温下,22.4LSO2与足量的O2反应,生成的SO3分子数为NA |
| C.常温下,将5.6g铁片投入足量的浓硫酸中,铁失去的电子数为0.3NA |
| D.1 molNa2O2与足量H2O反应,转移的电子数为NA |
为了证明铁和硫反应产物中铁的化合价,下面是某同学设计的实验过程的一部分:

请回答以下问题:
(7)操作②的作用是
(8)混合粉末 A 中硫粉过量的原因是
(9)下列溶液中通入SO2一定不会产生沉淀的是
| A.Ba(OH)2 | B.澄清石灰水 | C.Na2S | D.BaCl2 |
| A.各取少许溶液分别放入铜片 | B.分别与石蕊试液作用 |
| C.用玻璃棒各蘸少许液涂在纸上 | D.观察溶液的颜色 |
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】已知非金属单质硫(S)是淡黄色固体粉末,难溶于水。为了验证氯元素的非金属性比硫元素的非金属性强,某化学实验小组设计了如下实验,请回答下列问题:
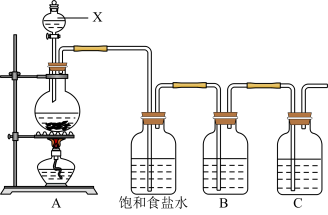
(1)请写出A装置中发生反应的离子方程式___________ 。
(2)饱和食盐水的作用是___________ 。
(3)装置B中盛放的试剂是___________ (选填下列所给试剂的编号),反应离子方程式是___________ 。
A.Na2S溶液 B.Na2SO3溶液 C.Na2SO4溶液
(4)装置C中盛放的是烧碱溶液,目的是:___________ 。
(5)还有哪些事实能够说明氯元素的非金属性比硫元素的非金属性强___________ (填编号)
①HCl比H2S稳定 ②HClO氧化性比H2SO4强
③HClO4酸性比H2SO4强 ④HCl酸性比H2S强
⑤氯原子最外层有7个电子,硫原子最外层有6个电子
⑥铁与Cl2反应生成FeCl3,而硫与铁反应生成FeS
(6)此装置有多种用途,若用此装置验证氯元素的非金属性比碘元素的强,需要在B装置中加入KI溶液,通入一段时间气体后向B中加入少量CCl4,振荡。能够证明氯元素的非金属性比碘元素的强的实验现象是___________ 。

(1)请写出A装置中发生反应的离子方程式
(2)饱和食盐水的作用是
(3)装置B中盛放的试剂是
A.Na2S溶液 B.Na2SO3溶液 C.Na2SO4溶液
(4)装置C中盛放的是烧碱溶液,目的是:
(5)还有哪些事实能够说明氯元素的非金属性比硫元素的非金属性强
①HCl比H2S稳定 ②HClO氧化性比H2SO4强
③HClO4酸性比H2SO4强 ④HCl酸性比H2S强
⑤氯原子最外层有7个电子,硫原子最外层有6个电子
⑥铁与Cl2反应生成FeCl3,而硫与铁反应生成FeS
(6)此装置有多种用途,若用此装置验证氯元素的非金属性比碘元素的强,需要在B装置中加入KI溶液,通入一段时间气体后向B中加入少量CCl4,振荡。能够证明氯元素的非金属性比碘元素的强的实验现象是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】下图为实验室制取氨气,二硫氨气体及相关性质实验的组合装置。
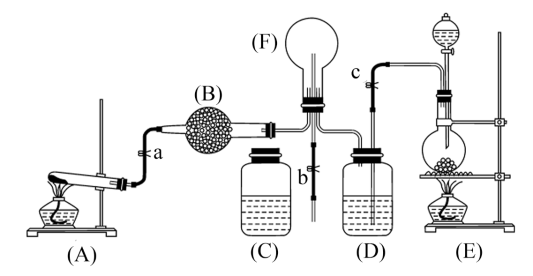
(1)A 、A 、A中取系统的化学反应为如果是E_____ 。
(2)仪器B的名称为_______ ,在此实验中B应加入_______ (写名)。
(3)当F中充满A中气体后,A停止制气,a ,打开弹簧夹c ,使先E中气体通入F中;
①如何测知F中已经充满了中产的气体:_______ ;
② D的作用是干燥的气体,D中盛是_______ (写名称);
③ E后,触发F中气体反应器的操作反应器燃烧瓶与塑料连接,并完成展开实验,F中触发的化学反应为进入,_______ 。
(4)A 、E中产生的气体都是有污染性的,其中包括E中产生尾气的成分为_______ 。

(1)A 、A 、A中取系统的化学反应为如果是E
(2)仪器B的名称为
(3)当F中充满A中气体后,A停止制气,a ,打开弹簧夹c ,使先E中气体通入F中;
①如何测知F中已经充满了中产的气体:
② D的作用是干燥的气体,D中盛是
③ E后,触发F中气体反应器的操作反应器燃烧瓶与塑料连接,并完成展开实验,F中触发的化学反应为进入,
(4)A 、E中产生的气体都是有污染性的,其中包括E中产生尾气的成分为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】二氧化硫是国内外允许使用的一种食品添加剂,可用于食物的增白、防腐等,但必须严格遵守国家有关标准使用。某学习小组设计了如图1装置用于制取SO2并验证其性质。
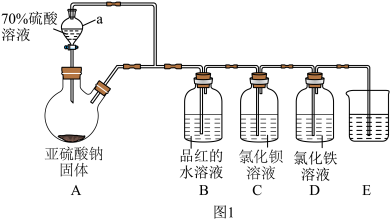
(1)仪器a的名称为_______ 。
(2)装置A中反应的化学方程式_______ 。
(3)烧杯E中的试剂可以是_______ 。(填序号)
a.饱和NaHSO3溶液 b.饱和Na2CO3溶液 c.NaOH溶液 d.饱和NaCl溶液
(4)实验时装置D中溶液变为浅绿色,检验氯化铁未反应完的实验操作及现象是_______ 。
(5)学生甲预测装置C中没有白色沉淀产生,但随着反应的进行,发现装置C中产生了少量白色沉淀(不溶于酸)。为进一步探究产生沉淀的原因,分别用煮沸和未煮沸过的蒸馏水配制的Ba(NO3)2和BaCl2溶液,进行如图2实验:
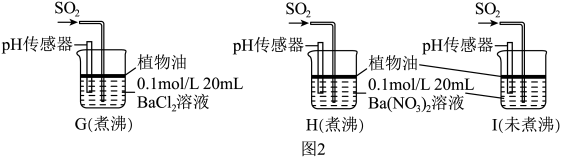
如图2实验中G、H、I烧杯中观察到的现象如表:
①对比C与G不同的现象,请写出C中出现白色沉淀的离子反应方程式_______ 。
②H中的白色沉淀是_______ (写化学式)。
③由I中出现白色沉淀的速率比H中快很多,可推得水溶液中的氧化性_______ >_______ (填化学式)。

(1)仪器a的名称为
(2)装置A中反应的化学方程式
(3)烧杯E中的试剂可以是
a.饱和NaHSO3溶液 b.饱和Na2CO3溶液 c.NaOH溶液 d.饱和NaCl溶液
(4)实验时装置D中溶液变为浅绿色,检验氯化铁未反应完的实验操作及现象是
(5)学生甲预测装置C中没有白色沉淀产生,但随着反应的进行,发现装置C中产生了少量白色沉淀(不溶于酸)。为进一步探究产生沉淀的原因,分别用煮沸和未煮沸过的蒸馏水配制的Ba(NO3)2和BaCl2溶液,进行如图2实验:

如图2实验中G、H、I烧杯中观察到的现象如表:
| 烧杯 | 实验现象 |
| G | 无白色沉淀产生,pH传感器测得溶液pH=5.3 |
| H | 有白色沉淀产生 |
| I | 有白色沉淀产生,I中出现白色沉淀比H中快很多 |
②H中的白色沉淀是
③由I中出现白色沉淀的速率比H中快很多,可推得水溶液中的氧化性
您最近一年使用:0次
【推荐3】如下图所示,某同学利用Na2SO3和浓H2SO4制取SO2并探究其性质。

(1)写出装置B中发生反应的离子方程式:___________ 。
(2)装置C中的实验现象是___________ ,该实验现象说明SO2具有___________ 性。
(3)能验证SO2具有酸性氧化物的通性的实验现象是___________ 。
(4)装置E的目的是探究SO2与品红作用的可逆性,请写出实验操作及现象:___________ 。
(5)探究H2SO3的酸性强于HClO,该同学用如下图所示装置达成实验目的。
A.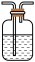 小苏打溶液B.
小苏打溶液B.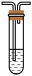 品红溶液C.
品红溶液C.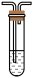 酸性KMnO4溶液D.
酸性KMnO4溶液D.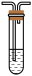 漂白粉溶液
漂白粉溶液
装置的连接顺序为纯净SO2→___________ (选填字母); D中反应的离子方程式为___________ 。

(1)写出装置B中发生反应的离子方程式:
(2)装置C中的实验现象是
(3)能验证SO2具有酸性氧化物的通性的实验现象是
(4)装置E的目的是探究SO2与品红作用的可逆性,请写出实验操作及现象:
(5)探究H2SO3的酸性强于HClO,该同学用如下图所示装置达成实验目的。
A.
 小苏打溶液B.
小苏打溶液B. 品红溶液C.
品红溶液C. 酸性KMnO4溶液D.
酸性KMnO4溶液D. 漂白粉溶液
漂白粉溶液装置的连接顺序为纯净SO2→
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】元素周期表反映元素之间的内在联系,是研究物质性质的重要工具。如表是元素周期表的一部分,请回答下列问题:
(1)元素④、⑤、⑧的简单离子半径由大到小的排序为___________ (填离子符号)。
(2)①和③两种元素组成一种盐X为六核化合物,X含有___________ 键,X的电子式___________ 。
(3)⑥的氧化物和⑧的最高价氧化物对应的水化物反应的离子方程式为___________ 。
(4)由①④⑤⑦四种元素共同组成两种酸式盐,写出两种酸式盐在溶液中发生反应的离子方程式___________ 。
| 周期 | IA | 0 | |||||||
| 1 | ① | IIA | … | IIIA | IVA | VA | VIA | VIIA | |
| 2 | ② | ③ | ④ | ||||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | |||||
(2)①和③两种元素组成一种盐X为六核化合物,X含有
(3)⑥的氧化物和⑧的最高价氧化物对应的水化物反应的离子方程式为
(4)由①④⑤⑦四种元素共同组成两种酸式盐,写出两种酸式盐在溶液中发生反应的离子方程式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】(NH4)2SO4是常见的化肥和化工原料,受热易分解。某兴趣小组拟探究其分解产物。
[查阅资料](NH4)2SO4在260℃和400℃时分解的产物不同。
[实验探究]该小组拟选用如图所示装置进行实验(夹持和加热装置略)。

(1)按图示连接好装置后,检查___________ ,再按图示加入试剂。
(2)实验起止的操作顺序为___________(填序号)。
I.探究(NH4)2SO4在260° C时分解的产物。
已知:装置B中盛有60 mL 0. 5 mol·L-1盐酸,反应一段时间后,观察到装置A中有液体剩余,C中品红溶液不褪色。取下装置B,其中剩余的稀盐酸恰好可与50 mL 0.2 mol·L-1NaOH溶液完全反应,经检验反应后的溶液中无 和
和 ;另检验出A中剩余的液体为NH4HSO4溶液。
;另检验出A中剩余的液体为NH4HSO4溶液。
(3)(NH4)2SO4在260 °C 分解得到的另一产物为___________ (填化学式),参加反应的(NH4)2SO4的质量为___________ g。
II.探究(NH4)2SO4、在400° C时分解的产物。
当装置A中无残留物时,停止实验。观察到装置A、B之间的导气管内有少量白色固体,C中品红溶液褪色。经检验,该白色固体和装置D内溶液中有 、无
、无 。进一步研究发现,气体产物中无氮氧化物。
。进一步研究发现,气体产物中无氮氧化物。
(4)装置A、B之间的导气管内的少量白色固体为___________ (填化学式)。
(5)检验装置D内溶液中有 、无
、无 的实验操作和现象为
的实验操作和现象为___________ 。
(6)(NH4)2SO4在400 °C分解的产物除NH3、H2O外,还有___________ (填化学式)。
[查阅资料](NH4)2SO4在260℃和400℃时分解的产物不同。
[实验探究]该小组拟选用如图所示装置进行实验(夹持和加热装置略)。

(1)按图示连接好装置后,检查
(2)实验起止的操作顺序为___________(填序号)。
| A.加热装置A |
| B.停止通入N2 |
| C.通入N2排尽空气 |
| D.停止加热 |
I.探究(NH4)2SO4在260° C时分解的产物。
已知:装置B中盛有60 mL 0. 5 mol·L-1盐酸,反应一段时间后,观察到装置A中有液体剩余,C中品红溶液不褪色。取下装置B,其中剩余的稀盐酸恰好可与50 mL 0.2 mol·L-1NaOH溶液完全反应,经检验反应后的溶液中无
 和
和 ;另检验出A中剩余的液体为NH4HSO4溶液。
;另检验出A中剩余的液体为NH4HSO4溶液。(3)(NH4)2SO4在260 °C 分解得到的另一产物为
II.探究(NH4)2SO4、在400° C时分解的产物。
当装置A中无残留物时,停止实验。观察到装置A、B之间的导气管内有少量白色固体,C中品红溶液褪色。经检验,该白色固体和装置D内溶液中有
 、无
、无 。进一步研究发现,气体产物中无氮氧化物。
。进一步研究发现,气体产物中无氮氧化物。(4)装置A、B之间的导气管内的少量白色固体为
(5)检验装置D内溶液中有
 、无
、无 的实验操作和现象为
的实验操作和现象为(6)(NH4)2SO4在400 °C分解的产物除NH3、H2O外,还有
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】下表为元素周期表的一部分,表中所列的字母分别代表一种化学元素,回答(1)(2)两小问
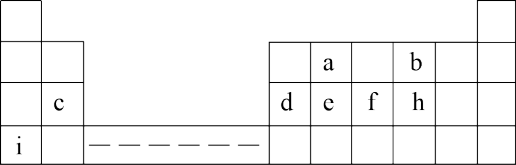
(1)a、b、c三种元素的原子半径由大到小的顺序是___________ (填元素符号);
(2)c、d、e三种元素最高价氧化物对应水化物中碱性最强的是_____ (填水化物的化学式)。
(3)配平下列离子方程式___ __MnO + ____Cl- + ____H+= ______Mn2+ + _____Cl2 + ___H2O
+ ____Cl- + ____H+= ______Mn2+ + _____Cl2 + ___H2O
(4)保持洁净安全的生存环境已成为全人类的共识。二氧化硫是引起酸雨的一种主要物质,必须严格控制排放。酸雨降落到地面后,其中的亚硫酸在空气中被氧气逐渐氧化生成硫酸,使酸性进一步增强,写出这一过程的化学方程式:___________ 。

(1)a、b、c三种元素的原子半径由大到小的顺序是
(2)c、d、e三种元素最高价氧化物对应水化物中碱性最强的是
(3)配平下列离子方程式
 + ____Cl- + ____H+= ______Mn2+ + _____Cl2 + ___H2O
+ ____Cl- + ____H+= ______Mn2+ + _____Cl2 + ___H2O(4)保持洁净安全的生存环境已成为全人类的共识。二氧化硫是引起酸雨的一种主要物质,必须严格控制排放。酸雨降落到地面后,其中的亚硫酸在空气中被氧气逐渐氧化生成硫酸,使酸性进一步增强,写出这一过程的化学方程式:
您最近一年使用:0次

 开展探究实验。
开展探究实验。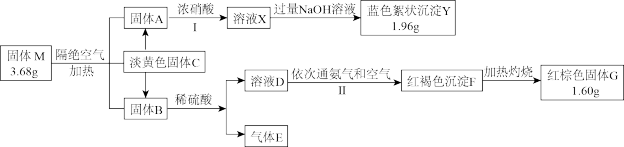
 为单质且可通过直接化合的方式生成
为单质且可通过直接化合的方式生成 和
和 。
。 中金属阳离子的方法
中金属阳离子的方法 脱除工业生产尾气中的气体
脱除工业生产尾气中的气体 ,可以生成
,可以生成

