在微生物作用的条件下,NH 经过两步反应被氧化成NO
经过两步反应被氧化成NO 。两步反应的能量变化示意图如图:
。两步反应的能量变化示意图如图:
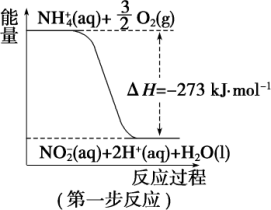
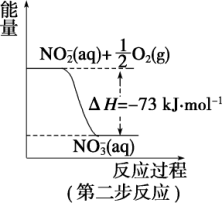
(1)第一步反应是_______ (填“放热”或“吸热”)反应,判断依据是_______ 。
(2)1 molNH (aq) 全部氧化成NO
(aq) 全部氧化成NO (aq)的热化学方程式是
(aq)的热化学方程式是_______ 。
(3) HCl与氧气在催化剂加热条件下可生成氯气:4HCl+O2 2Cl2+2H2O,已知某些化学键的键能数据如表:
2Cl2+2H2O,已知某些化学键的键能数据如表:
该反应的热化学方程式是_______ 。
(4)FeCl3溶液常用于腐蚀印刷电路铜板,发生的反应为2FeCl3+Cu=2FeCl2+CuCl2,若将此反应设计成原电池,则正极所用的电极材料为_______ ;电解质溶液为_______ ,当电路中转移0.2 mol 电子时,被腐蚀的负极反应物的质量为_______ g。
 经过两步反应被氧化成NO
经过两步反应被氧化成NO 。两步反应的能量变化示意图如图:
。两步反应的能量变化示意图如图:

(1)第一步反应是
(2)1 molNH
 (aq) 全部氧化成NO
(aq) 全部氧化成NO (aq)的热化学方程式是
(aq)的热化学方程式是(3) HCl与氧气在催化剂加热条件下可生成氯气:4HCl+O2
 2Cl2+2H2O,已知某些化学键的键能数据如表:
2Cl2+2H2O,已知某些化学键的键能数据如表:| 化学键 | H-Cl | O=O | Cl-Cl | H-O |
| 键能/kJ/mol | 431 | 498 | 243 | 463 |
该反应的热化学方程式是
(4)FeCl3溶液常用于腐蚀印刷电路铜板,发生的反应为2FeCl3+Cu=2FeCl2+CuCl2,若将此反应设计成原电池,则正极所用的电极材料为
更新时间:2021-06-24 10:44:06
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】按要求回答下列问题:
(1)已知:
则:H2(g) + Cl2(g) 2HCl(g) ΔH=
2HCl(g) ΔH=____________________ kJ/mol
(2)已知:乙醇C2H6O的燃烧热为1411.0 kJ/mol,则乙醇燃烧的热化学方程式可表示为_____________________________________________
(3)在200℃、101kPa时,H2与碘蒸气作用生成2molHI气体,放出14.9 kJ的热量。热化学方程式可表示为___________________________________________________________________ 。
(4)已知:① 2CH3OH(l)+3O2(g) 2CO2(g)+4H2O(g) ΔH1=-1275.6 kJ/mol
2CO2(g)+4H2O(g) ΔH1=-1275.6 kJ/mol
② 2CO(g)+O2(g) 2CO2(g) ΔH2=-566.0 k J/mol
2CO2(g) ΔH2=-566.0 k J/mol
③ H2O(g) H2O(l) ΔH3=-44.0 kJ/mol
H2O(l) ΔH3=-44.0 kJ/mol
甲醇CH3OH燃烧生成一氧化碳和液态水的热化学方程式是__________________________________ 。
(1)已知:
| 1 mol分子中的化学键断时需要吸收能量/kJ | H2(g) | Cl2(g) | HCl(g) |
| 436 | 243 | 431 |
则:H2(g) + Cl2(g)
 2HCl(g) ΔH=
2HCl(g) ΔH=(2)已知:乙醇C2H6O的燃烧热为1411.0 kJ/mol,则乙醇燃烧的热化学方程式可表示为
(3)在200℃、101kPa时,H2与碘蒸气作用生成2molHI气体,放出14.9 kJ的热量。热化学方程式可表示为
(4)已知:① 2CH3OH(l)+3O2(g)
 2CO2(g)+4H2O(g) ΔH1=-1275.6 kJ/mol
2CO2(g)+4H2O(g) ΔH1=-1275.6 kJ/mol② 2CO(g)+O2(g)
 2CO2(g) ΔH2=-566.0 k J/mol
2CO2(g) ΔH2=-566.0 k J/mol③ H2O(g)
 H2O(l) ΔH3=-44.0 kJ/mol
H2O(l) ΔH3=-44.0 kJ/mol甲醇CH3OH燃烧生成一氧化碳和液态水的热化学方程式是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】写出下列反应的热化学方程式:
(1)CuCl(s)与O2反应生成CuCl2(s)和一种黑色固体。在25℃、101KPa下,已知该反应每消耗1molCuCl(s),放热44.4kJ,该反应的热化学方程式是___________ 。
(2)晶体硅(熔点1410℃)是良好的半导体材料。由粗硅制纯硅过程如下:
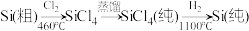
在上述由SiCl4制纯硅的反应中,测得每生成1.12kg纯硅需吸收akJ热量,写出该反应的热化学方程式:___________ 。
(3)化合物AX3和单质X2在一定条件下反应可生成化合物AX5.已知AX3的熔点和沸点分别为-93.6℃和76℃,AX5的熔点为167℃。室温时AX3与气体X2反应生成lmolAX5,放出热量123.8kJ。该反应的热化学方程式为___________ 。
(1)CuCl(s)与O2反应生成CuCl2(s)和一种黑色固体。在25℃、101KPa下,已知该反应每消耗1molCuCl(s),放热44.4kJ,该反应的热化学方程式是
(2)晶体硅(熔点1410℃)是良好的半导体材料。由粗硅制纯硅过程如下:
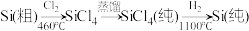
在上述由SiCl4制纯硅的反应中,测得每生成1.12kg纯硅需吸收akJ热量,写出该反应的热化学方程式:
(3)化合物AX3和单质X2在一定条件下反应可生成化合物AX5.已知AX3的熔点和沸点分别为-93.6℃和76℃,AX5的熔点为167℃。室温时AX3与气体X2反应生成lmolAX5,放出热量123.8kJ。该反应的热化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】Ⅰ.回答下列问题:
(1)在微生物作用的条件下,NH 经过两步反应被氧化成NO
经过两步反应被氧化成NO 。两步反应的能量变化示意图如图:
。两步反应的能量变化示意图如图:

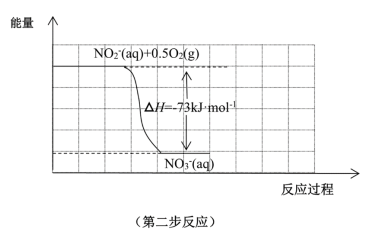
①第一步反应是____ (填“放热”或“吸热”)反应。
②1molNH (aq)全部氧化成NO
(aq)全部氧化成NO (aq)的热化学方程式是
(aq)的热化学方程式是___ 。
(2)已知H2(g)+Br2(l)=2HBr(g) ΔH=-72kJ·mol-1,蒸发1molBr2(l)需要吸收的能量为30kJ,其他相关数据如表:
则表中a=____ 。
Ⅱ.工业生产硝酸的尾气中含有氮氧化物NOx(NO和NO2的混合物),对生态环境和人类健康带来较大的威胁。
(3)工业上可用氨催化吸收法处理NOx,反应原理如下:4xNH3+6NOx (2x+3)N2+6xH2O。某化学兴趣小组模拟该处理过程的实验装置如图:
(2x+3)N2+6xH2O。某化学兴趣小组模拟该处理过程的实验装置如图:
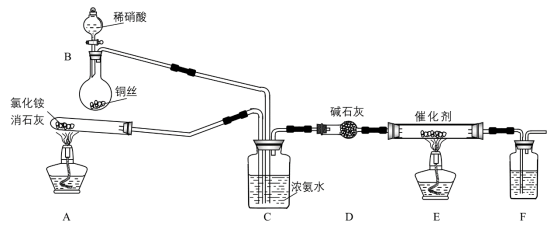
①装置E中发生反应的化学方程式为____ 。
②装置D中碱石灰的作用是____ 。
(4)工业上也常用Na2CO3溶液吸收法处理NOx。
已知:NO不能与Na2CO3溶液反应。
NO+NO2+Na2CO3=2NaNO2+CO2(Ⅰ)
2NO2+Na2CO3=NaNO2+NaNO3+CO2(Ⅱ)
当NOx被Na2CO3溶液完全吸收时,x的值不可能是____ (填字母)。
A.1.3 B.1.6 C.1.8
(1)在微生物作用的条件下,NH
 经过两步反应被氧化成NO
经过两步反应被氧化成NO 。两步反应的能量变化示意图如图:
。两步反应的能量变化示意图如图:

①第一步反应是
②1molNH
 (aq)全部氧化成NO
(aq)全部氧化成NO (aq)的热化学方程式是
(aq)的热化学方程式是(2)已知H2(g)+Br2(l)=2HBr(g) ΔH=-72kJ·mol-1,蒸发1molBr2(l)需要吸收的能量为30kJ,其他相关数据如表:
| 物质 | H2(g) | Br2(g) | HBr(g) |
| lmol分子中的化学键断裂时需要吸收的能量(kJ) | 436 | 200 | a |
Ⅱ.工业生产硝酸的尾气中含有氮氧化物NOx(NO和NO2的混合物),对生态环境和人类健康带来较大的威胁。
(3)工业上可用氨催化吸收法处理NOx,反应原理如下:4xNH3+6NOx
 (2x+3)N2+6xH2O。某化学兴趣小组模拟该处理过程的实验装置如图:
(2x+3)N2+6xH2O。某化学兴趣小组模拟该处理过程的实验装置如图:
①装置E中发生反应的化学方程式为
②装置D中碱石灰的作用是
(4)工业上也常用Na2CO3溶液吸收法处理NOx。
已知:NO不能与Na2CO3溶液反应。
NO+NO2+Na2CO3=2NaNO2+CO2(Ⅰ)
2NO2+Na2CO3=NaNO2+NaNO3+CO2(Ⅱ)
当NOx被Na2CO3溶液完全吸收时,x的值不可能是
A.1.3 B.1.6 C.1.8
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】请根据要求回答问题:
(1)图1所示是1molNO2(g)和1molCO(g)反应生成CO2(g)和NO(g)过程中的能量变化示意图,已知E1=134kJ•mol-1、E2=368kJ•mol-1。若在反应体系中加入催化剂,反应速率增大,E1_____ (填“增大”“减小”或“不变”,后同),△H_____ 。请写出NO2(g)和CO(g)反应生成CO2(g)和NO(g)的热化学方程式:_____ 。

(2)已知:①CH3OH(g)+H2O(g)=CO2(g)+3H2(g) △H=+49.0kJ•mol-1
②CH3OH(g)+ O2(g)=CO2(g)+2H2(g) △H=-192.9kJ•mol-1
O2(g)=CO2(g)+2H2(g) △H=-192.9kJ•mol-1
③H2O(g)=H2O(l) △H=-44kJ•mol-1
则甲醇蒸气燃烧生成液态水的热化学方程式为_____ 。
(3)如表所示是部分化学键的键能:
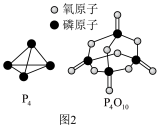
已知白磷的燃烧热为dkJ•mol-1,白磷及其完全燃烧的产物的结构如图2所示,则表中x=______ (用含a、b、c、d的代数式表示)。
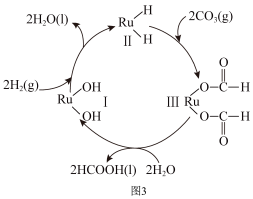
(4)钌及其化合物在合成工业上有广泛用途,如图3所示是用钌(Ru)基催化剂催化合成甲酸的过程示意图。每生成92g液态HCOOH放出62.4kJ的热量。根据图3写出生成1molHCOOH(l)的反应的热化学方程式:______ 。
(1)图1所示是1molNO2(g)和1molCO(g)反应生成CO2(g)和NO(g)过程中的能量变化示意图,已知E1=134kJ•mol-1、E2=368kJ•mol-1。若在反应体系中加入催化剂,反应速率增大,E1

(2)已知:①CH3OH(g)+H2O(g)=CO2(g)+3H2(g) △H=+49.0kJ•mol-1
②CH3OH(g)+
 O2(g)=CO2(g)+2H2(g) △H=-192.9kJ•mol-1
O2(g)=CO2(g)+2H2(g) △H=-192.9kJ•mol-1③H2O(g)=H2O(l) △H=-44kJ•mol-1
则甲醇蒸气燃烧生成液态水的热化学方程式为
(3)如表所示是部分化学键的键能:
| 化学键 | P-P | P-O | O=O | P=O |
| 键能/(kJ•mol-1) | a | b | c | x |

(4)钌及其化合物在合成工业上有广泛用途,如图3所示是用钌(Ru)基催化剂催化合成甲酸的过程示意图。每生成92g液态HCOOH放出62.4kJ的热量。根据图3写出生成1molHCOOH(l)的反应的热化学方程式:

您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】根据所学知识,回答问题。
(1)硫酸的水溶液呈酸性(用电离方程式解析):___________ 。
(2) 水溶液呈碱性(用电离方程式解析):
水溶液呈碱性(用电离方程式解析):___________ 。
(3) 溶液呈碱性的原因(用离子方程式解析):
溶液呈碱性的原因(用离子方程式解析):___________ 。
(4) 溶液呈酸性的原因(用离子方程式解析):
溶液呈酸性的原因(用离子方程式解析):___________ 。
(5)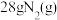 与适量的
与适量的 反应,生成
反应,生成 ,吸收
,吸收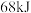 热量,写出其热化学方程式:
热量,写出其热化学方程式:___________ 。
(6)已知反应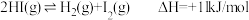 ,
, 、
、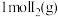 分子中化学键断裂时分别需要吸收
分子中化学键断裂时分别需要吸收 、
、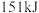 的能量,则
的能量,则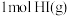 分子中化学键断裂时需吸收的能量为
分子中化学键断裂时需吸收的能量为___________ kJ。
(1)硫酸的水溶液呈酸性(用电离方程式解析):
(2)
 水溶液呈碱性(用电离方程式解析):
水溶液呈碱性(用电离方程式解析):(3)
 溶液呈碱性的原因(用离子方程式解析):
溶液呈碱性的原因(用离子方程式解析):(4)
 溶液呈酸性的原因(用离子方程式解析):
溶液呈酸性的原因(用离子方程式解析):(5)
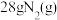 与适量的
与适量的 反应,生成
反应,生成 ,吸收
,吸收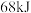 热量,写出其热化学方程式:
热量,写出其热化学方程式:(6)已知反应
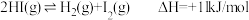 ,
, 、
、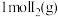 分子中化学键断裂时分别需要吸收
分子中化学键断裂时分别需要吸收 、
、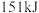 的能量,则
的能量,则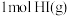 分子中化学键断裂时需吸收的能量为
分子中化学键断裂时需吸收的能量为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】将Zn棒和Cu棒用导线连接后,放入某电解质溶液中,构成如图所示装置。试回答下列问题:
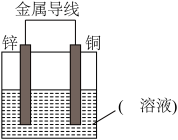
Ⅰ.若电解质溶液为稀硫酸,
(1)Zn棒为原电池的___ 极,其电极反应式为:___ 。
(2)Cu棒为原电池的___ 极,其电极反应式为:___ 。
Ⅱ.以KOH溶液为电解质溶液,写出甲烷燃料电池的电极反应式
(3)负极反应式:___ 。
正极反应式:___ 。

Ⅰ.若电解质溶液为稀硫酸,
(1)Zn棒为原电池的
(2)Cu棒为原电池的
Ⅱ.以KOH溶液为电解质溶液,写出甲烷燃料电池的电极反应式
(3)负极反应式:
正极反应式:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】甲、乙两位同学均想利用原电池反应验证金属的活动性顺序,并探究产物的有关性质。甲、乙同学设计的原电池如图所示,请回答下列问题:
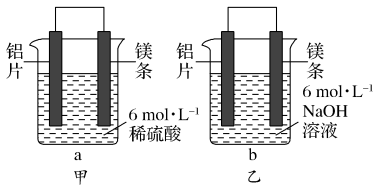
(1)a池中正极上的实验现象是____ 。
(2)b池中总反应的离子方程式为____ 。
(3)该实验证明了“利用金属活动性顺序直接判断原电池正负极”,这种做法__ (填“可靠”或“不可靠”),若不可靠,请提出另一种判断原电池正负极的可行方案____ (若你认为可靠,此空可不作答)。
(4)一段时间后,乙学生将b池两极取出,然后取少许b池溶液于烧杯中,向其中逐滴滴加6mol·L-1H2SO4溶液直至过量,可能观察到的现象是___ 。各阶段对应的离子方程式分别是____ 。

(1)a池中正极上的实验现象是
(2)b池中总反应的离子方程式为
(3)该实验证明了“利用金属活动性顺序直接判断原电池正负极”,这种做法
(4)一段时间后,乙学生将b池两极取出,然后取少许b池溶液于烧杯中,向其中逐滴滴加6mol·L-1H2SO4溶液直至过量,可能观察到的现象是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】把锌片和铁片放在盛有稀食盐水和酚酞试液混合溶液的玻璃皿中(如图所示平面图)
(1)经过一段时间后,两个实验中,首先观察到溶液变红的区域是_____ (填代号)。

A.Ⅰ和Ⅲ附近 B.Ⅰ和Ⅳ附近 C.Ⅱ和Ⅲ附近 D.Ⅱ和Ⅳ附近
(2)试用化学用语(电极反应或离子方程式)和简练的语言说明相应区域溶液变红的原因:
图1:_____________________
图2:_____________________
(3)从金属腐蚀的角度看,铁片受到防腐保护的是_____ (填“图1”或“图2”),这种防护方法的名称为_________ 。
(1)经过一段时间后,两个实验中,首先观察到溶液变红的区域是

A.Ⅰ和Ⅲ附近 B.Ⅰ和Ⅳ附近 C.Ⅱ和Ⅲ附近 D.Ⅱ和Ⅳ附近
(2)试用化学用语(电极反应或离子方程式)和简练的语言说明相应区域溶液变红的原因:
图1:
图2:
(3)从金属腐蚀的角度看,铁片受到防腐保护的是
您最近一年使用:0次



