根据流程回答问题
Ⅰ.从海带(含KI)中提取碘,某研究性学习小组设计了如图流程:
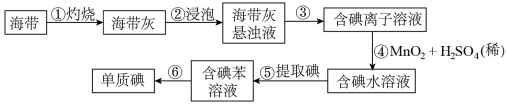
(1)步骤①中灼烧海带是在_______ (填仪器名称)中进行
(2)步骤③、⑤、⑥的实验操作分别为_______
(3)反应④的离子方程式为_______
(4)步骤⑤向碘水中加入苯,振荡静置后的现象为_______
Ⅱ.工业上用铝土矿(含有 杂质的
杂质的 ,
, 的含量a %)为原料冶炼铝的工艺流程如(所加试剂均过量):
的含量a %)为原料冶炼铝的工艺流程如(所加试剂均过量):
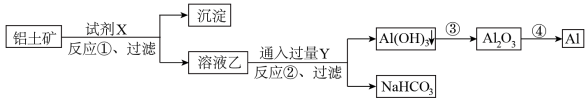
(5)试剂X是_______ (填化学式),上述反应过程中耗能最多的是_______ (填序号)
(6)反应②的离子方程式_______
(7)工业上生产1t Al,在生产过程中Al的损失率为b %,理论上需投入铝土矿_______ t(列出计算表达式即可)
Ⅰ.从海带(含KI)中提取碘,某研究性学习小组设计了如图流程:

(1)步骤①中灼烧海带是在
(2)步骤③、⑤、⑥的实验操作分别为
(3)反应④的离子方程式为
(4)步骤⑤向碘水中加入苯,振荡静置后的现象为
Ⅱ.工业上用铝土矿(含有
 杂质的
杂质的 ,
, 的含量a %)为原料冶炼铝的工艺流程如(所加试剂均过量):
的含量a %)为原料冶炼铝的工艺流程如(所加试剂均过量):
(5)试剂X是
(6)反应②的离子方程式
(7)工业上生产1t Al,在生产过程中Al的损失率为b %,理论上需投入铝土矿
更新时间:2021/07/02 08:43:46
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】以铝土矿(主要成分为 ,含
,含 和
和 等杂质)为原料制备耐高温陶瓷材料
等杂质)为原料制备耐高温陶瓷材料 和
和 晶体的工艺流程如下:
晶体的工艺流程如下:
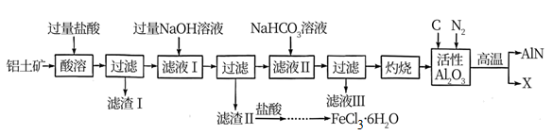
(1)滤渣Ⅰ的主要成分是_______ (填化学式)。
(2)向滤液Ⅰ中加入过量 溶液,发生的离子反应有
溶液,发生的离子反应有 、
、_______ 、_______ 。
(3)滤液Ⅲ中的 可以转化为
可以转化为 循环使用,写出转化反应的化学方程式:
循环使用,写出转化反应的化学方程式:_______ 。
(4)在滤渣Ⅱ中加入盐酸,经过蒸发浓缩、_______ 、_______ 、低温干燥,获得 晶体。
晶体。
(5)X是一种有毒气体,当制备AlN的反应中产生3.36L(标准状况)气体X时,制得AlN________ g。
 ,含
,含 和
和 等杂质)为原料制备耐高温陶瓷材料
等杂质)为原料制备耐高温陶瓷材料 和
和 晶体的工艺流程如下:
晶体的工艺流程如下:
(1)滤渣Ⅰ的主要成分是
(2)向滤液Ⅰ中加入过量
 溶液,发生的离子反应有
溶液,发生的离子反应有 、
、(3)滤液Ⅲ中的
 可以转化为
可以转化为 循环使用,写出转化反应的化学方程式:
循环使用,写出转化反应的化学方程式:(4)在滤渣Ⅱ中加入盐酸,经过蒸发浓缩、
 晶体。
晶体。(5)X是一种有毒气体,当制备AlN的反应中产生3.36L(标准状况)气体X时,制得AlN
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】明矾[KAl(SO4)2·12H2O]在生产、生活中有广泛用途:饮用水的净化;造纸工业上作施胶剂;食品工业的发酵剂等。利用炼铝厂的废料——铝灰(含Al、Al2O3及少量SiO2和FeO·xFe2O3)可制备明矾。工艺流程如下:回答下列问题:
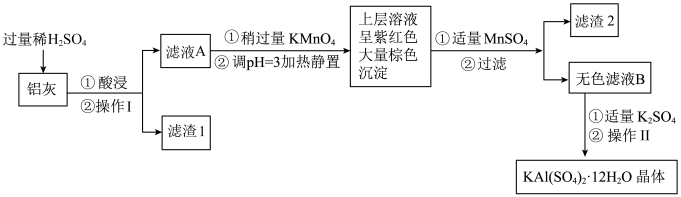
(1)明矾净水的原理是______________ (用离子方程式表示)。
(2)操作Ⅰ是________ ,操作Ⅱ是蒸发浓缩、__________ 、过滤、洗涤、干燥。
(3)检验滤液A中是否存在Fe2+的试剂是__________ (只用一种试剂)。
(4)将铝灰投入氢氧化钠溶液中生成气体的化学方程式是__________ ,在滤液A中加入高锰酸钾发生反应的离子方程式为(该条件下MnO4-转化为Mn2+):_______ 。
(5)已知:在pH=3、加热条件下,MnO4-可与Mn2+反应生成MnO2。加入MnSO4发生反应的离子方程式为:________ ,滤渣2含有的物质是________ 。

(1)明矾净水的原理是
(2)操作Ⅰ是
(3)检验滤液A中是否存在Fe2+的试剂是
(4)将铝灰投入氢氧化钠溶液中生成气体的化学方程式是
(5)已知:在pH=3、加热条件下,MnO4-可与Mn2+反应生成MnO2。加入MnSO4发生反应的离子方程式为:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】铝土矿(主要成分为Al2O3,还含有SiO2、Fe2O3)是工业上制备金属铝的主要原料。工业上提取铝的工艺流程如下:
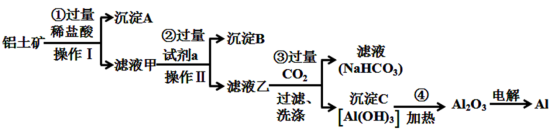
(1)沉淀A的化学式是_______ ,试剂a的化学式为_______ 。
(2)步骤③中通入过量CO2,产生沉淀C的离子方程式为_______
(3)步骤③中通入过量CO2气体而不加入过量盐酸的理由是_______
(4)Al2O3中所含的化学键的类型为_______
(5)在生活中,常利用Al与Fe2O3间的铝热反应来进行焊接钢轨。除了Fe2O3,铝粉还可以与很多金属氧化物组成铝热剂。下列氧化物中不能与铝粉组成铝热剂的是_______ 。
a.MgO b.ZnO c.Fe3O4 d.Na2O
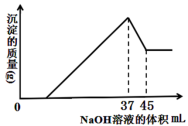
(6)准确称取8g铝土矿样品,加入过量的稀盐酸充分反应,过滤,然后,向滤液中加入10mol·L-1的NaOH溶液,产生沉淀的质量与加入NaOH溶液的体积关系如图所示,则样品中Al2O3的百分含量为___ 。

(1)沉淀A的化学式是
(2)步骤③中通入过量CO2,产生沉淀C的离子方程式为
(3)步骤③中通入过量CO2气体而不加入过量盐酸的理由是
(4)Al2O3中所含的化学键的类型为
(5)在生活中,常利用Al与Fe2O3间的铝热反应来进行焊接钢轨。除了Fe2O3,铝粉还可以与很多金属氧化物组成铝热剂。下列氧化物中不能与铝粉组成铝热剂的是
a.MgO b.ZnO c.Fe3O4 d.Na2O
(6)准确称取8g铝土矿样品,加入过量的稀盐酸充分反应,过滤,然后,向滤液中加入10mol·L-1的NaOH溶液,产生沉淀的质量与加入NaOH溶液的体积关系如图所示,则样品中Al2O3的百分含量为

您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】铟(49In)是一种重要的稀有金属,其主要用于液晶显示屏和半导体的生产。从铅、锌的冶炼过程中产生的高铟烟灰(主要含ZnO、PbO、Fe2O3、In2O3、In2S3)中提取铟的流程如图:
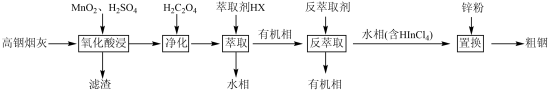
已知:滤液中铟以In3+的形式存在,In3+与Al3+相似,易水解。
回答下列问题:
(1)49In的原子结构示意图为____ 。
(2)“氧化酸浸”过程中In2S3难溶物中的疏元素被氧化为S,MnO2转化为Mn2+,该反应的离子方程式为____ ,滤渣的主要成分含有____ (填化学式)。
(3)有机萃取剂HX在酸性溶液中只萃取三价金属离子。“净化”时加入H2C2O4的作用是____ ,可用____ 溶液检测此离子是否除尽。
(4)“萃取”时发生反应In3++3HX InX3+3H+,pH对萃取率影响较大.不同的c(H+)下有机萃取剂对In3+的萃取率及分层时间如表:
InX3+3H+,pH对萃取率影响较大.不同的c(H+)下有机萃取剂对In3+的萃取率及分层时间如表:
注:*表示有悬浊液产生,导致两相分层困难。
pH过高,萃取率较低的原因是____ (用离子方程式表达)。pH过低,萃取率下降的原因是____ (用文字描述)。
(5)反萃取剂是___ (填化学式)。“置换”步骤发生的主要反应的化学方程式为____ 。
(6)粗铟可用电解法进行提纯,提纯过程中粗铟作____ (填“阴极”或“阳极”)。
(7)上述流程中可循环使用的物质有____ (填化学式)。

已知:滤液中铟以In3+的形式存在,In3+与Al3+相似,易水解。
回答下列问题:
(1)49In的原子结构示意图为
(2)“氧化酸浸”过程中In2S3难溶物中的疏元素被氧化为S,MnO2转化为Mn2+,该反应的离子方程式为
(3)有机萃取剂HX在酸性溶液中只萃取三价金属离子。“净化”时加入H2C2O4的作用是
(4)“萃取”时发生反应In3++3HX
 InX3+3H+,pH对萃取率影响较大.不同的c(H+)下有机萃取剂对In3+的萃取率及分层时间如表:
InX3+3H+,pH对萃取率影响较大.不同的c(H+)下有机萃取剂对In3+的萃取率及分层时间如表:| c(H+)/mol·L-1 | 分层时间/min | 萃取率/% |
| 0.01 | 10* | 69.6 |
| 0.1 | 6 | 77.2 |
| 1.0 | 4 | 94.1 |
| 2.0 | 4 | 82.1 |
| 2.5 | 3 | 74.1 |
pH过高,萃取率较低的原因是
(5)反萃取剂是
(6)粗铟可用电解法进行提纯,提纯过程中粗铟作
(7)上述流程中可循环使用的物质有
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】硫代硫酸钠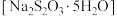 一种无色透明的晶体,易溶于水,难溶于乙醇,具有强烈的还原性,酸性条件下不稳定。常用作定影剂、还原剂、媒染剂、麦杆和毛的漂白剂以及纸浆漂白时的脱氯剂。某小组制备硫代硫酸钠的实验装置图如下:
一种无色透明的晶体,易溶于水,难溶于乙醇,具有强烈的还原性,酸性条件下不稳定。常用作定影剂、还原剂、媒染剂、麦杆和毛的漂白剂以及纸浆漂白时的脱氯剂。某小组制备硫代硫酸钠的实验装置图如下:
(1)仪器X的名称为___________ ;实验过程中若该装置中压强过大,可观察到的现象是___________ 。
(2)室温下,用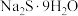 配制
配制 溶液,溶解需要较长时间且易变质产生浑浊,加热溶解时则会产生臭鸡蛋气味的
溶液,溶解需要较长时间且易变质产生浑浊,加热溶解时则会产生臭鸡蛋气味的___________ 气体(填化学式)。故 和
和 混合溶液的配制方法是:先将
混合溶液的配制方法是:先将 溶于温水,再将
溶于温水,再将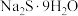 溶于
溶于 溶液中,得到透明溶液,且溶解时间大大缩短,目的是
溶液中,得到透明溶液,且溶解时间大大缩短,目的是___________ 。
(3)“单向阀”的作用是___________ 。
(4)实验过程中,随着 的通入,三颈烧瓶中先析出浅黄色沉淀且逐渐增多,然后沉淀量保持不变并产生无色无味气体,再后沉淀逐渐减少至溶液澄清,三步反应的总反应为
的通入,三颈烧瓶中先析出浅黄色沉淀且逐渐增多,然后沉淀量保持不变并产生无色无味气体,再后沉淀逐渐减少至溶液澄清,三步反应的总反应为 。用注射器取样检测溶液的
。用注射器取样检测溶液的 约为7时,需停止向三颈烧瓶中通入
约为7时,需停止向三颈烧瓶中通入 气体,其操作是
气体,其操作是___________ ;若继续通入 ,又会产生浅黄色沉淀,反应的离子方程式为
,又会产生浅黄色沉淀,反应的离子方程式为___________ 。
(5)反应混合液经低温(45~47℃)蒸发浓缩、加入试剂Y并冷却结晶、过滤、试剂Y洗涤、干燥,得到 粗产品,试剂Y的化学名称是
粗产品,试剂Y的化学名称是___________ ;提纯粗产品常用的实验方法的名称是___________ 。
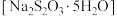 一种无色透明的晶体,易溶于水,难溶于乙醇,具有强烈的还原性,酸性条件下不稳定。常用作定影剂、还原剂、媒染剂、麦杆和毛的漂白剂以及纸浆漂白时的脱氯剂。某小组制备硫代硫酸钠的实验装置图如下:
一种无色透明的晶体,易溶于水,难溶于乙醇,具有强烈的还原性,酸性条件下不稳定。常用作定影剂、还原剂、媒染剂、麦杆和毛的漂白剂以及纸浆漂白时的脱氯剂。某小组制备硫代硫酸钠的实验装置图如下: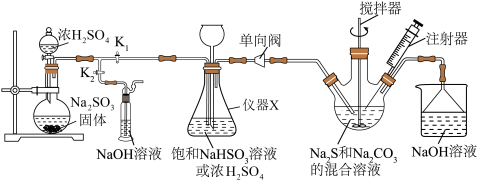
(1)仪器X的名称为
(2)室温下,用
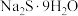 配制
配制 溶液,溶解需要较长时间且易变质产生浑浊,加热溶解时则会产生臭鸡蛋气味的
溶液,溶解需要较长时间且易变质产生浑浊,加热溶解时则会产生臭鸡蛋气味的 和
和 混合溶液的配制方法是:先将
混合溶液的配制方法是:先将 溶于温水,再将
溶于温水,再将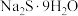 溶于
溶于 溶液中,得到透明溶液,且溶解时间大大缩短,目的是
溶液中,得到透明溶液,且溶解时间大大缩短,目的是(3)“单向阀”的作用是
(4)实验过程中,随着
 的通入,三颈烧瓶中先析出浅黄色沉淀且逐渐增多,然后沉淀量保持不变并产生无色无味气体,再后沉淀逐渐减少至溶液澄清,三步反应的总反应为
的通入,三颈烧瓶中先析出浅黄色沉淀且逐渐增多,然后沉淀量保持不变并产生无色无味气体,再后沉淀逐渐减少至溶液澄清,三步反应的总反应为 。用注射器取样检测溶液的
。用注射器取样检测溶液的 约为7时,需停止向三颈烧瓶中通入
约为7时,需停止向三颈烧瓶中通入 气体,其操作是
气体,其操作是 ,又会产生浅黄色沉淀,反应的离子方程式为
,又会产生浅黄色沉淀,反应的离子方程式为(5)反应混合液经低温(45~47℃)蒸发浓缩、加入试剂Y并冷却结晶、过滤、试剂Y洗涤、干燥,得到
 粗产品,试剂Y的化学名称是
粗产品,试剂Y的化学名称是
您最近一年使用:0次
【推荐3】Ni(OH)2作为合成镍钴锰三元电极材料的原料,工业上可用红土镍矿(主要成分为NiO、FeO、Fe2O3、MgO和SiO2)制备,工艺流程如图所示。回答下列问题:
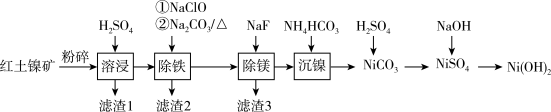
(1)“滤渣l”的成分为_____________ (写化学式)。
(2)“除铁"中,加入NaClO的目的是将溶液中的Fe2+氧化为Fe3+,写出该反应的离子方程式:________________________________________ ,为了证明加入NaClO已足量,可选择的试剂是__________ (填字母标号)。
a.KSCN溶液、氯水 b.K3[Fe(CN)6]溶液 c.NaOH溶液
(3)Na2CO3的作用是调节溶液pH使Fe3+沉淀,根据下表的数据,则调节溶液pH的范围是__________ 。
(4)“除镁”中,若溶液pH过小,Mg2+沉淀不完全,用化学平衡移动的原理解释其原因是______________________________________________________________________ 。
(5)“沉镍”时有能使澄清石灰水变浑浊的气体生成,则该反应的离子方程式为_______ 。

(1)“滤渣l”的成分为
(2)“除铁"中,加入NaClO的目的是将溶液中的Fe2+氧化为Fe3+,写出该反应的离子方程式:
a.KSCN溶液、氯水 b.K3[Fe(CN)6]溶液 c.NaOH溶液
(3)Na2CO3的作用是调节溶液pH使Fe3+沉淀,根据下表的数据,则调节溶液pH的范围是
金属离子 | Fe2+ | Fe3+ | Mg2+ | Ni2+ |
开始沉淀的pH | 6.3 | 1.5 | 8.9 | 6.9 |
沉淀完全的pH | 8.3 | 2.8 | 10.9 | 8.9 |
(4)“除镁”中,若溶液pH过小,Mg2+沉淀不完全,用化学平衡移动的原理解释其原因是
(5)“沉镍”时有能使澄清石灰水变浑浊的气体生成,则该反应的离子方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】实验室从含碘废液(除H2O外,含有CC14、I2、I-等)中回收碘,其实验过程如下:
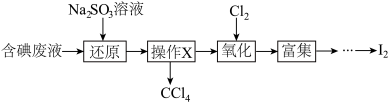
(1)向含碘废液中加入稍过量的Na2SO3溶液,将废液中的I2还原为I-,其离子方程式为________ 该操作将I2还原为I-的目的是________ 。
(2)操作X的名称为___________ 。
(3)氧化时,在三颈烧瓶中将含I-的水溶液用盐酸调至pH约为2,缓慢通入Cl2,在40℃左右反应(实验装置如下图所示)。实验控制在较低温度下进行的原因是___________ ;锥形瓶里盛放的溶液为_______ 。


(1)向含碘废液中加入稍过量的Na2SO3溶液,将废液中的I2还原为I-,其离子方程式为
(2)操作X的名称为
(3)氧化时,在三颈烧瓶中将含I-的水溶液用盐酸调至pH约为2,缓慢通入Cl2,在40℃左右反应(实验装置如下图所示)。实验控制在较低温度下进行的原因是


您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】食盐中的加碘剂选用的是碘酸钾( )。实验室可用采用如图实验流程制备碘酸钾。
)。实验室可用采用如图实验流程制备碘酸钾。

(1)操作①的名称为______ 。
(2)操作②包括萃取、______ ,萃取后分液漏斗内的现象______ 。
(3)试剂X是18电子分子,写出溶液M与X反应的离子反应方程式为______ 。
(4)由单质碘制备碘酸钾的化学方程式为______ 。
(5)同学甲认为操作③可以用蒸馏的方法,但同学乙认为不可以,原因是______ ;于是改用下列分离法,具体流程如下:
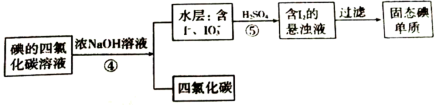
该分离方法叫______ 法,写出反应⑤离子反应方程式______ 。
 )。实验室可用采用如图实验流程制备碘酸钾。
)。实验室可用采用如图实验流程制备碘酸钾。
(1)操作①的名称为
(2)操作②包括萃取、
(3)试剂X是18电子分子,写出溶液M与X反应的离子反应方程式为
(4)由单质碘制备碘酸钾的化学方程式为
(5)同学甲认为操作③可以用蒸馏的方法,但同学乙认为不可以,原因是

该分离方法叫
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐3】海洋是一座巨大的化学资源宝库,如图是从海水中或海产品中提取若干种化学物质的流程图。
Ⅰ.海水提溴的流程如图所示: 气体,该反应的离子方程式为
气体,该反应的离子方程式为___________ 。
(2)步骤Ⅳ包含蒸馏,该操作不需要下列仪器中的___________ (填字母)。
a.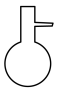 b.
b. c.
c.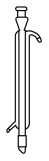 d.
d.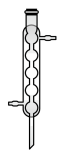 e.
e. f.
f.
Ⅱ.兴趣小组同学按如图实验过程,证明海带中存在碘元素。___________ 中灼烧(填仪器名称)
(4) 的作用是
的作用是___________ (用离子方程式解释)
(5)试剂a不能选择的是(填序号)___________。
(6)操作③的名称是___________ 。
(7)操作③中需要振荡排放气体,放气时分液漏斗的状态是___________。
Ⅰ.海水提溴的流程如图所示:
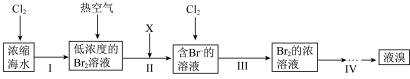
 气体,该反应的离子方程式为
气体,该反应的离子方程式为(2)步骤Ⅳ包含蒸馏,该操作不需要下列仪器中的
a.
 b.
b. c.
c. d.
d. e.
e. f.
f.
Ⅱ.兴趣小组同学按如图实验过程,证明海带中存在碘元素。
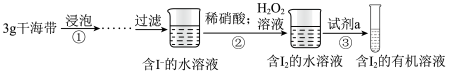
(4)
 的作用是
的作用是(5)试剂a不能选择的是(填序号)___________。
A. | B.苯 | C.酒精 | D.裂化汽油 |
(7)操作③中需要振荡排放气体,放气时分液漏斗的状态是___________。
A. | B. | C.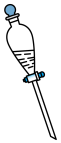 | D.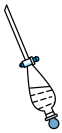 |
您最近一年使用:0次



