ClO2和NaClO2都是广泛使用的漂白剂、消毒剂。其中高浓度ClO2气体易发生爆炸,在生产、使用时需用其他气体进行稀释。某工厂生产ClO2和NaClO2的工艺流程如下:
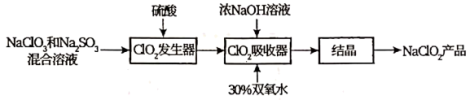
(1)NaClO2中Cl元素的化合价为___________ 。
(2)ClO2发生器中Na2SO3的作用是___________ 。
(3)写出在ClO2吸收器中发生反应的化学方程式___________ 。
(4)若加硫酸过快,发生器中Na2SO3的利用率降低,请结合方程式分析可能的原因___________ 。
(5)吸收器中的溶液经过___________ 、冷却结晶、过滤、___________ 、干燥等操作获得纯净的NaClO2。
(6)在碱性条件下,用ClO2无害化处理含 废水,生成物除H2O外,还生成一种无色气体与两种阴离子,它们分别是
废水,生成物除H2O外,还生成一种无色气体与两种阴离子,它们分别是___________ 。

(1)NaClO2中Cl元素的化合价为
(2)ClO2发生器中Na2SO3的作用是
(3)写出在ClO2吸收器中发生反应的化学方程式
(4)若加硫酸过快,发生器中Na2SO3的利用率降低,请结合方程式分析可能的原因
(5)吸收器中的溶液经过
(6)在碱性条件下,用ClO2无害化处理含
 废水,生成物除H2O外,还生成一种无色气体与两种阴离子,它们分别是
废水,生成物除H2O外,还生成一种无色气体与两种阴离子,它们分别是
更新时间:2021-07-09 20:22:26
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】“84消毒液”是生活中常用的消毒剂,可与硫酸反应制取氯气,反应原理为:NaClO + NaCl + H2SO4 Na2SO4+ Cl2+ H2O,为探究氯气的性质,某同学利用此原理制氯气并设计了如下所示的实验装置。
Na2SO4+ Cl2+ H2O,为探究氯气的性质,某同学利用此原理制氯气并设计了如下所示的实验装置。

(1)上述制备氯气的反应中,每生成1 mol Cl2,转移的电子的物质的量是_________ mol。
(2)依据上述反应原理,从下列装置中选择合适的制氯气装置(A处)__________ (填序号)。

(3)装置B、C中依次盛放的是干燥的红色布条和湿润的红色布条,其目的是_____ 。实验过程中该同学发现装置B中的布条也褪色,说明该装置存在明显的缺陷,改进的方法是_____ 。
(4)E中NaOH溶液吸收氯气时发生反应的离子方程式是___________ 。D中氯气可将SO 氧化,若通过实验验证该反应发生的是氧化还原反应,可采取的方法是
氧化,若通过实验验证该反应发生的是氧化还原反应,可采取的方法是____________ (写出操作、试剂和现象)。
 Na2SO4+ Cl2+ H2O,为探究氯气的性质,某同学利用此原理制氯气并设计了如下所示的实验装置。
Na2SO4+ Cl2+ H2O,为探究氯气的性质,某同学利用此原理制氯气并设计了如下所示的实验装置。
(1)上述制备氯气的反应中,每生成1 mol Cl2,转移的电子的物质的量是
(2)依据上述反应原理,从下列装置中选择合适的制氯气装置(A处)

(3)装置B、C中依次盛放的是干燥的红色布条和湿润的红色布条,其目的是
(4)E中NaOH溶液吸收氯气时发生反应的离子方程式是
 氧化,若通过实验验证该反应发生的是氧化还原反应,可采取的方法是
氧化,若通过实验验证该反应发生的是氧化还原反应,可采取的方法是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】含氯物质在生产、生活中有重要作用。舍勒在研究软锰矿(主要成分是MnO2,其摩尔质量为87 g/mol)的过程中,将它与浓盐酸混合加热,产生了一种黄绿色气体。
(1)写出浓盐酸与MnO2反应生成黄绿色气体的化学方程式为_________ ,用8.7 gMnO2与足量浓盐酸充分反应,生成Cl2的体积(标准状况下)为_________ L。
(2)实验室制取并收集干燥、纯净的该气体时,所需装置的接口连接顺序为:e接_________ (按气流方向,用小写字母表示)。所用仪器如下图所示:

(3)实验室中也可以用高锰酸钾与浓盐酸在常温下反应制取氯气。从下列仪器中选择制取氯气的装置是_________ (填字母),仪器P的名称为_________ 。
A.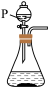 B.
B.  C.
C.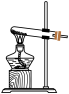
(4)在实验室里可用下图所示装置制取氯酸钾、次氯酸钠和探究氯水的性质。
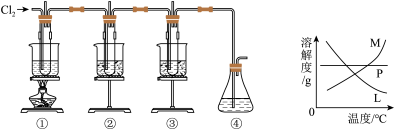
图中:①的试管里盛有15 mL 30%KOH溶液,置于热水浴中;
②的试管里盛有15 mL 8%NaOH溶液,置于冰水浴中;
③的试管里加有紫色石蕊试液;
④为尾气吸收装置。
写出②中制取次氯酸钠的离子方程式_________ 。为什么②装置要放在冰水浴中制取次氯酸钠_________ 。反应完毕经冷却后,①的试管中有大量晶体析出。图中符合该晶体溶解度曲线的是_________ (填写编号字母)。试管③紫色石蕊试液的颜色怎样变化?_________ 。
(1)写出浓盐酸与MnO2反应生成黄绿色气体的化学方程式为
(2)实验室制取并收集干燥、纯净的该气体时,所需装置的接口连接顺序为:e接

(3)实验室中也可以用高锰酸钾与浓盐酸在常温下反应制取氯气。从下列仪器中选择制取氯气的装置是
A.
 B.
B.  C.
C.
(4)在实验室里可用下图所示装置制取氯酸钾、次氯酸钠和探究氯水的性质。

图中:①的试管里盛有15 mL 30%KOH溶液,置于热水浴中;
②的试管里盛有15 mL 8%NaOH溶液,置于冰水浴中;
③的试管里加有紫色石蕊试液;
④为尾气吸收装置。
写出②中制取次氯酸钠的离子方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】现有几种元素的性质或原子结构如下表:
(1)元素X的一种同位素用来作相对原子质量的标准,这种同位素的原子符号是________ ;X的另一种同位素可用来测定文物年代,这种同位素的原子符号是________ 。
(2)元素Y形成的另一种单质,大量存在于地球的平流层中,被称作地球生物的保护伞,该单质的化学式是________ 。
(3)元素Z在海水中含量非常高,海水中含Z元素的主要化合物是________ (写化学式)。
(4)写出T的同主族短周期元素的单质在空气中燃烧的化学方程式_____ 。
(5)Z的单质可用来对自来水进行消毒,结合化学方程式说明其消毒原理__________ 。
| 元素编号 | 元素性质或原子结构 |
| T | 失去一个电子后,形成Ne的原子结构 |
| X | 最外层电子数是次外层电子数的2倍 |
| Y | 其单质之一是空气主要成分之一,且是最常见的助燃剂 |
| Z | 原子核外有3层电子,最外层电子数比次外层电子数少一个 |
(2)元素Y形成的另一种单质,大量存在于地球的平流层中,被称作地球生物的保护伞,该单质的化学式是
(3)元素Z在海水中含量非常高,海水中含Z元素的主要化合物是
(4)写出T的同主族短周期元素的单质在空气中燃烧的化学方程式
(5)Z的单质可用来对自来水进行消毒,结合化学方程式说明其消毒原理
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】磺酰氯 用于有机合成、医药、染料、农药等,也用作表面活性剂,熔点-54.1℃,沸点69.1℃,遇水发生剧烈水解.某学习小组用如图装置制备磺酰氯。
用于有机合成、医药、染料、农药等,也用作表面活性剂,熔点-54.1℃,沸点69.1℃,遇水发生剧烈水解.某学习小组用如图装置制备磺酰氯。
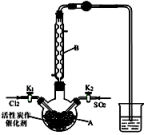
(已知: ).
).
(1)若用浓盐酸与二氧化锰为原料制取Cl2,反应的离子方程式方程式为____________________________
(2)仪器B的名称是______________ ,它在该实验中的作用是__________________ ,烧杯中盛放的溶液为_______________
(3)检验装置气密性的方法为___________________________ .向装置 中通入
中通入 和
和 后很快有液态物质生成.制备过程中需采用冰水浴,从化学反应原理角度分析可能原因为
后很快有液态物质生成.制备过程中需采用冰水浴,从化学反应原理角度分析可能原因为______________ .
(4)向分离提纯后的 中加水,出现白雾,振荡、静置得到无色溶液
中加水,出现白雾,振荡、静置得到无色溶液 .经分析
.经分析 与
与 反应属于非氧化还原反应,无色溶液
反应属于非氧化还原反应,无色溶液 中的阴离子除含少量
中的阴离子除含少量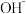 外,还含有其它两种阴离子,请写出该反应的化学方程式:
外,还含有其它两种阴离子,请写出该反应的化学方程式:_____________________ .
 用于有机合成、医药、染料、农药等,也用作表面活性剂,熔点-54.1℃,沸点69.1℃,遇水发生剧烈水解.某学习小组用如图装置制备磺酰氯。
用于有机合成、医药、染料、农药等,也用作表面活性剂,熔点-54.1℃,沸点69.1℃,遇水发生剧烈水解.某学习小组用如图装置制备磺酰氯。
(已知:
 ).
).(1)若用浓盐酸与二氧化锰为原料制取Cl2,反应的离子方程式方程式为
(2)仪器B的名称是
(3)检验装置气密性的方法为
 中通入
中通入 和
和 后很快有液态物质生成.制备过程中需采用冰水浴,从化学反应原理角度分析可能原因为
后很快有液态物质生成.制备过程中需采用冰水浴,从化学反应原理角度分析可能原因为(4)向分离提纯后的
 中加水,出现白雾,振荡、静置得到无色溶液
中加水,出现白雾,振荡、静置得到无色溶液 .经分析
.经分析 与
与 反应属于非氧化还原反应,无色溶液
反应属于非氧化还原反应,无色溶液 中的阴离子除含少量
中的阴离子除含少量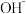 外,还含有其它两种阴离子,请写出该反应的化学方程式:
外,还含有其它两种阴离子,请写出该反应的化学方程式:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】过氧化钙晶体﹝CaO2·8H2O﹞较稳定,呈白色,微溶于水,广泛应用于环境杀菌、消毒。以贝壳为原料制备CaO2流程如下:
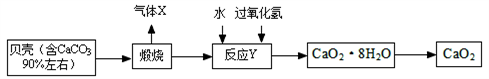
(1)气体X的名称是__________ ,实验室常用_____________ 溶液来吸收;将过氧化钙晶体与溶液分离的方法是________________ 。
(2)反应Y需控制温度在0~2℃,可将反应容器放在_________________ 中,该反应是化合反应,反应产物是CaO2·8H2O,请写出该反应的化学方程式_____________________________________ 。
(3)获得的过氧化钙晶体中常含有Ca(OH)2杂质,原因是___________________________ 。

(1)气体X的名称是
(2)反应Y需控制温度在0~2℃,可将反应容器放在
(3)获得的过氧化钙晶体中常含有Ca(OH)2杂质,原因是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】 和
和 都是锂离子电池的电极材料,可利用钛铁矿(主要成分为
都是锂离子电池的电极材料,可利用钛铁矿(主要成分为 ,还含有少量MgO、
,还含有少量MgO、 等杂质)来制备。工艺流程如图所示:
等杂质)来制备。工艺流程如图所示:
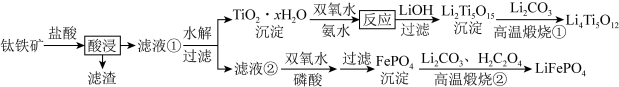
回答下列问题:
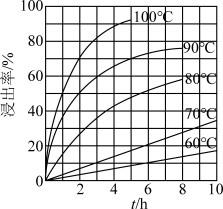
(1)“酸浸”实验中,铁的浸出率结果如图所示。由图可知,当铁的浸出率为70%时,所采用的实验条件为______ 。
(2)“酸浸”后,钛主要以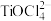 形式存在,写出相应反应的离子方程式
形式存在,写出相应反应的离子方程式_______ 。
(3) 沉淀与双氧水、氨水反应
沉淀与双氧水、氨水反应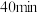 所得实验结果如下表所示:
所得实验结果如下表所示:
分析 时
时 转化率最高的原因
转化率最高的原因_________ 。
(4)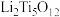 中Ti的化合价为+4,其中过氧键的数目为
中Ti的化合价为+4,其中过氧键的数目为__________ 。
 和
和 都是锂离子电池的电极材料,可利用钛铁矿(主要成分为
都是锂离子电池的电极材料,可利用钛铁矿(主要成分为 ,还含有少量MgO、
,还含有少量MgO、 等杂质)来制备。工艺流程如图所示:
等杂质)来制备。工艺流程如图所示:
回答下列问题:
(1)“酸浸”实验中,铁的浸出率结果如图所示。由图可知,当铁的浸出率为70%时,所采用的实验条件为

(2)“酸浸”后,钛主要以
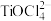 形式存在,写出相应反应的离子方程式
形式存在,写出相应反应的离子方程式(3)
 沉淀与双氧水、氨水反应
沉淀与双氧水、氨水反应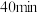 所得实验结果如下表所示:
所得实验结果如下表所示:温度/℃ | 30 | 35 | 40 | 45 | 50 |
| 92 | 95 | 97 | 93 | 88 |
分析
 时
时 转化率最高的原因
转化率最高的原因(4)
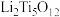 中Ti的化合价为+4,其中过氧键的数目为
中Ti的化合价为+4,其中过氧键的数目为
您最近一年使用:0次



