氮元素是重要的非金属元素,可形成多种铵盐、氮化物、叠氮化物及配合物等。
(1)基态氮原子价电子的轨道表达式(价电子排布图)为_______ ;第二周期元素原子中第一电离能大于氮原子的有_______ 种,NH4NO3中阴离子的空间构型为_______ 。
(2)C、N、O、S四种元素中,电负性最大的是_______ 。1mol[Co(NH3)6]Cl2中含有 键的数目为
键的数目为_______ ;已知NF3比NH3的沸点低得多,试解释原因_______ 。
(3)叠氮化钠(NaN3)用于汽车的安全气囊, 结构如图甲。
结构如图甲。 中存在的两个大
中存在的两个大 键可用符号
键可用符号 表示,一个
表示,一个 中键合电子(形成化学键的电子)总数为
中键合电子(形成化学键的电子)总数为_______ 。叠氮酸(HN3)结构如图乙,分子中②号N原子的杂化方式为_______ 。
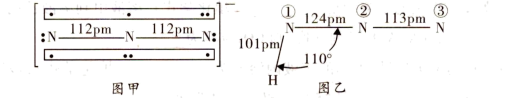
(4)含有多个配位原子的配体与同一中心离子(或原子)通过螯合配位成环而形成的配合物为螯合物。一种Fe3+配合物的结构如图丙所示,1mol该螯合物中通过螯合作用形成的配位键有_______ mol。
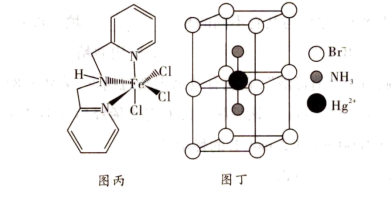
(5)某含氮的化合物晶胞结构如图丁所示,Br-作简单立方堆积,两个立方体共用的面中心存在一个Hg,NH3位于立方体的体心,相邻的Br的距离均为apm,阿伏加德罗常数的值为NA该物质的化学式为_______ ,该晶体的密度为_______ g·cm-3。
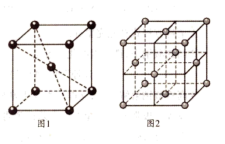
(6)Fe3+可以与SCN-、CN-等形成配合物。与SCN-互为等电子体且为非极性分子的化学式为_______ 。在一定条件下铁形成的晶体的基本结构单元如图1和图2所示,则图1和图2的结构中铁原子的配位数之比为_______ ,两种晶体中空间利用率较高的是_______ (填“图1”或“图2”)。
(1)基态氮原子价电子的轨道表达式(价电子排布图)为
(2)C、N、O、S四种元素中,电负性最大的是
 键的数目为
键的数目为(3)叠氮化钠(NaN3)用于汽车的安全气囊,
 结构如图甲。
结构如图甲。 中存在的两个大
中存在的两个大 键可用符号
键可用符号 表示,一个
表示,一个 中键合电子(形成化学键的电子)总数为
中键合电子(形成化学键的电子)总数为
(4)含有多个配位原子的配体与同一中心离子(或原子)通过螯合配位成环而形成的配合物为螯合物。一种Fe3+配合物的结构如图丙所示,1mol该螯合物中通过螯合作用形成的配位键有

(5)某含氮的化合物晶胞结构如图丁所示,Br-作简单立方堆积,两个立方体共用的面中心存在一个Hg,NH3位于立方体的体心,相邻的Br的距离均为apm,阿伏加德罗常数的值为NA该物质的化学式为
(6)Fe3+可以与SCN-、CN-等形成配合物。与SCN-互为等电子体且为非极性分子的化学式为

更新时间:2021-07-19 07:51:36
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】第ⅢA族的单质及一些化合物在工农业生产等领域有重要应用。回答下列问题:
(1)基态Ga原子价电子排布图为________ .
(2)经测定发现,N2O5固体由NO2+和NO3-两种离子组成,该固体中N原子杂化类型为___ ;与NO2+互为等电子体的微粒有_____ (写出一种)。
(3)铵盐大多不稳定,NH4F、NH4I中,较易分解的是_____ ,原因是______ .
(4)第二周期中,第一电离能介于B元素和N元素之间的元素有______ 种。
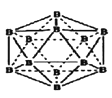
(5)晶体别有多种变体,但其基本结构单元都是由硼原子组成的正二十面体(见下图),每个顶点为一个硼原子,每个三角形均为等边三角形。若此结构单元为1个分子,则其分子式为____ .
(6)冰晶石(Na3AlF6)由两种微粒构成,冰晶石的晶胞结构如图甲所示,●位于大立方体的顶点和面心,ο位于大立方体的12条棱的中点和8个小立方体的体心,那么大立方体的体心处所代表的微粒是_________ (填微粒符号)。

(7)A1单质的晶体中原子的堆积方式如图乙所示,其晶胞特征如图丙所示,原子之间相互位置关系的平面图如图丁所示:
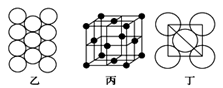
若已知Al的原子半径为dnm,NA代表阿伏伽德罗常数,Al的相对原子质量为M,则一个晶胞中Al原子的数目_____ 个;Al晶体的密度为_____ g/cm3(用字母表示)。
(1)基态Ga原子价电子排布图为
(2)经测定发现,N2O5固体由NO2+和NO3-两种离子组成,该固体中N原子杂化类型为
(3)铵盐大多不稳定,NH4F、NH4I中,较易分解的是
(4)第二周期中,第一电离能介于B元素和N元素之间的元素有
(5)晶体别有多种变体,但其基本结构单元都是由硼原子组成的正二十面体(见下图),每个顶点为一个硼原子,每个三角形均为等边三角形。若此结构单元为1个分子,则其分子式为

(6)冰晶石(Na3AlF6)由两种微粒构成,冰晶石的晶胞结构如图甲所示,●位于大立方体的顶点和面心,ο位于大立方体的12条棱的中点和8个小立方体的体心,那么大立方体的体心处所代表的微粒是

(7)A1单质的晶体中原子的堆积方式如图乙所示,其晶胞特征如图丙所示,原子之间相互位置关系的平面图如图丁所示:

若已知Al的原子半径为dnm,NA代表阿伏伽德罗常数,Al的相对原子质量为M,则一个晶胞中Al原子的数目
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】秋冬季我国北方大部分地区出现严重雾霾天气,引起雾霾的PM2.5微细粒子包含(NH4)2SO4、NH4NO3、有机颗粒物及扬尘等,城市雾霾中还含有铜等重金属元素。
(1)PM2.5富含大量的有毒、有害物质,易引发二次光化学烟雾,光化学烟雾中含有NOx、HCOOH、 等二次污染物。
等二次污染物。
①基态N原子的电子排布式___________ ;C、N和O的第一电离能由大到小的顺序为___________
②氨硼烷(NH3BH3)被认为是最具潜力的新型储氢材料之一,分子中存在配位键,提供孤电子对的成键原子是________ ,写出一种与氨硼烷互为等电子体的分子________ (填化学式)。
(2)PM2.5微细粒子包含(NH4)2SO4、NH4NO3等。
①(NH4)2SO4晶体中各种微粒间存在的作用力有________ (填序号)。
a.离子键 b.共价键 c.配位键 d.范德华力
②NH4NO3中阴离子的空间构型为________ ,阳离子的中心原子轨道采用________ 杂化。

(3)某种镁铝合金可作为储钠材料,该合金晶胞结构如图所示,晶胞棱长为anm,该合金的化学式为____________ ,晶体中每个镁原子周围距离最近的铝原子数目为___________ ,该晶体的密度为__________________ g/cm3(阿伏加 德罗常数的数值用NA表示)。
(1)PM2.5富含大量的有毒、有害物质,易引发二次光化学烟雾,光化学烟雾中含有NOx、HCOOH、
 等二次污染物。
等二次污染物。①基态N原子的电子排布式
②氨硼烷(NH3BH3)被认为是最具潜力的新型储氢材料之一,分子中存在配位键,提供孤电子对的成键原子是
(2)PM2.5微细粒子包含(NH4)2SO4、NH4NO3等。
①(NH4)2SO4晶体中各种微粒间存在的作用力有
a.离子键 b.共价键 c.配位键 d.范德华力
②NH4NO3中阴离子的空间构型为

(3)某种镁铝合金可作为储钠材料,该合金晶胞结构如图所示,晶胞棱长为anm,该合金的化学式为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】硼(B)是一种重要的元素,硼及其化合物在工农业生产、材料、医疗领域都有广泛的用途。回答下列问题:
(1)基态硼原子的核外电子轨道表示式为______ ,与同周期的铍元素相比,硼的的第一电离能小的原因是_____ 。
(2)氨硼烷(NH3BH3)是一种新型储氢材料,其分子中存在配位键,则氨硼烷分子结构式为______ 。
(3)六方氮化硼在高温高压下,可以转化为立方氮化硼,其结构如下图甲所示。

①立方氮化硼中,硼原子的杂化方式为___ ;图乙为体心立方晶胞结构,沿其体对角线垂直在纸平面上的投影图如图a所示,则立方氮化硼晶胞沿其体对角线垂直在纸平面上的投影图应是上图中的___ (将原子看作等径圆球,填“a”、“b”、“c”、“d”)。

②图甲中,B原子填充在N原子的四面体空隙,且占据此类空隙的比例为_________ ,如果该晶胞边长为a pm,c原子的坐标参数为(0,0,0),e为( ,
, ,0),f为(
,0),f为( ,0,
,0, ),则d原子的坐标参数为
),则d原子的坐标参数为________ ,该晶体的密度为_________ 。
(1)基态硼原子的核外电子轨道表示式为
(2)氨硼烷(NH3BH3)是一种新型储氢材料,其分子中存在配位键,则氨硼烷分子结构式为
(3)六方氮化硼在高温高压下,可以转化为立方氮化硼,其结构如下图甲所示。

①立方氮化硼中,硼原子的杂化方式为

②图甲中,B原子填充在N原子的四面体空隙,且占据此类空隙的比例为
 ,
, ,0),f为(
,0),f为( ,0,
,0, ),则d原子的坐标参数为
),则d原子的坐标参数为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】2020年2月15日,由国家科研攻关组的主要成员单位的专家组共同研判磷酸氯喹在细胞水平上能有效抑制新型冠状病毒(2019-nCoV)的感染。

(1)已知磷酸氯喹的结构如图所示,则所含C、N、O三种元素电负性由大到小的顺序为___________ 。
(2)在[Cu(NH3)4]2+中∠HNH比游离的氨气分子中∠HNH___________ ,(填“大”“小”或“相等"),原因是___________ 。
(3)第三周期的某主族元素,其第一至第五电离能数据如图1所示,则该元素对应的原子有___________ 种不同运动状态的电子。
(4)如图2所示,每条折线表示周期表ⅣA~ⅦA中的某一族元素氢化物的沸点变化。每个小黑点代表一种氢化物,其中a点代表的是___________ 。(填化学式)

(5)镁单质晶体中原子的堆积模型如图,它的堆积模型名称为___________ ;晶胞是图中的___________ (填a、b或c);配位数是___________ 。


(1)已知磷酸氯喹的结构如图所示,则所含C、N、O三种元素电负性由大到小的顺序为
(2)在[Cu(NH3)4]2+中∠HNH比游离的氨气分子中∠HNH
(3)第三周期的某主族元素,其第一至第五电离能数据如图1所示,则该元素对应的原子有
(4)如图2所示,每条折线表示周期表ⅣA~ⅦA中的某一族元素氢化物的沸点变化。每个小黑点代表一种氢化物,其中a点代表的是

(5)镁单质晶体中原子的堆积模型如图,它的堆积模型名称为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】大部分非金属元素分布在元素周期表的p区,非金属元素数量虽少,却构成了丰富的物质世界。回答下列问题:
(1)基态 原子的价电子排布式为
原子的价电子排布式为_______ , 、
、 、
、 的沸点由高到低的顺序依次为
的沸点由高到低的顺序依次为_______ 。
(2)超强酸“魔酸”是五氟化锑(SbF5))和氟磺酸(HSO3F)的混合物, 与
与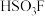 的结构如图:
的结构如图:

 中
中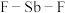 键的键角的度数分别为
键的键角的度数分别为_______ ,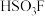 中所含元素电负性由大到小的顺序是
中所含元素电负性由大到小的顺序是_______ 。
(3)苯(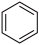 )和吡啶(
)和吡啶( )结构相似,均具有芳香性。分子中的离域
)结构相似,均具有芳香性。分子中的离域 键可用符号
键可用符号 表示,其中m代表参与形成离域
表示,其中m代表参与形成离域 键的原子数,n代表参与形成离域
键的原子数,n代表参与形成离域 键的电子数(如苯分子中的离域
键的电子数(如苯分子中的离域 键可表示为
键可表示为 ,则
,则 中的离域
中的离域 键可表示为
键可表示为_______ ,N原子采用杂化_______ 。
(4)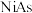 晶体有明显的金属性,是一种合金。
晶体有明显的金属性,是一种合金。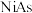 的晶体结构如图所示,六方晶胞底边长为
的晶体结构如图所示,六方晶胞底边长为 、高为
、高为 。晶胞中
。晶胞中 的分数坐标(
的分数坐标( ,
, ,
, )。
)。
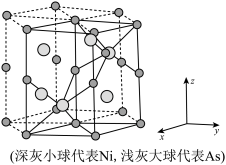
 原子的配位数
原子的配位数_______ ,晶胞中 的分数坐标
的分数坐标_______ ,晶胞密度为_______  。
。
(1)基态
 原子的价电子排布式为
原子的价电子排布式为 、
、 、
、 的沸点由高到低的顺序依次为
的沸点由高到低的顺序依次为(2)超强酸“魔酸”是五氟化锑(SbF5))和氟磺酸(HSO3F)的混合物,
 与
与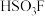 的结构如图:
的结构如图:
 中
中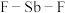 键的键角的度数分别为
键的键角的度数分别为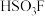 中所含元素电负性由大到小的顺序是
中所含元素电负性由大到小的顺序是(3)苯(
 )和吡啶(
)和吡啶( )结构相似,均具有芳香性。分子中的离域
)结构相似,均具有芳香性。分子中的离域 键可用符号
键可用符号 表示,其中m代表参与形成离域
表示,其中m代表参与形成离域 键的原子数,n代表参与形成离域
键的原子数,n代表参与形成离域 键的电子数(如苯分子中的离域
键的电子数(如苯分子中的离域 键可表示为
键可表示为 ,则
,则 中的离域
中的离域 键可表示为
键可表示为(4)
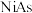 晶体有明显的金属性,是一种合金。
晶体有明显的金属性,是一种合金。 的晶体结构如图所示,六方晶胞底边长为
的晶体结构如图所示,六方晶胞底边长为 、高为
、高为 。晶胞中
。晶胞中 的分数坐标(
的分数坐标( ,
, ,
, )。
)。
 原子的配位数
原子的配位数 的分数坐标
的分数坐标 。
。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】近年来我国在高温超导材料的研究取得了重大突破,高温超导体仅出现在共价性很强的氧化物中,例如带有直线形的Cu-O-Cu链节的网格层对超导性有重要的作用。回答下列问题:
(1)基态Cu原子核外电子排布式为______ 。
(2)氧与其同周期且相邻两元素的第一电离能由大到小的顺序为______ 。
(3)氧的常见氢化物有两种,分别为H2O和H2O2。其中H2O的VSEPR模型为______ ;H2O2中氧原子的杂化方式为_______ 。
(4)硫酸铜溶于水后形成的水合铜离子的结构式为____ ,向硫酸铜溶液中逐滴加入氨水直至过量,观察到的现象为___ ,所得结论:与Cu2+形成配位键的能力H2O___ (填“强于”或“弱于”)NH3
(5)由Y、Ba、Cu、O四种元素构成的高温超导材料晶胞结构如图甲,图乙为沿z轴的投影图;其中CuO2网格层如图丙。
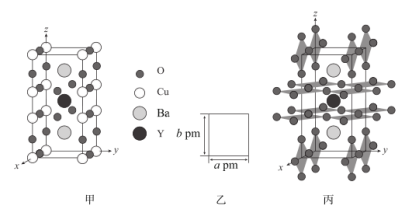
已知:网格层之间相互垂直或平行;z轴方向上的晶胞参数为cpm。
①该高温超导材料的化学式为______ 。
②若阿伏加德罗常数的值为NA,则晶体的密度为_____ g·cm-3(用含a、b、c和NA的表达式表示)。
(1)基态Cu原子核外电子排布式为
(2)氧与其同周期且相邻两元素的第一电离能由大到小的顺序为
(3)氧的常见氢化物有两种,分别为H2O和H2O2。其中H2O的VSEPR模型为
(4)硫酸铜溶于水后形成的水合铜离子的结构式为
(5)由Y、Ba、Cu、O四种元素构成的高温超导材料晶胞结构如图甲,图乙为沿z轴的投影图;其中CuO2网格层如图丙。

已知:网格层之间相互垂直或平行;z轴方向上的晶胞参数为cpm。
①该高温超导材料的化学式为
②若阿伏加德罗常数的值为NA,则晶体的密度为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】金属镍及其化合物在合金材料以及催化剂等方面应用广泛。试回答下列问题:
(1)Ni2+电子排布中,电子填充的能量最高的能级符号为______ 。
(2)金属Ni能与CO形成配合物Ni(CO)4,与CO互为等电子体的一种分子为______ (写化学式,下同),与CO互为等电子体的一种离子为______ 。
(3)丁二酮肟( )是检验Ni2+的灵敏试剂。丁二酮肟分子中C原子轨道杂化类型为
)是检验Ni2+的灵敏试剂。丁二酮肟分子中C原子轨道杂化类型为______ ,2mol丁二酮肟分子中所含σ键的数目为______ 。
(4)丁二酮肟常与NI2+形成图A所示的配合物,图B是硫代氧的结果:

①A的熔、沸点高于B的原因为______ 。
②B晶体含有化学键的类型为______ (填选项字母)。
A.σ键 B.金属键 C.配位键 D.π键
(5)人工合成的氧化镍往往存在缺陷,某缺陷氧化银的组成为Ni0.97O,其中Ni元素只有+2和+3两种价态,两种价态的镍离子数目之比为______ 。
(6)Ni2+与Mg2+、O2-形成晶体的晶胞结构如图所示(Ni2+未画出),则该晶体的化学式为______ 。
(1)Ni2+电子排布中,电子填充的能量最高的能级符号为
(2)金属Ni能与CO形成配合物Ni(CO)4,与CO互为等电子体的一种分子为
(3)丁二酮肟(
 )是检验Ni2+的灵敏试剂。丁二酮肟分子中C原子轨道杂化类型为
)是检验Ni2+的灵敏试剂。丁二酮肟分子中C原子轨道杂化类型为(4)丁二酮肟常与NI2+形成图A所示的配合物,图B是硫代氧的结果:

①A的熔、沸点高于B的原因为
②B晶体含有化学键的类型为
A.σ键 B.金属键 C.配位键 D.π键
(5)人工合成的氧化镍往往存在缺陷,某缺陷氧化银的组成为Ni0.97O,其中Ni元素只有+2和+3两种价态,两种价态的镍离子数目之比为
(6)Ni2+与Mg2+、O2-形成晶体的晶胞结构如图所示(Ni2+未画出),则该晶体的化学式为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐2】人类社会的发展与进步与材料的发展密不可分,而金属是人类常用的一类材料如铜、铁合金等等。
(1)基态Cu原子的价电子排布式为__________ ,在元素周期表中的位置为___________ 。
(2)Cu2O为半导体材料,可由乙醛(CH3CHO)和新制氢氧化铜反应得到。乙醛中碳原子的杂化方式有______________ ,乙醛分子中 键与
键与 键的数目之比为
键的数目之比为____________ 。
(3)制造单晶硅太阳能电池片时,一般掺杂微量的铜、碳、硼、氮等。铜、碳、硼、氮元素的电负性由大到小的顺序是_________________ 。(用元素符号表示)
(4)Cu(OH)2溶于氨水形成深蓝色的[Cu(NH3)4]2+,该配合物中NH3的价层电子对互斥模型为_____________ 。
(5)铁在不同温度范围有不同的晶体结构,在室温下为体心立方,当温度升高到912℃,则转变为面心立方。铁的体心立方堆积和面心立方最密堆积的配位数分别为____ 、_____ 。若铁原子半径为r pm,则铁为面心立方最密堆积时的晶体密度为___________ g/cm3(阿伏伽德罗常数的值用NA 表示,1pm=10-12m,写出计算式即可)。
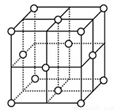
面心立方晶胞
(1)基态Cu原子的价电子排布式为
(2)Cu2O为半导体材料,可由乙醛(CH3CHO)和新制氢氧化铜反应得到。乙醛中碳原子的杂化方式有
 键与
键与 键的数目之比为
键的数目之比为(3)制造单晶硅太阳能电池片时,一般掺杂微量的铜、碳、硼、氮等。铜、碳、硼、氮元素的电负性由大到小的顺序是
(4)Cu(OH)2溶于氨水形成深蓝色的[Cu(NH3)4]2+,该配合物中NH3的价层电子对互斥模型为
(5)铁在不同温度范围有不同的晶体结构,在室温下为体心立方,当温度升高到912℃,则转变为面心立方。铁的体心立方堆积和面心立方最密堆积的配位数分别为

面心立方晶胞
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】新型铜锌锡疏化合物( )薄膜太阳能电池近年来已经成为可再生能源领域的研究热点。回答下列问题:
)薄膜太阳能电池近年来已经成为可再生能源领域的研究热点。回答下列问题:
(1) 的价电子排布式为
的价电子排布式为_______ , 位于元素周期表的
位于元素周期表的_______ 区。
(2) 第一电离能由大到小的顺序是
第一电离能由大到小的顺序是_______ 。
(3) 和
和 键角较小的是
键角较小的是_______ ,原因是_______ 。
(4)向 溶液中滴加氨水至过量,最终得到蓝色溶液,溶液中
溶液中滴加氨水至过量,最终得到蓝色溶液,溶液中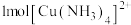 含有
含有_______ 个σ键。再向溶液中如入乙醇,得到深蓝色晶体,该晶体中不存在_______ (填标号)。
A.离子键 B.共价键 C.配位键 D.金属键 E.氢键
(5)具有6个配体的 的配合物
的配合物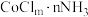 ,若
,若 此配合物与足量的
此配合物与足量的 溶液反应只生成
溶液反应只生成 沉淀,该配合物的化学式为
沉淀,该配合物的化学式为_______ (需区分内界和外界)
(6)氨缩脲( )分子中σ键与π键的数目之比为
)分子中σ键与π键的数目之比为_______ 。氨缩脲与胆矾溶液反应得到如图所示的紫色物质,1mol紫色物质中含配位键的数目为_______ 。

 )薄膜太阳能电池近年来已经成为可再生能源领域的研究热点。回答下列问题:
)薄膜太阳能电池近年来已经成为可再生能源领域的研究热点。回答下列问题:(1)
 的价电子排布式为
的价电子排布式为 位于元素周期表的
位于元素周期表的(2)
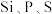 第一电离能由大到小的顺序是
第一电离能由大到小的顺序是(3)
 和
和 键角较小的是
键角较小的是(4)向
 溶液中滴加氨水至过量,最终得到蓝色溶液,溶液中
溶液中滴加氨水至过量,最终得到蓝色溶液,溶液中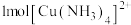 含有
含有A.离子键 B.共价键 C.配位键 D.金属键 E.氢键
(5)具有6个配体的
 的配合物
的配合物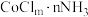 ,若
,若 此配合物与足量的
此配合物与足量的 溶液反应只生成
溶液反应只生成 沉淀,该配合物的化学式为
沉淀,该配合物的化学式为(6)氨缩脲(
 )分子中σ键与π键的数目之比为
)分子中σ键与π键的数目之比为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】氮的相关化合物在材料等方面有重要用途。回答下列问题:
(1)基态N原子的核外电子排布式为_______ ,第一电离能: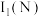
_______ 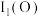 (填“大于”或“小于”)。
(填“大于”或“小于”)。
(2)N及其同族的P、As均可形成类似的氢化物, 、
、 ,
, 的沸点由高到低的顺序为
的沸点由高到低的顺序为_______ (填化学式)。
(3)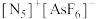 是一种全氮阳离子形成的高能物质,其结构如图所示,其中N原子的杂化轨道类型为
是一种全氮阳离子形成的高能物质,其结构如图所示,其中N原子的杂化轨道类型为_______ 。 与EDTA形成的螯合物的结构如图所示,1个该配合物中通过螯合作用形成的配位键有
与EDTA形成的螯合物的结构如图所示,1个该配合物中通过螯合作用形成的配位键有_______ 个,其中提供孤对电子的原子为_______ (写元素符号)。 ,则C点的原子坐标参数为
,则C点的原子坐标参数为_______ 。
②已知晶胞参数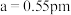 ,则该晶体的密度为
,则该晶体的密度为_______  (用
(用 表示阿伏加德罗常数,只列出计算表达式即可。)
表示阿伏加德罗常数,只列出计算表达式即可。)
(1)基态N原子的核外电子排布式为
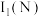
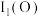 (填“大于”或“小于”)。
(填“大于”或“小于”)。(2)N及其同族的P、As均可形成类似的氢化物,
 、
、 ,
, 的沸点由高到低的顺序为
的沸点由高到低的顺序为(3)
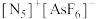 是一种全氮阳离子形成的高能物质,其结构如图所示,其中N原子的杂化轨道类型为
是一种全氮阳离子形成的高能物质,其结构如图所示,其中N原子的杂化轨道类型为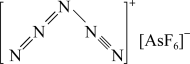
 与EDTA形成的螯合物的结构如图所示,1个该配合物中通过螯合作用形成的配位键有
与EDTA形成的螯合物的结构如图所示,1个该配合物中通过螯合作用形成的配位键有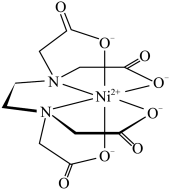

 ,则C点的原子坐标参数为
,则C点的原子坐标参数为②已知晶胞参数
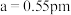 ,则该晶体的密度为
,则该晶体的密度为 (用
(用 表示阿伏加德罗常数,只列出计算表达式即可。)
表示阿伏加德罗常数,只列出计算表达式即可。)
您最近一年使用:0次
【推荐2】(1)钛被称为继铁、铝之后的第三金属,钛元素在元素周期表中的位置为___ ,其价电子排布式为___ 。
(2)写出一种与 互为等电子体的分子:
互为等电子体的分子:___ (填化学式)。基态Mg原子的核外电子占据了___ 种不同形状的原子轨道。
(3)TiCl4的熔点是-24.1℃,沸点是136.4℃,则固态TiCl4属于__ 晶体。
(4)超硬材料C3N4的热稳定性比金刚石的热稳定性强,其原因为_______ 。金刚石的晶胞结构如甲图所示,已知A原子的坐标参数为(0,0,0),B原子的坐标参数为(0, ,
, ),则C原子的坐标为
),则C原子的坐标为____ 。金刚石晶体中所含C—C键和C原子的数目之比为___ 。


(5)研究表明,NH3与H2O以氢键结合成NH3·H2O,NH3·H2O又可电离出 ,则NH3·H2O的结构式为
,则NH3·H2O的结构式为____ 。
(6)铜是人类发现比较早的一种金属,其晶胞结构如乙图所示。若铜的密度为ρg·cm-3,阿伏加德罗常数的值为NA,则两个钛原子间的最短距离为___ cm(用含有ρ、NA的代数式表示)。
(2)写出一种与
 互为等电子体的分子:
互为等电子体的分子:(3)TiCl4的熔点是-24.1℃,沸点是136.4℃,则固态TiCl4属于
(4)超硬材料C3N4的热稳定性比金刚石的热稳定性强,其原因为
 ,
, ),则C原子的坐标为
),则C原子的坐标为

(5)研究表明,NH3与H2O以氢键结合成NH3·H2O,NH3·H2O又可电离出
 ,则NH3·H2O的结构式为
,则NH3·H2O的结构式为(6)铜是人类发现比较早的一种金属,其晶胞结构如乙图所示。若铜的密度为ρg·cm-3,阿伏加德罗常数的值为NA,则两个钛原子间的最短距离为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】铜的化合物在工农业生产和化学实验室中都具有重要的作用。工业上常用氨气和醋酸二氨合铜{[Cu(NH3)2]Ac}的混合溶液来吸收一氧化碳(醋酸根离子CH3COO-简写为Ac-),反应方程式为:[Cu(NH3)2]Ac+CO+NH3 [Cu(NH3)3CO]Ac。
[Cu(NH3)3CO]Ac。
(1)Cu2+基态核外电子排布式为___ 。
(2)该反应中含有的第二周期非金属元素的电负性由大到小的顺序为___ 。
(3)CH3COOH分子中C原子的杂化类型为___ 。
(4)配合物[Cu(NH3)3CO]Ac的中心离子的配位数为___ 。
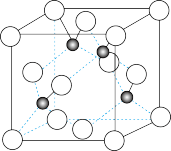
(5)A原子的价电子排布式为3s23p5,铜与A形成化合物的晶胞如图所示(黑球代表铜原子)。该晶体的化学式为___ 。
 [Cu(NH3)3CO]Ac。
[Cu(NH3)3CO]Ac。(1)Cu2+基态核外电子排布式为
(2)该反应中含有的第二周期非金属元素的电负性由大到小的顺序为
(3)CH3COOH分子中C原子的杂化类型为
(4)配合物[Cu(NH3)3CO]Ac的中心离子的配位数为
(5)A原子的价电子排布式为3s23p5,铜与A形成化合物的晶胞如图所示(黑球代表铜原子)。该晶体的化学式为

您最近一年使用:0次



