(1)向NaHSO4溶液中滴加Ba(OH)2溶液至中性,发生反应的离子方程式为___ ,若继续滴加Ba(OH)2溶液,又发生反应的离子方程式为_______ 。
(2)+6价铬的化合物毒性较大,常用NaHSO3将废液中的Cr2O 还原成Cr3+,该反应的离子方程式为
还原成Cr3+,该反应的离子方程式为______ 。
(3)向偏铝酸钠溶液中通入足量CO2的离子方程式为_____
(4)用电石制得的乙炔中常含有PH3和H2S杂质而带有臭味,可通过CuSO4溶液洗气除去。
①___ ____CuSO4+_______PH3+_______H2O=_____Cu3P↓+______H3PO4+____H2SO4,此反应中:氧化剂和还原剂物质的量之比为_______ ,若生成1mol Cu3P,转移电子数为______ 。
②H2S气体和CuSO4溶液反应有黑色沉淀产生,离子方程式为______
(5)检验某溶液中只有Fe2+而不含有Fe3+,方法是______
(2)+6价铬的化合物毒性较大,常用NaHSO3将废液中的Cr2O
 还原成Cr3+,该反应的离子方程式为
还原成Cr3+,该反应的离子方程式为(3)向偏铝酸钠溶液中通入足量CO2的离子方程式为
(4)用电石制得的乙炔中常含有PH3和H2S杂质而带有臭味,可通过CuSO4溶液洗气除去。
①
②H2S气体和CuSO4溶液反应有黑色沉淀产生,离子方程式为
(5)检验某溶液中只有Fe2+而不含有Fe3+,方法是
更新时间:2021-07-22 22:30:16
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】现有下列物质:①硫酸氢钠 ②过氧化钠 ③二氧化硫 ④铁 ⑤氨水 ⑥氯化氢 ⑦ ⑧乙醇 ⑨小苏打 ⑩澄清石灰水,按要求回答下列问题:
⑧乙醇 ⑨小苏打 ⑩澄清石灰水,按要求回答下列问题:
(1)以上物质能导电的是_______ (填序号),属于电解质的是_______ (填序号)。
(2)①在熔融状态的电离方程式为_______ 。
(3)①和⑨反应的离子方程式_______ 。
(4)②与⑥的水溶液反应的离子方程式_______ 。
(5)足量的⑩与⑨的水溶液反应的离子方程式_______ 。
 ⑧乙醇 ⑨小苏打 ⑩澄清石灰水,按要求回答下列问题:
⑧乙醇 ⑨小苏打 ⑩澄清石灰水,按要求回答下列问题:(1)以上物质能导电的是
(2)①在熔融状态的电离方程式为
(3)①和⑨反应的离子方程式
(4)②与⑥的水溶液反应的离子方程式
(5)足量的⑩与⑨的水溶液反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】按要求写出(1)(2)(3)反应的离子方程式和符合离子反应(4)的化学方程式。
(1)铁与硫酸反应:_____ 。
(2)Fe2O3与盐酸反应:_____ 。
(3)Ba(OH)2溶液与硫酸铜溶液反应:____ 。
(4)Ca2++CO =CaCO3↓
=CaCO3↓_____ 。
(1)铁与硫酸反应:
(2)Fe2O3与盐酸反应:
(3)Ba(OH)2溶液与硫酸铜溶液反应:
(4)Ca2++CO
 =CaCO3↓
=CaCO3↓
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】在3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O反应中,
(1)______ 元素被氧化, ______ 是氧化剂;
(2)______ 是氧化产物, ______ 发生氧化反应;
(3)被还原的HNO3与参加反应的HNO3物质的量之比是______ ;
(4)用双线桥标出该反应电子转移的方向和数目:3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O_________________ ;
(5)当有8mol HNO3被还原时,反应转移___________ 个电子;
(6)写出该反应的离子反应方程式___________________________ 。
(1)
(2)
(3)被还原的HNO3与参加反应的HNO3物质的量之比是
(4)用双线桥标出该反应电子转移的方向和数目:3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O
(5)当有8mol HNO3被还原时,反应转移
(6)写出该反应的离子反应方程式
您最近一年使用:0次
【推荐2】K2Cr2O7(橙色)、Cr2(SO4)3(绿色)、K2SO4、H2SO4、C2H5OH、CH3COOH和H2O分别属于同一氧化还原反应中的反应物和生成物,该反应原理可以用于检查司机是否酒后开车。
(1)该反应中的还原剂是________________ 。
(2)若司机酒后开车,检测仪器内物质显示出____________ 色。
(3)在反应中,铬元素的化合价从_______ 价变为________ 价。
(4)写出并配平该反应的化学方程式________________ 。
(5)如果在反应中生成1mol氧化产物,转移的电子总数为_____________ 。
(1)该反应中的还原剂是
(2)若司机酒后开车,检测仪器内物质显示出
(3)在反应中,铬元素的化合价从
(4)写出并配平该反应的化学方程式
(5)如果在反应中生成1mol氧化产物,转移的电子总数为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】磷化铝(AlP)和磷化氢(PH3)都是粮食储备常用的高效熏蒸杀虫剂。
(1)磷元素在元素周期表中的位置:_______ ,AlP遇水蒸气会发生反应放出PH3气体,PH3中的P原子的杂化方式为_______ 杂化,该反应的另一种产物的化学式为_______ 。
(2) 具有强还原性,能与
具有强还原性,能与 溶液反应,配平该反应的化学方程式:
溶液反应,配平该反应的化学方程式:_______ 。

(3)工业制备 的流程如图所示。
的流程如图所示。

① 次磷酸属于_______ 元酸。
② 白磷和烧碱溶液反应的化学方程式为:_______ 。
③ 若起始时有1 mol P4参加反应,则整个工业流程中共生成_______ mol  (不考虑产物损失)
(不考虑产物损失)
(1)磷元素在元素周期表中的位置:
(2)
 具有强还原性,能与
具有强还原性,能与 溶液反应,配平该反应的化学方程式:
溶液反应,配平该反应的化学方程式:
(3)工业制备
 的流程如图所示。
的流程如图所示。
① 次磷酸属于
② 白磷和烧碱溶液反应的化学方程式为:
③ 若起始时有1 mol P4参加反应,则整个工业流程中共生成
 (不考虑产物损失)
(不考虑产物损失)
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】某无色待测液中可能含有 、
、 、
、 、
、 、
、 等阳离子。某同学进行如下实验:
等阳离子。某同学进行如下实验:
I.加入过量的稀盐酸,有白色沉淀生成。
II.过滤,取少许滤液,向其中加入过量的稀硫酸,又有白色沉淀生成。
III.另取少量步骤II中的滤液,加入 溶液至溶液呈碱性,加热,可产生使湿润的红色石蕊试纸变蓝色的气体。
溶液至溶液呈碱性,加热,可产生使湿润的红色石蕊试纸变蓝色的气体。
请回答下列问题:
(1)待测液中一定含有的离子是_______ ,一定不含有的离子是_______ 。
(2)还有一种离子不能确定是否存在,检验这种离子的实验时观察到的现象是_______ 。
(3)请你写出“步骤III”中产生气体的离子方程式_______ 。
 、
、 、
、 、
、 、
、 等阳离子。某同学进行如下实验:
等阳离子。某同学进行如下实验:I.加入过量的稀盐酸,有白色沉淀生成。
II.过滤,取少许滤液,向其中加入过量的稀硫酸,又有白色沉淀生成。
III.另取少量步骤II中的滤液,加入
 溶液至溶液呈碱性,加热,可产生使湿润的红色石蕊试纸变蓝色的气体。
溶液至溶液呈碱性,加热,可产生使湿润的红色石蕊试纸变蓝色的气体。请回答下列问题:
(1)待测液中一定含有的离子是
(2)还有一种离子不能确定是否存在,检验这种离子的实验时观察到的现象是
(3)请你写出“步骤III”中产生气体的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】研究含氮元素物质的反应对生产、生活、科研等方面具有重要的意义。请回答下列问题: 不稳定,在水溶液中就会发生歧化反应,其中一种产物为
不稳定,在水溶液中就会发生歧化反应,其中一种产物为 。
。
请回答:
(1)写出肼的电子式______ 。
(2)写出反应I的化学方程式______ 。
(3)下列说法正确的是______。
(4)已知: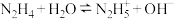 ,
, 与
与 溶液作用,产生常见气体M,并生成一种溶于稀硝酸的白色沉淀N。
溶液作用,产生常见气体M,并生成一种溶于稀硝酸的白色沉淀N。
①生成的气体M和白色沉淀N的成分分别是______ 、______ (填化学式)。
②请设计实验验证白色沉淀N的组成元素______ 。

已知:①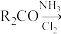
 (异肼)
(异肼)
 不稳定,在水溶液中就会发生歧化反应,其中一种产物为
不稳定,在水溶液中就会发生歧化反应,其中一种产物为 。
。请回答:
(1)写出肼的电子式
(2)写出反应I的化学方程式
(3)下列说法正确的是______。
A.碱性: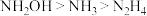 |
| B.肼可以用做还原剂,也可用做配合物的配体 |
| C.肼在水中的溶解度小于在苯中的溶解度 |
| D.反应Ⅱ中的产物之一可以循环利用 |
(4)已知:
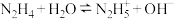 ,
, 与
与 溶液作用,产生常见气体M,并生成一种溶于稀硝酸的白色沉淀N。
溶液作用,产生常见气体M,并生成一种溶于稀硝酸的白色沉淀N。①生成的气体M和白色沉淀N的成分分别是
②请设计实验验证白色沉淀N的组成元素
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】完成下列问题。
(1)向CuCl2溶液中滴加NaOH溶液,现象:_______ ,离子方程式:_______ 。
(2)向Ba(OH)2溶液中加入稀硫酸,现象:_______ ,离子方程式:_______ 。
(3)某无色透明溶液可能存在大量Ag+、Mg2+、Fe3+、Cu2+、Cl-、NO 、CO
、CO 、K+中的一种或几种,请填写下列空白:
、K+中的一种或几种,请填写下列空白:
①取少量原溶液,加入过量稀盐酸,有白色沉淀生成,再加入过量稀硝酸,沉淀不消失,说明原溶液中肯定存在的离子是_______ 。
②取①的滤液加过量的NaOH溶液,出现白色沉淀,说明原溶液中肯定有_______ ,有关反应的离子方程式为_______ 。
③通过以上叙述可知溶液中肯定不存在的离子是_______ ,可能存在的离子是_______ 。
(1)向CuCl2溶液中滴加NaOH溶液,现象:
(2)向Ba(OH)2溶液中加入稀硫酸,现象:
(3)某无色透明溶液可能存在大量Ag+、Mg2+、Fe3+、Cu2+、Cl-、NO
 、CO
、CO 、K+中的一种或几种,请填写下列空白:
、K+中的一种或几种,请填写下列空白:①取少量原溶液,加入过量稀盐酸,有白色沉淀生成,再加入过量稀硝酸,沉淀不消失,说明原溶液中肯定存在的离子是
②取①的滤液加过量的NaOH溶液,出现白色沉淀,说明原溶液中肯定有
③通过以上叙述可知溶液中肯定不存在的离子是
您最近一年使用:0次

 “酸浸氧化”中,
“酸浸氧化”中,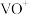 被
被 氧化成
氧化成 ,写出
,写出

