研究含氮元素物质的反应对生产、生活、科研等方面具有重要的意义。请回答下列问题: 不稳定,在水溶液中就会发生歧化反应,其中一种产物为
不稳定,在水溶液中就会发生歧化反应,其中一种产物为 。
。
请回答:
(1)写出肼的电子式______ 。
(2)写出反应I的化学方程式______ 。
(3)下列说法正确的是______。
(4)已知: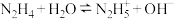 ,
, 与
与 溶液作用,产生常见气体M,并生成一种溶于稀硝酸的白色沉淀N。
溶液作用,产生常见气体M,并生成一种溶于稀硝酸的白色沉淀N。
①生成的气体M和白色沉淀N的成分分别是______ 、______ (填化学式)。
②请设计实验验证白色沉淀N的组成元素______ 。

已知:①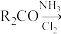
 (异肼)
(异肼)
 不稳定,在水溶液中就会发生歧化反应,其中一种产物为
不稳定,在水溶液中就会发生歧化反应,其中一种产物为 。
。请回答:
(1)写出肼的电子式
(2)写出反应I的化学方程式
(3)下列说法正确的是______。
A.碱性: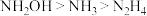 |
| B.肼可以用做还原剂,也可用做配合物的配体 |
| C.肼在水中的溶解度小于在苯中的溶解度 |
| D.反应Ⅱ中的产物之一可以循环利用 |
(4)已知:
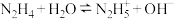 ,
, 与
与 溶液作用,产生常见气体M,并生成一种溶于稀硝酸的白色沉淀N。
溶液作用,产生常见气体M,并生成一种溶于稀硝酸的白色沉淀N。①生成的气体M和白色沉淀N的成分分别是
②请设计实验验证白色沉淀N的组成元素
更新时间:2024-05-22 08:34:31
|
相似题推荐
【推荐1】回答下列问题
(1)CN2H4是离子化合物且各原子均满足稳定结构,写出CN2H4的电子式为___________ 。
(2)Al(OH)3具有一元弱酸的性质,在水中电离产生的含铝微粒具有正四面体结构,写出电离方程式___________ 。
(3)H2O、CH3OH的沸点如下表:
H2O的沸点比CH3OH高的原因是___________ 。
(1)CN2H4是离子化合物且各原子均满足稳定结构,写出CN2H4的电子式为
(2)Al(OH)3具有一元弱酸的性质,在水中电离产生的含铝微粒具有正四面体结构,写出电离方程式
(3)H2O、CH3OH的沸点如下表:
| 物质 | H2O | CH3OH |
| 沸点/°C | 100 | 64.7 |
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】回答下列问题
(1)联氨(又称肼,N2H4,无色液体)分子的电子式为____ ,其中氮的化合价为____ 。
(2)HClO的电子式为____ 。
(3)该气体(H2S)分子的电子式为____ 。
(4)以硼酸为原料可制得硼氢化钠(NaBH4),它是有机合成中的重要还原剂,其电子式为___________ 。
(5)H、C、N、O、Na、Al、S、Cl中任选元素组成一种四原子共价化合物,写出其电子式:____________ 。
(1)联氨(又称肼,N2H4,无色液体)分子的电子式为
(2)HClO的电子式为
(3)该气体(H2S)分子的电子式为
(4)以硼酸为原料可制得硼氢化钠(NaBH4),它是有机合成中的重要还原剂,其电子式为
(5)H、C、N、O、Na、Al、S、Cl中任选元素组成一种四原子共价化合物,写出其电子式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】A + B → X + Y + H2O(未配平,反应条件略去)是中学常见反应的化学方程式,请回答:
(1)若Y为黄绿色气体:
①当A、B的物质的量之比为1∶4且A为黑色固体时,该反应的离子方程式是_______ ;
②当A、B的物质的量之比为1∶6时,写出该反应的化学方程式,并用双线桥表示反应过程中的电子转移:_______ 。
③实验室处理尾气Y时常用NaOH而不用NaHSO3溶液,其原因是(用离子反应方程式表示)_______ 。
(2)若A为单质,B为无色油状黏稠液体,当 A、B的物质的量之比为1∶2时,则A可能为_______ ,检查其中刺激性气体产物X的方法是_______ 。
(3)常温下A在B的浓溶液中会“钝化”,且A可溶于X溶液中,若A为金属单质,A和B以物质的量之比1∶4反应。
①过量的A和100mL2mol/L的B溶液充分反应后将溶液稀释至500mL后溶液中阴离子的物质的量浓度为_______ 。
②含 a mol X的溶液溶解了一定量A后,若溶液中两种金属阳离子的物质的量之比为1∶2时,则被还原的X是_______ mol。
(4)若A、B、X、Y均为化合物。向A溶液中加入硝酸酸化的AgNO3溶液,产生白色沉淀;B的焰色为黄色。则A与B按物质的量之比1:4反应后,溶液中溶质的化学式为_______ 。
(5)若A、B、X、Y均为化合物。X为极易溶于水的气体,则盐A是_______ 盐,X极易溶于水的原因是:_______ 。
(1)若Y为黄绿色气体:
①当A、B的物质的量之比为1∶4且A为黑色固体时,该反应的离子方程式是
②当A、B的物质的量之比为1∶6时,写出该反应的化学方程式,并用双线桥表示反应过程中的电子转移:
③实验室处理尾气Y时常用NaOH而不用NaHSO3溶液,其原因是(用离子反应方程式表示)
(2)若A为单质,B为无色油状黏稠液体,当 A、B的物质的量之比为1∶2时,则A可能为
(3)常温下A在B的浓溶液中会“钝化”,且A可溶于X溶液中,若A为金属单质,A和B以物质的量之比1∶4反应。
①过量的A和100mL2mol/L的B溶液充分反应后将溶液稀释至500mL后溶液中阴离子的物质的量浓度为
②含 a mol X的溶液溶解了一定量A后,若溶液中两种金属阳离子的物质的量之比为1∶2时,则被还原的X是
(4)若A、B、X、Y均为化合物。向A溶液中加入硝酸酸化的AgNO3溶液,产生白色沉淀;B的焰色为黄色。则A与B按物质的量之比1:4反应后,溶液中溶质的化学式为
(5)若A、B、X、Y均为化合物。X为极易溶于水的气体,则盐A是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】现有以下物质:①Fe2(SO4)3 ②Cu ③KIO3 ④Fe(OH)3胶体 ⑤FeSO4溶液 ⑥干冰 ⑦稀硝酸 ⑧乙醇 ⑨熔融碳酸钠。回答下列问题:
(1)以上物质中属于混合物的是_______ (填序号,下同);属于电解质的是_______ ;上述状态下能导电的是_______ 。
(2)①的电离方程式为_______ 。
(3)向④中逐滴滴加⑦,可观察到的现象是_______ 。
(4)⑤中混有少量①,除杂过程中选用的试剂为_______ 。
(5)向②中加入少量⑦,发生反应的离子方程式为_______ 。
(6)③可发生如下反应 (未配平);配平该反应并用双线桥法分析电子转移的情况:
(未配平);配平该反应并用双线桥法分析电子转移的情况:_______ ;每生成1.27 g I2,反应中转移电子的物质的量为_______ 。
(1)以上物质中属于混合物的是
(2)①的电离方程式为
(3)向④中逐滴滴加⑦,可观察到的现象是
(4)⑤中混有少量①,除杂过程中选用的试剂为
(5)向②中加入少量⑦,发生反应的离子方程式为
(6)③可发生如下反应
 (未配平);配平该反应并用双线桥法分析电子转移的情况:
(未配平);配平该反应并用双线桥法分析电子转移的情况:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】回答下列问题:
(1)推测原子序数为82的元素在元素周期表中的位置是___________
(2)高铁酸钾(K2FeO4)是一种强氧化剂,可作为水处理剂和高容量电池材料。FeCl3与KClO在强碱性条件下反应可制取K2FeO4,同时生成KCl,其反应的离子方程式为___________
(3)bmLAl2(SO4)3溶液中含有agSO ,若把此溶液取一半加水稀释至2bmL,则稀释后溶液中Al3+的物质的量浓度为
,若把此溶液取一半加水稀释至2bmL,则稀释后溶液中Al3+的物质的量浓度为___________ mol/L
(4)向一定量的Fe、FeO、Fe2O3、Fe3O4的混合物中加入100mL1mol·L-1的盐酸,好使混合物完全反应,放出11.2mL(标准状况)气体,所得溶液中加入KSCN溶液不变红色。用足量的CO在高温下还原相同质量的该混合物,所得铁的质量为___________ 克
(5)在浓度均为4.0mol/L的盐酸和硫酸各100mL溶液中,分别加入等质量的铁粉,充分反应后生成气体体积比为2:3则加入铁粉的质量是___________ 克
(6)a克碳酸钠与碳酸氢钠的混合物,加热灼烧,固体质量为b克,求碳酸钠的质量分数___________
(7)0.2mol/LNa2SO360mL,恰好与含0.1mol/LK2M2O7的溶液40mL完全反应,试推测元素M在还原产物中的化合价___________ 价
(1)推测原子序数为82的元素在元素周期表中的位置是
(2)高铁酸钾(K2FeO4)是一种强氧化剂,可作为水处理剂和高容量电池材料。FeCl3与KClO在强碱性条件下反应可制取K2FeO4,同时生成KCl,其反应的离子方程式为
(3)bmLAl2(SO4)3溶液中含有agSO
 ,若把此溶液取一半加水稀释至2bmL,则稀释后溶液中Al3+的物质的量浓度为
,若把此溶液取一半加水稀释至2bmL,则稀释后溶液中Al3+的物质的量浓度为(4)向一定量的Fe、FeO、Fe2O3、Fe3O4的混合物中加入100mL1mol·L-1的盐酸,好使混合物完全反应,放出11.2mL(标准状况)气体,所得溶液中加入KSCN溶液不变红色。用足量的CO在高温下还原相同质量的该混合物,所得铁的质量为
(5)在浓度均为4.0mol/L的盐酸和硫酸各100mL溶液中,分别加入等质量的铁粉,充分反应后生成气体体积比为2:3则加入铁粉的质量是
(6)a克碳酸钠与碳酸氢钠的混合物,加热灼烧,固体质量为b克,求碳酸钠的质量分数
(7)0.2mol/LNa2SO360mL,恰好与含0.1mol/LK2M2O7的溶液40mL完全反应,试推测元素M在还原产物中的化合价
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】Fe2(SO4)3溶液可除去煤中以黄铁矿(FeS2)形式存在的硫元素,反应如下:
______FeS2 + ______Fe2(SO4)3 +______H2O →______FeSO4 + ______H2SO4
(1)试配平反应的化学方程式,并用单线桥标出电子转移方向及数目_____ ;还原剂是_______ ,还原产物是_________ ,被还原的元素是__________ 。
(2)Fe2(SO4)3溶液呈_____ 性,用离子方程式解释其原因________ 。
(3)检验上述反应中Fe2(SO4)3是否消耗完的实验方案:_________________________ 。
(4)该方法的优点之一是Fe2(SO4)3易再生。向反应后的溶液中通入__________ ,就能达到使Fe2(SO4)3再生的目的,方便且价廉。
(5)实验室.配制一定量FeSO4溶液时,需加入少量_____ 和_______ 其目的是_______ 。
______FeS2 + ______Fe2(SO4)3 +______H2O →______FeSO4 + ______H2SO4
(1)试配平反应的化学方程式,并用单线桥标出电子转移方向及数目
(2)Fe2(SO4)3溶液呈
(3)检验上述反应中Fe2(SO4)3是否消耗完的实验方案:
(4)该方法的优点之一是Fe2(SO4)3易再生。向反应后的溶液中通入
(5)实验室.配制一定量FeSO4溶液时,需加入少量
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】有一瓶澄清的溶液,其中可能含H+、 、K+、Al3+、Cu2+、Fe3+、
、K+、Al3+、Cu2+、Fe3+、 、I- 中的一种或几种,取该溶液进行如下实验:
、I- 中的一种或几种,取该溶液进行如下实验:
①用pH试纸检验,表明溶液呈强酸性。
②取部分溶液,加入数滴新制的氯水及少量的CC14,振荡后CC14层显紫色。
③另取部分溶液,逐滴加入稀NaOH溶液,使溶液从酸性逐渐转变为碱性,在滴加过程中有白色沉淀生产,后白色沉淀完全消失。
④将③得到的碱性溶液加热,有气体放出,该气体能使湿润的红色石蕊试纸变蓝。
根据上述实验事实回答:
(1) 在溶液中,肯定存在的离子有_______ ,肯定不存在的离子有______ 。
(2) 不能确定是否存在的离子有______ 。证明它(们)是否存在的实验方法是______ 。
(3)写出步骤②涉及的离子方程式,并用单线桥标出电子转移的方向和数目______ 。
(4)写出步骤④涉及的离子方程式______ 。
 、K+、Al3+、Cu2+、Fe3+、
、K+、Al3+、Cu2+、Fe3+、 、I- 中的一种或几种,取该溶液进行如下实验:
、I- 中的一种或几种,取该溶液进行如下实验:①用pH试纸检验,表明溶液呈强酸性。
②取部分溶液,加入数滴新制的氯水及少量的CC14,振荡后CC14层显紫色。
③另取部分溶液,逐滴加入稀NaOH溶液,使溶液从酸性逐渐转变为碱性,在滴加过程中有白色沉淀生产,后白色沉淀完全消失。
④将③得到的碱性溶液加热,有气体放出,该气体能使湿润的红色石蕊试纸变蓝。
根据上述实验事实回答:
(1) 在溶液中,肯定存在的离子有
(2) 不能确定是否存在的离子有
(3)写出步骤②涉及的离子方程式,并用单线桥标出电子转移的方向和数目
(4)写出步骤④涉及的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】有一包白色固体物质,可能含有CuSO4、Na2SO4、KNO3、NaNO3、Na2CO3、MgCl2中的一种或几种,现进行如下实验:
(1)将白色固体溶于水中,得到无色透明溶液。
(2)取少量上述溶液两份,其中一份滴加BaCl2溶液,立即产生白色沉淀,再加入稀硝酸,沉淀没有溶解。另一份溶液中滴加NaOH溶液,有白色沉淀生成。
根据以上实验现象可知,该白色固体中一定含有_________ ,一定没有________ ,可能有______________ 。
(1)将白色固体溶于水中,得到无色透明溶液。
(2)取少量上述溶液两份,其中一份滴加BaCl2溶液,立即产生白色沉淀,再加入稀硝酸,沉淀没有溶解。另一份溶液中滴加NaOH溶液,有白色沉淀生成。
根据以上实验现象可知,该白色固体中一定含有
您最近一年使用:0次



