Fe2(SO4)3溶液可除去煤中以黄铁矿(FeS2)形式存在的硫元素,反应如下:
______FeS2 + ______Fe2(SO4)3 +______H2O →______FeSO4 + ______H2SO4
(1)试配平反应的化学方程式,并用单线桥标出电子转移方向及数目_____ ;还原剂是_______ ,还原产物是_________ ,被还原的元素是__________ 。
(2)Fe2(SO4)3溶液呈_____ 性,用离子方程式解释其原因________ 。
(3)检验上述反应中Fe2(SO4)3是否消耗完的实验方案:_________________________ 。
(4)该方法的优点之一是Fe2(SO4)3易再生。向反应后的溶液中通入__________ ,就能达到使Fe2(SO4)3再生的目的,方便且价廉。
(5)实验室.配制一定量FeSO4溶液时,需加入少量_____ 和_______ 其目的是_______ 。
______FeS2 + ______Fe2(SO4)3 +______H2O →______FeSO4 + ______H2SO4
(1)试配平反应的化学方程式,并用单线桥标出电子转移方向及数目
(2)Fe2(SO4)3溶液呈
(3)检验上述反应中Fe2(SO4)3是否消耗完的实验方案:
(4)该方法的优点之一是Fe2(SO4)3易再生。向反应后的溶液中通入
(5)实验室.配制一定量FeSO4溶液时,需加入少量
更新时间:2019-11-20 20:07:57
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】实验室用MnO2跟浓盐酸共热反应制取Cl2,化学方程式是4HCl(浓)+MnO2 Cl2↑+MnCl2+2H2O
Cl2↑+MnCl2+2H2O
(1)HCl所表现的性质有___________ 。
(2)用双线桥法分析该反应电子转移的方向和数目___________ 。
(3)实验中,多余的Cl2可用___________ 来吸收处理, 写出该反应的离子方程式___________ 。
 Cl2↑+MnCl2+2H2O
Cl2↑+MnCl2+2H2O(1)HCl所表现的性质有
(2)用双线桥法分析该反应电子转移的方向和数目
(3)实验中,多余的Cl2可用
您最近一年使用:0次
【推荐2】完成下列问题。
(1)有下列反应:
①SO3+H2O=H2SO4
②Cl2+H2O=HCl+HClO
③2F2+2H2O=4HF+O2
④CO2+2NaOH=Na2CO3+H2O
上述反应中不属于氧化还原反应的是_______ (填序号,下同);H2O只作还原剂的是________ ;属于氧化还原反应,但其中的H2O既不被氧化,又不被还原的是___________ 。
(2)为治理汽车尾气中的NO和CO对环境的污染,可在汽车排气管上安装催化转化器,发生如下反应:2NO+2CO N2+2CO2。
N2+2CO2。
①用双线桥标出电子转移的方向和数目___________ 。
②若消耗标况22.4 L的NO得到还原产物的质量为_____ g,转移电子的物质的量为_______ mol。
(1)有下列反应:
①SO3+H2O=H2SO4
②Cl2+H2O=HCl+HClO
③2F2+2H2O=4HF+O2
④CO2+2NaOH=Na2CO3+H2O
上述反应中不属于氧化还原反应的是
(2)为治理汽车尾气中的NO和CO对环境的污染,可在汽车排气管上安装催化转化器,发生如下反应:2NO+2CO
 N2+2CO2。
N2+2CO2。①用双线桥标出电子转移的方向和数目
②若消耗标况22.4 L的NO得到还原产物的质量为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】Ⅰ.工业上利用电解饱和食盐水生产氯气(Cl2)、烧碱和氢气的化学方程式是:2NaCl+2H2O 2NaOH+Cl2↑+H2↑。
2NaOH+Cl2↑+H2↑。
(1)用双线桥表示出电子转移的方向和数目________ ,题干中反应改写成离子方程式是____ 。
(2)电解食盐水的过程中,被还原的元素是____________ ,氧化产物是______ 。
Ⅱ.四氧化三铁(Fe3O4)磁性纳米颗粒稳定、容易生产且用途广泛,是临床诊断、生物技术和环境化学领域多种潜在应用的有力工具。水热法制备Fe3O4纳米颗粒的反应是:3Fe2++2S2O32-+O2+xOH-=Fe3O4↓+S4O62-+2H2O。请回答下列问题。
(1)水热法制备Fe3O4纳米颗粒的反应中,还原剂是__________ 。
(2)反应的化学方程式中x=______ 。
(3)每生成1 mol Fe3O4,反应转移的电子为____ mol,被Fe2+还原的O2的物质的量为_____ mol。
 2NaOH+Cl2↑+H2↑。
2NaOH+Cl2↑+H2↑。(1)用双线桥表示出电子转移的方向和数目
(2)电解食盐水的过程中,被还原的元素是
Ⅱ.四氧化三铁(Fe3O4)磁性纳米颗粒稳定、容易生产且用途广泛,是临床诊断、生物技术和环境化学领域多种潜在应用的有力工具。水热法制备Fe3O4纳米颗粒的反应是:3Fe2++2S2O32-+O2+xOH-=Fe3O4↓+S4O62-+2H2O。请回答下列问题。
(1)水热法制备Fe3O4纳米颗粒的反应中,还原剂是
(2)反应的化学方程式中x=
(3)每生成1 mol Fe3O4,反应转移的电子为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】(1)写出CH3COOH的电离方程式:___ 。
(2)写出NaClO的水解离子方程式:___ 。
(3)CaSO4转化为CaCO3的离子方程式为:___ 。
(4)用已知浓度的NaOH溶液测定未知浓度的醋酸,选用的指示剂___ 。用已知浓度的HCl溶液测定未知浓度的氨水,选用的指示剂___ 。
(5)用a mol·L-1的HCl滴定未知浓度的NaOH溶液,用酚酞作指示剂,达到滴定终点的现象是___ 。
(2)写出NaClO的水解离子方程式:
(3)CaSO4转化为CaCO3的离子方程式为:
(4)用已知浓度的NaOH溶液测定未知浓度的醋酸,选用的指示剂
(5)用a mol·L-1的HCl滴定未知浓度的NaOH溶液,用酚酞作指示剂,达到滴定终点的现象是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】化合物 (
(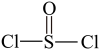 )是一种液态化合物,沸点77 ℃,在盛有
)是一种液态化合物,沸点77 ℃,在盛有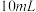 水的锥形瓶中小心地滴加8~10滴
水的锥形瓶中小心地滴加8~10滴 ,可观察到反应剧烈,液面上有白雾形成,并逸出有气味的气体,该气体可使沾有品红试液的滤纸褪色。轻轻振荡锥形瓶,待白雾消失后往溶液中滴加
,可观察到反应剧烈,液面上有白雾形成,并逸出有气味的气体,该气体可使沾有品红试液的滤纸褪色。轻轻振荡锥形瓶,待白雾消失后往溶液中滴加 溶液,有不溶于稀硝酸的白色沉淀析出。
溶液,有不溶于稀硝酸的白色沉淀析出。
(1)根据以上实验,写出 与水反应的化学方程式:
与水反应的化学方程式:_____________________________________ 。
(2)蒸干 溶液得不到
溶液得不到 固体,只能得到
固体,只能得到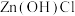 ,所以工业上往往用
,所以工业上往往用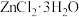 和
和 混合后共热来制取无水
混合后共热来制取无水 。
。
①写出蒸干 溶液过程中发生的化学反应方程式
溶液过程中发生的化学反应方程式__________________________________________________ 。
②写出该种制法可行性的原因:_______________________________________________ ,_______________________________________________________________________ 。(至少写出两个原因)。
 (
(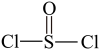 )是一种液态化合物,沸点77 ℃,在盛有
)是一种液态化合物,沸点77 ℃,在盛有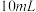 水的锥形瓶中小心地滴加8~10滴
水的锥形瓶中小心地滴加8~10滴 ,可观察到反应剧烈,液面上有白雾形成,并逸出有气味的气体,该气体可使沾有品红试液的滤纸褪色。轻轻振荡锥形瓶,待白雾消失后往溶液中滴加
,可观察到反应剧烈,液面上有白雾形成,并逸出有气味的气体,该气体可使沾有品红试液的滤纸褪色。轻轻振荡锥形瓶,待白雾消失后往溶液中滴加 溶液,有不溶于稀硝酸的白色沉淀析出。
溶液,有不溶于稀硝酸的白色沉淀析出。(1)根据以上实验,写出
 与水反应的化学方程式:
与水反应的化学方程式:(2)蒸干
 溶液得不到
溶液得不到 固体,只能得到
固体,只能得到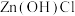 ,所以工业上往往用
,所以工业上往往用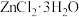 和
和 混合后共热来制取无水
混合后共热来制取无水 。
。①写出蒸干
 溶液过程中发生的化学反应方程式
溶液过程中发生的化学反应方程式②写出该种制法可行性的原因:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】完成下列填空:硼氧化钠(NaBH4)是合成中常用的还原剂。采用NaBO2为主要原料制备NaBH4(B元素化合价为+3)的反应为:NaBO2+SiO2+Na+H2 NaBH4+Na2SiO3(未配平);硅酸钠俗称泡花碱,又名水玻璃,在工业生产中也有广泛应用(已知硅酸为难溶性弱酸)
NaBH4+Na2SiO3(未配平);硅酸钠俗称泡花碱,又名水玻璃,在工业生产中也有广泛应用(已知硅酸为难溶性弱酸)
完成下列填空:
(1)上述反应中,原子最外层有两个未成对电子的元素是_____ (填元素符号)。SiO2熔点高的原因是_____ 。
(2)上述反应中H2与Na的物质的量之比为_____ 。
(3)硅酸钠水溶液产生硅酸(H2SiO3),硬化粘结,且有碱性,其原因是_____ (用离子方程式表示)。铸造工艺中可用氯化铵作为水玻璃的硬化剂。试用平衡原理加以解释_____ 。
(4)NaBH4可使许多金属离子还原成金属单质。例如它从含金离子(Au3+)的废液中提取Au.配平该反应的离子方程式:_____ Au3++_____ BH4﹣+_____ OH-→_____ Au+_____ BO2﹣+_____ H2O。
(5)最新研究发现以NaBH4和H2O2为原料,NaOH溶液作电解质溶液,可以设计成全液流电池,则每消耗1L6mol/L H2O2溶液,理论上流过电路中的电子数为_____ 。
 NaBH4+Na2SiO3(未配平);硅酸钠俗称泡花碱,又名水玻璃,在工业生产中也有广泛应用(已知硅酸为难溶性弱酸)
NaBH4+Na2SiO3(未配平);硅酸钠俗称泡花碱,又名水玻璃,在工业生产中也有广泛应用(已知硅酸为难溶性弱酸)完成下列填空:
(1)上述反应中,原子最外层有两个未成对电子的元素是
(2)上述反应中H2与Na的物质的量之比为
(3)硅酸钠水溶液产生硅酸(H2SiO3),硬化粘结,且有碱性,其原因是
(4)NaBH4可使许多金属离子还原成金属单质。例如它从含金离子(Au3+)的废液中提取Au.配平该反应的离子方程式:
(5)最新研究发现以NaBH4和H2O2为原料,NaOH溶液作电解质溶液,可以设计成全液流电池,则每消耗1L6mol/L H2O2溶液,理论上流过电路中的电子数为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】根据硅和二氧化硅的性质,回答下列问题:
(1)月球上某矿石经处理得到的MgO中含有少量SiO2,除去SiO2的离子方程式为___ 。
(2)由粗硅制纯硅过程如下:Si(粗) SiCl4
SiCl4 SiCl4(纯)
SiCl4(纯) Si(纯),请写出上述过程中有关反应的化学方程式:
Si(纯),请写出上述过程中有关反应的化学方程式:___ ,___ 。
(1)月球上某矿石经处理得到的MgO中含有少量SiO2,除去SiO2的离子方程式为
(2)由粗硅制纯硅过程如下:Si(粗)
 SiCl4
SiCl4 SiCl4(纯)
SiCl4(纯) Si(纯),请写出上述过程中有关反应的化学方程式:
Si(纯),请写出上述过程中有关反应的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】污染物的有效去除和资源的充分利用是化学造福人类的重要研究课题。工业上以硫铁矿为原料制硫酸所产生的尾气除了含有N2、O2外,还含有SO2。为了保护环境,同时提高硫酸工业的综合经济效益,应尽可能将尾气中的SO2转化为有用的产品。
治理方案Ⅰ:
(1)将尾气通入氨水中,能发生多个反应,写出其中可能发生的两个氧化还原反应的化学方程式:_______________ 、_______________ 。
治理方案Ⅱ:
某研究小组利用软锰矿(主要成分为MnO2,另含有少量铁、铝、铜、镍等金属化合物)作脱硫剂,通过如下流程既去除尾气中的SO2,又制得电池材料MnO2 (反应条件已省略)。
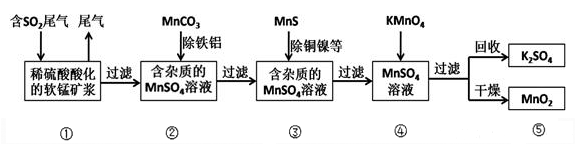
请回答下列问题:
(2)用MnCO3能除去溶液中Al3+和Fe3+其原因是___________________________ ,用MnS除去溶液中的Cu2+的离子方程式为_______________ 。
(3)流程图④过程中发生的主要反应的化学方程式为___________________ 。
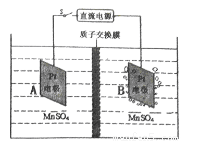
(4)MnO2可作超级电容器材料。工业上用下图所示装置制备MnO2。接通电源后,A电极的电极反应式为:_______________ ,当制备lmol MnO2,则膜两侧电解液的质量变化差(△m左-△m右)为_______________ g。
治理方案Ⅰ:
(1)将尾气通入氨水中,能发生多个反应,写出其中可能发生的两个氧化还原反应的化学方程式:
治理方案Ⅱ:
某研究小组利用软锰矿(主要成分为MnO2,另含有少量铁、铝、铜、镍等金属化合物)作脱硫剂,通过如下流程既去除尾气中的SO2,又制得电池材料MnO2 (反应条件已省略)。

请回答下列问题:
(2)用MnCO3能除去溶液中Al3+和Fe3+其原因是
(3)流程图④过程中发生的主要反应的化学方程式为
(4)MnO2可作超级电容器材料。工业上用下图所示装置制备MnO2。接通电源后,A电极的电极反应式为:

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】铁、钴(Co)、镍(Ni)是同族元素,主要化合价均为+2、+3价,都是较活泼的金属,它们的化合物在工业上有重要的应用。完成下列填空:
(1)Co2+和Fe3+均可与KSCN溶液发生相似的反应。向CoCl2溶液中加入KSCN溶液,生成某种带有两个单位负电荷的蓝色离子,其化学式为_______________________ 。
(2)碳酸镍可用于电镀、陶瓷器着色等。镍矿渣中镍元素的主要存在形式是Ni(OH)2和NiS,从镍矿渣出发制备碳酸镍的反应如下:
第一步:向镍矿渣中加入稀硫酸和NaClO3浸取出Ni2+。
反应的离子方程式有:
①__________ ;
②___NiS+___ +___H+→___Ni2++___S+___Cl-+___H2O
+___H+→___Ni2++___S+___Cl-+___H2O
配平反应②。__________
第二步:再加入Na2CO3溶液,产生的沉淀即为碳酸镍。
检验Ni2+是否沉淀完全的方法是_____________________________________ 。
(1)Co2+和Fe3+均可与KSCN溶液发生相似的反应。向CoCl2溶液中加入KSCN溶液,生成某种带有两个单位负电荷的蓝色离子,其化学式为
(2)碳酸镍可用于电镀、陶瓷器着色等。镍矿渣中镍元素的主要存在形式是Ni(OH)2和NiS,从镍矿渣出发制备碳酸镍的反应如下:
第一步:向镍矿渣中加入稀硫酸和NaClO3浸取出Ni2+。
反应的离子方程式有:
①
②___NiS+___
 +___H+→___Ni2++___S+___Cl-+___H2O
+___H+→___Ni2++___S+___Cl-+___H2O配平反应②。
第二步:再加入Na2CO3溶液,产生的沉淀即为碳酸镍。
检验Ni2+是否沉淀完全的方法是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】某无色透明溶液中可能含有下列离子中的一种或几种:Na+、Mg2+、Cu2+、OH-、Cl-、 、
、 、
、 。现进行如下实验:
。现进行如下实验:
①滴加紫色石蕊溶液检验,溶液变蓝色。
②另取少量溶液逐滴滴加盐酸至过量,无气体放出,再加入BaCl2溶液后,有白色沉淀生成。
③另取少量溶液用硝酸酸化后,加入AgNO3溶液有白色沉淀生成。
(1)根据上述实验推断:原溶液中肯定有___ 离子,肯定没有___ 离子,不能肯定存在___ 离子。
(2)写出相关反应的离子方程式____
 、
、 、
、 。现进行如下实验:
。现进行如下实验:①滴加紫色石蕊溶液检验,溶液变蓝色。
②另取少量溶液逐滴滴加盐酸至过量,无气体放出,再加入BaCl2溶液后,有白色沉淀生成。
③另取少量溶液用硝酸酸化后,加入AgNO3溶液有白色沉淀生成。
(1)根据上述实验推断:原溶液中肯定有
(2)写出相关反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】某课外活动小组收集了一种合金进行研究。
(1)外观暗灰色,表皮光滑。
(2)在酒精灯上灼烧,火焰呈绿色;合金片熔化,但不滴落。
(3)取刮去表皮的金属10.0 g,放入足量稀硫酸中,收集到标准状况下的H 2 9.96 L。
(4)另取刮去表皮的金属10.0 g,放入足量NaOH(aq)中,也收集到标准状况下的H 2 9.96 L。
试据此判断,合金中一定含有的元素是______ 。
A.Cu B.Mg C.Al D.Fe
如果该合金中只含两种元素,它们的质量比是______ 。
(1)外观暗灰色,表皮光滑。
(2)在酒精灯上灼烧,火焰呈绿色;合金片熔化,但不滴落。
(3)取刮去表皮的金属10.0 g,放入足量稀硫酸中,收集到标准状况下的H 2 9.96 L。
(4)另取刮去表皮的金属10.0 g,放入足量NaOH(aq)中,也收集到标准状况下的H 2 9.96 L。
试据此判断,合金中一定含有的元素是
A.Cu B.Mg C.Al D.Fe
如果该合金中只含两种元素,它们的质量比是
您最近一年使用:0次



