为了验证氯气的氧化性,将氯气分别通入①KI溶液、②H2S溶液、③FeBr2溶液中:
(1)如果要将①中反应后的单质氧化产物从水溶液中分离,需先进行_______ (填操作名称),然后进行分液即可;
(2)溶液②中出现淡黄色的沉淀,且反应后溶液呈强酸性,试写出反应的化学方程式_______ ;
(3)反应③进行一段时间后振荡,溶液呈黄色,罗同学提出溶液变色的原因可能生成Br2或Fe3+,请问他该如何通过实验确认生成Br2(限选用的试剂有:酸性高锰酸钾溶液、氢氧化钠溶液、四氯化碳、硝酸银溶液、淀粉—碘化钾溶液)_______ ;如果生成的是Fe3+,请写出氯化铁溶液腐蚀铜板的离子方程式:_______ 。
(4)已知:①氧化还原反应有先后顺序,同种氧化剂和还原性不同的还原剂反应时,还原性强的先被氧化
②还原性: >I->Fe2+>Br-
>I->Fe2+>Br-
向含 、Fe2+、Br-、I-各0.1mol的溶液中通入标准状况下的Cl2,通入Cl2的体积和溶液中相关离子的物质的量的关系图如下
、Fe2+、Br-、I-各0.1mol的溶液中通入标准状况下的Cl2,通入Cl2的体积和溶液中相关离子的物质的量的关系图如下

请回答:
①图A中纵坐标代表的相关离子是_______ 。
②图B中发生的离子方程式_______ 。
③当溶液中四种离子恰好完全被氧化时,溶液中阴离子的物质的量为___ 。(不考虑水的微弱电离)
(1)如果要将①中反应后的单质氧化产物从水溶液中分离,需先进行
(2)溶液②中出现淡黄色的沉淀,且反应后溶液呈强酸性,试写出反应的化学方程式
(3)反应③进行一段时间后振荡,溶液呈黄色,罗同学提出溶液变色的原因可能生成Br2或Fe3+,请问他该如何通过实验确认生成Br2(限选用的试剂有:酸性高锰酸钾溶液、氢氧化钠溶液、四氯化碳、硝酸银溶液、淀粉—碘化钾溶液)
(4)已知:①氧化还原反应有先后顺序,同种氧化剂和还原性不同的还原剂反应时,还原性强的先被氧化
②还原性:
 >I->Fe2+>Br-
>I->Fe2+>Br-向含
 、Fe2+、Br-、I-各0.1mol的溶液中通入标准状况下的Cl2,通入Cl2的体积和溶液中相关离子的物质的量的关系图如下
、Fe2+、Br-、I-各0.1mol的溶液中通入标准状况下的Cl2,通入Cl2的体积和溶液中相关离子的物质的量的关系图如下
请回答:
①图A中纵坐标代表的相关离子是
②图B中发生的离子方程式
③当溶液中四种离子恰好完全被氧化时,溶液中阴离子的物质的量为
更新时间:2021-08-07 11:12:36
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
【推荐1】实验室用如下装置制取氯气,并用氯气进行实验。回答下列问题:

(1)A中盛有浓盐酸,B中盛有MnO2,写出反应的化学方程式___________ 。
(2)D中放入浓H2SO4的目的是___________ 。
(3)E中为红色干布条,F中为红色湿布条,可观察到的现象是___________ 。
(4)G处的现象是___________ 。
(5)家庭中常用消毒液(主要成分NaClO)与洁厕灵(主要成分盐酸)清洁卫生。消毒液与洁厕灵不能同时使用,原因是(用离子方程式表示)___________ 。

(1)A中盛有浓盐酸,B中盛有MnO2,写出反应的化学方程式
(2)D中放入浓H2SO4的目的是
(3)E中为红色干布条,F中为红色湿布条,可观察到的现象是
(4)G处的现象是
(5)家庭中常用消毒液(主要成分NaClO)与洁厕灵(主要成分盐酸)清洁卫生。消毒液与洁厕灵不能同时使用,原因是(用离子方程式表示)
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】下图中,B、D、E、F、G是氧化物且B为红棕色固体,F、K是氢化物且F为常温常压下常见无色液体,C、H是日常生活中最常见的金属单质,J是黄绿色气体。O是白色沉淀且B、H、L、M、N、O中含有同种元素,I是基础化学工业的重要产品(图中部分反应物和生成物没有列出)。
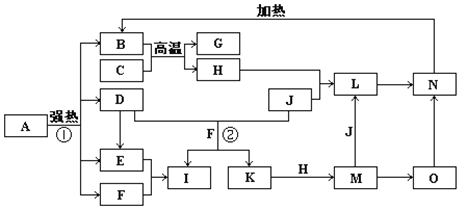
请按要求回答:
(1)写出G、L的化学式G:_____________________ ,L:______________________
(2)反应②的离子方程式________________________________________________ 。
(3)写出反应M→L的离子方程式为________________________________________ 。
(4)若将O敞口久置,变质过程中的现象为___________________________________
发生的化学方程式为__________________________________________________ 。

请按要求回答:
(1)写出G、L的化学式G:
(2)反应②的离子方程式
(3)写出反应M→L的离子方程式为
(4)若将O敞口久置,变质过程中的现象为
发生的化学方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】某学习小组进行 的性质探究。
的性质探究。
Ⅰ.利用点滴板实验,首先向a中滴加数滴浓盐酸,然后迅速用培养皿盖上整个点滴板,一段时间后出现不同现象:b中溶液变成棕黄色;c中溶液褪色;d中试纸变蓝色(碘遇淀粉变蓝)。

(1)下列判断正确的是__________ (填字母序号)。
A.a中 是氧化剂 B.b中现象表明
是氧化剂 B.b中现象表明 部分被氧化
部分被氧化
C.c中现象证明 具有漂白性 D.d中现象证明氧化性:
具有漂白性 D.d中现象证明氧化性: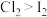
E.a、b、c、d中均有氧化还原反应发生
Ⅱ.该小组设想将少量 通入含相同浓度的
通入含相同浓度的 和
和 的混合溶液中,想比较
的混合溶液中,想比较 和
和 的还原性的强弱。
的还原性的强弱。
(2)现有如下几种装置:
A. B.
B. C.
C. D.
D. E.
E.
实验必须 的装置是
_____ (按 气流方向的顺序填写);
气流方向的顺序填写);
实验开始后,控制通入少量氯气,通过观察混合溶液颜色的变化_______ (填“能”或“不能”)判断反应的先后顺序,理由__________ 。
(3)为了得出结论某同学设计实验如图所示:

写出预期相关现象和所对应的结论__________ (有几种写几种)。
 的性质探究。
的性质探究。Ⅰ.利用点滴板实验,首先向a中滴加数滴浓盐酸,然后迅速用培养皿盖上整个点滴板,一段时间后出现不同现象:b中溶液变成棕黄色;c中溶液褪色;d中试纸变蓝色(碘遇淀粉变蓝)。

(1)下列判断正确的是
A.a中
 是氧化剂 B.b中现象表明
是氧化剂 B.b中现象表明 部分被氧化
部分被氧化C.c中现象证明
 具有漂白性 D.d中现象证明氧化性:
具有漂白性 D.d中现象证明氧化性: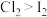
E.a、b、c、d中均有氧化还原反应发生
Ⅱ.该小组设想将少量
 通入含相同浓度的
通入含相同浓度的 和
和 的混合溶液中,想比较
的混合溶液中,想比较 和
和 的还原性的强弱。
的还原性的强弱。(2)现有如下几种装置:
A.
 B.
B. C.
C. D.
D. E.
E.
实验

 气流方向的顺序填写);
气流方向的顺序填写);实验开始后,控制通入少量氯气,通过观察混合溶液颜色的变化
(3)为了得出结论某同学设计实验如图所示:

写出预期相关现象和所对应的结论
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】现有金属单质A、B和气体甲、乙、丙以及物质C、D、E、F,它们之间能发生如下反应。(图中有些反应的产物和反应条件没有标出)

(1)A的原子结构示意图为_____________ ,丙的化学式为_____________ 。
(2)金属A、B和气体甲、乙、丙以及物质C、D、E、F中不能导电的有__________________ 、属于电解质的有___________ 。(填“A”“B”“甲”“乙”“丙”“C”“D”“E”“F”)
(3)写出转化①发生的化学方程式:____________________ ,写出转化④发生的离子方程式:____________________ 。
(4)将Na2O2投入到E溶液中,可以观察到的现象是:_____________ 。

(1)A的原子结构示意图为
(2)金属A、B和气体甲、乙、丙以及物质C、D、E、F中不能导电的有
(3)写出转化①发生的化学方程式:
(4)将Na2O2投入到E溶液中,可以观察到的现象是:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】实验室以孔雀石[主要成分是CuCO3·Cu(OH)2,还含有少量杂质FeO、Fe2O3、SiO2]为原料制备CuSO4·5H2O步骤如下:
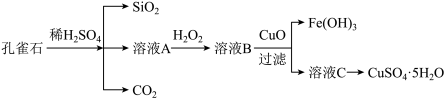
请回答下列问题:
(1)溶液A的金属离子有Fe3+和______________ 。
(2)溶液A中加入H2O2的目的是______________ ,发生的离子方程式为_____________________ 。
(3)由溶液C获得CuSO4·5H2O,需要经过加热蒸发、______________ 、过滤等操作。
(4)溶液B与CuO反应生成Fe(OH)3和溶液C的化学方程式为________________________ 。

请回答下列问题:
(1)溶液A的金属离子有Fe3+和
(2)溶液A中加入H2O2的目的是
(3)由溶液C获得CuSO4·5H2O,需要经过加热蒸发、
(4)溶液B与CuO反应生成Fe(OH)3和溶液C的化学方程式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】磷酸亚铁 为黄白色至米色粉末﹐难溶于水和醋酸,溶于无机酸,可作为营养增补剂(铁质强化剂)。合成磷酸亚铁时的主要离子反应为:
为黄白色至米色粉末﹐难溶于水和醋酸,溶于无机酸,可作为营养增补剂(铁质强化剂)。合成磷酸亚铁时的主要离子反应为: 
(1)合成磷酸亚铁时,在三颈烧瓶中先加入维生素C稀溶液(具有还原性)作底液,再向烧瓶中滴入 与
与 的混合溶液,再滴入
的混合溶液,再滴入 溶液,水浴加热、保持
溶液,水浴加热、保持 左右不断搅拌(装置如图所示)。
左右不断搅拌(装置如图所示)。

①配制合成所需的 溶液时,蒸馏水事先要煮沸、冷却,煮沸的目的是
溶液时,蒸馏水事先要煮沸、冷却,煮沸的目的是___________ 。
②用维生素C作底液而不用铁粉,其主要原因是___________ 。
③合成时需保持 左右,控制pH不能太大也不能太小的原因是
左右,控制pH不能太大也不能太小的原因是___________ 。
(2)从三颈烧瓶得到产品需要过滤﹑洗涤等步骤,判断沉淀洗涤干净的操作是___________ 。
(3)合成磷酸亚铁所需的 在工业上可由硫铁矿烧渣(主要成分为
在工业上可由硫铁矿烧渣(主要成分为 、
、 、
、 )制备,其工业流程如下(相关金属离子生成氢氧化物沉淀的pH如下表所示):
)制备,其工业流程如下(相关金属离子生成氢氧化物沉淀的pH如下表所示):

①矿渣的主要成分是___________ (填化学式)。
②加入 溶液调pH的范围是
溶液调pH的范围是___________ 。
③“酸化、调pH、结晶”过程中都需要进行的分离操作是___________ 。
 为黄白色至米色粉末﹐难溶于水和醋酸,溶于无机酸,可作为营养增补剂(铁质强化剂)。合成磷酸亚铁时的主要离子反应为:
为黄白色至米色粉末﹐难溶于水和醋酸,溶于无机酸,可作为营养增补剂(铁质强化剂)。合成磷酸亚铁时的主要离子反应为: 
(1)合成磷酸亚铁时,在三颈烧瓶中先加入维生素C稀溶液(具有还原性)作底液,再向烧瓶中滴入
 与
与 的混合溶液,再滴入
的混合溶液,再滴入 溶液,水浴加热、保持
溶液,水浴加热、保持 左右不断搅拌(装置如图所示)。
左右不断搅拌(装置如图所示)。
①配制合成所需的
 溶液时,蒸馏水事先要煮沸、冷却,煮沸的目的是
溶液时,蒸馏水事先要煮沸、冷却,煮沸的目的是②用维生素C作底液而不用铁粉,其主要原因是
③合成时需保持
 左右,控制pH不能太大也不能太小的原因是
左右,控制pH不能太大也不能太小的原因是(2)从三颈烧瓶得到产品需要过滤﹑洗涤等步骤,判断沉淀洗涤干净的操作是
(3)合成磷酸亚铁所需的
 在工业上可由硫铁矿烧渣(主要成分为
在工业上可由硫铁矿烧渣(主要成分为 、
、 、
、 )制备,其工业流程如下(相关金属离子生成氢氧化物沉淀的pH如下表所示):
)制备,其工业流程如下(相关金属离子生成氢氧化物沉淀的pH如下表所示):
| 金属离子 | 开始沉淀的pH | 沉淀完全的pH |
 | 1.1 | 3.2 |
 | 3.0 | 5.0 |
 | 5.8 | 8.8 |
②加入
 溶液调pH的范围是
溶液调pH的范围是③“酸化、调pH、结晶”过程中都需要进行的分离操作是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
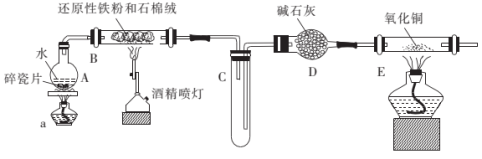
【推荐1】某校化学小组学生利用如图所示装置进行“铁与水蒸气反应”的实验,并对产物组成进行探究(图中夹持及尾气处理装置均已略去)。请回答下列问题:__ 。
(2)硬质玻璃管B中发生反应的化学方程式为__ 。
(3)实验中先点燃酒精灯a再点燃酒精喷灯,可能的原因是__ 。
(4)装置E中的现象是__ 。
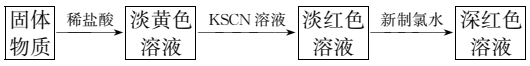
(5)利用反应后的固体物质进行如图实验:___ 。
②该同学将上述实验中的新制氯水改为H2O2溶液,也能出现深红色溶液,用离子方程式表示溶液颜色加深的原因:__ 。
③电子工业中,人们常用FeCl3溶液腐蚀铜板来制作印刷电路板,请写出FeCl3溶液与铜反应的离子方程式:__ 。
(2)硬质玻璃管B中发生反应的化学方程式为
(3)实验中先点燃酒精灯a再点燃酒精喷灯,可能的原因是
(4)装置E中的现象是
(5)利用反应后的固体物质进行如图实验:
②该同学将上述实验中的新制氯水改为H2O2溶液,也能出现深红色溶液,用离子方程式表示溶液颜色加深的原因:
③电子工业中,人们常用FeCl3溶液腐蚀铜板来制作印刷电路板,请写出FeCl3溶液与铜反应的离子方程式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】已知A为生活中常见的金属单质,下列物质相互转化如图所示:
 (课本已经改成焰色试验)
(课本已经改成焰色试验)
试回答:
(1)写出A的化学式_______ ,D的化学式________ 。
(2)向G溶液加入A的有关离子反应方程式_______ 。
(3)在反应Fe2O3+3CO 2Fe+3CO2中,还原剂是
2Fe+3CO2中,还原剂是_____ (填化学式,下同),还原产物是______ 每生成5.6g铁单质,转移的电子数为_______ NA。
(4)写出E转化为F的化学方程式_______ 。
(5)G溶液常用作腐蚀数在绝缘板上的铜箔,请写出该反应的离子方程式:______ 。
(6)向一个铝质易拉罐中充满CO2,然后往罐中注入足量的浓NaOH溶液,立即用胶布封严罐口。一会儿听到罐内发出“咔、咔”的响声,且易拉罐变瘪:再过一会儿易拉罐又鼓起来恢复原样。完成下列空白。
①易拉罐变瘪的反应的离子方程式为:_______ 。
②易拉罐又鼓起来的反应的离子方程式为:_______ 。
 (课本已经改成焰色试验)
(课本已经改成焰色试验)试回答:
(1)写出A的化学式
(2)向G溶液加入A的有关离子反应方程式
(3)在反应Fe2O3+3CO
 2Fe+3CO2中,还原剂是
2Fe+3CO2中,还原剂是(4)写出E转化为F的化学方程式
(5)G溶液常用作腐蚀数在绝缘板上的铜箔,请写出该反应的离子方程式:
(6)向一个铝质易拉罐中充满CO2,然后往罐中注入足量的浓NaOH溶液,立即用胶布封严罐口。一会儿听到罐内发出“咔、咔”的响声,且易拉罐变瘪:再过一会儿易拉罐又鼓起来恢复原样。完成下列空白。
①易拉罐变瘪的反应的离子方程式为:
②易拉罐又鼓起来的反应的离子方程式为:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】用覆铜板制作印刷电路板时,常用 FeCl3 溶液作腐蚀液。某化学兴趣小组在实验室进行了模拟。
【模拟实验 I】
向盛有 4mL 0.2mol/L FeCl3 溶液的试管中,加入一块铜片(Cu 过量),反应一段时间后,溶液黄色褪去。
【分析解释】
(1)FeCl3 与 Cu 反应的离子方程式是___________ 。
(2)为检验反应生成的 Fe2+,最宜选择的试剂是___________ (填字母)。
a.KSCN 溶液 b.NaOH 溶液 c.K3[Fe(CN)6]溶液
【继续实验 II】
为验证上述实验中 Fe3+是否完全反应,该小组同学取上层清液于另一支试管中, 滴入 3 滴 0.1mol/L KSCN 溶液。结果发现,上层清液中立即产生白色沉淀,同时滴入处局部出现红色,振荡后红色立即消失。
【查阅资料】
为解释该异常现象产生的原因,同学们查阅资料得知:
①2CuCl2+4KSCN=2CuSCN↓+(SCN)2+4KCl;
②CuSCN为白色固体,几乎不溶于水;
③(SCN)2与Cl2 性质相似。
【继续实验 III】
【分析解释】
(3)实验 II 中白色沉淀的成分是___________ (填化学式)。
(4)请结合资料,用离子方程式解释实验II中“滴入 KSCN 溶液处局部出现红色”的原因_______ 。
【模拟实验 I】
向盛有 4mL 0.2mol/L FeCl3 溶液的试管中,加入一块铜片(Cu 过量),反应一段时间后,溶液黄色褪去。
【分析解释】
(1)FeCl3 与 Cu 反应的离子方程式是
(2)为检验反应生成的 Fe2+,最宜选择的试剂是
a.KSCN 溶液 b.NaOH 溶液 c.K3[Fe(CN)6]溶液
【继续实验 II】
为验证上述实验中 Fe3+是否完全反应,该小组同学取上层清液于另一支试管中, 滴入 3 滴 0.1mol/L KSCN 溶液。结果发现,上层清液中立即产生白色沉淀,同时滴入处局部出现红色,振荡后红色立即消失。
【查阅资料】
为解释该异常现象产生的原因,同学们查阅资料得知:
①2CuCl2+4KSCN=2CuSCN↓+(SCN)2+4KCl;
②CuSCN为白色固体,几乎不溶于水;
③(SCN)2与Cl2 性质相似。
【继续实验 III】
| 实验方案 | 现象 | |
| 步骤 1 | 取 4mL 0.2mol/L 的 FeCl2 溶液,向其中滴加 3 滴 0.1mol/L 的 KSCN 溶液。 | 无明显现象 |
| 步骤 2 | 取 4mL 0.1mol/L 的 CuCl2 溶液,向其中滴加 3 滴 0.1mol/L 的 KSCN 溶液。 | 产生白色沉淀 |
(3)实验 II 中白色沉淀的成分是
(4)请结合资料,用离子方程式解释实验II中“滴入 KSCN 溶液处局部出现红色”的原因
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】某小组探究Na2SO3溶液和KIO3溶液的反应。
实验I:向某浓度的KIO3酸性溶液(过量)中加入Na2SO3溶液(含淀粉),一段时间(ts)后,溶液突然变蓝。
查阅资料知:IO 在酸性溶液中氧化I-,发生的反应为IO
在酸性溶液中氧化I-,发生的反应为IO +5I-+6H+=3I2+3H2O。
+5I-+6H+=3I2+3H2O。
(1)针对ts前溶液未变蓝,小组做出如下假设:
i.ts前未生成I2,是由于反应的活化能__ (填“大”或“小”),反应速率慢导致的。
ii.ts前生成了I2,但由于存在Na2SO3,Na2SO3将生成的I2还原。
(2)下述实验证实了假设ii合理。
实验II:向实验I的蓝色溶液中加入__ ,蓝色迅速消失,后再次变蓝。
(3)进一步研究Na2SO3溶液和KIO3溶液反应的过程,装置如图。
实验III:K闭合后,电流表的指针偏转情况记录如表:
①K闭合后,取b极区溶液加入盐酸酸化的BaCl2溶液,生成白色沉淀。
②0~t1s时,从a极区取溶液于试管中,滴加淀粉溶液,溶液变蓝;直接向a极区滴加淀粉溶液,溶液未变蓝。判断a极的电极反应式为__ 。
③结合反应解释t2~t3s时指针回到“0”处的原因___ 。
(4)综合实验Ⅰ、Ⅱ、Ⅲ,下列说法正确的是__ (填字母代号)。
A.对比实验Ⅰ、Ⅱ,ts后溶液变蓝,I中SO 被完全氧化
被完全氧化
B.对比实验Ⅰ、Ⅲ,ts前IO 未发生反应
未发生反应
C.实验Ⅲ中指针返回X处的原因,可能是I2氧化SO
实验I:向某浓度的KIO3酸性溶液(过量)中加入Na2SO3溶液(含淀粉),一段时间(ts)后,溶液突然变蓝。
查阅资料知:IO
 在酸性溶液中氧化I-,发生的反应为IO
在酸性溶液中氧化I-,发生的反应为IO +5I-+6H+=3I2+3H2O。
+5I-+6H+=3I2+3H2O。(1)针对ts前溶液未变蓝,小组做出如下假设:
i.ts前未生成I2,是由于反应的活化能
ii.ts前生成了I2,但由于存在Na2SO3,Na2SO3将生成的I2还原。
(2)下述实验证实了假设ii合理。
实验II:向实验I的蓝色溶液中加入
(3)进一步研究Na2SO3溶液和KIO3溶液反应的过程,装置如图。
实验III:K闭合后,电流表的指针偏转情况记录如表:
| 表盘 |  |  | ||
| 时间/s | 0~t1 | t2~t3 | t4 | |
| 偏转位置 | 右偏至“Y”处 | 指针回到“0”处,又返至“X”处;如此周期性往复多次…… | 指针归零 | |
②0~t1s时,从a极区取溶液于试管中,滴加淀粉溶液,溶液变蓝;直接向a极区滴加淀粉溶液,溶液未变蓝。判断a极的电极反应式为
③结合反应解释t2~t3s时指针回到“0”处的原因
(4)综合实验Ⅰ、Ⅱ、Ⅲ,下列说法正确的是
A.对比实验Ⅰ、Ⅱ,ts后溶液变蓝,I中SO
 被完全氧化
被完全氧化B.对比实验Ⅰ、Ⅲ,ts前IO
 未发生反应
未发生反应C.实验Ⅲ中指针返回X处的原因,可能是I2氧化SO

您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】铜及其化合物向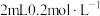
 溶液中滴加
溶液中滴加
 溶液,发现溶液变绿,继续滴加产生棕黄色沉淀,经检验,棕黄色沉淀中不含
溶液,发现溶液变绿,继续滴加产生棕黄色沉淀,经检验,棕黄色沉淀中不含 ,含有
,含有 、
、 和
和 。已知:Cu+
。已知:Cu+ Cu+Cu2+, Cu2+
Cu+Cu2+, Cu2+ CuI↓(白色)+I2。
CuI↓(白色)+I2。
(1)用稀硫酸证实沉淀中含有 的实验现象是
的实验现象是___________ 。
(2)向洗净的棕黄色沉淀中加入足量KI溶液,产生白色沉淀,继续向上层清液中加入淀粉溶液并没有变蓝的现象出现,请结合离子反应方程式解释不变蓝的原因________ 。
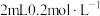
 溶液中滴加
溶液中滴加
 溶液,发现溶液变绿,继续滴加产生棕黄色沉淀,经检验,棕黄色沉淀中不含
溶液,发现溶液变绿,继续滴加产生棕黄色沉淀,经检验,棕黄色沉淀中不含 ,含有
,含有 、
、 和
和 。已知:Cu+
。已知:Cu+ Cu+Cu2+, Cu2+
Cu+Cu2+, Cu2+ CuI↓(白色)+I2。
CuI↓(白色)+I2。(1)用稀硫酸证实沉淀中含有
 的实验现象是
的实验现象是(2)向洗净的棕黄色沉淀中加入足量KI溶液,产生白色沉淀,继续向上层清液中加入淀粉溶液并没有变蓝的现象出现,请结合离子反应方程式解释不变蓝的原因
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐3】煤是我国重要的化石燃料。
(1)煤液化过程中产生的 可生产硫酸,部分过程如图所示:
可生产硫酸,部分过程如图所示:
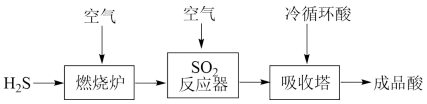
 反应器中的化学方程式是
反应器中的化学方程式是_______ 。
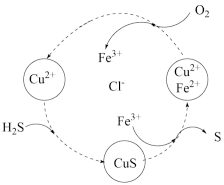
(2) 还可用于回收单质硫,转化如图所示。其中化合价保持不变的元素有
还可用于回收单质硫,转化如图所示。其中化合价保持不变的元素有_______ ,该图示总反应的化学方程式为_______ 。
(3)煤燃烧产生的废气中含有 ,可以用工业废碱渣(主要成分为
,可以用工业废碱渣(主要成分为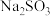 )来吸收,还可以得到亚硫酸钠(
)来吸收,还可以得到亚硫酸钠(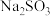 )粗品。其流程如图:
)粗品。其流程如图:
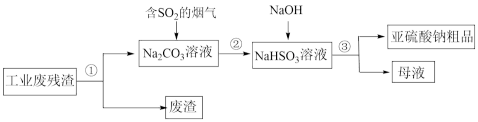
①上述流程中,加入NaOH后,发生反应的化学方程式为_______ 。
②亚硫酸钠粗品中含有少量 ,设计实验证明亚硫酸钠粗品含有少量
,设计实验证明亚硫酸钠粗品含有少量 的方案是:在一支试管中,加入少量亚硫酸钠粗品,用适量蒸馏水溶解,
的方案是:在一支试管中,加入少量亚硫酸钠粗品,用适量蒸馏水溶解,_______ ,出现白色沉淀,则证明含有 。
。
(4)已知有VL(已换算成标准状况)尾气,通入足量 吸收再加足量
吸收再加足量 溶液充分反应后(不考虑尾气中其他成分的反应),过滤、洗涤、干燥、称量得到bg沉淀。
溶液充分反应后(不考虑尾气中其他成分的反应),过滤、洗涤、干燥、称量得到bg沉淀。 吸收
吸收 的化学方程式是
的化学方程式是_______ ;尾气中 的含量(体积分数)的计算式是
的含量(体积分数)的计算式是_______ 。
(1)煤液化过程中产生的
 可生产硫酸,部分过程如图所示:
可生产硫酸,部分过程如图所示:
 反应器中的化学方程式是
反应器中的化学方程式是(2)
 还可用于回收单质硫,转化如图所示。其中化合价保持不变的元素有
还可用于回收单质硫,转化如图所示。其中化合价保持不变的元素有
(3)煤燃烧产生的废气中含有
 ,可以用工业废碱渣(主要成分为
,可以用工业废碱渣(主要成分为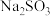 )来吸收,还可以得到亚硫酸钠(
)来吸收,还可以得到亚硫酸钠(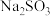 )粗品。其流程如图:
)粗品。其流程如图:
①上述流程中,加入NaOH后,发生反应的化学方程式为
②亚硫酸钠粗品中含有少量
 ,设计实验证明亚硫酸钠粗品含有少量
,设计实验证明亚硫酸钠粗品含有少量 的方案是:在一支试管中,加入少量亚硫酸钠粗品,用适量蒸馏水溶解,
的方案是:在一支试管中,加入少量亚硫酸钠粗品,用适量蒸馏水溶解, 。
。(4)已知有VL(已换算成标准状况)尾气,通入足量
 吸收再加足量
吸收再加足量 溶液充分反应后(不考虑尾气中其他成分的反应),过滤、洗涤、干燥、称量得到bg沉淀。
溶液充分反应后(不考虑尾气中其他成分的反应),过滤、洗涤、干燥、称量得到bg沉淀。 吸收
吸收 的化学方程式是
的化学方程式是 的含量(体积分数)的计算式是
的含量(体积分数)的计算式是
您最近一年使用:0次



