美国化学家路易斯(GilbertNewtonLewis)提出的酸碱电子理论认为:凡能接受电子对的物质称为酸(如H+),能接受几对电子对则称几元酸,凡能给出电子对的物质称为碱(如NH3)。N2H4的IUPAC中文命名是肼,又称为联氨,它由NH3中的一个氢原子被一个NH2取代而成,它是一种重要的还原剂,常与NO2、F2一起作火箭燃料。
(1)根据路易斯酸碱电子理论,N2H4是几元酸或碱?答:___________ 。
(2)写出N2H4与NO2作火箭推动剂的反应方程式:___________
(3)用NaClO氧化NH3可以制备N2H4,写出方程式:___________
(4)用碳酸二甲酯和一水合肼在70°C下可合成碳酰肼(CON4H6)。请画出碳酰肼的结构式:___________
(1)根据路易斯酸碱电子理论,N2H4是几元酸或碱?答:
(2)写出N2H4与NO2作火箭推动剂的反应方程式:
(3)用NaClO氧化NH3可以制备N2H4,写出方程式:
(4)用碳酸二甲酯和一水合肼在70°C下可合成碳酰肼(CON4H6)。请画出碳酰肼的结构式:
更新时间:2021-08-17 19:41:40
|
相似题推荐
解答题-有机推断题
|
较易
(0.85)
名校
解题方法
【推荐1】石油不仅是重要的矿物能源,更可以通过综合利用得到多种有机化工产品。乙烯是石油化工最重要的基础原料,请根据以下框图回答:

(1)乙烯分子的空间结构为_____________ ;C官能团名称是________ 。
(2)A→B的化学方程式_________________ 。
(3)A+C→乙酸乙酯的化学方程式________ ;实验室常用饱和碳酸钠溶液来收集乙酸乙酯其作用为___________ 。
(4)“乙烯→A”的反应类型是__________ 反应。下列物质在一定条件下都能与乙烯反应,其中反应类型与“乙烯→A”的不相同的是_____________ (填序号)。
①氢气②氯化氢③氧气④溴水

(1)乙烯分子的空间结构为
(2)A→B的化学方程式
(3)A+C→乙酸乙酯的化学方程式
(4)“乙烯→A”的反应类型是
①氢气②氯化氢③氧气④溴水
您最近一年使用:0次
解答题-有机推断题
|
较易
(0.85)
名校
【推荐2】A、B、C、D是四种常见的有机物,其中A的产量通常用来衡量一个国家的石油化工发展水平,B与C在浓硫酸和加热条件下发生反应,生成的有机物有特殊香味;A、B、C、D在一定条件下的转化关系如图所示(反应条件已省略):

(1)C中官能团的名称为___ ,③的化学方程式为__ 。
(2)丙烯酸(CH2=CH-COOH)的性质可能有___ 。(多选)
A.加成反应 B.取代反应 C.中和反应 D.氧化反应
(3)用一种方法鉴别B和C,所用试剂是__ 。
(4)丙烯酸乙酯的结构简式为___ 。

(1)C中官能团的名称为
(2)丙烯酸(CH2=CH-COOH)的性质可能有
A.加成反应 B.取代反应 C.中和反应 D.氧化反应
(3)用一种方法鉴别B和C,所用试剂是
(4)丙烯酸乙酯的结构简式为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
【推荐1】根据元素在周期表中的位置能推测元素的原子结构以及相关物质的性质,下图是元素周期表的一部分,请根据图中字母所示元素的位置回答问题。
(1)元素P的原子结构示意图为________ ;元素 的最高价氧化物的电子式为
的最高价氧化物的电子式为________ 。
(2)元素 、
、 、
、 形成的简单离子中,半径由大到小的顺序为
形成的简单离子中,半径由大到小的顺序为_______ (填离子符号)。
(3)下列说法中,正确的有________ (填序号)。
①元素 的单质有多种同素异形体 ②
的单质有多种同素异形体 ②  中仅含离子键,
中仅含离子键,  中仅含共价键
中仅含共价键
③ 和
和  都是离子化合物 ④
都是离子化合物 ④ 比
比  的沸点更高
的沸点更高
(4)已知 离子的核内有
离子的核内有 个中子,
个中子, 的质量数为
的质量数为 ,则
,则 离子里含有电子的物质的量为
离子里含有电子的物质的量为_____  。
。
X | |||||||||||||||||
Y | Z | ||||||||||||||||
M | N | W | T | ||||||||||||||
P |
(1)元素P的原子结构示意图为
 的最高价氧化物的电子式为
的最高价氧化物的电子式为(2)元素
 、
、 、
、 形成的简单离子中,半径由大到小的顺序为
形成的简单离子中,半径由大到小的顺序为(3)下列说法中,正确的有
①元素
 的单质有多种同素异形体 ②
的单质有多种同素异形体 ②  中仅含离子键,
中仅含离子键,  中仅含共价键
中仅含共价键③
 和
和  都是离子化合物 ④
都是离子化合物 ④ 比
比  的沸点更高
的沸点更高(4)已知
 离子的核内有
离子的核内有 个中子,
个中子, 的质量数为
的质量数为 ,则
,则 离子里含有电子的物质的量为
离子里含有电子的物质的量为 。
。
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐2】A、B、C、D都是短周期元素,原子半径D>C>A>B,其中A、B处于同一周期,A 的最外层电子数是次外层电子数的2倍,A、C处于同一主族。C原子核内的质子数等于A、B原子核内的质子数之和,C原子最外层电子数是D原子最外层电子数的4倍。试回答下列问题。
(1)元素分别是:A_______ ,D_______ (填元素名称)。
(2)A、B2种元素分别形成的气态氢化物的稳定性由小到大的顺序是_______ 。(填化学式)
(3)A与B形成的三原子分子的电子式是_______ 。组成的化合物属于_______ (填“离子化合物”或“共价化合物”),B与D形成的原子个数之比为1∶1的化合物的电子式是_______ ,含有的化学键是_______ 和_______ 。
(4)用电子式表示化合物D2B的形成过程_______ 。
(1)元素分别是:A
(2)A、B2种元素分别形成的气态氢化物的稳定性由小到大的顺序是
(3)A与B形成的三原子分子的电子式是
(4)用电子式表示化合物D2B的形成过程
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐1】完成下列问题:
(1)GaAs的熔点为1238℃,可作半导体材料,而GaCl3的熔点为77.9℃。
①预测GaCl3的晶体类型可能为______ 。
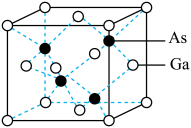
②GaAs晶胞结构如图所示,则晶胞中每个Ga原子周围有_____ 个紧邻等距的As原子;该晶体的密度为ρg•cm-3,阿伏加德罗常数为NA,则晶体中最近的两个Ga原子的核间距离为______ cm(列出计算式)。
(2)ZnO晶体中部分O原子被N原子替代后可以改善半导体的性能,Zn-N键中离子键成分的百分数小于Zn-O键,原因是______ 。
(3)CH3Mn(CO)5与I2反应可用于制备CH3I,反应前后锰的配位数不变,CH3Mn(CO)5与I2反应的化学方程式为______ 。
(4)将含有末成对电子的物质置于外磁场中,会使磁场强度增大,称其为顺磁性物质。下列物质中,属于顺磁性物质的是______ (填标号)。
(1)GaAs的熔点为1238℃,可作半导体材料,而GaCl3的熔点为77.9℃。
①预测GaCl3的晶体类型可能为
②GaAs晶胞结构如图所示,则晶胞中每个Ga原子周围有

(2)ZnO晶体中部分O原子被N原子替代后可以改善半导体的性能,Zn-N键中离子键成分的百分数小于Zn-O键,原因是
(3)CH3Mn(CO)5与I2反应可用于制备CH3I,反应前后锰的配位数不变,CH3Mn(CO)5与I2反应的化学方程式为
(4)将含有末成对电子的物质置于外磁场中,会使磁场强度增大,称其为顺磁性物质。下列物质中,属于顺磁性物质的是
| A.[Cu(NH3)2]Cl | B.[Zn(NH3)4]SO4 | C.[Cu(NH3)4]SO4 | D.Na2[Zn(OH)4] |
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐2】东晋《华阳国志·南中志》卷四中已有关于白铜的记载,云南镍白铜(铜镍合金)闻名中外,曾主要用于造币,亦可用于制作仿银饰品。回答下列问题:
(1)镍元素基态原子的电子排布式为______ ,3d能级上的未成对电子数为_______ 。
(2)硫酸镍溶于氨水形成[Ni(NH3)6]SO4蓝色溶液。
①[Ni(NH3)6]SO4中阴离子的立体构型是________ 。
②在[Ni(NH3)6]SO4中Ni2+与NH3之间形成的化学键类型为______ ,提供孤电子对的成键原子是______ 。
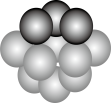
(3)铜晶体铜原子的堆积方式如图所示。
①基态铜在元素周期表中位置_________ 。
②每个铜原子周围距离最近的铜原子数目_________ 。
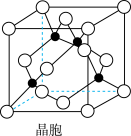
(4)某M原子的外围电子排布式为3s23p5,铜与M形成化合物的晶胞如图所示(黑点代表铜原子)。
①该晶体的化学式为_________ 。
②已知铜和M的电负性分别为1.9和3.0,则铜与M形成的化合物属于______ (填“离子”或“共价”)化合物。
(1)镍元素基态原子的电子排布式为
(2)硫酸镍溶于氨水形成[Ni(NH3)6]SO4蓝色溶液。
①[Ni(NH3)6]SO4中阴离子的立体构型是
②在[Ni(NH3)6]SO4中Ni2+与NH3之间形成的化学键类型为
(3)铜晶体铜原子的堆积方式如图所示。

①基态铜在元素周期表中位置
②每个铜原子周围距离最近的铜原子数目
(4)某M原子的外围电子排布式为3s23p5,铜与M形成化合物的晶胞如图所示(黑点代表铜原子)。

①该晶体的化学式为
②已知铜和M的电负性分别为1.9和3.0,则铜与M形成的化合物属于
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐3】I.某学生欲用已知物质的量浓度的盐酸来测定未知物质的量浓度的NaOH溶液时,选择甲基橙作指示剂。请填写下列空白:
(1)在中和滴定的过程中有如下操作:①用标准盐酸润洗滴定管 ②往滴定管内注入标准盐酸溶液 ③检查滴定管是否漏水 ④滴定,则在操作过程中正确的顺序是_______ (写序号)
(2)在滴定时,左手把握酸式滴定管的活塞,右手摇动锥形瓶,眼睛注视_______ ;滴定终点的判定依据是_______ 。
(3)下列操作中可能使所测氢氧化钠溶液的浓度数值偏低的是_______ 。
A.酸式滴定管未用标准盐酸溶液润洗就直接注入标准盐酸溶液
B.滴定前盛放氢氧化钠溶液的锥形瓶用蒸馏水洗净后没有干燥
C.酸式滴定管在滴定前有气泡,滴定后气泡消失
D.读取盐酸体积时,开始仰视读数,滴定结束时俯视读数
II.[Cu(NH3)4]2+在实验室中制备方法如下:向盛有硫酸铜水溶液的试管里加入氨水,首先形成蓝色沉淀,继续添加氨水,沉淀溶解,得到深蓝色的透明溶液。
(4)请写出蓝色沉淀溶解得到深蓝色溶液的离子方程式_______ 。
(5)[Cu(NH3)4]2+中的配体为_______ ,提供孤电子对的配位原子是_______ 。
(1)在中和滴定的过程中有如下操作:①用标准盐酸润洗滴定管 ②往滴定管内注入标准盐酸溶液 ③检查滴定管是否漏水 ④滴定,则在操作过程中正确的顺序是
(2)在滴定时,左手把握酸式滴定管的活塞,右手摇动锥形瓶,眼睛注视
(3)下列操作中可能使所测氢氧化钠溶液的浓度数值偏低的是
A.酸式滴定管未用标准盐酸溶液润洗就直接注入标准盐酸溶液
B.滴定前盛放氢氧化钠溶液的锥形瓶用蒸馏水洗净后没有干燥
C.酸式滴定管在滴定前有气泡,滴定后气泡消失
D.读取盐酸体积时,开始仰视读数,滴定结束时俯视读数
II.[Cu(NH3)4]2+在实验室中制备方法如下:向盛有硫酸铜水溶液的试管里加入氨水,首先形成蓝色沉淀,继续添加氨水,沉淀溶解,得到深蓝色的透明溶液。
(4)请写出蓝色沉淀溶解得到深蓝色溶液的离子方程式
(5)[Cu(NH3)4]2+中的配体为
您最近一年使用:0次




