东晋《华阳国志·南中志》卷四中已有关于白铜的记载,云南镍白铜(铜镍合金)闻名中外,曾主要用于造币,亦可用于制作仿银饰品。回答下列问题:
(1)镍元素基态原子的电子排布式为______ ,3d能级上的未成对电子数为_______ 。
(2)硫酸镍溶于氨水形成[Ni(NH3)6]SO4蓝色溶液。
①[Ni(NH3)6]SO4中阴离子的立体构型是________ 。
②在[Ni(NH3)6]SO4中Ni2+与NH3之间形成的化学键类型为______ ,提供孤电子对的成键原子是______ 。
(3)铜晶体铜原子的堆积方式如图所示。
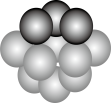
①基态铜在元素周期表中位置_________ 。
②每个铜原子周围距离最近的铜原子数目_________ 。
(4)某M原子的外围电子排布式为3s23p5,铜与M形成化合物的晶胞如图所示(黑点代表铜原子)。
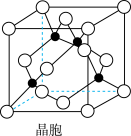
①该晶体的化学式为_________ 。
②已知铜和M的电负性分别为1.9和3.0,则铜与M形成的化合物属于______ (填“离子”或“共价”)化合物。
(1)镍元素基态原子的电子排布式为
(2)硫酸镍溶于氨水形成[Ni(NH3)6]SO4蓝色溶液。
①[Ni(NH3)6]SO4中阴离子的立体构型是
②在[Ni(NH3)6]SO4中Ni2+与NH3之间形成的化学键类型为
(3)铜晶体铜原子的堆积方式如图所示。

①基态铜在元素周期表中位置
②每个铜原子周围距离最近的铜原子数目
(4)某M原子的外围电子排布式为3s23p5,铜与M形成化合物的晶胞如图所示(黑点代表铜原子)。

①该晶体的化学式为
②已知铜和M的电负性分别为1.9和3.0,则铜与M形成的化合物属于
更新时间:2020-09-07 17:27:09
|
相似题推荐
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐1】下表列出了前20号元素中某些元素性质的一些数据:
试回答下列问题:
(1)以上10种元素中,第一电离能最小的是___________ (填元素符号)。
(2)上述⑤、⑥、⑦三种元素中的某两种元素形成的化合物中,每一个原子都满足8e 稳定结构的物质可能是___________ (写分子式,只答一条即可)。元素⑨和⑩形成的化合物的化学式为___________ ;元素①的原子价电子排布式是___________ 。
(3)①、⑥、⑦、⑩四种元素的电负性,由强到弱的顺序是___________ (填化学式)。
(4)③和⑨两元素比较,非金属性较弱的是___________ (填名称),可以验证你的结论的是下列中的___________ (填序号)。
A.气态氢化物的稳定性 B.单质分子中的键能
C.两元素的电负性 D.最高价含氧酸的酸性
| 性质元素 | 原子半径(1019m) | 最高价态 | 最低价态 |
| ① | 1.02 | +6 | 2 |
| ② | 2.27 | +1 | — |
| ③ | 0.74 | — | 2 |
| ④ | 1.43 | +3 | — |
| ⑤ | 0.77 | +4 | 4 |
| ⑥ | 1.10 | +5 | 3 |
| ⑦ | 0.99 | +7 | 1 |
| ⑧ | 1.86 | +1 | — |
| ⑨ | 0.75 | +5 | 3 |
| ⑩ | 1.17 | +4 | 4 |
(1)以上10种元素中,第一电离能最小的是
(2)上述⑤、⑥、⑦三种元素中的某两种元素形成的化合物中,每一个原子都满足8e 稳定结构的物质可能是
(3)①、⑥、⑦、⑩四种元素的电负性,由强到弱的顺序是
(4)③和⑨两元素比较,非金属性较弱的是
A.气态氢化物的稳定性 B.单质分子中的键能
C.两元素的电负性 D.最高价含氧酸的酸性
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐2】我国科学家制备的NiO/Al2O3/Pt催化剂能实现氨硼烷(H3NBH3)高效制备氢气的目的,制氢原理:H3NBH3+4CH3OH NH4B(OCH3)4+3H2↑。请回答下列问题:
NH4B(OCH3)4+3H2↑。请回答下列问题:
(1)基态氮原子的价电子排布式为_______ 。
(2)硼烷又称硼氢化合物,随着硼原子数的增加,硼烷由气态经液态至固态,其原因为_______ 。
(3)某有机硼化合物的结构简式如图所示,其中氮原子的杂化轨道类型为_______ 。
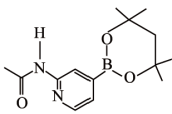
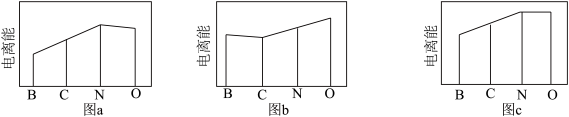
(4)图a、b、c分别表示B、C、N、O的逐级电离能变化趋势(纵坐标的标度不同)。第二电离能的变化图是_______ (填标号)。
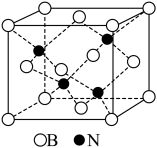
(5)含有多个配位原子的配体与同一中心离子(或原子)通过螯合配位成环而形成的配合物为螯合物。一种Ni2+与EDTA形成的螯合物的结构如图所示,

1个该配合物中通过螯合作用形成的配位键有_______ 个,在形成配位键前后C-N-C键角将_______ (填“增大"“减少”或“不变”)。
(6)BN晶体的晶胞如图所示,B、N的原子半径分别为apm和bpm,密度为2.25g·cm-3,阿伏伽德罗常数的值为NA,BN晶胞中原子的体积占晶胞体积的百分率为_______ 。
 NH4B(OCH3)4+3H2↑。请回答下列问题:
NH4B(OCH3)4+3H2↑。请回答下列问题:(1)基态氮原子的价电子排布式为
(2)硼烷又称硼氢化合物,随着硼原子数的增加,硼烷由气态经液态至固态,其原因为
(3)某有机硼化合物的结构简式如图所示,其中氮原子的杂化轨道类型为

(4)图a、b、c分别表示B、C、N、O的逐级电离能变化趋势(纵坐标的标度不同)。第二电离能的变化图是

(5)含有多个配位原子的配体与同一中心离子(或原子)通过螯合配位成环而形成的配合物为螯合物。一种Ni2+与EDTA形成的螯合物的结构如图所示,

1个该配合物中通过螯合作用形成的配位键有
(6)BN晶体的晶胞如图所示,B、N的原子半径分别为apm和bpm,密度为2.25g·cm-3,阿伏伽德罗常数的值为NA,BN晶胞中原子的体积占晶胞体积的百分率为

您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐3】按要求回答下列问题:
(1)黄铜矿(CuFeS2)是炼铜的最主要矿物。火法冶炼黄铜矿的过程中,其中一步反应是2Cu2O+Cu2S 6Cu+SO2↑。则29Cu的外围电子轨道表示式为
6Cu+SO2↑。则29Cu的外围电子轨道表示式为____ ;比较Cu2O与Cu2S,熔点较高的是____ ,原因为____ 。
(2)一种铜金合金晶体具有面心立方最密堆积结构,在晶胞中Cu原子处于面心,Au原子处于顶点,则该合金中Cu原子与Au原子数量之比为____ ;该晶体中原子之间的作用力是____ 。
(3)上述晶体具有储氢功能,氢原子可进入到由Cu原子与Au原子构成的四面体空隙中。若将Cu原子与Au原子等同看待,该晶体储氢后的晶胞结构与CaF2的结构相似(如图),该晶体储氢后的化学式应为____ 。

(4)铁有δ、γ、α三种同素异形体(如图),γ晶体晶胞中所含有的铁原子数为____ ,δ、α两种晶胞中铁原子的配位数之比为____ 。

(1)黄铜矿(CuFeS2)是炼铜的最主要矿物。火法冶炼黄铜矿的过程中,其中一步反应是2Cu2O+Cu2S
 6Cu+SO2↑。则29Cu的外围电子轨道表示式为
6Cu+SO2↑。则29Cu的外围电子轨道表示式为(2)一种铜金合金晶体具有面心立方最密堆积结构,在晶胞中Cu原子处于面心,Au原子处于顶点,则该合金中Cu原子与Au原子数量之比为
(3)上述晶体具有储氢功能,氢原子可进入到由Cu原子与Au原子构成的四面体空隙中。若将Cu原子与Au原子等同看待,该晶体储氢后的晶胞结构与CaF2的结构相似(如图),该晶体储氢后的化学式应为

(4)铁有δ、γ、α三种同素异形体(如图),γ晶体晶胞中所含有的铁原子数为

您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐1】我国科学家是近成功合成了世界上首个五氮阴离子盐 (用R代表)。回答下列问题:
(用R代表)。回答下列问题:
(1)氮原子价层电子的轨道表达式(电子排布图)为_______ ,其能量最高的电子排布的轨道呈_______ 形。
(2)经X射线辐射测得化合物R的晶体结构,其局部结构如图所示。
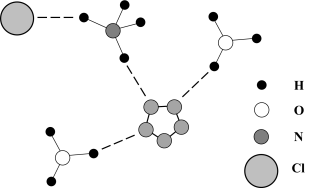
①从结构角度分析,R中两种阳离子的相同之处为_______ ,不同之处为_______ (填标号)
A.中心原子的杂化类型 B.中心原子的价层电子对数
C.立体结构 D.共价键类型
②R中阴离子 中的σ键总数为
中的σ键总数为_______ 个。分子中的大π键可用符号 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为
表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为 ),则
),则 中的大π键应表示为
中的大π键应表示为_______ 。
③比较键角: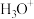
_______  ,并用物质结构的观点解释原因:
,并用物质结构的观点解释原因:_______ 。
④元素H、O、N的电负性由小到大的顺序_______ 。
 (用R代表)。回答下列问题:
(用R代表)。回答下列问题:(1)氮原子价层电子的轨道表达式(电子排布图)为
(2)经X射线辐射测得化合物R的晶体结构,其局部结构如图所示。

①从结构角度分析,R中两种阳离子的相同之处为
A.中心原子的杂化类型 B.中心原子的价层电子对数
C.立体结构 D.共价键类型
②R中阴离子
 中的σ键总数为
中的σ键总数为 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为
表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为 ),则
),则 中的大π键应表示为
中的大π键应表示为③比较键角:
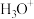
 ,并用物质结构的观点解释原因:
,并用物质结构的观点解释原因:④元素H、O、N的电负性由小到大的顺序
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐2】甲硅烷 可用于制备多种新型无机非金属材料。
可用于制备多种新型无机非金属材料。
(1)Si原子与H原子结合时,Si表现为正价,则电负性:Si_________ H(填“>”“<”或“=”), 分子的空间结构为
分子的空间结构为_________________ 。
(2)利用 与
与 可制得氮化硅(
可制得氮化硅( )材料。
)材料。
①热稳定性:
___________  (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
② 中
中 的键角
的键角__________  中
中 的键角(“>”“<”或“=”),其键角差异的原因是
的键角(“>”“<”或“=”),其键角差异的原因是_____________________________ 。
(3)利用 与
与 反应可制得碳化硅晶体,晶胞结构如图,硅原子位于立方体的顶点和面心,碳原子位于立方体的内部。
反应可制得碳化硅晶体,晶胞结构如图,硅原子位于立方体的顶点和面心,碳原子位于立方体的内部。__________ ,SiC的晶体类型是_____________ 。
②已知碳化硅的晶胞边长为a nm(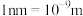 ),阿伏伽德罗常数为
),阿伏伽德罗常数为 。则碳化硅晶体的密度为
。则碳化硅晶体的密度为_____________  (列出计算式)。
(列出计算式)。
 可用于制备多种新型无机非金属材料。
可用于制备多种新型无机非金属材料。(1)Si原子与H原子结合时,Si表现为正价,则电负性:Si
 分子的空间结构为
分子的空间结构为(2)利用
 与
与 可制得氮化硅(
可制得氮化硅( )材料。
)材料。①热稳定性:

 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。②
 中
中 的键角
的键角 中
中 的键角(“>”“<”或“=”),其键角差异的原因是
的键角(“>”“<”或“=”),其键角差异的原因是(3)利用
 与
与 反应可制得碳化硅晶体,晶胞结构如图,硅原子位于立方体的顶点和面心,碳原子位于立方体的内部。
反应可制得碳化硅晶体,晶胞结构如图,硅原子位于立方体的顶点和面心,碳原子位于立方体的内部。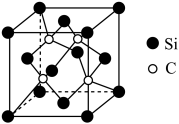
②已知碳化硅的晶胞边长为a nm(
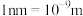 ),阿伏伽德罗常数为
),阿伏伽德罗常数为 。则碳化硅晶体的密度为
。则碳化硅晶体的密度为 (列出计算式)。
(列出计算式)。
您最近一年使用:0次
【推荐3】A、B、C、D、E、F均为36号以前的元素,原子序数依次增大。A的最外层电子数与次外层电子数相等。B元素的价层电子排布是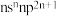 ,C元素
,C元素 价离子与B的离子电子层结构相同,D元素基态原子的最高能级有一个未成对电子且电子云为哑铃形,E元素基态的
价离子与B的离子电子层结构相同,D元素基态原子的最高能级有一个未成对电子且电子云为哑铃形,E元素基态的 价离子的
价离子的 轨道为半充满,F元素基态原子的最外层只有一个电子。回答下列问题:
轨道为半充满,F元素基态原子的最外层只有一个电子。回答下列问题:
(1)C的元素符号是______ 。上述六种元素中,位于周期表d区、 区的分别是
区的分别是___________ 、______ (填元素符号)。
(2)基态D原子的电子排布式是______ ,A、B、D电负性由大到小的顺序是______ (填元素符号)。
(3)向含 价F离子的水溶液中滴加氨水至过量,产生的现象是
价F离子的水溶液中滴加氨水至过量,产生的现象是___________ ,发生反应的离子方程式为___________ 、___________ 。
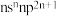 ,C元素
,C元素 价离子与B的离子电子层结构相同,D元素基态原子的最高能级有一个未成对电子且电子云为哑铃形,E元素基态的
价离子与B的离子电子层结构相同,D元素基态原子的最高能级有一个未成对电子且电子云为哑铃形,E元素基态的 价离子的
价离子的 轨道为半充满,F元素基态原子的最外层只有一个电子。回答下列问题:
轨道为半充满,F元素基态原子的最外层只有一个电子。回答下列问题:(1)C的元素符号是
 区的分别是
区的分别是(2)基态D原子的电子排布式是
(3)向含
 价F离子的水溶液中滴加氨水至过量,产生的现象是
价F离子的水溶液中滴加氨水至过量,产生的现象是
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐1】Fe3+与SCN-形成的配离子颜色极似血液,常被用于电影特技和魔术表演。回答下列问题:
(1)写出Fe3+的电子排布式:___________ ;SCN-的结构式为________
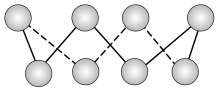
(2)基态硫原子中,核外占据最高能级电子的电子云轮廓图形状为_________ 。硫的一种同素异形体分子式为S8,其结构如图所示,其中S原子的杂化轨道类型为______ 。S8易溶于二硫化碳的原因是__________________________________________________ 。
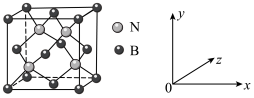
(3)已知立方氮化硼晶体内存在配位键,则其晶体中配位键与普通共价键数目之比为______ 。原子坐标参数可表示晶胞内部各原子的相对位置,图中a处B的原子坐标参数为(0, 0, 0),则距离该B原子最近的N原子坐标参数为_________ 。
(4)单质铁的晶体结构如图所示,该堆积方式名称为________ 。已知该晶胞的密度为ρ g/cm3,则铁原子半径的计算式为______________ pm。

(1)写出Fe3+的电子排布式:
(2)基态硫原子中,核外占据最高能级电子的电子云轮廓图形状为

(3)已知立方氮化硼晶体内存在配位键,则其晶体中配位键与普通共价键数目之比为

(4)单质铁的晶体结构如图所示,该堆积方式名称为

您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐2】I.某学生欲用已知物质的量浓度的盐酸来测定未知物质的量浓度的NaOH溶液时,选择甲基橙作指示剂。请填写下列空白:
(1)在滴定时,左手把握酸式滴定管的活塞,右手摇动锥形瓶,眼睛注视_ ;滴定终点的判定依据是__ 。
(2)下列操作中可能使所测氢氧化钠溶液的浓度数值偏低的是__ 。
A.酸式滴定管未用标准盐酸溶液润洗就直接注入标准盐酸溶液
B.滴定前盛放氢氧化钠溶液的锥形瓶用蒸馏水洗净后没有干燥
C.酸式滴定管在滴定前有气泡,滴定后气泡消失
D.读取盐酸体积时,开始仰视读数,滴定结束时俯视读数
II.[Cu(NH3)4]2+在实验室中制备方法如下:向盛有硫酸铜水溶液的试管里加入氨水,首先形成蓝色沉淀,继续添加氨水,沉淀溶解,得到深蓝色的透明溶液。
(3)请写出蓝色沉淀溶解得到深蓝色溶液的离子方程式___ 。
(4)[Cu(NH3)4]2+中的配体为___ ,提供孤电子对的配位原子是___ 。
(1)在滴定时,左手把握酸式滴定管的活塞,右手摇动锥形瓶,眼睛注视
(2)下列操作中可能使所测氢氧化钠溶液的浓度数值偏低的是
A.酸式滴定管未用标准盐酸溶液润洗就直接注入标准盐酸溶液
B.滴定前盛放氢氧化钠溶液的锥形瓶用蒸馏水洗净后没有干燥
C.酸式滴定管在滴定前有气泡,滴定后气泡消失
D.读取盐酸体积时,开始仰视读数,滴定结束时俯视读数
II.[Cu(NH3)4]2+在实验室中制备方法如下:向盛有硫酸铜水溶液的试管里加入氨水,首先形成蓝色沉淀,继续添加氨水,沉淀溶解,得到深蓝色的透明溶液。
(3)请写出蓝色沉淀溶解得到深蓝色溶液的离子方程式
(4)[Cu(NH3)4]2+中的配体为
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
【推荐3】美国化学家路易斯(GilbertNewtonLewis)提出的酸碱电子理论认为:凡能接受电子对的物质称为酸(如H+),能接受几对电子对则称几元酸,凡能给出电子对的物质称为碱(如NH3)。N2H4的IUPAC中文命名是肼,又称为联氨,它由NH3中的一个氢原子被一个NH2取代而成,它是一种重要的还原剂,常与NO2、F2一起作火箭燃料。
(1)根据路易斯酸碱电子理论,N2H4是几元酸或碱?答:___________ 。
(2)写出N2H4与NO2作火箭推动剂的反应方程式:___________
(3)用NaClO氧化NH3可以制备N2H4,写出方程式:___________
(4)用碳酸二甲酯和一水合肼在70°C下可合成碳酰肼(CON4H6)。请画出碳酰肼的结构式:___________
(1)根据路易斯酸碱电子理论,N2H4是几元酸或碱?答:
(2)写出N2H4与NO2作火箭推动剂的反应方程式:
(3)用NaClO氧化NH3可以制备N2H4,写出方程式:
(4)用碳酸二甲酯和一水合肼在70°C下可合成碳酰肼(CON4H6)。请画出碳酰肼的结构式:
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐1】金属镍与镧(La)形成的合金是一种良好的储氢材料,其晶胞结构示意图如下图所示。
(1)该合金的化学式为__________________ ;
(2)一定条件下,该贮氢材料能快速、可逆地存储和释放氢气,若每个晶胞可吸收 3 个 H2, 这一过程用化学方程式表示为:______________________________________ 。
(3)下列关于该贮氢材料及氢气的说法中,正确的是_________ ( 填序号 )
A.该材料中镧原子和镍原子之间存在化学键,是原子晶体
B.氢分子被吸收时首先要在合金表面解离变成氢原子,同时放出热量
C.该材料贮氢时采用常温高压比采用常温常压更好
D.氢气很难液化是因为虽然其分子内氢键很强,但其分子间作用力很弱
(4)晶体铜是面心立方堆积,在铜的一个晶胞中,把顶点上的铜原子换成Au,可得一种合金,该合金也具有储氢功能,储氢时,氢原子进入到Au和Cu原子构成的的四面体空隙中,则达到最大储氢量的化学式为_____________ 。
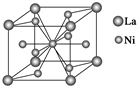
(1)该合金的化学式为
(2)一定条件下,该贮氢材料能快速、可逆地存储和释放氢气,若每个晶胞可吸收 3 个 H2, 这一过程用化学方程式表示为:
(3)下列关于该贮氢材料及氢气的说法中,正确的是
A.该材料中镧原子和镍原子之间存在化学键,是原子晶体
B.氢分子被吸收时首先要在合金表面解离变成氢原子,同时放出热量
C.该材料贮氢时采用常温高压比采用常温常压更好
D.氢气很难液化是因为虽然其分子内氢键很强,但其分子间作用力很弱
(4)晶体铜是面心立方堆积,在铜的一个晶胞中,把顶点上的铜原子换成Au,可得一种合金,该合金也具有储氢功能,储氢时,氢原子进入到Au和Cu原子构成的的四面体空隙中,则达到最大储氢量的化学式为
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐2】2022年10月18日《自然化学》发表我国科学家研究成果,发现AgCrS2(AMX2家族成员之一,A为一价金属,M为三价金属,X为氧族元素)在室温下具有超离子行为。回答下列问题:
(1)基态硫原子核外电子排布式为___________ 。
(2)氧族元素有氧、硫、硒、碲等元素,其中电负性最大的元素是___________ ,科学家用亚硒酸盐和硫酸盐跟踪固氨酶,研究反应机理。 中硫的杂化轨道类型是
中硫的杂化轨道类型是___________ , 的空间结构模型为
的空间结构模型为___________ 。
(3)配合物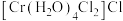 中铬的化合价为
中铬的化合价为___________ ,配离子为___________ ,中心离子配位数为___________ 。
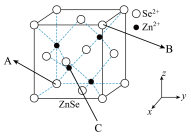
(4)ZnSe晶胞与ZnS晶胞相似(如图),ZnSe晶胞中部分原子的分数坐标为:A点 (0,0,0),B点
(0,0,0),B点 的坐标为
的坐标为___________ ,从该晶胞中找出距离B点Se2-最远的 的位置
的位置___________ (用分数坐标表示),该晶胞中晶胞中 的个数为
的个数为___________ 个,若晶胞中的边长为acm,阿伏加德罗常数的值为 ,请计算ZnSe晶胞的密度
,请计算ZnSe晶胞的密度___________ 
(1)基态硫原子核外电子排布式为
(2)氧族元素有氧、硫、硒、碲等元素,其中电负性最大的元素是
 中硫的杂化轨道类型是
中硫的杂化轨道类型是 的空间结构模型为
的空间结构模型为(3)配合物
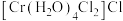 中铬的化合价为
中铬的化合价为(4)ZnSe晶胞与ZnS晶胞相似(如图),ZnSe晶胞中部分原子的分数坐标为:A点
 (0,0,0),B点
(0,0,0),B点 的坐标为
的坐标为 的位置
的位置 的个数为
的个数为 ,请计算ZnSe晶胞的密度
,请计算ZnSe晶胞的密度

您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐3】以CuSO4、NaOH和抗坏血酸为原料,可制备Cu₂O。_____ 。
(2) 的空间构型为
的空间构型为_____ (用文字描述);Cu2+与OH−反应能生成[Cu(OH)4]2−,[Cu(OH)4]2−中的配位原子为_____ (填元素符号)。
(3)抗坏血酸的分子结构如图1所示,分子中碳原子的轨道杂化类型为_____ ;推测抗坏血酸在水中的溶解性:_____ (填“难溶于水”或“易溶于水”)。
(4)一个Cu2O晶胞(见图2)中,Cu原子的数目为_____ 。


(2)
 的空间构型为
的空间构型为(3)抗坏血酸的分子结构如图1所示,分子中碳原子的轨道杂化类型为
(4)一个Cu2O晶胞(见图2)中,Cu原子的数目为
您最近一年使用:0次



