A、B、C、D、E、F均为36号以前的元素,原子序数依次增大。A的最外层电子数与次外层电子数相等。B元素的价层电子排布是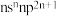 ,C元素
,C元素 价离子与B的离子电子层结构相同,D元素基态原子的最高能级有一个未成对电子且电子云为哑铃形,E元素基态的
价离子与B的离子电子层结构相同,D元素基态原子的最高能级有一个未成对电子且电子云为哑铃形,E元素基态的 价离子的
价离子的 轨道为半充满,F元素基态原子的最外层只有一个电子。回答下列问题:
轨道为半充满,F元素基态原子的最外层只有一个电子。回答下列问题:
(1)C的元素符号是______ 。上述六种元素中,位于周期表d区、 区的分别是
区的分别是___________ 、______ (填元素符号)。
(2)基态D原子的电子排布式是______ ,A、B、D电负性由大到小的顺序是______ (填元素符号)。
(3)向含 价F离子的水溶液中滴加氨水至过量,产生的现象是
价F离子的水溶液中滴加氨水至过量,产生的现象是___________ ,发生反应的离子方程式为___________ 、___________ 。
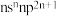 ,C元素
,C元素 价离子与B的离子电子层结构相同,D元素基态原子的最高能级有一个未成对电子且电子云为哑铃形,E元素基态的
价离子与B的离子电子层结构相同,D元素基态原子的最高能级有一个未成对电子且电子云为哑铃形,E元素基态的 价离子的
价离子的 轨道为半充满,F元素基态原子的最外层只有一个电子。回答下列问题:
轨道为半充满,F元素基态原子的最外层只有一个电子。回答下列问题:(1)C的元素符号是
 区的分别是
区的分别是(2)基态D原子的电子排布式是
(3)向含
 价F离子的水溶液中滴加氨水至过量,产生的现象是
价F离子的水溶液中滴加氨水至过量,产生的现象是
更新时间:2023-07-18 11:52:22
|
相似题推荐
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐1】图表是元素周期表的一部分,表中所列的数字分别代表某一种元素。
请完成下列空白。
(1)当今考古工作者利用元素⑤的核素即_______ ,测定一些文物的年代,该核素的中子数为_______ 。
(2)画出最外层电子数等于最内层电子数的元素的原子结构示意图:_____ 。
(3)能证明元素⑧比⑨的非金属性强的实验操作及现象_______ 。
(4)写出①与⑥形成的三原子分子的电子式是_______ 。
(5)元素⑥与⑦的气态氢化物的稳定性强弱:_______ >_______ (填化学式)。
(6)②元素与⑨元素形成化合物的化学式是_______ ,用电子式表示该化合物的形成过程 _______ 。
| 周期 | ⅠA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ⑤ | ⑥ | ||||||
| 3 | ② | ③ | ④ | ⑦ | ⑧ | |||
| 4 | ⑨ | |||||||
(1)当今考古工作者利用元素⑤的核素即
(2)画出最外层电子数等于最内层电子数的元素的原子结构示意图:
(3)能证明元素⑧比⑨的非金属性强的实验操作及现象
(4)写出①与⑥形成的三原子分子的电子式是
(5)元素⑥与⑦的气态氢化物的稳定性强弱:
(6)②元素与⑨元素形成化合物的化学式是
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐2】前20号元素A、B、C、D,A元素所处的周期数、主族序数、原子序数均相等;B的原子半径是其所在主族中最小的,B的最高价氧化物对应水化物的化学式为HBO3;C元素原子的最外层电子数比次外层少2个;C的阴离子与D的阳离子具有相同的电子排布,两元素可形成化合物D2C。
(1)D元素的名称____________ ; B元素的原子结构示意图________________ ;
(2)C在周期表中的位置___________ ;
(3)化合物D2C的电子式_____________ ;
(4)B的氢化物的水溶液加入B的最高价氧化物对应水化物的稀溶液,反应的离子方程式为:_____ ;
(5)有人认为,A单质是一种优质能源,你认为它作为能源的优点是:____ 。
(1)D元素的名称
(2)C在周期表中的位置
(3)化合物D2C的电子式
(4)B的氢化物的水溶液加入B的最高价氧化物对应水化物的稀溶液,反应的离子方程式为:
(5)有人认为,A单质是一种优质能源,你认为它作为能源的优点是:
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
【推荐3】A、B、C、D、E、F是元素周期表前四周期中的常见元素,其原子序数依次增大。A元素的一种核素的质量数是14,中子数是8;B元素基态原子的最外层有3个未成对电子,次外层有2个电子;C是地壳中含量最多的一种元素;D元素基态原子核外9个原子轨道上填充了电子且有1个未成对电子;E是一种常见的金属元素,可形成多种氧化物,其中一种氧化物是具有磁性的黑色物质;F元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子。请完成以下空白:
(1)D元素的基态原子中,核外电子占据的最高能层的符号为___________ ,基态C离子占据的最高能级共有___________ 个原子轨道。
(2)B元素的基态原子价层电子的电子排布图为___________ 。
(3)请解释E3+离子比E2+离子稳定的原因:___________ 。
(4)基态F二价阳离子的核外电子排布式为___________ 。
(5)A、B、C三种元素的第一电离能从大到小为___________ (用元素符号表示)。
(6)BD3与水反应产生有漂白性的物质,写出该反应的化学方程式___________ 。
(1)D元素的基态原子中,核外电子占据的最高能层的符号为
(2)B元素的基态原子价层电子的电子排布图为
(3)请解释E3+离子比E2+离子稳定的原因:
(4)基态F二价阳离子的核外电子排布式为
(5)A、B、C三种元素的第一电离能从大到小为
(6)BD3与水反应产生有漂白性的物质,写出该反应的化学方程式
您最近一年使用:0次
【推荐1】金属和非金属分界线附近的元素(如 、
、 、
、 ),可用于制造半导体材料,是科学研究的热点。试回答下列问题:
),可用于制造半导体材料,是科学研究的热点。试回答下列问题:
(1)锗( )是一种重要的半导体材料,写出基态
)是一种重要的半导体材料,写出基态 原子的价层电子排布式,说明价电子在其最高能级上的分布遵循的原则。
原子的价层电子排布式,说明价电子在其最高能级上的分布遵循的原则。________
(2) 是一种非晶态半导体,也称玻璃半导体。区分晶体与非晶体的最可靠的科学方法是
是一种非晶态半导体,也称玻璃半导体。区分晶体与非晶体的最可靠的科学方法是________ ?
(3) 等是人工合成的新型半导体材料,其晶体结构与金刚石相似,如图所示。每个
等是人工合成的新型半导体材料,其晶体结构与金刚石相似,如图所示。每个 原子周围有
原子周围有________ 个距离最近的 原子?每个晶胞中有
原子?每个晶胞中有________ 个 原子?
原子?

 、
、 、
、 ),可用于制造半导体材料,是科学研究的热点。试回答下列问题:
),可用于制造半导体材料,是科学研究的热点。试回答下列问题:(1)锗(
 )是一种重要的半导体材料,写出基态
)是一种重要的半导体材料,写出基态 原子的价层电子排布式,说明价电子在其最高能级上的分布遵循的原则。
原子的价层电子排布式,说明价电子在其最高能级上的分布遵循的原则。(2)
 是一种非晶态半导体,也称玻璃半导体。区分晶体与非晶体的最可靠的科学方法是
是一种非晶态半导体,也称玻璃半导体。区分晶体与非晶体的最可靠的科学方法是(3)
 等是人工合成的新型半导体材料,其晶体结构与金刚石相似,如图所示。每个
等是人工合成的新型半导体材料,其晶体结构与金刚石相似,如图所示。每个 原子周围有
原子周围有 原子?每个晶胞中有
原子?每个晶胞中有 原子?
原子?
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐2】氮化钛广泛用于耐高温、耐磨损及航空航天等领域。一种氮化钛的制备反应为:6TiCl4+8NH3 = 6TiN+24HCl+N2 ,回答下列问题:
(1)钛在元素周期表中的位置为_____________ ,基态Ti原子价层电子的轨道表达式为________ 。
(2)氮可与其他元素形成正离子,如NH4Cl中的NH4+,N2O5中的NO2+。组成这两种正离子的元素中第一电离能由小到大的顺序为____________ ;NH4+的空间构型为___________ ;NO2+中氮原子的杂化形式为_______ ,其中σ键与π键的数目比为_________ 。
(3)四氯化钛晶体的熔点为-23 ℃,沸点为136 ℃,则TiCl4晶体的类型为___________ ,该晶体中微粒之间的作用力为___________ 。
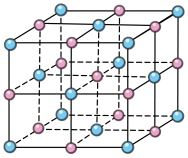
(4)一种TiN金黄色晶体晶胞结构与NaCl相同(如图),该晶胞中N原子数目为_______ ;该氮化钛的密度为5.4 g/cm3,则其晶胞参数a=___________ pm(用NA表示阿伏加德常数的数值,只列算式)。
(1)钛在元素周期表中的位置为
(2)氮可与其他元素形成正离子,如NH4Cl中的NH4+,N2O5中的NO2+。组成这两种正离子的元素中第一电离能由小到大的顺序为
(3)四氯化钛晶体的熔点为-23 ℃,沸点为136 ℃,则TiCl4晶体的类型为
(4)一种TiN金黄色晶体晶胞结构与NaCl相同(如图),该晶胞中N原子数目为

您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐3】锗(Ge)是典型的半导体元素,在电子、材料等领域应用广泛。回答下列问题:
(1)基态Ge原子的电子排布式为_______ ,有_______ 个未成对电子。
(2)比较下列锗卤化物的熔点和沸点,分析其变化规律及原因:_______ 。
(3)Ge单晶具有金刚石型结构,其中Ge原子的杂化方式为_______ ,微粒之间存在的作用力是_______ 。
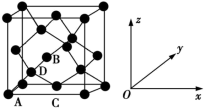
(4)原子坐标参数,表示晶胞内部各原子的相对位置。如图为Ge单晶的晶胞,其中原子坐标参数A为(0,0,0);B为( ,0,
,0, );C为(
);C为( ,
, ,0);则D原子的坐标参数为
,0);则D原子的坐标参数为_______ 。
(1)基态Ge原子的电子排布式为
(2)比较下列锗卤化物的熔点和沸点,分析其变化规律及原因:
| GeCl4 | GeBr4 | GeI4 | |
| 熔点/℃ | -49.5 | 26 | 146 |
| 沸点/℃ | 83.1 | 186 | 约400 |
(4)原子坐标参数,表示晶胞内部各原子的相对位置。如图为Ge单晶的晶胞,其中原子坐标参数A为(0,0,0);B为(
 ,0,
,0, );C为(
);C为( ,
, ,0);则D原子的坐标参数为
,0);则D原子的坐标参数为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐1】X、Y、Z、W、R为原子序数依次增大的前四周期元素。基态X原子的价电子排布式为nsnnpn+1;Y的+2价阳离子核外电子排布与氖原子相同;Z元素的第一至第四电离能分别是:I1=578kJ∙mol-1、I2=1817kJ∙mol-1、I3=2745kJ∙mol-1、I4=11575kJ∙mol-1;W的最高正价与最低负价的代数和为6:基态R2+的M层有5个未成对电子。
回答下列问题:
(1)R元素在元素周期表中的位置为___________ ,原子序数比R少1的元素原子基态核外排布式为:___________ 。
(2)元素的气态原子得到一个电子所放出的能量称为第一电子亲合能。气态原子结合电子越容易,电子亲合能越大。X和W的第一电子亲合能X___________ W(填“>”或“<”),利用原子结构知识解释原因___________ 。
(3)X、Z、W的简单离子半径由大到小的顺序是___________ (填离子符号)。
(4)Z单质与NaOH反应的离子反应方程式为___________ 。
回答下列问题:
(1)R元素在元素周期表中的位置为
(2)元素的气态原子得到一个电子所放出的能量称为第一电子亲合能。气态原子结合电子越容易,电子亲合能越大。X和W的第一电子亲合能X
(3)X、Z、W的简单离子半径由大到小的顺序是
(4)Z单质与NaOH反应的离子反应方程式为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐2】下表列出了前20号元素中某些元素性质的一些数据:
试回答下列问题:
(1)以上10种元素中,第一电离能最小的是___________ (填元素符号)。
(2)上述⑤、⑥、⑦三种元素中的某两种元素形成的化合物中,每一个原子都满足8e 稳定结构的物质可能是___________ (写分子式,只答一条即可)。元素⑨和⑩形成的化合物的化学式为___________ ;元素①的原子价电子排布式是___________ 。
(3)①、⑥、⑦、⑩四种元素的电负性,由强到弱的顺序是___________ (填化学式)。
(4)③和⑨两元素比较,非金属性较弱的是___________ (填名称),可以验证你的结论的是下列中的___________ (填序号)。
A.气态氢化物的稳定性 B.单质分子中的键能
C.两元素的电负性 D.最高价含氧酸的酸性
| 性质元素 | 原子半径(1019m) | 最高价态 | 最低价态 |
| ① | 1.02 | +6 | 2 |
| ② | 2.27 | +1 | — |
| ③ | 0.74 | — | 2 |
| ④ | 1.43 | +3 | — |
| ⑤ | 0.77 | +4 | 4 |
| ⑥ | 1.10 | +5 | 3 |
| ⑦ | 0.99 | +7 | 1 |
| ⑧ | 1.86 | +1 | — |
| ⑨ | 0.75 | +5 | 3 |
| ⑩ | 1.17 | +4 | 4 |
(1)以上10种元素中,第一电离能最小的是
(2)上述⑤、⑥、⑦三种元素中的某两种元素形成的化合物中,每一个原子都满足8e 稳定结构的物质可能是
(3)①、⑥、⑦、⑩四种元素的电负性,由强到弱的顺序是
(4)③和⑨两元素比较,非金属性较弱的是
A.气态氢化物的稳定性 B.单质分子中的键能
C.两元素的电负性 D.最高价含氧酸的酸性
您最近一年使用:0次
【推荐3】我国科学家利用碲化锆(ZrTe2)和砷化镉(Cd3As2)为材料成功地验证了三维两字霍尔效应,并发现了金属—绝缘体的转换。回答下列问题:
(1)基态砷原子的价电子排布式为____ 。
(2)As与Ge、Se同周期且相邻,它们的第一电离能由大到小的顺序为____ (用元素符号表示)。
(3)与砷(As)同主族的N、P两种元素的氢化物水溶液的碱性:NH3>PH3原因是____ 。
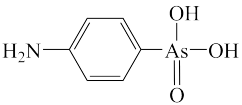
(4)含砷有机物“对氨基苯砷酸”的结构简式如图,砷原子轨道杂化类型为____ 。
(5)Cd2+与NH3形成的配离子[Cd(NH3)4]2+中,2个NH3被2个Cl-替代只得到1种结构,[Cd(NH3)4]2+的立体构型是____ ,1mol[Cd(NH3)4]2+含____ molσ键。
(1)基态砷原子的价电子排布式为
(2)As与Ge、Se同周期且相邻,它们的第一电离能由大到小的顺序为
(3)与砷(As)同主族的N、P两种元素的氢化物水溶液的碱性:NH3>PH3原因是
(4)含砷有机物“对氨基苯砷酸”的结构简式如图,砷原子轨道杂化类型为

(5)Cd2+与NH3形成的配离子[Cd(NH3)4]2+中,2个NH3被2个Cl-替代只得到1种结构,[Cd(NH3)4]2+的立体构型是
您最近一年使用:0次



