我国科学家利用碲化锆(ZrTe2)和砷化镉(Cd3As2)为材料成功地验证了三维两字霍尔效应,并发现了金属—绝缘体的转换。回答下列问题:
(1)基态砷原子的价电子排布式为____ 。
(2)As与Ge、Se同周期且相邻,它们的第一电离能由大到小的顺序为____ (用元素符号表示)。
(3)与砷(As)同主族的N、P两种元素的氢化物水溶液的碱性:NH3>PH3原因是____ 。
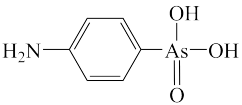
(4)含砷有机物“对氨基苯砷酸”的结构简式如图,砷原子轨道杂化类型为____ 。
(5)Cd2+与NH3形成的配离子[Cd(NH3)4]2+中,2个NH3被2个Cl-替代只得到1种结构,[Cd(NH3)4]2+的立体构型是____ ,1mol[Cd(NH3)4]2+含____ molσ键。
(1)基态砷原子的价电子排布式为
(2)As与Ge、Se同周期且相邻,它们的第一电离能由大到小的顺序为
(3)与砷(As)同主族的N、P两种元素的氢化物水溶液的碱性:NH3>PH3原因是
(4)含砷有机物“对氨基苯砷酸”的结构简式如图,砷原子轨道杂化类型为

(5)Cd2+与NH3形成的配离子[Cd(NH3)4]2+中,2个NH3被2个Cl-替代只得到1种结构,[Cd(NH3)4]2+的立体构型是
更新时间:2022-04-15 19:48:54
|
相似题推荐
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐1】a、b、c、d、e、f分别是H、C、N、Na、Si、Cu六种元素中的其中一种,已知:下图甲表示的是这六种元素单质的熔点高低顺序,其中c、d均是热和电的良导体,f形成的某种单质硬度最大。
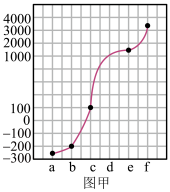
回答下列问题:
(1)a、b、f三种元素的电负性从小到大的顺序为___________ (用元素符号表示);
(2)元素b的单质的一个分子中含有___________ 个σ键和___________ 个π键;
(3)c单质分别与氟气和氯气形成化合物甲和乙,则甲的熔点___________ 乙的熔点(填>或<);
(4)元素d的基态原子的价电子排布式为___________ ;
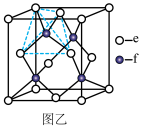
(5)元素e和f可形成化合物丙(丙的晶胞结构如图乙所示),则丙的化学式为___________ 丙的晶体类型为___________ ,在丙中,每个e原子周围最近的e原子数目为___________ 若晶胞参数为apm,则丙的密度表达式为___________ g・cm-3(用NA表示阿伏加德罗常数的值,丙的摩尔质量为Mg・mol-1)。

回答下列问题:
(1)a、b、f三种元素的电负性从小到大的顺序为
(2)元素b的单质的一个分子中含有
(3)c单质分别与氟气和氯气形成化合物甲和乙,则甲的熔点
(4)元素d的基态原子的价电子排布式为
(5)元素e和f可形成化合物丙(丙的晶胞结构如图乙所示),则丙的化学式为

您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐2】锰的单质及其化合物的用途非常广泛 回答下列问题:
回答下列问题:
⑴基态锰原子的外围电子排布式为______________________ ,其d轨道中未成对电子数为__________ 。
⑵MnO的熔点(1650℃)比MnS的熔点(1610℃)高原因是_____________________________________ 。
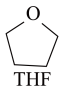
⑶锰的一种配合物的化学式为Mn(BH4)2(THF)3,THF的结构简式如图所示。
①THF中的元素的电负性从大到小的顺序是__________________ 。
②与Mn2+形成配位键的原子为______ (填元素符号)。
③BH4-的空间构型为_______ ,其中B原子的杂化轨道类型为________ 。
④写出两种与BH4-互为等电子体的分子或离子___________ 。
⑷一种磁性材料的单晶胞结构如图所示。
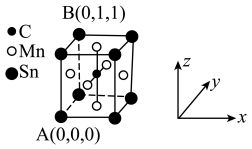
①该晶胞中碳原子的原子坐标为________ 。
②Mn在晶体中的堆积方式为_______ (填“简单立方”“体心立方”或“面心立方最密”)堆积。
③若该晶胞的边长为a pm,NA表示阿伏加 德罗常数的数值,则该晶体密度的表达式为ρ =___________________ g∙cm-3。
 回答下列问题:
回答下列问题:
⑴基态锰原子的外围电子排布式为
⑵MnO的熔点(1650℃)比MnS的熔点(1610℃)高原因是
⑶锰的一种配合物的化学式为Mn(BH4)2(THF)3,THF的结构简式如图所示。
①THF中的元素的电负性从大到小的顺序是
②与Mn2+形成配位键的原子为
③BH4-的空间构型为
④写出两种与BH4-互为等电子体的分子或离子
⑷一种磁性材料的单晶胞结构如图所示。

①该晶胞中碳原子的原子坐标为
②Mn在晶体中的堆积方式为
③若该晶胞的边长为a pm,NA表示阿伏加 德罗常数的数值,则该晶体密度的表达式为ρ =
您最近一年使用:0次
【推荐3】A、B、C、D、E、F是6种原子序数依次增大的前四周期元素,部分元素性质或原子结构如下:
(1)E元素的基态原子的核外电子排布式为_______ 。
(2)用电子式表示化合物DC2的形成过程:_______ 。
(3)A、B、C三种元素简单氢化物的沸点由高到低的顺序为_______ (用化学式表示)。
(4)F元素的单质与A元素的最高价氧化物对应水化物的稀溶液反应的化学方程式为_______ 。
| 元素 | 元素性质或原子结构 |
| A | 基态原子价层电子排布为nsnnpn+1 |
| C | 元素周期表中电负性最大的元素 |
| D | 原子核外有三个电子层,且最外层电子数是核外电子总数的 |
| E | E3+的3d轨道为半充满状态 |
| F | 基态原子的M层全充满,N层只有一个电子 |
(2)用电子式表示化合物DC2的形成过程:
(3)A、B、C三种元素简单氢化物的沸点由高到低的顺序为
(4)F元素的单质与A元素的最高价氧化物对应水化物的稀溶液反应的化学方程式为
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐1】Ⅰ.蒙脱石散对消化道内的病毒、病菌及其产生的毒素、气体等有极强的固定、抑制作用,常用于成人及儿童急性、慢性腹泻。蒙脱石散的有效成分可表示为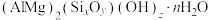 。
。
(1)基态
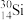 原子的核外电子排布式为
原子的核外电子排布式为(2)O、Mg、Al、Si四种元素的第一电离能从大到小的顺序为
(3)
 是无色透明液体,可以与N-甲基咪唑
是无色透明液体,可以与N-甲基咪唑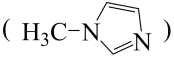 等物质反应。
等物质反应。①将用毛皮摩擦过的橡胶棒靠近 液流,液体流
液流,液体流
②一个N-甲基咪唑分子中含有
(4)硅酸盐与二氧化硅一样,都是以硅氧四面体作为基本结构单元。硅氧四面体可以表示成
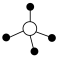 :其中●表示氧原子,中心◯表示硅原子,其俯视图为
:其中●表示氧原子,中心◯表示硅原子,其俯视图为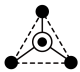 。
。① 晶胞可理解成将金刚石晶胞(如图1所示)中的C原子置换成Si原子,然后在
晶胞可理解成将金刚石晶胞(如图1所示)中的C原子置换成Si原子,然后在 之间插入O原子而形成。
之间插入O原子而形成。
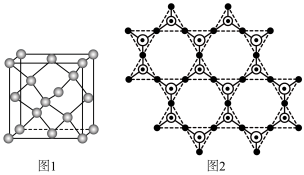
推测 晶胞中含有
晶胞中含有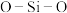 的键角为
的键角为
②蒙脱石散中的“(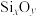 )”是一种大片层状的多硅酸根,其可能结构如图2所示,则
)”是一种大片层状的多硅酸根,其可能结构如图2所示,则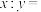
Ⅱ.以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子的分数坐标。四方晶系的晶胞结构如图所示,晶胞棱边夹角均为90°,晶胞中部分原子的分数坐标如下表所示。
坐标原子 | x | y | z |
Cd | 0 | 0 | 0 |
Sn | 0 | 0 | 0.5 |
As | 0.25 | 0.25 | 0.125 |
(5)一个晶胞中有
 最近的Sn
最近的Sn 晶体中与Sn距离最近的As有
晶体中与Sn距离最近的As有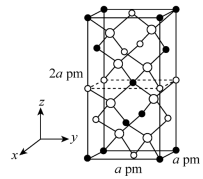
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐2】下表是元素周期表的一部分,表中所列的字母分别代表一种元素。
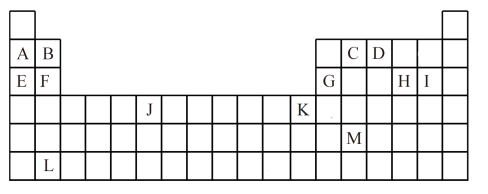
试回答下列问题:
(1)一个J原子(基态)中未成对电子数为_____ ,L的原子序数为_____ ,M的简化电子排布式为_____ 。
(2)K位于元素周期表中第_____ 周期、_____ 族,属于_____ 区元素;
(3)根据对角线规则及已知元素性质,写出B、E元素最高价氧化物的水化物在溶液反应的离子方程式_____ 。
(4)下列有关说法正确的是_____

试回答下列问题:
(1)一个J原子(基态)中未成对电子数为
(2)K位于元素周期表中第
(3)根据对角线规则及已知元素性质,写出B、E元素最高价氧化物的水化物在溶液反应的离子方程式
(4)下列有关说法正确的是_____
A.第一电离能 | B.电负性 |
C.原子半径 | D.最高价含氧酸的酸性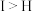 |
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐3】氮的化合物应用广泛。
(1)Reineckesalt的结构如图所示:
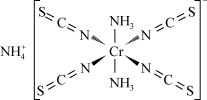
其中配位原子为_______ (填元素符号),阳离子的空间结构为_______ , 中碳原子杂化方式为
中碳原子杂化方式为_______ 。
(2)重铬酸铵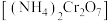 为桔黄色单斜结晶,常用作有机合成催化剂,
为桔黄色单斜结晶,常用作有机合成催化剂, 的结构如图。
的结构如图。
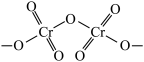
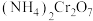 中N、O、
中N、O、 三种元素第一电离能由大到小的顺序是
三种元素第一电离能由大到小的顺序是_______ (填元素符号), 该物质中含σ键的数目为
该物质中含σ键的数目为_______  。
。
(3) 是
是 的一种配合物,
的一种配合物, 的结构为
的结构为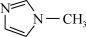 。
。 的某种衍生物与甘氨酸形成的离子化合物
的某种衍生物与甘氨酸形成的离子化合物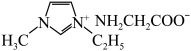 常温下为液态而非固态,原因是
常温下为液态而非固态,原因是_______ 。
(4)已知:多原子分子中,若原子都在同一平面上且这些原子有相互平行的p轨道,则p电子可在多个原子间运动,形成“离域 键”(或大
键”(或大 键)。大
键)。大 键可用
键可用 表示,其中m、n分别代表参与形成大
表示,其中m、n分别代表参与形成大 键的原子个数和电子数,如苯分子中大
键的原子个数和电子数,如苯分子中大 键表示为
键表示为 。
。
①下列微粒中存在“离域 键”的是
键”的是_______ 。
A. B.
B.
C. D.
D.
② 中阴离子
中阴离子 与
与 互为等电子体,均为直线型结构,
互为等电子体,均为直线型结构, 中的2个大
中的2个大 键可表示为
键可表示为_______ 。
(5)符号“ ”没有给出的信息是_______。
”没有给出的信息是_______。
(6)下列实验事实不能用氢键来解释的是_______。
(7)下列图像是 、
、 、
、 等离子晶体结构图或者是从其中分割出来的部分结构图。其中属于
等离子晶体结构图或者是从其中分割出来的部分结构图。其中属于 的晶体结构的图是
的晶体结构的图是
(8)键能的大小可以衡量化学键的强弱。下列说法中错误的是
(1)Reineckesalt的结构如图所示:

其中配位原子为
 中碳原子杂化方式为
中碳原子杂化方式为(2)重铬酸铵
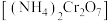 为桔黄色单斜结晶,常用作有机合成催化剂,
为桔黄色单斜结晶,常用作有机合成催化剂, 的结构如图。
的结构如图。
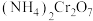 中N、O、
中N、O、 三种元素第一电离能由大到小的顺序是
三种元素第一电离能由大到小的顺序是 该物质中含σ键的数目为
该物质中含σ键的数目为 。
。(3)
 是
是 的一种配合物,
的一种配合物, 的结构为
的结构为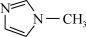 。
。 的某种衍生物与甘氨酸形成的离子化合物
的某种衍生物与甘氨酸形成的离子化合物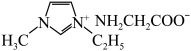 常温下为液态而非固态,原因是
常温下为液态而非固态,原因是(4)已知:多原子分子中,若原子都在同一平面上且这些原子有相互平行的p轨道,则p电子可在多个原子间运动,形成“离域
 键”(或大
键”(或大 键)。大
键)。大 键可用
键可用 表示,其中m、n分别代表参与形成大
表示,其中m、n分别代表参与形成大 键的原子个数和电子数,如苯分子中大
键的原子个数和电子数,如苯分子中大 键表示为
键表示为 。
。①下列微粒中存在“离域
 键”的是
键”的是A.
 B.
B.
C.
 D.
D.
②
 中阴离子
中阴离子 与
与 互为等电子体,均为直线型结构,
互为等电子体,均为直线型结构, 中的2个大
中的2个大 键可表示为
键可表示为(5)符号“
 ”没有给出的信息是_______。
”没有给出的信息是_______。| A.能层 | B.能级 |
| C.电子云在空间的伸展方向 | D.电子的自旋方向 |
A. 比 比 稳定 稳定 |
| B.乙醇能与水以任意比互溶 |
| C.邻羟基苯甲醛的沸点低于对羟基苯甲醛 |
| D.接近沸点的水蒸气的相对分子质量测量值大于18 |
 、
、 、
、 等离子晶体结构图或者是从其中分割出来的部分结构图。其中属于
等离子晶体结构图或者是从其中分割出来的部分结构图。其中属于 的晶体结构的图是
的晶体结构的图是A.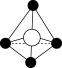 | B.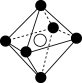 | C. | D.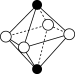 |
| 化学键 |  |  |  |  |  |  |
键能 | 460 | 360 | 436 | 431 | 176 | 347 |
A. 的熔点比 的熔点比 熔点低 熔点低 |
B. 的稳定性比 的稳定性比 稳定性高 稳定性高 |
C. 的键能大于 的键能大于 |
D.拆开 晶体硅中的化学键所吸收的能量为 晶体硅中的化学键所吸收的能量为 |
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
【推荐1】“防晒霜”能有效地减轻紫外光对皮肤的伤害,其原因是其有效成分的分子中含有π键。研究表明,有效成分分子中的π键电子可在吸收紫外光后被激发,可以阻挡部分紫外光对皮肤的伤害,如对甲氧基肉桂酸辛酯、水杨酸辛酯均为“防晒霜”的主要成分。
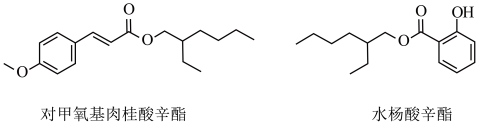
(1)对甲氧基肉桂酸辛酯和水杨酸辛酯均由H、C、O三种元素组成,按要求回答问题:
①基态O原子的核外电子排布式为_______ ,其中电子占据最高能级的电子云轮廓图为_____ 形。
其同周期元素中,第一电离能最大的是___________ (写元素符号)。
②在基态C原子中,核外存在___________ 对自旋相反的电子。
③三种元素电负性大小顺序为____________ 。
④水杨酸辛酯分子中碳原子的杂化方式有___________ 。
(2)早在公元前3000年,人们发现柳树皮具有解热镇痛功效。1838年意大利化学家拉菲勒·皮里亚以柳树皮为原料制得水杨酸,此后科学家对水杨酸的分子结构进行一系列修饰,合成出疗效更佳的长效缓释阿司匹林。

①已知苯酚(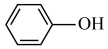 )具有弱酸性,其Ka=1.1×10-10,水杨酸第一级电离形成离子
)具有弱酸性,其Ka=1.1×10-10,水杨酸第一级电离形成离子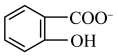 可以形成分子内氢键。在相同温度下,水杨酸的二级电离平衡常数Ka2
可以形成分子内氢键。在相同温度下,水杨酸的二级电离平衡常数Ka2___________ Ka(苯酚)(填“>”、“<”或“=”),其原因是___________ 。
②对羟基苯甲酸(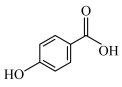 )是水杨酸的同分异构体,其沸点比水杨酸沸点
)是水杨酸的同分异构体,其沸点比水杨酸沸点___________ 。(填“高”、“低”或“相同”),原因是___________ 。
③用于合成阿司匹林的有机物A的结构简式为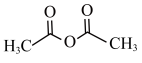 ,A分子中π键和σ键的个数之比为
,A分子中π键和σ键的个数之比为___________ 。

(1)对甲氧基肉桂酸辛酯和水杨酸辛酯均由H、C、O三种元素组成,按要求回答问题:
①基态O原子的核外电子排布式为
其同周期元素中,第一电离能最大的是
②在基态C原子中,核外存在
③三种元素电负性大小顺序为
④水杨酸辛酯分子中碳原子的杂化方式有
(2)早在公元前3000年,人们发现柳树皮具有解热镇痛功效。1838年意大利化学家拉菲勒·皮里亚以柳树皮为原料制得水杨酸,此后科学家对水杨酸的分子结构进行一系列修饰,合成出疗效更佳的长效缓释阿司匹林。

①已知苯酚(
 )具有弱酸性,其Ka=1.1×10-10,水杨酸第一级电离形成离子
)具有弱酸性,其Ka=1.1×10-10,水杨酸第一级电离形成离子 可以形成分子内氢键。在相同温度下,水杨酸的二级电离平衡常数Ka2
可以形成分子内氢键。在相同温度下,水杨酸的二级电离平衡常数Ka2②对羟基苯甲酸(
 )是水杨酸的同分异构体,其沸点比水杨酸沸点
)是水杨酸的同分异构体,其沸点比水杨酸沸点③用于合成阿司匹林的有机物A的结构简式为
 ,A分子中π键和σ键的个数之比为
,A分子中π键和σ键的个数之比为
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
【推荐2】回答下列问题
(1)铁元素在元素周期表中的位置为___________ ,其形成的离子常见的有 和
和 ,基态
,基态 的价电子的排布式为
的价电子的排布式为___________ ,相同条件下, 比
比 稳定,原因是
稳定,原因是___________ 。
(2)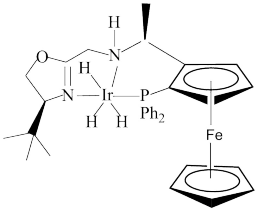 一种二茂铁为骨架的新型手性膦氮配合物结构示意图(见上),其中
一种二茂铁为骨架的新型手性膦氮配合物结构示意图(见上),其中 为苯基,
为苯基, 为铱元素。该结构中电负性最大的元素为
为铱元素。该结构中电负性最大的元素为___________ (填元素符号,下同),分子中第二周期元素的第一电离能由大到小的顺序为___________ ,分子中不含有的化学键类型是___________ (填标号)。
A.离子键B.配位键C.极性共价键D.非极性共价键E. 键、
键、 键
键
(3) 与
与 位于同一周期且最外层电子构型相同,铁的熔点和沸点均比钙的高,其原因是
位于同一周期且最外层电子构型相同,铁的熔点和沸点均比钙的高,其原因是___________
(1)铁元素在元素周期表中的位置为
 和
和 ,基态
,基态 的价电子的排布式为
的价电子的排布式为 比
比 稳定,原因是
稳定,原因是(2)
 一种二茂铁为骨架的新型手性膦氮配合物结构示意图(见上),其中
一种二茂铁为骨架的新型手性膦氮配合物结构示意图(见上),其中 为苯基,
为苯基, 为铱元素。该结构中电负性最大的元素为
为铱元素。该结构中电负性最大的元素为A.离子键B.配位键C.极性共价键D.非极性共价键E.
 键、
键、 键
键(3)
 与
与 位于同一周期且最外层电子构型相同,铁的熔点和沸点均比钙的高,其原因是
位于同一周期且最外层电子构型相同,铁的熔点和沸点均比钙的高,其原因是
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐3】甲硅烷 可用于制备多种新型无机非金属材料。
可用于制备多种新型无机非金属材料。
(1)Si原子与H原子结合时,Si表现为正价,则电负性:Si_________ H(填“>”“<”或“=”), 分子的空间结构为
分子的空间结构为_________________ 。
(2)利用 与
与 可制得氮化硅(
可制得氮化硅( )材料。
)材料。
①热稳定性:
___________  (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
② 中
中 的键角
的键角__________  中
中 的键角(“>”“<”或“=”),其键角差异的原因是
的键角(“>”“<”或“=”),其键角差异的原因是_____________________________ 。
(3)利用 与
与 反应可制得碳化硅晶体,晶胞结构如图,硅原子位于立方体的顶点和面心,碳原子位于立方体的内部。
反应可制得碳化硅晶体,晶胞结构如图,硅原子位于立方体的顶点和面心,碳原子位于立方体的内部。
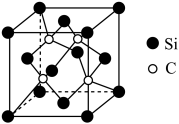
①碳化硅晶体中每个Si原子周围距离最近的C原子数目为__________ ,SiC的晶体类型是_____________ 。
②已知碳化硅的晶胞边长为a nm(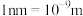 ),阿伏伽德罗常数为
),阿伏伽德罗常数为 。则碳化硅晶体的密度为
。则碳化硅晶体的密度为_____________  (列出计算式)。
(列出计算式)。
 可用于制备多种新型无机非金属材料。
可用于制备多种新型无机非金属材料。(1)Si原子与H原子结合时,Si表现为正价,则电负性:Si
 分子的空间结构为
分子的空间结构为(2)利用
 与
与 可制得氮化硅(
可制得氮化硅( )材料。
)材料。①热稳定性:

 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。②
 中
中 的键角
的键角 中
中 的键角(“>”“<”或“=”),其键角差异的原因是
的键角(“>”“<”或“=”),其键角差异的原因是(3)利用
 与
与 反应可制得碳化硅晶体,晶胞结构如图,硅原子位于立方体的顶点和面心,碳原子位于立方体的内部。
反应可制得碳化硅晶体,晶胞结构如图,硅原子位于立方体的顶点和面心,碳原子位于立方体的内部。
①碳化硅晶体中每个Si原子周围距离最近的C原子数目为
②已知碳化硅的晶胞边长为a nm(
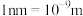 ),阿伏伽德罗常数为
),阿伏伽德罗常数为 。则碳化硅晶体的密度为
。则碳化硅晶体的密度为 (列出计算式)。
(列出计算式)。
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐1】铜是生活中常见的金属,铜及其化合物在不同环境中能呈现出不同的颜色:

回答下列问题:
(1)Cu基态核外电子排布式为___ ;科学家通过X射线测得Cu(H2O)4SO4·H2O结构示意图可简单表示如图:
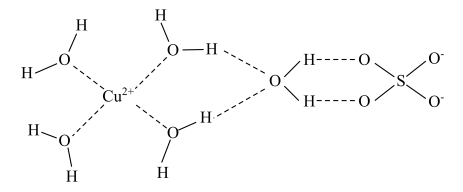
图中虚线表示的作用力为___ 。
(2)已知Cu+(SCN)2 Cu+(SCN)2,1mol(SCN)2分子中含有的π键数目为
Cu+(SCN)2,1mol(SCN)2分子中含有的π键数目为___ ,写出2个与SCN-互为等电子体的分子的化学式___ 。
(3)金属铜单独与氨水或单独与过氧化氢都不能反应,但可与氨水和过氧化氢的混合溶液反应,其原因是___ ,反应的化学方程式为___ 。
(4)在Cu(H2O)4SO4·H2O晶体中,[Cu(NH3)4]2+为平面正方形结构,则呈正四面体结构的原子团是___ ,其中心原子的杂化轨道类型是___ 。
(5)已知Cu的晶胞结构如图所示,铜原子的配位数为___ ,又知晶胞边长为3.61×10-8cm,则Cu的密度为___ (保留三位有效数字)。


回答下列问题:
(1)Cu基态核外电子排布式为

图中虚线表示的作用力为
(2)已知Cu+(SCN)2
 Cu+(SCN)2,1mol(SCN)2分子中含有的π键数目为
Cu+(SCN)2,1mol(SCN)2分子中含有的π键数目为(3)金属铜单独与氨水或单独与过氧化氢都不能反应,但可与氨水和过氧化氢的混合溶液反应,其原因是
(4)在Cu(H2O)4SO4·H2O晶体中,[Cu(NH3)4]2+为平面正方形结构,则呈正四面体结构的原子团是
(5)已知Cu的晶胞结构如图所示,铜原子的配位数为

您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
【推荐2】目前新能源汽车电池主要是磷酸铁锂(LiFePO4)和三元锂电池(正极含有Ni、Co、Mn三种元素)。回答下列问题:
(1)基态Co原子核外有___________ 对电子对,其最外层电子所在能级的电子云轮廓形状为___________ 。
(2)LiFePO4中四种元素的第一电离能由大到小的顺序是___________ (填元素符号),其阴离子的立体构型名称是___________ 。
(3)检验Ni2+的方法:加入丁二酮肟试剂立即生成鲜红色的二丁二酮肟合镍(II)螯合物。反应方程式如下:
2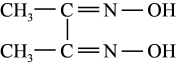 (丁二酮肟)+Ni2+
(丁二酮肟)+Ni2+
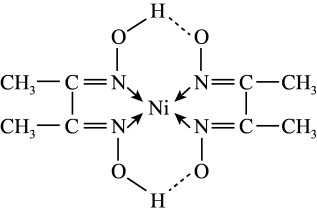 (二丁二酮肟合镍(II))+2H+
(二丁二酮肟合镍(II))+2H+
①试比较丁二酮肟与丁二酮(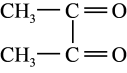 )熔点高低,并说明理由
)熔点高低,并说明理由___________ 。
②二丁二酮肟合镍(II)螯合物中不存在的作用力有___________ (填正确答案标号)。
A.离子键 B.配位键 C.极性共价键 D.非极性共价键 E.氢键
(4)原子核外电子有两种相反的自旋状态,分别用+ 和-
和- 表示,称为电子的自旋磁量子数。基态Mn原子的价电子自旋磁量子数的代数和为
表示,称为电子的自旋磁量子数。基态Mn原子的价电子自旋磁量子数的代数和为___________ 。
(1)基态Co原子核外有
(2)LiFePO4中四种元素的第一电离能由大到小的顺序是
(3)检验Ni2+的方法:加入丁二酮肟试剂立即生成鲜红色的二丁二酮肟合镍(II)螯合物。反应方程式如下:
2
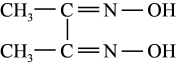 (丁二酮肟)+Ni2+
(丁二酮肟)+Ni2+
 (二丁二酮肟合镍(II))+2H+
(二丁二酮肟合镍(II))+2H+①试比较丁二酮肟与丁二酮(
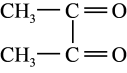 )熔点高低,并说明理由
)熔点高低,并说明理由②二丁二酮肟合镍(II)螯合物中不存在的作用力有
A.离子键 B.配位键 C.极性共价键 D.非极性共价键 E.氢键
(4)原子核外电子有两种相反的自旋状态,分别用+
 和-
和- 表示,称为电子的自旋磁量子数。基态Mn原子的价电子自旋磁量子数的代数和为
表示,称为电子的自旋磁量子数。基态Mn原子的价电子自旋磁量子数的代数和为
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐3】矾是一些金属硫酸盐的统称,其中皓矾的化学式为 ,可用作媒染剂、木材防腐剂。下图是
,可用作媒染剂、木材防腐剂。下图是 的结构示意图:
的结构示意图: 离子。
离子。
1. 分子的分子构型为
分子的分子构型为___________ ,中心原子杂化方式为___________ 杂化。
2. 的沸点
的沸点___________ (填>、<或=)水的沸点,原因可能是___________ 。
3. 中,
中, 与
与 间的作用力为
间的作用力为___________ , 与
与 间的作用力为
间的作用力为___________ 。
4. 与
与 中的中心原子均为
中的中心原子均为 杂化,
杂化, 中H—O—H键角
中H—O—H键角___________ (填>、<或=) 中O—S—O键角,原因是
中O—S—O键角,原因是___________ 。
5.写出 溶于氨水的化学方程式
溶于氨水的化学方程式___________ 。
6. 受热失水时,随着温度的升高,先失去一个水分子,变为
受热失水时,随着温度的升高,先失去一个水分子,变为 ,再失去其它的水,首先失去的水分子应为
,再失去其它的水,首先失去的水分子应为___________ (填①或②),原因是___________ 。
 ,可用作媒染剂、木材防腐剂。下图是
,可用作媒染剂、木材防腐剂。下图是 的结构示意图:
的结构示意图: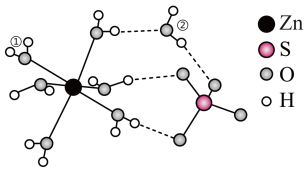
 离子。
离子。1.
 分子的分子构型为
分子的分子构型为2.
 的沸点
的沸点3.
 中,
中, 与
与 间的作用力为
间的作用力为 与
与 间的作用力为
间的作用力为4.
 与
与 中的中心原子均为
中的中心原子均为 杂化,
杂化, 中H—O—H键角
中H—O—H键角 中O—S—O键角,原因是
中O—S—O键角,原因是5.写出
 溶于氨水的化学方程式
溶于氨水的化学方程式6.
 受热失水时,随着温度的升高,先失去一个水分子,变为
受热失水时,随着温度的升高,先失去一个水分子,变为 ,再失去其它的水,首先失去的水分子应为
,再失去其它的水,首先失去的水分子应为
您最近一年使用:0次



