Ⅰ.蒙脱石散对消化道内的病毒、病菌及其产生的毒素、气体等有极强的固定、抑制作用,常用于成人及儿童急性、慢性腹泻。蒙脱石散的有效成分可表示为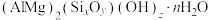 。
。
(1)基态
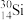 原子的核外电子排布式为
原子的核外电子排布式为(2)O、Mg、Al、Si四种元素的第一电离能从大到小的顺序为
(3)
 是无色透明液体,可以与N-甲基咪唑
是无色透明液体,可以与N-甲基咪唑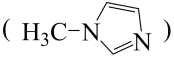 等物质反应。
等物质反应。①将用毛皮摩擦过的橡胶棒靠近 液流,液体流
液流,液体流
②一个N-甲基咪唑分子中含有
(4)硅酸盐与二氧化硅一样,都是以硅氧四面体作为基本结构单元。硅氧四面体可以表示成
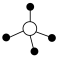 :其中●表示氧原子,中心◯表示硅原子,其俯视图为
:其中●表示氧原子,中心◯表示硅原子,其俯视图为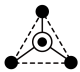 。
。① 晶胞可理解成将金刚石晶胞(如图1所示)中的C原子置换成Si原子,然后在
晶胞可理解成将金刚石晶胞(如图1所示)中的C原子置换成Si原子,然后在 之间插入O原子而形成。
之间插入O原子而形成。
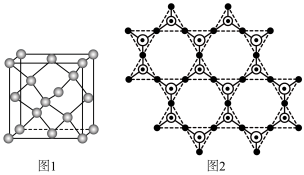
推测 晶胞中含有
晶胞中含有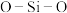 的键角为
的键角为
②蒙脱石散中的“(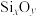 )”是一种大片层状的多硅酸根,其可能结构如图2所示,则
)”是一种大片层状的多硅酸根,其可能结构如图2所示,则
Ⅱ.以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子的分数坐标。四方晶系的晶胞结构如图所示,晶胞棱边夹角均为90°,晶胞中部分原子的分数坐标如下表所示。
坐标原子 | x | y | z |
Cd | 0 | 0 | 0 |
Sn | 0 | 0 | 0.5 |
As | 0.25 | 0.25 | 0.125 |
(5)一个晶胞中有
 最近的Sn
最近的Sn 晶体中与Sn距离最近的As有
晶体中与Sn距离最近的As有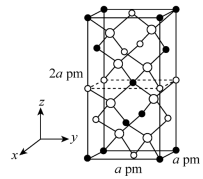
更新时间:2024-03-27 23:39:57
|
相似题推荐
【推荐1】下表是元素周期表的一部分,表中的字母分别代表一种化学元素。

(1)上述元素中,原子中未成对电子数最多的是___________ (填字母),写出该元素基态原子的核外电子排布式: ___________ 。
(2)根据下表所提供的电离能数据,回答下列问题。
①表中X可能为以上13种元素中的 _____________ (填字母)元素。用元素符号表示X和j形成的一种化合物的化学式: _____________ 。
②Y是周期表中第_____________ 族元素。

(1)上述元素中,原子中未成对电子数最多的是
(2)根据下表所提供的电离能数据,回答下列问题。
| 锂 | X | Y | |
| I1 | 520 | 496 | 580 |
| I2 | 7296 | 4562 | 1820 |
| I3 | 11799 | 6912 | 2750 |
| I4 | 9543 | 11600 |
②Y是周期表中第
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐2】过渡金属元素铬(Cr)是不锈钢的重要成分,在工农业生产和国防建设中有着广泛应用。回答下列问题:
(1)Cr 是第___________ 周期第___________ 族元素。
(2)基态 Cr 原子的核外电子有___________ 种空间运动状态,有___________ 个未成对电子。
(3)Cr3+能形成多种配位化合物。[Cr(NH3)3(H2O)2Cl]2+中,中心离子的配位数为___________ 。
(4)[Cr(NH3)3(H2O)2Cl]2+的配体分子 NH3 中 N 的杂化轨道类型是___________ ,H2O 的键角小于 NH3,原因是___________ 。
(5)在金属材料中添加 AlCr2 颗粒,可以增强材料的耐腐蚀性、硬度和机械性能。AlCr2 具有体心四方结构,如下图所示,处于顶角位置的是___________ 原子。若 NA 表示阿伏加德罗常数的值,则该晶体的密度为___________ g∙cm−3(用含 a、c 和 NA 的代数式表示)。晶胞中长、宽为a nm,高为c nm。
(1)Cr 是第
(2)基态 Cr 原子的核外电子有
(3)Cr3+能形成多种配位化合物。[Cr(NH3)3(H2O)2Cl]2+中,中心离子的配位数为
(4)[Cr(NH3)3(H2O)2Cl]2+的配体分子 NH3 中 N 的杂化轨道类型是
(5)在金属材料中添加 AlCr2 颗粒,可以增强材料的耐腐蚀性、硬度和机械性能。AlCr2 具有体心四方结构,如下图所示,处于顶角位置的是

您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
解题方法
【推荐3】活性氧化锌能对太阳光线和其他大气物质形成防护,常用于敏感皮肤的面霜和化妆品。工业上用菱锌矿(主要成分为ZnCO3,还含有Ni、Cd、Fe、Cu等元素及少量不溶于水的杂质)制备ZnO,工艺流程图所示:
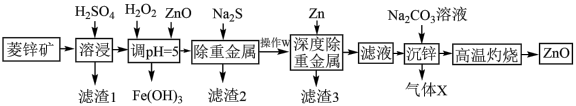
(1)写出Ni、Fe元素在周期表中的位置_______ ,常温下Fe2+比Fe3+更容易被氧化变质,请从结构角度加以解释_______ 。
(2)加入H2O2的目的是_______ ;“调pH”时除ZnO外还可以选用的物质是_______ 。
a.氨水 b.氢氧化铁 c.氢氧化锌
(3)常温下、pH=5时,Fe3+的浓度降到了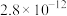 mol/L,此时Fe(OH)3的溶度积常数的数值为
mol/L,此时Fe(OH)3的溶度积常数的数值为_______ 。证明Fe3+已除尽的化学方法是_______ 。
(4)已知沉锌时固体产物是Zn2(OH)2CO3,请写出该过程的离子方程式:_______ 。
(5)粗锌中含有少量Al、Fe、Cu等杂质,可用电解法制备高纯度锌,下列叙述正确的是_______。
(6)活性氧化锌纯度测定,已知:1.0mL1.0mol/LEDTA标准溶液相当于氧化锌质量为0.080克。取w克所得活性氧化锌样品配成含Zn2+的待测液,用c mol/LEDTA标准液进行滴定,消耗标准液VmL。计算产品中氧化锌纯度为_______ 。
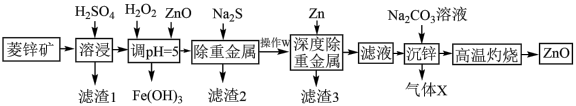
(1)写出Ni、Fe元素在周期表中的位置
(2)加入H2O2的目的是
a.氨水 b.氢氧化铁 c.氢氧化锌
(3)常温下、pH=5时,Fe3+的浓度降到了
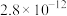 mol/L,此时Fe(OH)3的溶度积常数的数值为
mol/L,此时Fe(OH)3的溶度积常数的数值为(4)已知沉锌时固体产物是Zn2(OH)2CO3,请写出该过程的离子方程式:
(5)粗锌中含有少量Al、Fe、Cu等杂质,可用电解法制备高纯度锌,下列叙述正确的是_______。
| A.粗锌作阳极,纯锌作阴极,电解质溶液是硫酸锌溶液 |
| B.电解过程中,阳极质量的减少与阴极质量的增加相等 |
| C.电解后,溶液中存在的金属阳离子只有Al3+、Fe2+和Zn2+ |
| D.电解后,电解槽底部的阳极泥中只有Cu |
(6)活性氧化锌纯度测定,已知:1.0mL1.0mol/LEDTA标准溶液相当于氧化锌质量为0.080克。取w克所得活性氧化锌样品配成含Zn2+的待测液,用c mol/LEDTA标准液进行滴定,消耗标准液VmL。计算产品中氧化锌纯度为
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
【推荐1】氮、氧、硫、磷是与生命活动密切相关的元素。回答下列问题:
(1)SO2分子的VSEPR模型名称是___________
(2)N、O、P三种元素第一电离能由大到小的顺序是___________
(3)SCN-中C原子的杂化类型为___________ 杂化,1 mol SCN-中含π键的数目为___________ NA。
(4)晶胞有两个基本要素:
①原子坐标参数,表示晶胞内部各原子的相对位置。磷化硼是一种超硬耐磨的涂层材料,其晶胞结构如图所示,其中原子坐标参数A为(0,0,0);B为( ,
, ,0);D为(1,1,1)。则C的原子坐标参数为
,0);D为(1,1,1)。则C的原子坐标参数为___________

②晶胞参数,描述晶胞的大小和形状。P原子与B原子的最近距离为a cm,则磷化硼晶胞的边长为___________ cm。(用含a的代数式表示)
(1)SO2分子的VSEPR模型名称是
(2)N、O、P三种元素第一电离能由大到小的顺序是
(3)SCN-中C原子的杂化类型为
(4)晶胞有两个基本要素:
①原子坐标参数,表示晶胞内部各原子的相对位置。磷化硼是一种超硬耐磨的涂层材料,其晶胞结构如图所示,其中原子坐标参数A为(0,0,0);B为(
 ,
, ,0);D为(1,1,1)。则C的原子坐标参数为
,0);D为(1,1,1)。则C的原子坐标参数为
②晶胞参数,描述晶胞的大小和形状。P原子与B原子的最近距离为a cm,则磷化硼晶胞的边长为
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐2】近年来,我国的材料技术如陶瓷基复合材料氮化硼(BN)、太阳能电池材料砷化镓(GaAs)、新型储氢材料、光电材料等发展迅猛,请按要求回答下列问题。
(1)基态N原子的轨道表示式为_______ ,B与N的电负性由大到小的顺序为_______ (用元素符号表示)。
(2)基态砷原子的价层电子排布式为_______ ,占据最高能级的电子所在的原子轨道为_______ 形。
(3)硼氢化钠(NaBH4,其中氢元素显-1价)是研究最广泛的储氢材料之一,硼原子在成键时,能将一个2s电子激发进入2p能级参与形成化学键,该过程形成的原子光谱为_______ 光谱(填“吸收”或“发射”),与硼处于同一周期的元素中,第一电离能大于硼的主族元素有_______ 种。
(4)铜配合物在光电材料方面的应用非常广泛,其中基态Cu原子的核外电子排布式为_______ ,Cu在元素周期表中属于_______ 区。
(1)基态N原子的轨道表示式为
(2)基态砷原子的价层电子排布式为
(3)硼氢化钠(NaBH4,其中氢元素显-1价)是研究最广泛的储氢材料之一,硼原子在成键时,能将一个2s电子激发进入2p能级参与形成化学键,该过程形成的原子光谱为
(4)铜配合物在光电材料方面的应用非常广泛,其中基态Cu原子的核外电子排布式为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐3】如图是元素周期表的一部分,根据元素在周期表中的位置,回答下列问题:
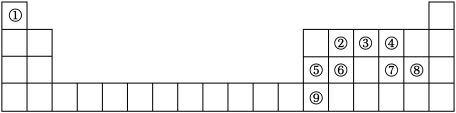
(1)⑤号元素基态原子最高能级的电子占据的原子轨道电子云轮廓为___________ 形。
(2)②③④号元素的第一电离能由大到小的顺序为___________ (用元素符号表示)。
(3)元素①②形成的一种化合物是石油化学工业重要的基本原料,写出该化合物中σ键与π键的数目之比为___________ 。
(4)元素⑦⑧可形成原子个数比为 的共价化合物,分子中各原子最外层均达到8电子的稳定结构,试写出其结构式:
的共价化合物,分子中各原子最外层均达到8电子的稳定结构,试写出其结构式:___________ 。
(5)元素③⑥形成的化合物是一种性质优良的无机非金属材料,具有熔点高,硬度大,电绝缘性好,化学性质稳定等性质,它的晶体类型是___________ 。
(6)元素⑨可形成的卤化物的熔点如表所示:
三种物质的熔点呈现以上规律的原因是___________ 。

(1)⑤号元素基态原子最高能级的电子占据的原子轨道电子云轮廓为
(2)②③④号元素的第一电离能由大到小的顺序为
(3)元素①②形成的一种化合物是石油化学工业重要的基本原料,写出该化合物中σ键与π键的数目之比为
(4)元素⑦⑧可形成原子个数比为
 的共价化合物,分子中各原子最外层均达到8电子的稳定结构,试写出其结构式:
的共价化合物,分子中各原子最外层均达到8电子的稳定结构,试写出其结构式:(5)元素③⑥形成的化合物是一种性质优良的无机非金属材料,具有熔点高,硬度大,电绝缘性好,化学性质稳定等性质,它的晶体类型是
(6)元素⑨可形成的卤化物的熔点如表所示:
| 卤化物 | 氟化物 | 氯化物 | 溴化物 |
| 熔点/℃ | 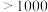 | 77.75 | 122.3 |
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐1】A、B、C、D、E、F均为前四周期的元素,原子序数依次增大,A的核外电子数等于其电子层数,B的最外层电子数是次外层电子数的3倍,A和C、B和E同主族,B、C、D的离子具有相同的电子层结构,D的离子是同周期中离子半径最小的,F原子中共有6个未成对电子。
请回答下列问题:
(1)写出下列元素的元素符号:A____ 、C_____ 、E_____ 、F_____ 。
(2)元素A和元素B可以形成A2B物质甲,写出甲的分子式____ ,甲为_____ (填“极性”或“非极性”)分子。
(3)元素A和元素E形成化合物乙,用电子式表示化合物乙_______________ ;常温下甲为液态,乙为气态,试解释原因__________________________ 。
(4)元素A与元素C形成化合物丙,丙的水溶液显碱性,试用化学方程式解释其原因:_________________ 。
(5)元素C、元素D的最高价氧化物的水化物相互反应的离子方程式是__________ 。
(6)写出元素F的外围电子排布式_______________________ 。
请回答下列问题:
(1)写出下列元素的元素符号:A
(2)元素A和元素B可以形成A2B物质甲,写出甲的分子式
(3)元素A和元素E形成化合物乙,用电子式表示化合物乙
(4)元素A与元素C形成化合物丙,丙的水溶液显碱性,试用化学方程式解释其原因:
(5)元素C、元素D的最高价氧化物的水化物相互反应的离子方程式是
(6)写出元素F的外围电子排布式
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
【推荐2】我国将力争在2030年前实现碳达峰,2060年前实现碳中和的目标,因此二氧化碳的固定以及转化将成为重要的研究课题。
I.在 催化下CO2和H2反应生成甲醇:
催化下CO2和H2反应生成甲醇: 。
。
II.新型 水介质电池放电时,温室气体CO2被转化为储氢物质HCOOH。
水介质电池放电时,温室气体CO2被转化为储氢物质HCOOH。
请回答下列问题:
(1)I中涉及的CO2、H2、CH3OH、H2O,属于非极性分子的是___________ ,基态O原子核外有___________ 种不同空间运动状态的电子。
(2)HCOOH分子中σ键和π键数目之比为___________ 。
(3)反应 中,碳原子的杂化方式由
中,碳原子的杂化方式由___________ 转变为___________ 。CH3OH的沸点高于CH3SH,原因是___________ 。
(4)一种铜的配合物为 ,其配体为
,其配体为___________ 。
I.在
 催化下CO2和H2反应生成甲醇:
催化下CO2和H2反应生成甲醇: 。
。II.新型
 水介质电池放电时,温室气体CO2被转化为储氢物质HCOOH。
水介质电池放电时,温室气体CO2被转化为储氢物质HCOOH。请回答下列问题:
(1)I中涉及的CO2、H2、CH3OH、H2O,属于非极性分子的是
(2)HCOOH分子中σ键和π键数目之比为
(3)反应
 中,碳原子的杂化方式由
中,碳原子的杂化方式由(4)一种铜的配合物为
 ,其配体为
,其配体为
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
名校
解题方法
【推荐3】某烟道气的主要成分是CO2,并含有少量硫氧化物、氮氧化物等杂质。其中的硫元素可在高温下通过CH4的作用回收,主要反应如下:2SO2(g)+CH4(g)⇌CO2(g)+2H2O(g)+S2(g)+Q(Q>0)
(1)以mol/(L•min)为单位,SO2的反应速率是S2生成速率的_________ 倍。
(2)恒容条件下,不能说明该反应已经达到平衡状态的是_______ (选填编号)
a.混合气体中水蒸气含量不再变化
b.混合气体密度不发生变化
c.容器内压强不再变化
d.混合物平均相对分子质量不再变化
达到平衡后升高体系温度,则平衡常数K_________ (填“增大”、“减小”、或“不变”)。
(3)请在下式中标出上述反应中电子转移的方向和数目:_____
2SO2(g)+CH4(g)⇌…该反应的氧化产物是_________ 。SO2的主要性质除氧化性、漂白性外还有________ 性。
(4)该反应混合物中有两种极性分子,分别是______ 和_____ ;固态硫的分子式可能是S8,它与S2互为________ 。
(5)烟道气中的NO2也能与CH4反应并生成无害气体,完全转化3.0molNO2气体时,需要甲烷的物质的量为__________ mol.
(1)以mol/(L•min)为单位,SO2的反应速率是S2生成速率的
(2)恒容条件下,不能说明该反应已经达到平衡状态的是
a.混合气体中水蒸气含量不再变化
b.混合气体密度不发生变化
c.容器内压强不再变化
d.混合物平均相对分子质量不再变化
达到平衡后升高体系温度,则平衡常数K
(3)请在下式中标出上述反应中电子转移的方向和数目:
2SO2(g)+CH4(g)⇌…该反应的氧化产物是
(4)该反应混合物中有两种极性分子,分别是
(5)烟道气中的NO2也能与CH4反应并生成无害气体,完全转化3.0molNO2气体时,需要甲烷的物质的量为
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐1】完成下列问题。
(1)指出溴在周期表中的位置:_ ,属于_ 区。
(2)用二氧化碳生产化工产品,有利于二氧化碳的大量回收。二氧化碳和乙二醇在ZnO或锌盐催化下可合成碳酸乙烯酯。
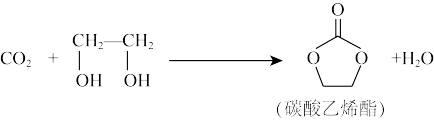
碳酸乙烯酯中碳原子杂化轨道类型为____ ;1mol碳酸乙烯酯中含有的 键数目为
键数目为____ 。
(3)苯胺( )与甲苯(
)与甲苯(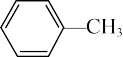 )的相对分子质量相近,但苯胺的熔点、沸点分别高于甲苯的熔点、沸点,原因是
)的相对分子质量相近,但苯胺的熔点、沸点分别高于甲苯的熔点、沸点,原因是_____ 。
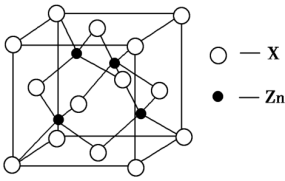
(4)下图表示锌与某非金属元素X形成的化合物晶胞,其中Zn和X通过共价键结合,该化合物的化学式为__ 。
(1)指出溴在周期表中的位置:
(2)用二氧化碳生产化工产品,有利于二氧化碳的大量回收。二氧化碳和乙二醇在ZnO或锌盐催化下可合成碳酸乙烯酯。

碳酸乙烯酯中碳原子杂化轨道类型为
 键数目为
键数目为(3)苯胺(
 )与甲苯(
)与甲苯( )的相对分子质量相近,但苯胺的熔点、沸点分别高于甲苯的熔点、沸点,原因是
)的相对分子质量相近,但苯胺的熔点、沸点分别高于甲苯的熔点、沸点,原因是(4)下图表示锌与某非金属元素X形成的化合物晶胞,其中Zn和X通过共价键结合,该化合物的化学式为

您最近一年使用:0次
【推荐2】氧化铈( )是一种广泛应用的稀土氧化物,具有吸收强紫外线的能力,可以用于光催化降解有机污染物。现以氟碳铈矿(含
)是一种广泛应用的稀土氧化物,具有吸收强紫外线的能力,可以用于光催化降解有机污染物。现以氟碳铈矿(含 、
、 、
、 等)为原料制备氧化铈,其工艺流程如图所示;
等)为原料制备氧化铈,其工艺流程如图所示;
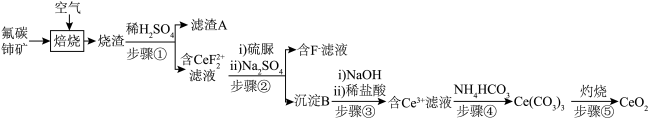
已知:①稀土离子易与 形成复盐沉淀。
形成复盐沉淀。
步骤②中 )发生的反应为:
)发生的反应为:
② 在空气中易被氧化为
在空气中易被氧化为 。
。
回答下列问题:
(1) 中
中 元素的化合价为
元素的化合价为___________ 。
(2)滤渣A的主要成分是___________ 。
(3)操作①所需的玻璃实验仪器有烧杯、___________ 。
(4)加入硫脲的目的是___________ 。
(5)步骤④中发生的离子方程式为___________ 。
(6)步骤④中生成的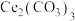 中
中 的空间构型是
的空间构型是___________ 。
(7)氧化铈的晶体结构如图所示,其已知晶胞参数为a pm,阿伏伽德罗常数为 ,则晶胞中铈离子间最短的距离为
,则晶胞中铈离子间最短的距离为___________ ,晶体密度为___________  (写出计算式)。
(写出计算式)。
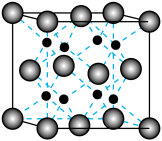
 )是一种广泛应用的稀土氧化物,具有吸收强紫外线的能力,可以用于光催化降解有机污染物。现以氟碳铈矿(含
)是一种广泛应用的稀土氧化物,具有吸收强紫外线的能力,可以用于光催化降解有机污染物。现以氟碳铈矿(含 、
、 、
、 等)为原料制备氧化铈,其工艺流程如图所示;
等)为原料制备氧化铈,其工艺流程如图所示;
已知:①稀土离子易与
 形成复盐沉淀。
形成复盐沉淀。步骤②中
 )发生的反应为:
)发生的反应为:
②
 在空气中易被氧化为
在空气中易被氧化为 。
。回答下列问题:
(1)
 中
中 元素的化合价为
元素的化合价为(2)滤渣A的主要成分是
(3)操作①所需的玻璃实验仪器有烧杯、
(4)加入硫脲的目的是
(5)步骤④中发生的离子方程式为
(6)步骤④中生成的
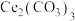 中
中 的空间构型是
的空间构型是(7)氧化铈的晶体结构如图所示,其已知晶胞参数为a pm,阿伏伽德罗常数为
 ,则晶胞中铈离子间最短的距离为
,则晶胞中铈离子间最短的距离为 (写出计算式)。
(写出计算式)。
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐3】完成下列问题。
(1)有下列粒子:①CH4 ②CH2O ③HCN ④NH3 ⑤ ⑥BF3 ⑦H2O。
⑥BF3 ⑦H2O。
①含有极性键的非极性分子的是______ (填编号,下同)。
②所有原子共平面的是_______ ,共线的是_______ 。
(2)过氧乙酸(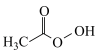 )也是一种常用消毒剂。在过氧乙酸中碳原子的杂化方式有
)也是一种常用消毒剂。在过氧乙酸中碳原子的杂化方式有______ ,分子中σ键和π键的个数比为_______ 。
(3) GaAs的熔点为1238℃,且熔融状态不导电,其晶胞结构如图所示,该晶体的类型为
GaAs的熔点为1238℃,且熔融状态不导电,其晶胞结构如图所示,该晶体的类型为_____ ,每个 原子周围最近的
原子周围最近的 原子数目为
原子数目为______ 。已知GaAs的密度为d g/cm3,摩尔质量为M g/mol,阿伏加德罗常数用NA表示,则晶胞的棱长为_____ nm(列式表示)。_____ (填字母)。
A.CO2 B.SiF4 C.SCl2 D. E.H3O+
E.H3O+
请分析键角大小比较的一般方法_____ 。
(1)有下列粒子:①CH4 ②CH2O ③HCN ④NH3 ⑤
 ⑥BF3 ⑦H2O。
⑥BF3 ⑦H2O。①含有极性键的非极性分子的是
②所有原子共平面的是
(2)过氧乙酸(
 )也是一种常用消毒剂。在过氧乙酸中碳原子的杂化方式有
)也是一种常用消毒剂。在过氧乙酸中碳原子的杂化方式有(3)
 GaAs的熔点为1238℃,且熔融状态不导电,其晶胞结构如图所示,该晶体的类型为
GaAs的熔点为1238℃,且熔融状态不导电,其晶胞结构如图所示,该晶体的类型为 原子周围最近的
原子周围最近的 原子数目为
原子数目为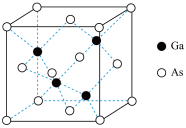
A.CO2 B.SiF4 C.SCl2 D.
 E.H3O+
E.H3O+请分析键角大小比较的一般方法
您最近一年使用:0次



