A、B、C、D、E、F是元素周期表前四周期中的常见元素,其原子序数依次增大。A元素的一种核素的质量数是14,中子数是8;B元素基态原子的最外层有3个未成对电子,次外层有2个电子;C是地壳中含量最多的一种元素;D元素基态原子核外9个原子轨道上填充了电子且有1个未成对电子;E是一种常见的金属元素,可形成多种氧化物,其中一种氧化物是具有磁性的黑色物质;F元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子。请完成以下空白:
(1)D元素的基态原子中,核外电子占据的最高能层的符号为___________ ,基态C离子占据的最高能级共有___________ 个原子轨道。
(2)B元素的基态原子价层电子的电子排布图为___________ 。
(3)请解释E3+离子比E2+离子稳定的原因:___________ 。
(4)基态F二价阳离子的核外电子排布式为___________ 。
(5)A、B、C三种元素的第一电离能从大到小为___________ (用元素符号表示)。
(6)BD3与水反应产生有漂白性的物质,写出该反应的化学方程式___________ 。
(1)D元素的基态原子中,核外电子占据的最高能层的符号为
(2)B元素的基态原子价层电子的电子排布图为
(3)请解释E3+离子比E2+离子稳定的原因:
(4)基态F二价阳离子的核外电子排布式为
(5)A、B、C三种元素的第一电离能从大到小为
(6)BD3与水反应产生有漂白性的物质,写出该反应的化学方程式
更新时间:2022-01-23 21:22:37
|
相似题推荐
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐1】A、B、C、D、E均为短周期元素,原子序数依次增大,请根据表中信息回答下列问题:
(1)G在元素周期表中的位置________ 。
(2)B最简单气态氢化物的结构式____ ,属于____ 化合物(填“离子”或“共价”);E的最高价氧化物的水化物电子式____ ,所含化学键类型________ 。
(3)C、D、E、F、G简单离子半径由大到小顺序为:____ (填离子符号)。
(4)用电子式表示G的氢化物的形成过程______ 。
(5)A元素的某氧化物与E元素的某含氧化合物反应生成单质的化学方程式是_______ 。
(6)E、F两元素最高价氧化物对应水化物相互反应的离子方程式:____ 。
| 元素 | 元素性质或结构 |
| A | 最外层电子数是其内层电子数的2倍 |
| B | B元素的单质在空气中含量最多 |
| C | C元素在地壳中含量最多 |
| D | D是同周期中原子半径最小的元素 |
| E | E元素在同周期中金属性最强 |
| F | F元素的最外层电子数等于周期序数 |
| G | G元素原子M层上电子数比L上少2个电子。 |
(2)B最简单气态氢化物的结构式
(3)C、D、E、F、G简单离子半径由大到小顺序为:
(4)用电子式表示G的氢化物的形成过程
(5)A元素的某氧化物与E元素的某含氧化合物反应生成单质的化学方程式是
(6)E、F两元素最高价氧化物对应水化物相互反应的离子方程式:
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐2】根据提供条件推断元素,并按要求填空:
(1)原子核外有3个电子层,其最外层电子数为7,最高价氧化物化学式________ ,最高价氧化物对应水化物化学式______ ,其最高价氧化物对应水化物与NaOH反应的化学方程式为_________ 。
(2)第三周期元素,其最外层电子数与电子层数相同。该元素最高价氧化物的化学式为________ ,最高价氧化物对应水化物与氢氧化钠反应的化学方程式为_______ 。
(3)原子序数依次递增的同周期4种元素,它们氢化物的质子数与电子数都与Ar相同,这些氢化物的化学式分别为____________ 、__________ 、_________ 、______ 。
(4)某元素的最高正价与最低负价的代数和为4,且最高价氧化物中含氧元素质量分数为60%。则该元素最高价氧化物的化学式为__________ ,该氧化物属________ (填“离子”或“共价”)化合物。
(1)原子核外有3个电子层,其最外层电子数为7,最高价氧化物化学式
(2)第三周期元素,其最外层电子数与电子层数相同。该元素最高价氧化物的化学式为
(3)原子序数依次递增的同周期4种元素,它们氢化物的质子数与电子数都与Ar相同,这些氢化物的化学式分别为
(4)某元素的最高正价与最低负价的代数和为4,且最高价氧化物中含氧元素质量分数为60%。则该元素最高价氧化物的化学式为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐3】有A、B、C、D、E五种元素,它们的核电荷数依次增大,且都小于20。其中A为非金属元素,A和E属于同一族,它们原子的最外层电子排布式为ns1。B和D也属于同一族,它们原子最外层的p能级电子数是s能级电子数的两倍,C原子最外层上电子数等于D原子最外层上电子数的一半。请回答下列问题:
(1)A是____ ,B是____ ,C是_____ ,D是____ ,E是____ 。
(2)由这五种元素组成的一种化合物是(写化学式)____ 。写出该物质的一种主要用途:____ 。
(3)写出C元素基态原子的电子排布式:___ 。
(4)用电子排布图表示D元素原子的外围电子排布为____ 。
(1)A是
(2)由这五种元素组成的一种化合物是(写化学式)
(3)写出C元素基态原子的电子排布式:
(4)用电子排布图表示D元素原子的外围电子排布为
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
【推荐1】C、N、Si、Ni等元素在新型材料的研制中有着重要应用,请回答下列问题:
(1)Ni元素的价层电子排布式为______ ,C、N、Si的第一电离能由大到小的顺序为______ 。
(2)研究发现, 固体由
固体由 和
和 两种离子组成,
两种离子组成, 空间构型为
空间构型为______ ; 和
和 二者相比较,
二者相比较, 键角更大,原因是
键角更大,原因是______ 。
(3)碳的一种同素异形体——石墨,其晶体片层结构俯视图如下A,晶胞结构如B,其中图A中的虚线表示的平行四边形即图B中的底面。石墨晶胞含碳原子个数为______ 。已知石墨的密度为 ,C—C键键长为a cm,阿伏加德罗常数的值为
,C—C键键长为a cm,阿伏加德罗常数的值为 ,石墨晶体的层间距为d cm,计算d为
,石墨晶体的层间距为d cm,计算d为______ cm。

(1)Ni元素的价层电子排布式为
(2)研究发现,
 固体由
固体由 和
和 两种离子组成,
两种离子组成, 空间构型为
空间构型为 和
和 二者相比较,
二者相比较, 键角更大,原因是
键角更大,原因是(3)碳的一种同素异形体——石墨,其晶体片层结构俯视图如下A,晶胞结构如B,其中图A中的虚线表示的平行四边形即图B中的底面。石墨晶胞含碳原子个数为
 ,C—C键键长为a cm,阿伏加德罗常数的值为
,C—C键键长为a cm,阿伏加德罗常数的值为 ,石墨晶体的层间距为d cm,计算d为
,石墨晶体的层间距为d cm,计算d为
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐2】原子序数依次递增的A、B、C、D、E五种元素,其中只有E是第四周期元素,A的一种核素中没有中子,B原子基态时最外层电子数是其内层电子数的2倍,D原子基态时2p原子轨道上有2个未成对的电子,E元素的原子结构中3d能级上未成对电子数是成对电子数的2倍。回答下列问题:
(1)E的+2价离子基态核外电子排布式为_______ 。
(2)A、B、C、D原子中,电负性最大的是_______ (元素符号)
(3)1 mol B2A4分子中σ键的数目为______ 。B4A6为链状结构,其分子中B原子轨道的杂化类型只有一种,则杂化类型为_______ 。
(4)C的简单氢化物在D 的简单氢化物中具有很大的溶解度,其主要原因是______ 。
(5)E和C形成的一种化合物的晶胞结构如图所示,该化合物的化学式为______ 。
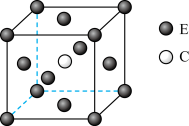
(1)E的+2价离子基态核外电子排布式为
(2)A、B、C、D原子中,电负性最大的是
(3)1 mol B2A4分子中σ键的数目为
(4)C的简单氢化物在D 的简单氢化物中具有很大的溶解度,其主要原因是
(5)E和C形成的一种化合物的晶胞结构如图所示,该化合物的化学式为

您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐3】X、Y、Z、W四种短周期主族元素,原子序数依次递增,X原子中有3个能量相等且自旋方向相同的电子,Y是地壳中含量最多的元素,Y与W同主族,Z在短周期主族元素中金属性最强。回答下列问题:
(1)X、Y、Z、W四种元素的原子半径从大到小的顺序为_______ (填元素符号)。
(2)元素Y的原子轨道表示式为_______ 。
(3)元素X与元素Y的简单气态氢化物中,稳定性较强的是_______ (填电子式)。
(4)Z原子的结构示意图为_______ 。
(5)W元素在元素周期表中的位置为_______ ,其价电子排布式为_______ 。
(1)X、Y、Z、W四种元素的原子半径从大到小的顺序为
(2)元素Y的原子轨道表示式为
(3)元素X与元素Y的简单气态氢化物中,稳定性较强的是
(4)Z原子的结构示意图为
(5)W元素在元素周期表中的位置为
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐1】砷化镓(GaAs)是当前最重要、技术成熟度最高的半导体材料之一,我国“玉兔二号”月球车就是通过砷化镓太阳能电池提供能量。
(1)GaAs、GaN结构相似,晶体类型都为共价晶体,沸点GaAs___________ GaN(填“>”或“<”,下同),第一电离能Ga___________ As。
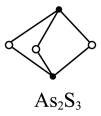
(2)成语“信口雌黄”中雌黄的分子式为As2S3,分子结构如图,As原子的杂化方式为___________ 。
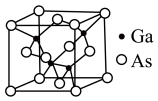
(3)GaAs的晶胞结构如图,在GaAs晶体中,与As原子最近且等距离的As原子数为______ 。
(4)若砷化镓晶胞边长为apm,则Ga与最近As的核间距为___________ cm。
(1)GaAs、GaN结构相似,晶体类型都为共价晶体,沸点GaAs
(2)成语“信口雌黄”中雌黄的分子式为As2S3,分子结构如图,As原子的杂化方式为

(3)GaAs的晶胞结构如图,在GaAs晶体中,与As原子最近且等距离的As原子数为

(4)若砷化镓晶胞边长为apm,则Ga与最近As的核间距为
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐2】Li是最轻的固体金属,采用Li作为负极材料的电池具有小而轻、能量密度大等优良性能,得到广泛应用。回答下列问题:
(1)下列Li原子电子排布图表示的状态中,能量最低和最高的分别为___ 、___ (填标号)。
A.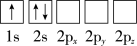
B.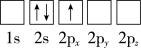
C.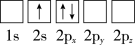
D.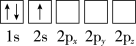
(2)Li+与H−具有相同的电子构型,r(Li+)小于r(H−),原因是___ 。
(3)LiAlH4是有机合成中常用的还原剂,LiAlH4中的阴离子(AlH )空间构型是
)空间构型是___ 、中心原子的杂化形式为___ 。
(4)Li2O是离子晶体,其晶格能可通过如图的Born−Haber循环计算得到。
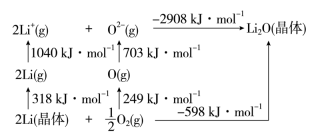
可知,Li原子的第一电离能为___ kJ·mol−1,O=O键键能为___ kJ·mol−1。
(1)下列Li原子电子排布图表示的状态中,能量最低和最高的分别为
A.

B.

C.

D.

(2)Li+与H−具有相同的电子构型,r(Li+)小于r(H−),原因是
(3)LiAlH4是有机合成中常用的还原剂,LiAlH4中的阴离子(AlH
 )空间构型是
)空间构型是(4)Li2O是离子晶体,其晶格能可通过如图的Born−Haber循环计算得到。
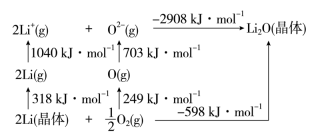
可知,Li原子的第一电离能为
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐3】碳、铜、锡及其化合物有许多用途。回答下列问题。
(1)在元素周期表里,锡和碳同族,锡位于第五周期。基态锡原子的最外层电子排布式为______ 。
(2)磷化铜(Cu3P2)用于制造磷青铜,磷青铜是含少量锡、磷的铜合金。磷化铜与水反应产生有毒的磷化氢(PH3)气体,PH3分子的热稳定性比NH3__________ (填“强”或“弱”);P、S的第二电离能(I2)的大小关系为I2(P) __________ I2(S)(填“>”“<”或“=”),原因是_______________ 。
(3)CH3CH2COOH中C的杂化方式有_________ ;1mol苯中含σ键的数目为________ 。
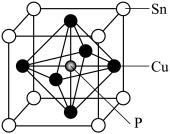
(4)磷青铜晶体的晶胞结构如图所示,该晶体中P原子与最近的Cu原子的核间距为a nm,则晶体密度为__________ g·cm−3(用含NA的代数式表示);该晶体中P原子位于由铜原子形成的正八面体的空隙中,则该正八面体的边长为________ nm。
(1)在元素周期表里,锡和碳同族,锡位于第五周期。基态锡原子的最外层电子排布式为
(2)磷化铜(Cu3P2)用于制造磷青铜,磷青铜是含少量锡、磷的铜合金。磷化铜与水反应产生有毒的磷化氢(PH3)气体,PH3分子的热稳定性比NH3
(3)CH3CH2COOH中C的杂化方式有
(4)磷青铜晶体的晶胞结构如图所示,该晶体中P原子与最近的Cu原子的核间距为a nm,则晶体密度为

您最近一年使用:0次



