前20号元素A、B、C、D,A元素所处的周期数、主族序数、原子序数均相等;B的原子半径是其所在主族中最小的,B的最高价氧化物对应水化物的化学式为HBO3;C元素原子的最外层电子数比次外层少2个;C的阴离子与D的阳离子具有相同的电子排布,两元素可形成化合物D2C。
(1)D元素的名称____________ ; B元素的原子结构示意图________________ ;
(2)C在周期表中的位置___________ ;
(3)化合物D2C的电子式_____________ ;
(4)B的氢化物的水溶液加入B的最高价氧化物对应水化物的稀溶液,反应的离子方程式为:_____ ;
(5)有人认为,A单质是一种优质能源,你认为它作为能源的优点是:____ 。
(1)D元素的名称
(2)C在周期表中的位置
(3)化合物D2C的电子式
(4)B的氢化物的水溶液加入B的最高价氧化物对应水化物的稀溶液,反应的离子方程式为:
(5)有人认为,A单质是一种优质能源,你认为它作为能源的优点是:
9-10高一下·浙江金华·期中 查看更多[1]
(已下线)2010年浙江永康市第一中学高一第二学期期中考试
更新时间:2019-01-30 18:14:09
|
相似题推荐
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐1】有A、B、C、D、E、F、G七种元素,它们的核电荷数依次增大,且都小于20,已知:A失去一个电子后就成为一个质子;B最外层的电子数是次外层电子数的2倍;C是地壳中含量最多的元素;D是一种金属元素;E元素原子K层与M层电子数相等;F和C具有相同的最外层电子数;G的最外层电子比次外层电子少一个。请回答以下问题:
(1)写出E离子的结构示意图是:_______
(2)写出 的结构式是:
的结构式是:_______
(3)写出D和F所形成的化合物的电子式是:_______
(4)B、C、D三种元素可形成一种化合物,该物质所含的化学键类型有_______
(5)用电子式表示A和G形成的化合物的形成过程:_______
(1)写出E离子的结构示意图是:
(2)写出
 的结构式是:
的结构式是:(3)写出D和F所形成的化合物的电子式是:
(4)B、C、D三种元素可形成一种化合物,该物质所含的化学键类型有
(5)用电子式表示A和G形成的化合物的形成过程:
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
【推荐2】一种用于“点击化学”的新化合物由W、X、Y、Z四种前20号元素组成,且原子序数依次增大。X原子的最外层电子数是次外层电子数的3倍,X、Z原子最外层电子数相同;Y元素的负离子核外电子排布和氖原子相同,Y原子的最外层电子数与W原子的核外电子总数相等。
(1)Y原子的结构示意图为___________ ,W离子的电子式是___________ 。
(2)比较微粒半径大小: X原子___________ Z原子,X离子___________ Y离子(选A表示“>”、B表示“=”或C表示“<”)。
(3)含Z元素的含氧酸且为弱酸的化学式___________ ,含W元素的一种酸式盐,受热分解后无固体物质剩余,该酸式盐的化学式为___________ 。
(4)含W元素的10电子离子有___________ (写出1种化学式,下同),除含X元素外,还含一种元素的18电子微粒有___________ 。
(1)Y原子的结构示意图为
(2)比较微粒半径大小: X原子
(3)含Z元素的含氧酸且为弱酸的化学式
(4)含W元素的10电子离子有
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐3】下表为元素周期表的一部分,表中序号各代表某一元素。请回答下列问题。
(1)③的原子结构示意图是___________ 。
(2)①~⑨中非金属性最强的元素是___________ (填化学式)。
(3)写出元素符号:③_______ ,
(4)元素⑦和⑨组成的化合物中含有的化学键是___________ (填“共价键”或“离子键”)。
(5)元素①的名称为___________ 。
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | VA | ⅥA | ⅦA | 0 |
| 2 | ⑦ | ⑧ | ⑩ | |||||
| 3 | ① | ③ | ⑤ | ⑥ | ⑨ | |||
| 4 | ② | ④ |
(2)①~⑨中非金属性最强的元素是
(3)写出元素符号:③
(4)元素⑦和⑨组成的化合物中含有的化学键是
(5)元素①的名称为
您最近一年使用:0次
【推荐1】锰酸锂( )是锂电池的正极材料,有望取代
)是锂电池的正极材料,有望取代 。一种以废旧电池正极材料(主要成分为
。一种以废旧电池正极材料(主要成分为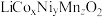 ,其中Co为+3价,还含少量铝箔、炭黑和有机黏合剂)为原料制备
,其中Co为+3价,还含少量铝箔、炭黑和有机黏合剂)为原料制备 的流程如下:
的流程如下:
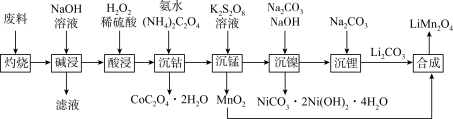
回答下列问题:
(1)Ni位于元素周期表中___________ 区。
(2) 的结构为:
的结构为: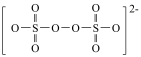 ,用“□”圈出
,用“□”圈出 中体现强氧化性的基团
中体现强氧化性的基团___________ 。
(3)“灼烧”的目的是除去___________ 、___________ 。
(4)根据“酸浸”前后物质价态的变化,推测双氧水发生反应的产物是___________ 。
(5)“沉锰”过程中,溶液先变为紫红色,一段时间后紫红色褪去。已知:加入 溶液之前,锰以
溶液之前,锰以 形式存在且溶液为弱酸性。则溶液变为紫红色的原因是
形式存在且溶液为弱酸性。则溶液变为紫红色的原因是___________ (用离子方程式表示)。由流程推测,“紫红色褪去”后,还可观察到的实验现象是___________ 。
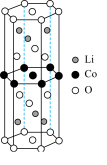
(6) 材料在脱锂过程中形成的某种晶体为六方晶系,结构如图。晶胞Li、Co、O的个数比为
材料在脱锂过程中形成的某种晶体为六方晶系,结构如图。晶胞Li、Co、O的个数比为___________ 。
 )是锂电池的正极材料,有望取代
)是锂电池的正极材料,有望取代 。一种以废旧电池正极材料(主要成分为
。一种以废旧电池正极材料(主要成分为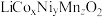 ,其中Co为+3价,还含少量铝箔、炭黑和有机黏合剂)为原料制备
,其中Co为+3价,还含少量铝箔、炭黑和有机黏合剂)为原料制备 的流程如下:
的流程如下:
回答下列问题:
(1)Ni位于元素周期表中
(2)
 的结构为:
的结构为: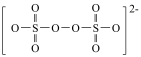 ,用“□”圈出
,用“□”圈出 中体现强氧化性的基团
中体现强氧化性的基团(3)“灼烧”的目的是除去
(4)根据“酸浸”前后物质价态的变化,推测双氧水发生反应的产物是
(5)“沉锰”过程中,溶液先变为紫红色,一段时间后紫红色褪去。已知:加入
 溶液之前,锰以
溶液之前,锰以 形式存在且溶液为弱酸性。则溶液变为紫红色的原因是
形式存在且溶液为弱酸性。则溶液变为紫红色的原因是(6)
 材料在脱锂过程中形成的某种晶体为六方晶系,结构如图。晶胞Li、Co、O的个数比为
材料在脱锂过程中形成的某种晶体为六方晶系,结构如图。晶胞Li、Co、O的个数比为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
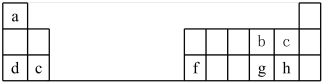
【推荐2】元素周期表对化学的发展有很大影响,在材料、能源、环境和生命科学研究上发挥着越来越重要的作用。下表是元素周期表的一部分。
(2)a-h元素的最高价氧化物对应的水化物中,酸性最强的是___________ (填化学式)。
(3)b元素有三种稳定核素,其式量分别为16、17、18,则三种核素的中子数之比为___________ 。
(4)c、g、h三种元素形成的气态氢化物中,稳定性最小的物质的结构式是___________ 。
(5)d元素的简单离子的结构示意图为___________ 。
(6)d的最高价氧化物对应水化物与f的最高价氧化物对应水化物的溶液反应的离子方程式为___________ 。
(7)若d单质着火,可用于灭火的物质是___________。
(8)下列关于元素周期表的叙述正确的是___________。
| A.第三周期第6族 | B.第三周期VI主族 |
| C.第三周期第6A族 | D.第三周期VIA族 |
(3)b元素有三种稳定核素,其式量分别为16、17、18,则三种核素的中子数之比为
(4)c、g、h三种元素形成的气态氢化物中,稳定性最小的物质的结构式是
(5)d元素的简单离子的结构示意图为
(6)d的最高价氧化物对应水化物与f的最高价氧化物对应水化物的溶液反应的离子方程式为
(7)若d单质着火,可用于灭火的物质是___________。
| A.自来水 | B.CO2 | C.干沙子 | D.湿抹布 |
| A.元素周期表中所含元素最多的族是BVII族 |
| B.IA族的元素全部是金属元素 |
| C.在元素周期表中金属与非金属的分界处可以找到半导体材料 |
| D.只有IIA族元素的原子最外层有2个电子 |
您最近一年使用:0次
【推荐3】2020年12月17日,我国“嫦娥五号”返回器携月壤成功着陆。根据已经发表的研究成果可知,月壤中存在天然的铁、金、银、铅、锌、铜、锑、铼等矿物颗粒。
(1)写出铜的基态原子的电子排布式___________ 。
(2)Fe在周期表中位于第___________ 周期第___________ 族,属于___________ 区。
(3)基态Fe原子有___________ 个未成对电子,Fe3+的电子排布式为___________ 。
(4)基态Al3+核外共有___________ 种不同运动状态的电子。
(5)采取的月壤中未发现钒(V)元素,其价层电子的轨道表示式为___________ 。钒(V)的某种氧化物的晶胞结构如图(1)所示。该晶体的化学式为___________ 。
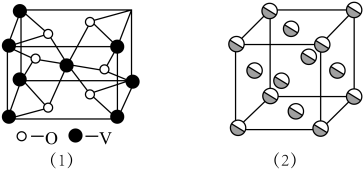
(6)金晶体的晶胞结构如图(2)所示。设金原子的直径为dcm,用NA表示阿伏加德罗常数,M表示金的摩尔质量,金的密度为___________ g/cm3(用d、M、NA表示)。
(1)写出铜的基态原子的电子排布式
(2)Fe在周期表中位于第
(3)基态Fe原子有
(4)基态Al3+核外共有
(5)采取的月壤中未发现钒(V)元素,其价层电子的轨道表示式为

(6)金晶体的晶胞结构如图(2)所示。设金原子的直径为dcm,用NA表示阿伏加德罗常数,M表示金的摩尔质量,金的密度为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐1】A、B、C、D、E均是短周期元素,其原子序数依次增大,A和B同周期,A和D同主族,A原子最外层电子数是内层电子数的二倍,B元素族序数是周期数的三倍,B的阴离子与C的阳离子电子层结构相同,C的单质与B的单质在不同条件下反应,可生成C2B或C2B2,E是所在周期中原子半径最小的元素。请回答:
(1)D在元素周期表中的位置是___________________________ 。
(2)C2B的电子式是__________________ 。
(3)B、C、E的离子半径由大到小的顺序为__________________ (用化学式回答,下同);A、D、E元素最高价氧化物对应水化物的酸性由强到弱为_________________ 。
(4)B的气态氢化物与H2S相比沸点高的是_________ (用化学式回答);原因是___________ 。
(5)水中锰含量超标,容易使洁具和衣物染色,使水产生异味,EB2可以用来除去水中超标的Mn2+,生成黑色沉淀MnO2,当消耗13.50gEB2时,共转移了1mol电子,则反应的离子方程式:_____________ 。
(1)D在元素周期表中的位置是
(2)C2B的电子式是
(3)B、C、E的离子半径由大到小的顺序为
(4)B的气态氢化物与H2S相比沸点高的是
(5)水中锰含量超标,容易使洁具和衣物染色,使水产生异味,EB2可以用来除去水中超标的Mn2+,生成黑色沉淀MnO2,当消耗13.50gEB2时,共转移了1mol电子,则反应的离子方程式:
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐2】位于前四周期的6种主族元素A、B、C、D、E、F原子序数依次增大,其中B、D同主族, D、E同周期。A、B、C在周期表中相邻,且三种元素的原子最外层电子数之和为18。F是其所在周期中最活泼的金属元素。根据推断回答下列问题:
(1)A在周期表中的位置_____ ;写出A单质的电子式________ 。
(2)用“>”或“<”填空:
(3)—定条件,在水溶液中1molE-、 (x=1,2,3,4)的能量(KJ)相对大小如图所示。
(x=1,2,3,4)的能量(KJ)相对大小如图所示。
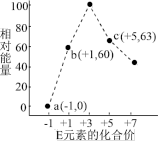
①c点对应的微粒是_______ (填离子符号)。
②b→a+c反应的离子方程式为________ ,该反应是______ 反应(填“吸热”或“放热”)。
(1)A在周期表中的位置
(2)用“>”或“<”填空:
| 离子半径 | 非金属性 | 酸性 | 氢化物的稳定性 |
| F+ | A | D的最高价氧化物的水化物 | C的氢化物 |
(3)—定条件,在水溶液中1molE-、
 (x=1,2,3,4)的能量(KJ)相对大小如图所示。
(x=1,2,3,4)的能量(KJ)相对大小如图所示。
①c点对应的微粒是
②b→a+c反应的离子方程式为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐3】M是第四周期元素,最外层只有1个电子,次外层的所有原子轨道均充满电子。元素Y的负一价离子的最外层电子数与次外层的相同。回答下列问题:
(1)写出M原子的外围电子排布式_____ 。
(2)画出Y的负一价离子的电子式_____ ,元素Y的含氧酸中,酸性最强的是_____ (写化学式)。
(3)Y的同周期元素中,第一电离能最大的是______ (写元素符号);同周期主族元素从左到右,原子半径逐渐______ ,原因是______ 。
(4)M与Y形成的一种化合物MY,该化合物难溶于水但易溶于氨水,此化合物的氨水溶液遇到空气则被氧化为深蓝色,深蓝色溶液中阳离子的化学式为______ 。
(1)写出M原子的外围电子排布式
(2)画出Y的负一价离子的电子式
(3)Y的同周期元素中,第一电离能最大的是
(4)M与Y形成的一种化合物MY,该化合物难溶于水但易溶于氨水,此化合物的氨水溶液遇到空气则被氧化为深蓝色,深蓝色溶液中阳离子的化学式为
您最近一年使用:0次



