锗(Ge)是典型的半导体元素,在电子、材料等领域应用广泛。回答下列问题:
(1)基态Ge原子的电子排布式为_______ ,有_______ 个未成对电子。
(2)比较下列锗卤化物的熔点和沸点,分析其变化规律及原因:_______ 。
(3)Ge单晶具有金刚石型结构,其中Ge原子的杂化方式为_______ ,微粒之间存在的作用力是_______ 。
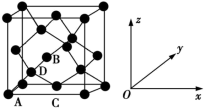
(4)原子坐标参数,表示晶胞内部各原子的相对位置。如图为Ge单晶的晶胞,其中原子坐标参数A为(0,0,0);B为( ,0,
,0, );C为(
);C为( ,
, ,0);则D原子的坐标参数为
,0);则D原子的坐标参数为_______ 。
(1)基态Ge原子的电子排布式为
(2)比较下列锗卤化物的熔点和沸点,分析其变化规律及原因:
| GeCl4 | GeBr4 | GeI4 | |
| 熔点/℃ | -49.5 | 26 | 146 |
| 沸点/℃ | 83.1 | 186 | 约400 |
(4)原子坐标参数,表示晶胞内部各原子的相对位置。如图为Ge单晶的晶胞,其中原子坐标参数A为(0,0,0);B为(
 ,0,
,0, );C为(
);C为( ,
, ,0);则D原子的坐标参数为
,0);则D原子的坐标参数为
更新时间:2022-12-20 16:38:35
|
相似题推荐
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐1】周期表中前20种元素X、Y、Z、W原子序数依次增大,它们的结构性质等信息如下表所述:
请根据信息回答有关问题:
(1)写出对应元素的名称:X:___ Y:___ Z:___ W:___ 。
(2)元素X的原子核外共有___ 种不同运动状态,其基态原子中最高能量能级轮廓图形状___ 。
(3)Y的价层电子排布图___ ,其电子云在空间有___ 种方向。
(4)化合物WZ的电子式为___ ,其焰色反应呈紫色,其原因是___ 。
| 元素 | 结构性质等信息 |
| X | 基态原子有三个能级,每个能级上的电子数都相等 |
| Y | 该元素原子外围电子排布式为nsnnpn+1 |
| Z | 常温常压下,该元素构成的单质是一种有毒的黄绿色气体 |
| W | 前四周期主族元素中原子半径最大的元素,且该元素的某种合金可做原子反应堆导热剂 |
(1)写出对应元素的名称:X:
(2)元素X的原子核外共有
(3)Y的价层电子排布图
(4)化合物WZ的电子式为
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐2】回答下列问题:
(1)某种金属互化物具有自范性,原子在三维空间呈周期性有序排列,该金属互化物属于______ (填“晶体”或“非晶体”),可通过______ 方法鉴别。
(2) 基态核外电子排布式为
基态核外电子排布式为______
(3)苯胺(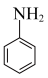 )与甲苯(
)与甲苯(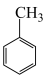 )的相对分子质量相近,但苯胺的沸点高于甲苯,其原因是
)的相对分子质量相近,但苯胺的沸点高于甲苯,其原因是______ 。
(4) 中心原子轨道的杂化类型为
中心原子轨道的杂化类型为______ 。
(5)某含铬化合物立方晶胞如图所示。与钙原子最近且等距离的氧原子有______ 个;钙和氧的最近距离为 ,NA为阿伏加德罗常数值,则该晶体密度为
,NA为阿伏加德罗常数值,则该晶体密度为______  (用含
(用含 、
、 的代数式表示)。
的代数式表示)。
(1)某种金属互化物具有自范性,原子在三维空间呈周期性有序排列,该金属互化物属于
(2)
 基态核外电子排布式为
基态核外电子排布式为(3)苯胺(
 )与甲苯(
)与甲苯( )的相对分子质量相近,但苯胺的沸点高于甲苯,其原因是
)的相对分子质量相近,但苯胺的沸点高于甲苯,其原因是(4)
 中心原子轨道的杂化类型为
中心原子轨道的杂化类型为(5)某含铬化合物立方晶胞如图所示。与钙原子最近且等距离的氧原子有
 ,NA为阿伏加德罗常数值,则该晶体密度为
,NA为阿伏加德罗常数值,则该晶体密度为 (用含
(用含 、
、 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
【推荐3】我国科学家利用碲化锆(ZrTe2)和砷化镉(Cd3As2)为材料成功地验证了三维两字霍尔效应,并发现了金属—绝缘体的转换。回答下列问题:
(1)基态砷原子的价电子排布式为____ 。
(2)As与Ge、Se同周期且相邻,它们的第一电离能由大到小的顺序为____ (用元素符号表示)。
(3)与砷(As)同主族的N、P两种元素的氢化物水溶液的碱性:NH3>PH3原因是____ 。
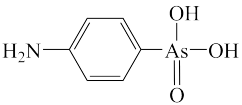
(4)含砷有机物“对氨基苯砷酸”的结构简式如图,砷原子轨道杂化类型为____ 。
(5)Cd2+与NH3形成的配离子[Cd(NH3)4]2+中,2个NH3被2个Cl-替代只得到1种结构,[Cd(NH3)4]2+的立体构型是____ ,1mol[Cd(NH3)4]2+含____ molσ键。
(1)基态砷原子的价电子排布式为
(2)As与Ge、Se同周期且相邻,它们的第一电离能由大到小的顺序为
(3)与砷(As)同主族的N、P两种元素的氢化物水溶液的碱性:NH3>PH3原因是
(4)含砷有机物“对氨基苯砷酸”的结构简式如图,砷原子轨道杂化类型为

(5)Cd2+与NH3形成的配离子[Cd(NH3)4]2+中,2个NH3被2个Cl-替代只得到1种结构,[Cd(NH3)4]2+的立体构型是
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
【推荐1】由P、S、Cl、Ni等元素组成的新型材料有着广泛的用途,试回答下列问题:
(1)基态Cl原子的核外电子排布式为___________ 。P、S、Cl的第一电离能由大到小的顺序为___________
(2) 分子中中心原子的杂化轨道类型是
分子中中心原子的杂化轨道类型是___________ ,该分子的空间结构为___________ 。
(3)已知NiO的晶体结构如图1所示,若NiO晶胞中A的坐标为(0,0,0),B的坐标为(1,1,0),则C的坐标为___________ 。

(4)一定温度下,NiO晶体可以自发地分散并形成“单分子层”,可以认为 作密置单层排列,
作密置单层排列, 填充其中(如图2所示),已知
填充其中(如图2所示),已知 的半径为am,则每平方米分散的该晶体的质量为
的半径为am,则每平方米分散的该晶体的质量为___________ g(用 表示阿伏加德罗常数的值)。
表示阿伏加德罗常数的值)。
(1)基态Cl原子的核外电子排布式为
(2)
 分子中中心原子的杂化轨道类型是
分子中中心原子的杂化轨道类型是(3)已知NiO的晶体结构如图1所示,若NiO晶胞中A的坐标为(0,0,0),B的坐标为(1,1,0),则C的坐标为

(4)一定温度下,NiO晶体可以自发地分散并形成“单分子层”,可以认为
 作密置单层排列,
作密置单层排列, 填充其中(如图2所示),已知
填充其中(如图2所示),已知 的半径为am,则每平方米分散的该晶体的质量为
的半径为am,则每平方米分散的该晶体的质量为 表示阿伏加德罗常数的值)。
表示阿伏加德罗常数的值)。
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐2】不锈钢是由铁、铬、碳及众多不同元素所组成的合金。目前铬被广泛应用于冶金、化工、铸铁、耐火等领域。
(1)Cr基态原子价层电子的轨道表示式为______ 。其核外有______ 种能量状态的电子。
(2)金属铬的第二电离能(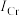 )和锰的第二电离能(
)和锰的第二电离能(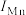 )分别为11590.6 kJ⋅mol
)分别为11590.6 kJ⋅mol 、1509.0 kJ⋅mol
、1509.0 kJ⋅mol ,
,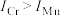 的原因是
的原因是____________ 。
(3)过氧化铬( )中Cr的化合价为
)中Cr的化合价为 ,则分子中σ键、π键的数目之比为
,则分子中σ键、π键的数目之比为______ 。
(4) 的熔点(83℃)比
的熔点(83℃)比 的熔点(1100℃)低得多,这是因为
的熔点(1100℃)低得多,这是因为____________ 。
(5)Cr的一种配合物结构如图所示,该配合物中碳原子的杂化方式是______ ,阳离子中Cr的配位数为______ ,阴离子 的空间构型为
的空间构型为______ 。
(1)Cr基态原子价层电子的轨道表示式为
(2)金属铬的第二电离能(
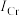 )和锰的第二电离能(
)和锰的第二电离能(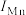 )分别为11590.6 kJ⋅mol
)分别为11590.6 kJ⋅mol 、1509.0 kJ⋅mol
、1509.0 kJ⋅mol ,
,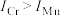 的原因是
的原因是(3)过氧化铬(
 )中Cr的化合价为
)中Cr的化合价为 ,则分子中σ键、π键的数目之比为
,则分子中σ键、π键的数目之比为(4)
 的熔点(83℃)比
的熔点(83℃)比 的熔点(1100℃)低得多,这是因为
的熔点(1100℃)低得多,这是因为(5)Cr的一种配合物结构如图所示,该配合物中碳原子的杂化方式是
 的空间构型为
的空间构型为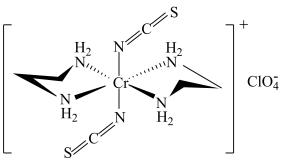
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐3】硫及其化合物有许多用途,相关物质的物理常数如表所示:
回答下列问题:
(1)Fe在元素周期表的位置为__ ,基态S原子电子占据最高能级的电子云轮廓图为__ 形。
(2)根据价层电子对互斥理论,H2S、SO2、SO3的气态分子中,中心原子价层电子对数不同于其他分子的是__ 。
(3)图a为S8的结构,其熔点和沸点要比二氧化硫的熔点和沸点高很多,主要原因为___ 。
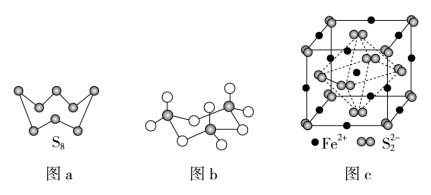
(4)气态三氧化硫以单分子形式存在,其分子的立体构型为__ 形,其中共价键的类型有__ 种;固体三氧化硫中存在如图b所示的三聚分子,该分子中S原子的杂化轨道类型为__ 。
(5)FeS2晶体的晶胞如图c所示。晶胞边长为apm、FeS2的密度为ρg·cm-3,阿伏加 德罗常数的值为NA,则FeS2的摩尔质量M的计算表达式为__ g·mol-1;晶胞中Fe2+位于S22-所形成的正八面体的体心,该正八面体的边长为___ pm。
| H2S | S8 | FeS2 | SO2 | SO3 | H2SO4 | |
| 熔点/℃ | -85.5 | 115.2 | >600(分解) | -75.5 | 16.8 | 10.3 |
| 沸点/℃ | -60.3 | 444.6 | -10.0 | 45.0 | 337.0 |
回答下列问题:
(1)Fe在元素周期表的位置为
(2)根据价层电子对互斥理论,H2S、SO2、SO3的气态分子中,中心原子价层电子对数不同于其他分子的是
(3)图a为S8的结构,其熔点和沸点要比二氧化硫的熔点和沸点高很多,主要原因为

(4)气态三氧化硫以单分子形式存在,其分子的立体构型为
(5)FeS2晶体的晶胞如图c所示。晶胞边长为apm、FeS2的密度为ρg·cm-3,阿伏加 德罗常数的值为NA,则FeS2的摩尔质量M的计算表达式为
您最近一年使用:0次
【推荐1】金属和非金属分界线附近的元素(如 、
、 、
、 ),可用于制造半导体材料,是科学研究的热点。试回答下列问题:
),可用于制造半导体材料,是科学研究的热点。试回答下列问题:
(1)锗( )是一种重要的半导体材料,写出基态
)是一种重要的半导体材料,写出基态 原子的价层电子排布式,说明价电子在其最高能级上的分布遵循的原则。
原子的价层电子排布式,说明价电子在其最高能级上的分布遵循的原则。________
(2) 是一种非晶态半导体,也称玻璃半导体。区分晶体与非晶体的最可靠的科学方法是
是一种非晶态半导体,也称玻璃半导体。区分晶体与非晶体的最可靠的科学方法是________ ?
(3) 等是人工合成的新型半导体材料,其晶体结构与金刚石相似,如图所示。每个
等是人工合成的新型半导体材料,其晶体结构与金刚石相似,如图所示。每个 原子周围有
原子周围有________ 个距离最近的 原子?每个晶胞中有
原子?每个晶胞中有________ 个 原子?
原子?

 、
、 、
、 ),可用于制造半导体材料,是科学研究的热点。试回答下列问题:
),可用于制造半导体材料,是科学研究的热点。试回答下列问题:(1)锗(
 )是一种重要的半导体材料,写出基态
)是一种重要的半导体材料,写出基态 原子的价层电子排布式,说明价电子在其最高能级上的分布遵循的原则。
原子的价层电子排布式,说明价电子在其最高能级上的分布遵循的原则。(2)
 是一种非晶态半导体,也称玻璃半导体。区分晶体与非晶体的最可靠的科学方法是
是一种非晶态半导体,也称玻璃半导体。区分晶体与非晶体的最可靠的科学方法是(3)
 等是人工合成的新型半导体材料,其晶体结构与金刚石相似,如图所示。每个
等是人工合成的新型半导体材料,其晶体结构与金刚石相似,如图所示。每个 原子周围有
原子周围有 原子?每个晶胞中有
原子?每个晶胞中有 原子?
原子?
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐2】下表为长式周期表的一部分,其中的编号代表对应的元素。
(1)写出上表中元素⑾原子的外围电子排布式___________ 。元素⑿正三价离子的核外电子排布式_________________ 元素⑥负一价离子的结构示意图__________ 。
(2)元素⑦与⑥形成的化合物的电子式为:___________ ,其形成的化合物的晶体类型是:____________
(3)元素④、⑤的第一电离能较大的是:___________ (用元素符号表示)。元素⑤、⑥电负性较大的是:______________ (用元素符号表示)。
(4)④、⑤、⑥三种元素形成的离子,离子半径最大的是:___________ 。(用离子符号表示)
(5)⑦、⑧与水反应最剧烈的物质是___________ 。(填化学式)
(6)元素(11)在一定条件下形成的晶体的基本结构单元如下图1和图2所示,则在图1和图2的结构中与该元素一个原子等距离且最近的原子数之比为:___________ 。

| ① | |||||||||||||||||
| ② | ③ | ④ | ⑤ | ⑥ | |||||||||||||
| ⑦ | ⑧ | ⑨ | ⑩ | ||||||||||||||
| ⑾ | ⑿ | ⒀ |
(2)元素⑦与⑥形成的化合物的电子式为:
(3)元素④、⑤的第一电离能较大的是:
(4)④、⑤、⑥三种元素形成的离子,离子半径最大的是:
(5)⑦、⑧与水反应最剧烈的物质是
(6)元素(11)在一定条件下形成的晶体的基本结构单元如下图1和图2所示,则在图1和图2的结构中与该元素一个原子等距离且最近的原子数之比为:

您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐3】(乙酸锰可用于制造钠离子电池的负极材料。可用如下反应制得乙酸锰:4Mn(NO3)2•6H2O+26(CH3CO)2O=4(CH3COO)3Mn+8HNO2+3O2↑+40CH3COOH
(1)Mn3+基态核外电子排布式为___ 。
(2)NO3-中氮原子轨道的杂化类型是___ 。
(3)与HNO2互为等电子体的一种阴离子的化学式为___ 。
(4)配合物[Mn(CH3OH)6]2+中配位原子是___ 。
(5)CH3COOH能与H2O任意比混溶的原因,除它们都是极性分子外还有___ 。
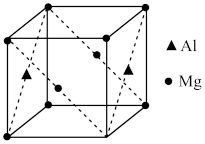
(6)镁铝合金经过高温淬火获得一种储钠材料,其晶胞为立方结构(如图所示),图中原子位于顶点或面心。该晶体中每个铝原子周围距离最近的镁原子数目为___ 。
(1)Mn3+基态核外电子排布式为
(2)NO3-中氮原子轨道的杂化类型是
(3)与HNO2互为等电子体的一种阴离子的化学式为
(4)配合物[Mn(CH3OH)6]2+中配位原子是
(5)CH3COOH能与H2O任意比混溶的原因,除它们都是极性分子外还有
(6)镁铝合金经过高温淬火获得一种储钠材料,其晶胞为立方结构(如图所示),图中原子位于顶点或面心。该晶体中每个铝原子周围距离最近的镁原子数目为

您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐1】氮化钛广泛用于耐高温、耐磨损及航空航天等领域。一种氮化钛的制备反应为:6TiCl4+8NH3 = 6TiN+24HCl+N2 ,回答下列问题:
(1)钛在元素周期表中的位置为_____________ ,基态Ti原子价层电子的轨道表达式为________ 。
(2)氮可与其他元素形成正离子,如NH4Cl中的NH4+,N2O5中的NO2+。组成这两种正离子的元素中第一电离能由小到大的顺序为____________ ;NH4+的空间构型为___________ ;NO2+中氮原子的杂化形式为_______ ,其中σ键与π键的数目比为_________ 。
(3)四氯化钛晶体的熔点为-23 ℃,沸点为136 ℃,则TiCl4晶体的类型为___________ ,该晶体中微粒之间的作用力为___________ 。
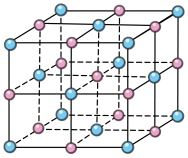
(4)一种TiN金黄色晶体晶胞结构与NaCl相同(如图),该晶胞中N原子数目为_______ ;该氮化钛的密度为5.4 g/cm3,则其晶胞参数a=___________ pm(用NA表示阿伏加德常数的数值,只列算式)。
(1)钛在元素周期表中的位置为
(2)氮可与其他元素形成正离子,如NH4Cl中的NH4+,N2O5中的NO2+。组成这两种正离子的元素中第一电离能由小到大的顺序为
(3)四氯化钛晶体的熔点为-23 ℃,沸点为136 ℃,则TiCl4晶体的类型为
(4)一种TiN金黄色晶体晶胞结构与NaCl相同(如图),该晶胞中N原子数目为

您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐2】镓(Ga)是一种重要的金属,镓的化合物广泛应用于半导体、太阳能、液态合金、医疗化工等诸多领域,被称为电子工业的“脊梁”。
(1)基态Ga原子的价层电子的轨道表示式是___________________ 。
(2) 在270°C左右以二聚体
在270°C左右以二聚体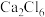 存在,结构式如图。
存在,结构式如图。
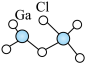
① 可以形成二聚体的原因是
可以形成二聚体的原因是__________________________ 。
② 和
和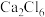 中Ga原子采用的杂化方式分别是
中Ga原子采用的杂化方式分别是_________________ 。
③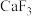 的熔点为1000℃,
的熔点为1000℃, 的熔点为77.9℃,
的熔点为77.9℃,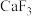 的熔点远远高于
的熔点远远高于 的熔点,从结构角度解释原因
的熔点,从结构角度解释原因_____ 。
(3) 可与
可与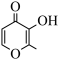 (甲基麦芽酚)形成配合物Ga(
(甲基麦芽酚)形成配合物Ga( )3。甲基麦芽酚的分子式是
)3。甲基麦芽酚的分子式是______________ ,甲基麦芽酚中,与 形成配位键的原子是
形成配位键的原子是________ 。
(1)基态Ga原子的价层电子的轨道表示式是
(2)
 在270°C左右以二聚体
在270°C左右以二聚体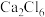 存在,结构式如图。
存在,结构式如图。
①
 可以形成二聚体的原因是
可以形成二聚体的原因是②
 和
和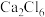 中Ga原子采用的杂化方式分别是
中Ga原子采用的杂化方式分别是③
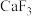 的熔点为1000℃,
的熔点为1000℃, 的熔点为77.9℃,
的熔点为77.9℃,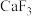 的熔点远远高于
的熔点远远高于 的熔点,从结构角度解释原因
的熔点,从结构角度解释原因(3)
 可与
可与 (甲基麦芽酚)形成配合物Ga(
(甲基麦芽酚)形成配合物Ga( )3。甲基麦芽酚的分子式是
)3。甲基麦芽酚的分子式是 形成配位键的原子是
形成配位键的原子是
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐3】回答下列问题
(1)Na原子核外共有______ 种不同运动状态的电子,有_____ 种不同能量的电子。
(2)相同压强下,部分元素氟化物的熔点见下表:
试解释上表中氟化物熔点差异的原因:_______ 。
(3)SiF4分子的空间构型为_______ 。
(4)热稳定性:NH3______PH3(填“>”“<”)。沸点:Br2>Cl2,试分析原因__________ 。
(5)试配平该反应的化学方程式,并用短线标出电子转移方向及总数__________ 。
NaIO3+ NaHSO3→ NaHSO4+ Na2SO4+ I2+ H2O
(1)Na原子核外共有
(2)相同压强下,部分元素氟化物的熔点见下表:
| 氟化物 | NaF | MgF2 | SiF4 |
| 熔点/℃ | 1266 | 1534 | 183 |
(3)SiF4分子的空间构型为
(4)热稳定性:NH3______PH3(填“>”“<”)。沸点:Br2>Cl2,试分析原因
(5)试配平该反应的化学方程式,并用短线标出电子转移方向及总数
NaIO3+ NaHSO3→ NaHSO4+ Na2SO4+ I2+ H2O
您最近一年使用:0次



