周期表中前20种元素X、Y、Z、W原子序数依次增大,它们的结构性质等信息如下表所述:
请根据信息回答有关问题:
(1)写出对应元素的名称:X:___ Y:___ Z:___ W:___ 。
(2)元素X的原子核外共有___ 种不同运动状态,其基态原子中最高能量能级轮廓图形状___ 。
(3)Y的价层电子排布图___ ,其电子云在空间有___ 种方向。
(4)化合物WZ的电子式为___ ,其焰色反应呈紫色,其原因是___ 。
| 元素 | 结构性质等信息 |
| X | 基态原子有三个能级,每个能级上的电子数都相等 |
| Y | 该元素原子外围电子排布式为nsnnpn+1 |
| Z | 常温常压下,该元素构成的单质是一种有毒的黄绿色气体 |
| W | 前四周期主族元素中原子半径最大的元素,且该元素的某种合金可做原子反应堆导热剂 |
(1)写出对应元素的名称:X:
(2)元素X的原子核外共有
(3)Y的价层电子排布图
(4)化合物WZ的电子式为
20-21高二·四川乐山·期中 查看更多[4]
(已下线)1.1 原子结构(素养提优B练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修2)(已下线)1.1 原子结构(C级检测练)-2020-2021学年高二化学章节分层检测ABC(人教版2019选择性必修2)(已下线)第1章 原子结构与元素性质(基础过关)-2020-2021学年高二化学单元测试定心卷(鲁科版2019选择性必修2)四川省乐山十校2020-2021学年高二上学期半期联考化学试题
更新时间:2020-11-22 16:35:40
|
相似题推荐
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐1】A、B、C、D、 E、F代表6种元素。请填空:
(1)A元素基态原子的最外层有3个未成对电子,次外层有2个电子,其元素符号为___________ 。
(2)B元素的负一价离子和C元素的正一价离子的电子层结构都与氩相同,B的元素符号为___________ ,C的元素符号为___________ 。
(3)D元素的正三价离子的3d能级为半充满,D的元素符号为___________
(4)E元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,E的元素符号为___________
(5)F元素的原子最外层电子排布式为nsnnpn+2,则n=___________ ;原子中能量最高的是___________ 电子。
(6)下列Li原子电子排布图表示的状态中,能量最低和最高的分别为___________ ,___________ (填标号)
A.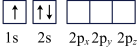 B.
B.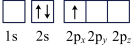 C.
C.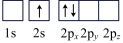 D.
D.
(7)Li+与H-具有相同的电子构型,r(Li+)小于r(H-),原因是___________ ,某原子的电子排布式为 [Ne]3s23p1,则该原子的元素符号为___________ ,最高正价为___________ ,该原子位于元素周期表第___________ 周期第___________ 族,位于元素周期表___________ 区。
(1)A元素基态原子的最外层有3个未成对电子,次外层有2个电子,其元素符号为
(2)B元素的负一价离子和C元素的正一价离子的电子层结构都与氩相同,B的元素符号为
(3)D元素的正三价离子的3d能级为半充满,D的元素符号为
(4)E元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,E的元素符号为
(5)F元素的原子最外层电子排布式为nsnnpn+2,则n=
(6)下列Li原子电子排布图表示的状态中,能量最低和最高的分别为
A.
 B.
B. C.
C. D.
D.
(7)Li+与H-具有相同的电子构型,r(Li+)小于r(H-),原因是
您最近半年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐1】现有四种元素,其中A、B、C为短周期主族元素,D为第四周期元素,它们的原子序数依次增大。请根据下列相关信息,回答问题。
(1)已知BA5为离子化合物,写出其电子式:_____ 。
(2)B基态原子中能量最高的电子,其电子云在空间有______ 个方向,原子轨道呈______ 形。
(3)某同学根据上述信息,推断C基态原子的核外电子排布图为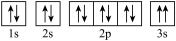 。该同学所画的电子排布图违背了
。该同学所画的电子排布图违背了____ 。
(4)D位于_______ 族_______ 区,价电子排布式为_______ 。
元素 | 相关信息 |
A | 元素的核外电子数和电子层数相等,也是宇宙中最丰富的元素 |
B | 元素原子的核外p电子数比s电子数少1 |
C | 原子的第一至第四电离能分别是I1=738 kJ·mol-1;I2=1 451 kJ·mol-1;I3=7 733 kJ·mol-1;I4=10 540 kJ·mol-1 |
D | 在周期表的第七列 |
(2)B基态原子中能量最高的电子,其电子云在空间有
(3)某同学根据上述信息,推断C基态原子的核外电子排布图为
 。该同学所画的电子排布图违背了
。该同学所画的电子排布图违背了(4)D位于
您最近半年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐2】在元素周期表的一百多种化学元素中,非金属元素仅有24种,但在社会生活中占有着重要的位置。
(1)根据元素周期表的分区,非金属元素分布在元素周期表的__________ 区。
(2)原子中运动的电子有两种相反的自旋状态,若一种自旋状态用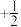 表示,与之相反的用
表示,与之相反的用 表示,称为电子的自旋磁量子数。对于基态的磷原子,其核外电子占据的最高能层符号为
表示,称为电子的自旋磁量子数。对于基态的磷原子,其核外电子占据的最高能层符号为__________ ,自旋磁量子数的代数和为__________ 。
(3)元素的基态气态原子得到一个电子形成气态负一价离子时所放出的能量称作第一电子亲和能( )。第二周期部分元素的
)。第二周期部分元素的 变化趋势如图所示。试分析碳元素的
变化趋势如图所示。试分析碳元素的 大于氮元素的
大于氮元素的 的原因
的原因__________ 。

(4)写出一种与 互为等电子体的一种分子的化学式:
互为等电子体的一种分子的化学式:__________ 。
(5)乙醇( )能与水以任意比例互溶,但与其结构相似的乙硫醇(
)能与水以任意比例互溶,但与其结构相似的乙硫醇(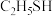 )微溶于水,原因是
)微溶于水,原因是__________ 。
(6)分子中的大 键可用符号
键可用符号 表示,其中m代表参与形成大
表示,其中m代表参与形成大 键的原子数,n代表参与形成大
键的原子数,n代表参与形成大 键的电子数,则与苯分子具有相似结构的吡啶(
键的电子数,则与苯分子具有相似结构的吡啶(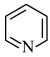 )中的大
)中的大 键应表示为
键应表示为__________ 。
(7)由两种不同的卤素组成的化合物叫卤素互化物(如BrCl等),其性质与卤素单质相似。试写出BrCl与水发生反应的化学方程式:__________ 。
(1)根据元素周期表的分区,非金属元素分布在元素周期表的
(2)原子中运动的电子有两种相反的自旋状态,若一种自旋状态用
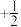 表示,与之相反的用
表示,与之相反的用 表示,称为电子的自旋磁量子数。对于基态的磷原子,其核外电子占据的最高能层符号为
表示,称为电子的自旋磁量子数。对于基态的磷原子,其核外电子占据的最高能层符号为(3)元素的基态气态原子得到一个电子形成气态负一价离子时所放出的能量称作第一电子亲和能(
 )。第二周期部分元素的
)。第二周期部分元素的 变化趋势如图所示。试分析碳元素的
变化趋势如图所示。试分析碳元素的 大于氮元素的
大于氮元素的 的原因
的原因
(4)写出一种与
 互为等电子体的一种分子的化学式:
互为等电子体的一种分子的化学式:(5)乙醇(
 )能与水以任意比例互溶,但与其结构相似的乙硫醇(
)能与水以任意比例互溶,但与其结构相似的乙硫醇(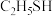 )微溶于水,原因是
)微溶于水,原因是(6)分子中的大
 键可用符号
键可用符号 表示,其中m代表参与形成大
表示,其中m代表参与形成大 键的原子数,n代表参与形成大
键的原子数,n代表参与形成大 键的电子数,则与苯分子具有相似结构的吡啶(
键的电子数,则与苯分子具有相似结构的吡啶( )中的大
)中的大 键应表示为
键应表示为(7)由两种不同的卤素组成的化合物叫卤素互化物(如BrCl等),其性质与卤素单质相似。试写出BrCl与水发生反应的化学方程式:
您最近半年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐1】元素周期表是化学中最重要的基本工具之一、它可以帮助化学家更好地研究元素,在科学研究和工业应用中有广泛应用。近年来我国科学家发现了一系列意义重大的铁系超导材料,其中一类为Fe—Sm—As—F—O组成的化合物。
(1)比较离子半径:F-___________ O2-(填“大于”“等于”或“小于”)。
(2)Sm的价层电子排布式为4f66s2,Sm3+的价层电子排布式为___________ 。
(3)元素As与P同族,请举一事实说明非金属性P元素比As元素强___________ 。
(4)已知H3PO4为三元酸,其结构式为: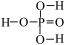 。次磷酸(H3PO2)中P的成键情况与H3PO4中的相同,则H3PO2的结构式是
。次磷酸(H3PO2)中P的成键情况与H3PO4中的相同,则H3PO2的结构式是___________ 。若将足量的KOH与次磷酸(H3PO2)充分反应,则化学方程式为___________ 。
(5)已知KH2PO4溶液呈酸性,可能的原因是___________ 。
(1)比较离子半径:F-
(2)Sm的价层电子排布式为4f66s2,Sm3+的价层电子排布式为
(3)元素As与P同族,请举一事实说明非金属性P元素比As元素强
(4)已知H3PO4为三元酸,其结构式为:
 。次磷酸(H3PO2)中P的成键情况与H3PO4中的相同,则H3PO2的结构式是
。次磷酸(H3PO2)中P的成键情况与H3PO4中的相同,则H3PO2的结构式是(5)已知KH2PO4溶液呈酸性,可能的原因是
您最近半年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐2】过渡金属元素铬(Cr)是不锈钢的重要成分,在工农业生产和国防建设中有着广泛应用。回答下列问题:
(1)Cr 是第___________ 周期第___________ 族元素。
(2)基态 Cr 原子的核外电子有___________ 种空间运动状态,有___________ 个未成对电子。
(3)Cr3+能形成多种配位化合物。[Cr(NH3)3(H2O)2Cl]2+中,中心离子的配位数为___________ 。
(4)[Cr(NH3)3(H2O)2Cl]2+的配体分子 NH3 中 N 的杂化轨道类型是___________ ,H2O 的键角小于 NH3,原因是___________ 。
(5)在金属材料中添加 AlCr2 颗粒,可以增强材料的耐腐蚀性、硬度和机械性能。AlCr2 具有体心四方结构,如下图所示,处于顶角位置的是___________ 原子。若 NA 表示阿伏加德罗常数的值,则该晶体的密度为___________ g∙cm−3(用含 a、c 和 NA 的代数式表示)。晶胞中长、宽为a nm,高为c nm。
(1)Cr 是第
(2)基态 Cr 原子的核外电子有
(3)Cr3+能形成多种配位化合物。[Cr(NH3)3(H2O)2Cl]2+中,中心离子的配位数为
(4)[Cr(NH3)3(H2O)2Cl]2+的配体分子 NH3 中 N 的杂化轨道类型是
(5)在金属材料中添加 AlCr2 颗粒,可以增强材料的耐腐蚀性、硬度和机械性能。AlCr2 具有体心四方结构,如下图所示,处于顶角位置的是

您最近半年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐1】请按要求填空:
(1)下列轨道表示式能表示基态氮原子的是___________(填标号)。
(2)HCHO的中心原子的价层电子对数为___________ ;其中基态氧原子的核外电子的空间运动状态有___________ 种。
(3)已知邻羟基苯甲酸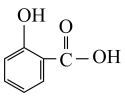 与对羟基苯甲酸
与对羟基苯甲酸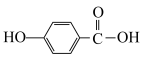 的沸点相差较大,根据结构分析,前者的沸点
的沸点相差较大,根据结构分析,前者的沸点___________ (填高于”或“低于”)后者,并解释原因:___________ 。
(4)普鲁士蓝{KFe[Fe(CN)6]}中不同价态铁元素的简单微粒较稳定的离子的简化核外电子排布式为___________ ,该离子更稳定的原因是___________ 。
(1)下列轨道表示式能表示基态氮原子的是___________(填标号)。
A.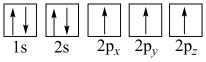 | B. |
C. | D. |
(2)HCHO的中心原子的价层电子对数为
(3)已知邻羟基苯甲酸
 与对羟基苯甲酸
与对羟基苯甲酸 的沸点相差较大,根据结构分析,前者的沸点
的沸点相差较大,根据结构分析,前者的沸点(4)普鲁士蓝{KFe[Fe(CN)6]}中不同价态铁元素的简单微粒较稳定的离子的简化核外电子排布式为
您最近半年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐2】今有A、B、C、D四种元素,已知A元素是地壳中含量最多的元素;B元素为金属元素,它的原子核外K、L层上电子数之和等于M、N层电子数之和;C元素是第三周期第一电离能最小的元素;D元素在第三周期中电负性最大.
(1)试推断A、B、C、D四种元素的符号:A________ 、B________ 、C________ 、D________ .
(2)写出A元素原子的核外电子排布式:____________ ;写出B元素原子核外电子排布的价电子排布式:__________ ;用电子排布图表示C原子的核外电子排布情况:_______________ .
(1)试推断A、B、C、D四种元素的符号:A
(2)写出A元素原子的核外电子排布式:
您最近半年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐3】有A、B、C、D四种元素,其原子序数依次增大,且质子数均小于18。A元素原子的最外层只有1个电子,该元素阳离子与N3-核外电子排布相同;B元素原子核外各轨道上均无成单电子;C元素原子的价电子排布为ns2np2;D-的核外电子构型与Ar相同。
(1)写出A、C、D的元素符号:A________ ,C________ ,D________ 。
(2)写出B元素电子的电子排布式________ ;D元素电子的电子排布图______________ 。
(1)写出A、C、D的元素符号:A
(2)写出B元素电子的电子排布式
您最近半年使用:0次



