今有A、B、C、D四种元素,已知A元素是地壳中含量最多的元素;B元素为金属元素,它的原子核外K、L层上电子数之和等于M、N层电子数之和;C元素是第三周期第一电离能最小的元素;D元素在第三周期中电负性最大.
(1)试推断A、B、C、D四种元素的符号:A________ 、B________ 、C________ 、D________ .
(2)写出A元素原子的核外电子排布式:____________ ;写出B元素原子核外电子排布的价电子排布式:__________ ;用电子排布图表示C原子的核外电子排布情况:_______________ .
(1)试推断A、B、C、D四种元素的符号:A
(2)写出A元素原子的核外电子排布式:
19-20高二下·新疆伊犁·期中 查看更多[2]
新疆生产建设兵团第四师第一中学2019-2020学年高二下学期期中考试化学试题(已下线)1.1 原子结构(A级基础练)-2020-2021学年高二化学章节分层检测ABC(人教版2019选择性必修2)
更新时间:2020-11-17 11:27:31
|
相似题推荐
解答题-无机推断题
|
较易
(0.85)
名校
【推荐1】前四周期元素X、Y、Z、W核电荷数依次增大,核电荷数之和为58;Y原子的M层p轨道有3个未成对电子;Z与Y同周期,且在该周期中电负性最大;W原子的L层电子数与最外层电子数之比为4:1,其d轨道中的电子数与最外层电子数之比为5:2。
(1)写出Z元素在元素周期表中的位置:___________ 。
(2) 与X形成共价化合物A,Z与X形成共价化合物B,A与B还原性较强的是
与X形成共价化合物A,Z与X形成共价化合物B,A与B还原性较强的是___________  写分子式
写分子式 。
。
(3) 的最高价氧化物的水化物的化学式为
的最高价氧化物的水化物的化学式为___________ ;
(4) 单质
单质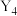 与
与 在一定条件下恰好完全反应生成
在一定条件下恰好完全反应生成 化合物C,一个C分子中所含有的σ键数目为
化合物C,一个C分子中所含有的σ键数目为___________ ;
(5)含W元素的最高化合价的含氧酸根离子是___________ ,该含氧酸根离子在分析化学中有重要作用,在酸性条件下该含氧酸根离子可将 氧化成
氧化成 ,请写出该反应的离子方程式
,请写出该反应的离子方程式___________ 。
(1)写出Z元素在元素周期表中的位置:
(2)
 与X形成共价化合物A,Z与X形成共价化合物B,A与B还原性较强的是
与X形成共价化合物A,Z与X形成共价化合物B,A与B还原性较强的是 写分子式
写分子式 。
。(3)
 的最高价氧化物的水化物的化学式为
的最高价氧化物的水化物的化学式为(4)
 单质
单质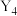 与
与 在一定条件下恰好完全反应生成
在一定条件下恰好完全反应生成 化合物C,一个C分子中所含有的σ键数目为
化合物C,一个C分子中所含有的σ键数目为(5)含W元素的最高化合价的含氧酸根离子是
 氧化成
氧化成 ,请写出该反应的离子方程式
,请写出该反应的离子方程式
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐2】W、X、Y、Z是短周期元素,其部分性质如表:
(1)X的简单氢化物的结构式_____ ,Y和W形成的化合物YW2的电子式_____ 。
(2)元素Z在周期表中的位置_____ 。
(3)比较X、Y最高价氧化物对应的水化物的酸性:_____ >_____ (填化学式)。
| W | 单质是淡黄色固体 |
| X | 在地壳中的含量居第二位 |
| Y | 原子最外层电子数是电子总数的 |
| Z | 第三周期简单离子半径最小 |
(2)元素Z在周期表中的位置
(3)比较X、Y最高价氧化物对应的水化物的酸性:
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
【推荐3】J、L、M、R、T 是原子序数依次增大的短周期主族元素,J、R 在周期表中的相对位置如表; J 原子最外层电子数是其内层电子数的 2 倍;L 的最简单气态氢化物甲的水溶液显碱性;M 是地壳中含量最多的金属元素。
(1)M 的离子结构示意图为_______ ;元素 T 在周期表中位于第________ 周期第_______ 族。
(2)J 元素是_________ (用元素符号表示);J 和氢组成的 10 电子化合物的化学式为_________ 。
(3)M 和 T 形成的化合物属于_______ (填“离子化合物”、或“共价化合物”),其中所有原 子都满足最外层 8 电子结构的分子是_______ (填化学式),电子式为_______ 。
(4)元素 M 形成的简单离子的水溶液与甲的水溶液反应的离子方程式_______ 。
J | ||||
R |
(2)J 元素是
(3)M 和 T 形成的化合物属于
(4)元素 M 形成的简单离子的水溶液与甲的水溶液反应的离子方程式
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐1】已知X、Y、Z、M、G、Q是六种短周期主族元素,原子序数依次增大。X、Z、Q的单质在常温下呈气态:Y的原子最外层电子数是其电子层数的2倍:X与M同主族;Z、G分别是地壳中含量最高的非金属元素和金属元素。
请回答下列问题:
(1)Z在元素周期表中的位置为__________ 。
(2)M、G的阳离子氧化性更强的是(写化学式)________ 。
(3)Z和Q的最低价氢化物沸点更高的是(写化学式)_________ 。
(4)上述元素的最高价氧化物对应的水化物酸性最强的是(写化学式)________ 。
(5) M2Z2的电子式为________ 。
(6)常温下,能与G的单质发生反应的是(填字母序号)________ 。
A. CuSO4溶液 B.浓硫酸 C. NaOH溶液 D.Na2CO3固体
请回答下列问题:
(1)Z在元素周期表中的位置为
(2)M、G的阳离子氧化性更强的是(写化学式)
(3)Z和Q的最低价氢化物沸点更高的是(写化学式)
(4)上述元素的最高价氧化物对应的水化物酸性最强的是(写化学式)
(5) M2Z2的电子式为
(6)常温下,能与G的单质发生反应的是(填字母序号)
A. CuSO4溶液 B.浓硫酸 C. NaOH溶液 D.Na2CO3固体
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐2】元素周期表是学习化学的重要工具,它隐含许多信息和规律。
(1)下表所列是五种短周期的原子半径及主要化合价(已知铍的原子半径为0.089nm)
(1)用元素代号标出它们在周期表中对应位置__________ (以下为周期表的一部分)

(2) 元素处于周期表中
元素处于周期表中______ 周期______ 族
(3)在元素周期表中______ 的分界处,可以找到制半导体材料的元素
(4)上述五种元素的最高价氧化物对应水化物酸性最强的是______ (填化学式)
(5)C、E形成化合物为______ (填化学式)
(1)下表所列是五种短周期的原子半径及主要化合价(已知铍的原子半径为0.089nm)
| 元素代号 | A | B | C | D | E |
| 原子半径/nm | 0.16 |  | 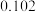 | 0.099 | 0.074 |
| 主要化合价 | +2 | +3 | +6,-2 | -1 | -2 |

(2)
 元素处于周期表中
元素处于周期表中(3)在元素周期表中
(4)上述五种元素的最高价氧化物对应水化物酸性最强的是
(5)C、E形成化合物为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐3】四种短周期元素A、B、C、D的性质或结构信息如下。
信息①:原子半径大小:A>B>C>D
信息②:四种元素之间形成的某三种分子的比例模型及部分性质:
请根据上述信息回答下列问题。
(1)甲、乙、丙中含有的共同元素是_______ (填名称)。
(2)B元素在周期表中的位置为_______________ 。
(3)上述元素的原子M层有一个未成对p电子的是_______ (填元素符号)。
(4)丙的电子式为__________ ,丙与SO2水溶液可发生氧化还原反应,生成两种强酸,化学反应方程式为__________________ 。
信息①:原子半径大小:A>B>C>D
信息②:四种元素之间形成的某三种分子的比例模型及部分性质:
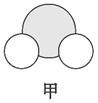 | 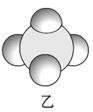 |  |
| 是地球上最常见的物质之一,常温为液态,是包括人类在内所有生命生存的重要资源,也是生物体最重要的组成部分 | 无色,无味且易燃,是21世纪的主要能源 | 弱酸,有强氧化性,可以用于消毒杀菌 |
请根据上述信息回答下列问题。
(1)甲、乙、丙中含有的共同元素是
(2)B元素在周期表中的位置为
(3)上述元素的原子M层有一个未成对p电子的是
(4)丙的电子式为
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
【推荐1】如图是元素周期表的一部分,根据元素在周期表中的位置,回答下列问题:
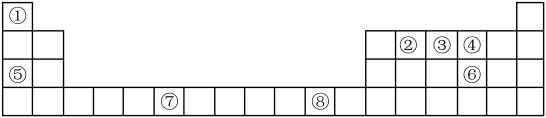
(1)⑧号元素在周期表中的位置是___________ ,其最高能层的电子占据的原子轨道电于云轮廓为___________ 形。
(2)④、⑤、⑥的简单离子的离子半径由小到大的顺序为___________ (用元素符号表示、下同)。
(3)元素①②③可形成原子个数比为1:1:1的共价化合物,分子中各原子最外层均达到8电子或2电子的稳定结构,试写出其电子式___________ ,该分子为___________ (填“极性分子”或“非极性分子”)。
(4)画出⑦的基态原子价层电子轨道表示式___________ 。
(5)④的简单氢化物比⑥的简单氢化物沸点更高,原因是___________ 。

(1)⑧号元素在周期表中的位置是
(2)④、⑤、⑥的简单离子的离子半径由小到大的顺序为
(3)元素①②③可形成原子个数比为1:1:1的共价化合物,分子中各原子最外层均达到8电子或2电子的稳定结构,试写出其电子式
(4)画出⑦的基态原子价层电子轨道表示式
(5)④的简单氢化物比⑥的简单氢化物沸点更高,原因是
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐2】钛(Ti)被誉为“21世纪的金属”。工业上将TiO2与焦炭混合,通入Cl2高温下制得TiCl4;再将TiCl4提纯后,在氩气保护下与镁高温反应制得Ti。其反应如下:
①TiO2+2Cl2+2C TiCl4+2CO
TiCl4+2CO
②TiCl4+2Mg Ti+2MgCl2
Ti+2MgCl2
回答下列问题:
(1)Ti元素原子的价电子排布式为_____________________ 。
(2)与CO互为等电子体的分子是___________ 。
(3)已知TiCl4在通常情况下是无色液体,熔点为–37℃,沸点为136℃;TiCl4在潮湿空气中易水解产生白雾,同时产生H2TiO3固体。
① TiCl4为______ 化合物(填“离子”或“共价”)。
② TiCl4分子为正四面体形,则Ti为________ 杂化。
③ TiCl4在潮湿空气中水解的化学方程式是_____________________________________ 。
④TiO2、Cl2和C反应制得的TiCl4最好的提纯方法是____________ (填操作名称)。
(4)配离子[TiCl(H2O)5]2+的中心离子化合价为____ ,中心离子配位数为____ 。
①TiO2+2Cl2+2C
 TiCl4+2CO
TiCl4+2CO ②TiCl4+2Mg
 Ti+2MgCl2
Ti+2MgCl2回答下列问题:
(1)Ti元素原子的价电子排布式为
(2)与CO互为等电子体的分子是
(3)已知TiCl4在通常情况下是无色液体,熔点为–37℃,沸点为136℃;TiCl4在潮湿空气中易水解产生白雾,同时产生H2TiO3固体。
① TiCl4为
② TiCl4分子为正四面体形,则Ti为
③ TiCl4在潮湿空气中水解的化学方程式是
④TiO2、Cl2和C反应制得的TiCl4最好的提纯方法是
(4)配离子[TiCl(H2O)5]2+的中心离子化合价为
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
【推荐3】磷及其化合物在工农业生产中具有重要用途。如图所示为提纯白磷样品(含惰性杂质)的工艺流程。回答下列问题:
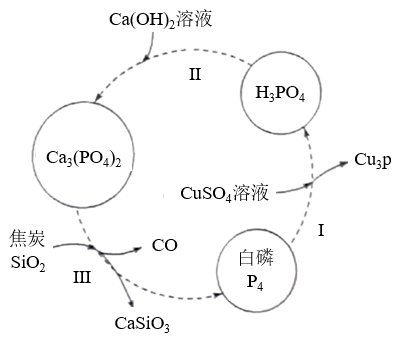
(1)过程III的化学方程式为________ 。
(2)基态Cu原子价层电子排布式为_______ ,在第四周期过渡金属中,基态原子未成对电子数最多的元素是________ (填元素符号)。非金属元素C、O、P、S的电负性由大到小的顺序为___________ 。
(3)元素铜与镍的第二电离能分别为ICu=1958kJ·mol-1、INi=1753kJ·mol-1,ICu>INi的原因是_____ 。
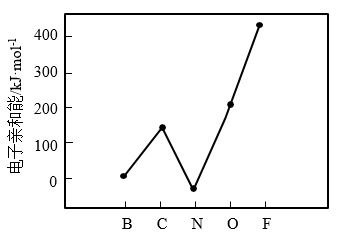
(4)元素的基态气态原子得到一个电子形成气态负一价离子时所放出的能量称作第一电子亲和能(E1)。第二周期部分元素的E1变化趋势如图所示,氮元素的E1呈现异常的原因是_____ 。

(1)过程III的化学方程式为
(2)基态Cu原子价层电子排布式为
(3)元素铜与镍的第二电离能分别为ICu=1958kJ·mol-1、INi=1753kJ·mol-1,ICu>INi的原因是
(4)元素的基态气态原子得到一个电子形成气态负一价离子时所放出的能量称作第一电子亲和能(E1)。第二周期部分元素的E1变化趋势如图所示,氮元素的E1呈现异常的原因是

您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐1】实验室用电石( )制乙炔时会产生
)制乙炔时会产生 和
和 杂质气体,可用
杂质气体,可用 溶液除去。
溶液除去。
(1) 的价电子排布图为
的价电子排布图为_______ 。
(2) 和
和 的沸点:
的沸点:
_______  (填“>”“<”或“=”),原因是
(填“>”“<”或“=”),原因是_______ 。
(3) 溶液中
溶液中 以
以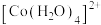 的形式存在,1.5mol
的形式存在,1.5mol 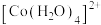 中σ键的数目为
中σ键的数目为_______ 。
(4)已知键角: ,原因是
,原因是_______ 。
(5)已知 晶体的晶胞结构与NaCl晶体的晶胞结构相似,但因
晶体的晶胞结构与NaCl晶体的晶胞结构相似,但因 晶体中有哑铃形的
晶体中有哑铃形的 存在而使晶胞沿一个方向拉长,晶胞参数分别为a nm、a nm、b nm,
存在而使晶胞沿一个方向拉长,晶胞参数分别为a nm、a nm、b nm, 为阿伏加德罗常数的值,则该晶体的密度是
为阿伏加德罗常数的值,则该晶体的密度是_______  (用含a、b、
(用含a、b、 的表达式表示)。
的表达式表示)。
 )制乙炔时会产生
)制乙炔时会产生 和
和 杂质气体,可用
杂质气体,可用 溶液除去。
溶液除去。(1)
 的价电子排布图为
的价电子排布图为(2)
 和
和 的沸点:
的沸点:
 (填“>”“<”或“=”),原因是
(填“>”“<”或“=”),原因是(3)
 溶液中
溶液中 以
以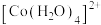 的形式存在,1.5mol
的形式存在,1.5mol 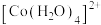 中σ键的数目为
中σ键的数目为(4)已知键角:
 ,原因是
,原因是(5)已知
 晶体的晶胞结构与NaCl晶体的晶胞结构相似,但因
晶体的晶胞结构与NaCl晶体的晶胞结构相似,但因 晶体中有哑铃形的
晶体中有哑铃形的 存在而使晶胞沿一个方向拉长,晶胞参数分别为a nm、a nm、b nm,
存在而使晶胞沿一个方向拉长,晶胞参数分别为a nm、a nm、b nm, 为阿伏加德罗常数的值,则该晶体的密度是
为阿伏加德罗常数的值,则该晶体的密度是 (用含a、b、
(用含a、b、 的表达式表示)。
的表达式表示)。
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐2】硅烷广泛应用在现代高科技领域。制备硅烷的反应为:SiF4+NaAlH4=SiH4+NaAlF4.
(1)①基态硅原子的价层电子轨道表示式为_____ ,基态硅原子的电子有_____ 种空间运动状态。
②SiF4中,硅的化合价为+4价。硅显正化合价的原因是_____ 。
③下列说法正确的是_____ (填字母)。
a.SiH4的稳定性比CH4的差
b.SiH4中4个Si-H的键长相同,H-Si-H的键角为90°
c.SiH4中硅原子以4个sp3杂化轨道分别与4个氢原子的1s轨道重叠,形成4个Si-Hσ键
④SiF4的沸点(-86℃)高于SiH4的沸点(-112℃),原因是_____ 。
⑤键角:SiF4_____ SiH4,原因_____ 。
(2)NaAlH4的晶胞结构如图所示,晶胞的体积为a2b×10-21cm3。
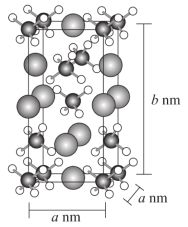
① 的VSEPR模型名称为
的VSEPR模型名称为_____ 。
②用NA表示阿伏加德罗常数的值。NaAlH4晶体密度为_____ g•cm-3(用含a、b、NA的代数式表示)。
③NaAlH4是一种具有应用潜能的储氢材料,其释氢过程可用化学方程式表示为:3NaAlH4═Na3AlH6+2Al+3H2↑。掺杂22Ti替换晶体中部分Al,更利于NaAlH4中H的解离,使体系更容易释放氢。从结构的角度推测其可能的原因:_____ 。
(1)①基态硅原子的价层电子轨道表示式为
②SiF4中,硅的化合价为+4价。硅显正化合价的原因是
③下列说法正确的是
a.SiH4的稳定性比CH4的差
b.SiH4中4个Si-H的键长相同,H-Si-H的键角为90°
c.SiH4中硅原子以4个sp3杂化轨道分别与4个氢原子的1s轨道重叠,形成4个Si-Hσ键
④SiF4的沸点(-86℃)高于SiH4的沸点(-112℃),原因是
⑤键角:SiF4
(2)NaAlH4的晶胞结构如图所示,晶胞的体积为a2b×10-21cm3。

①
 的VSEPR模型名称为
的VSEPR模型名称为②用NA表示阿伏加德罗常数的值。NaAlH4晶体密度为
③NaAlH4是一种具有应用潜能的储氢材料,其释氢过程可用化学方程式表示为:3NaAlH4═Na3AlH6+2Al+3H2↑。掺杂22Ti替换晶体中部分Al,更利于NaAlH4中H的解离,使体系更容易释放氢。从结构的角度推测其可能的原因:
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐3】由于铁氮化合物具有非常优异的磁性能、机械性能和耐腐蚀性,受到研究人员的广泛关注。γˊ−Fe4N是一种性能优异的铁氮化合物,其可由氨气与羰基铁粉[Fe(CO)5]反应得到。
(1)Fe变为Fe2+时是失去___________ 轨道电子,Fe3+价层电子排布图为___________ 。
(2)氨气中N的杂化类型是___________ ,NH3中H−N−H的键角比NH4+中H−N−H的键角___________ (填“大”或“小”),理由是___________ 。
(3) 与CO中均存在化学键的类型有
与CO中均存在化学键的类型有___________ (填标号)。
A.离子键 B.氢键 C.配位键 D.共价键 E.金属键
(4)羰基铁粉[Fe(CO)5]中铁元素的配位数是___________ ,配位原子为___________ 。
(5)氨气与羰基铁粉的反应中涉及元素电负性由大到小的顺序为___________ 。
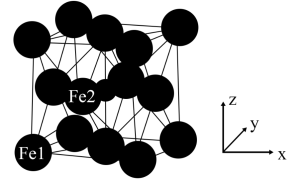
(6)γ−Fe4N的晶胞如图所示,设晶胞中Fe1点的原子坐标为(0,0,0),N点的原子坐标为( ,
, ,
, ),则Fe2点的原子坐标为
),则Fe2点的原子坐标为___________ 。已知该晶体的密度为dg/cm3,阿伏加德罗常数的值为NA,则晶胞参数a为___________ nm(用含d和NA的代数式表示)。
(1)Fe变为Fe2+时是失去
(2)氨气中N的杂化类型是
(3)
 与CO中均存在化学键的类型有
与CO中均存在化学键的类型有A.离子键 B.氢键 C.配位键 D.共价键 E.金属键
(4)羰基铁粉[Fe(CO)5]中铁元素的配位数是
(5)氨气与羰基铁粉的反应中涉及元素电负性由大到小的顺序为
(6)γ−Fe4N的晶胞如图所示,设晶胞中Fe1点的原子坐标为(0,0,0),N点的原子坐标为(
 ,
, ,
, ),则Fe2点的原子坐标为
),则Fe2点的原子坐标为
您最近一年使用:0次



