由于铁氮化合物具有非常优异的磁性能、机械性能和耐腐蚀性,受到研究人员的广泛关注。γˊ−Fe4N是一种性能优异的铁氮化合物,其可由氨气与羰基铁粉[Fe(CO)5]反应得到。
(1)Fe变为Fe2+时是失去___________ 轨道电子,Fe3+价层电子排布图为___________ 。
(2)氨气中N的杂化类型是___________ ,NH3中H−N−H的键角比NH4+中H−N−H的键角___________ (填“大”或“小”),理由是___________ 。
(3) 与CO中均存在化学键的类型有
与CO中均存在化学键的类型有___________ (填标号)。
A.离子键 B.氢键 C.配位键 D.共价键 E.金属键
(4)羰基铁粉[Fe(CO)5]中铁元素的配位数是___________ ,配位原子为___________ 。
(5)氨气与羰基铁粉的反应中涉及元素电负性由大到小的顺序为___________ 。
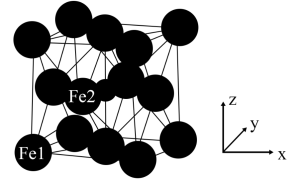
(6)γ−Fe4N的晶胞如图所示,设晶胞中Fe1点的原子坐标为(0,0,0),N点的原子坐标为( ,
, ,
, ),则Fe2点的原子坐标为
),则Fe2点的原子坐标为___________ 。已知该晶体的密度为dg/cm3,阿伏加德罗常数的值为NA,则晶胞参数a为___________ nm(用含d和NA的代数式表示)。
(1)Fe变为Fe2+时是失去
(2)氨气中N的杂化类型是
(3)
 与CO中均存在化学键的类型有
与CO中均存在化学键的类型有A.离子键 B.氢键 C.配位键 D.共价键 E.金属键
(4)羰基铁粉[Fe(CO)5]中铁元素的配位数是
(5)氨气与羰基铁粉的反应中涉及元素电负性由大到小的顺序为
(6)γ−Fe4N的晶胞如图所示,设晶胞中Fe1点的原子坐标为(0,0,0),N点的原子坐标为(
 ,
, ,
, ),则Fe2点的原子坐标为
),则Fe2点的原子坐标为
更新时间:2021-12-31 12:40:09
|
相似题推荐
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐1】碳、铜、锡及其化合物有许多用途。回答下列问题。
(1)在元素周期表里,锡和碳同族,锡位于第五周期。基态锡原子的最外层电子排布式为______ 。
(2)磷化铜(Cu3P2)用于制造磷青铜,磷青铜是含少量锡、磷的铜合金。磷化铜与水反应产生有毒的磷化氢(PH3)气体,PH3分子的热稳定性比NH3__________ (填“强”或“弱”);P、S的第二电离能(I2)的大小关系为I2(P) __________ I2(S)(填“>”“<”或“=”),原因是_______________ 。
(3)CH3CH2COOH中C的杂化方式有_________ ;1mol苯中含σ键的数目为________ 。
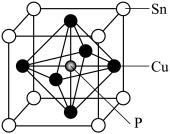
(4)磷青铜晶体的晶胞结构如图所示,该晶体中P原子与最近的Cu原子的核间距为a nm,则晶体密度为__________ g·cm−3(用含NA的代数式表示);该晶体中P原子位于由铜原子形成的正八面体的空隙中,则该正八面体的边长为________ nm。
(1)在元素周期表里,锡和碳同族,锡位于第五周期。基态锡原子的最外层电子排布式为
(2)磷化铜(Cu3P2)用于制造磷青铜,磷青铜是含少量锡、磷的铜合金。磷化铜与水反应产生有毒的磷化氢(PH3)气体,PH3分子的热稳定性比NH3
(3)CH3CH2COOH中C的杂化方式有
(4)磷青铜晶体的晶胞结构如图所示,该晶体中P原子与最近的Cu原子的核间距为a nm,则晶体密度为

您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐2】已知A、B、C、D、E、F都是周期表中前四周期的元素,它们的核电荷数A<B<C<D<E<F。其中A原子核外有三个未成对电子;化合物B2E为离子晶体,E原子核外的M层中只有两对成对电子;C元素是地壳中含量最高的金属元素;D单质的晶体类型在同周期的单质中没有相同的; F原子最外层电子数与B的相同,其余各层均充满电子。请根据以上信息,回答下列问题(注:A、B、C、D、E、F用所对应的元素符号表示):
(1)A、B、C、D的第一电离能由小到大的顺序为___________ (用元素符号表示)。
(2)B的氯化物的熔点比MgO的熔点___________ (填“高”或“低”)。
(3)F的外围电子排布式是___________ 。
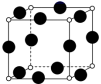
(4)A、F形成某种化合物的晶胞结构如图所示(其中A显−3价),则其化学式为___________ (每个球均表示1个原子)。
(5)A、C形成的化合物具有高沸点和高硬度,是一种新型无机非金属材料,其晶体中所含的化学键类型为___________ 。
(1)A、B、C、D的第一电离能由小到大的顺序为
(2)B的氯化物的熔点比MgO的熔点
(3)F的外围电子排布式是
(4)A、F形成某种化合物的晶胞结构如图所示(其中A显−3价),则其化学式为

(5)A、C形成的化合物具有高沸点和高硬度,是一种新型无机非金属材料,其晶体中所含的化学键类型为
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
解题方法
【推荐3】6月17日,我国第三艘航空母舰命名为“中国人民解放军海军福建舰”,舷号为“18”。航母的甲板用钢具有高强度、大板面、拒磁、高韧性、抗低温(零下38°C)等特性。
(1)铁中掺入铬,铬含量在10.5%以上,它的耐腐蚀性能显著增加。基态铬原子的价电子排布式为_______ ,基态铁原子核外有_______ 个电子云伸展方向。
(2)硅油是一种不同聚合度链状结构的聚有机硅氧烷。它具有耐热性、电绝缘性、耐候性等优点,因此可用于保护甲板,其结构简式如图所示。

硅油中碳原子的杂化方式为_______ 杂化,O−Si的键能比C−Si的_______ (填“大”或“小”),其原因是_______ 。
(3)铁的常见的两种氧化物为FeO、 ,FeO的熔点比
,FeO的熔点比 的
的_______ (填“高”或“低”),其原因是_______ 。
(4)铁粉在高温氮氛围下能够形成强磁性铁氮化合物,其晶胞结构如图所示,则该铁氮化合物的化学式为_______ ,设晶胞密度为ρg∙cm−3, 为阿伏加德罗常数的值,则该晶胞中氮原子到顶点铁原子之间的距离为
为阿伏加德罗常数的值,则该晶胞中氮原子到顶点铁原子之间的距离为_______ cm(用代数式表示)。

(1)铁中掺入铬,铬含量在10.5%以上,它的耐腐蚀性能显著增加。基态铬原子的价电子排布式为
(2)硅油是一种不同聚合度链状结构的聚有机硅氧烷。它具有耐热性、电绝缘性、耐候性等优点,因此可用于保护甲板,其结构简式如图所示。

硅油中碳原子的杂化方式为
(3)铁的常见的两种氧化物为FeO、
 ,FeO的熔点比
,FeO的熔点比 的
的(4)铁粉在高温氮氛围下能够形成强磁性铁氮化合物,其晶胞结构如图所示,则该铁氮化合物的化学式为
 为阿伏加德罗常数的值,则该晶胞中氮原子到顶点铁原子之间的距离为
为阿伏加德罗常数的值,则该晶胞中氮原子到顶点铁原子之间的距离为
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐1】铝镍钴系永磁合金以铁,镍、铝元素为主要成分,还含有铜、钴、钛等元素.具有高剩磁和低温度系数,磁性稳定.现多用于仪表工业中制造磁电系仪表、流量计、微特电机,继电器等。
(1)铁、钴、镍元素性质非常相似,原子半径接近但依次减小,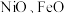 的晶体结构类型与氯化钠相同.基态钴原子价电子轨道表示式为
的晶体结构类型与氯化钠相同.基态钴原子价电子轨道表示式为________ ,熔沸点:
____  (填“<”“>”或“=”)。
(填“<”“>”或“=”)。
(2) 俗称摩尔盐,相对于
俗称摩尔盐,相对于 而言,摩尔盐不易失水,不易被空气氧化,在化学分析实验中常用于配制
而言,摩尔盐不易失水,不易被空气氧化,在化学分析实验中常用于配制 (Ⅱ)的标准溶液,硫酸亚铁铵晶体中亚铁离子稳定存在的原因是
(Ⅱ)的标准溶液,硫酸亚铁铵晶体中亚铁离子稳定存在的原因是___________ 。
(3)氢能源发展的关键环节是新型储氢材料,氨硼烷 常温下以固体稳定存在,极易溶于水,是一种理想的新型储氢材料。
常温下以固体稳定存在,极易溶于水,是一种理想的新型储氢材料。
①氨硼烷分子中B原子采取_________ 杂化。
②氨硼烷晶体中存在的作用力有范德华力,极性键、________ 和________ 。
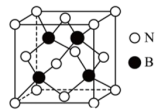
(4)立方氮化硼 晶体的晶胞结构如图1所示,N原子为面心立方最密堆积。
晶体的晶胞结构如图1所示,N原子为面心立方最密堆积。
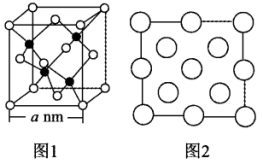
图2是立方氮化硼晶胞的俯视投影图.请在图中用“●”标明B原子的相对位置________ 。
(1)铁、钴、镍元素性质非常相似,原子半径接近但依次减小,
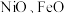 的晶体结构类型与氯化钠相同.基态钴原子价电子轨道表示式为
的晶体结构类型与氯化钠相同.基态钴原子价电子轨道表示式为
 (填“<”“>”或“=”)。
(填“<”“>”或“=”)。(2)
 俗称摩尔盐,相对于
俗称摩尔盐,相对于 而言,摩尔盐不易失水,不易被空气氧化,在化学分析实验中常用于配制
而言,摩尔盐不易失水,不易被空气氧化,在化学分析实验中常用于配制 (Ⅱ)的标准溶液,硫酸亚铁铵晶体中亚铁离子稳定存在的原因是
(Ⅱ)的标准溶液,硫酸亚铁铵晶体中亚铁离子稳定存在的原因是(3)氢能源发展的关键环节是新型储氢材料,氨硼烷
 常温下以固体稳定存在,极易溶于水,是一种理想的新型储氢材料。
常温下以固体稳定存在,极易溶于水,是一种理想的新型储氢材料。①氨硼烷分子中B原子采取
②氨硼烷晶体中存在的作用力有范德华力,极性键、
(4)立方氮化硼
 晶体的晶胞结构如图1所示,N原子为面心立方最密堆积。
晶体的晶胞结构如图1所示,N原子为面心立方最密堆积。
图2是立方氮化硼晶胞的俯视投影图.请在图中用“●”标明B原子的相对位置
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐2】现有六种元素,其中A、B、C、D、E为短周期主族元素,F为第四周期元素,它们的原子序数依次增大。请根据下列相关信息,回答问题。
(1)某同学根据上述信息,推断A基态原子的核外电子排布为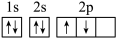 ,该同学所画的电子排布图违背了
,该同学所画的电子排布图违背了_______ 。
(2)B元素的电负性_______ (填“大于”“小于”或“等于”)C元素的电负性。B元素的第一电离能_______ (填“大于”“小于”或“等于”)C元素的第一电离能。
(3)E基态原子中能量最高的电子,其电子云在空间有_______ 个方向。
(4)下列关于F原子的价层电子轨道表示式正确的是_______(填字母)。
(5)与F同周期,原子序数为24的元素M,其基态原子的核外电子排布式为_______ 。
(6)元素铜与镍的第二电离能分别为ICu=1959kJ·mol-1,INi=1753kJ·mol-1,ICu>INi原因是_______ 。
(7)AC 的空间结构为
的空间结构为_______ 中心原子的杂化轨道类型为_______ 。
| A元素形成的物质种类繁多,其形成的一种固体单质工业上常用作切割工具 |
| B元素原子的核外p电子数比s电子数少1 |
| C元素基态原子p轨道有两个未成对电子 |
| D原子的第一至第四电离能分别是:I1=738kJ·mol-1;I2=1451kJ·mol-1;I3=7733kJ·mol-1;I4=10540kJ·mol-1 |
| E原子核外所有p轨道全满或半满 |
| F在周期表的第8纵列 |
 ,该同学所画的电子排布图违背了
,该同学所画的电子排布图违背了(2)B元素的电负性
(3)E基态原子中能量最高的电子,其电子云在空间有
(4)下列关于F原子的价层电子轨道表示式正确的是_______(填字母)。
A.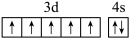 | B.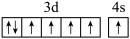 |
C.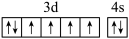 | D.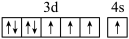 |
(6)元素铜与镍的第二电离能分别为ICu=1959kJ·mol-1,INi=1753kJ·mol-1,ICu>INi原因是
(7)AC
 的空间结构为
的空间结构为
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐3】东晋《华阳国志·南中志》卷四中已有关于白铜的记载,云南镍白铜(铜镍合金)闻名中外,曾主要用于造币,亦可用于制作仿银饰品。回答下列问题:
(1)镍元素基态原子的价电于排布图为_______ 。
(2)硫酸镍溶于氨水形成[Ni(NH3)6]SO4蓝色溶液。
①[Ni(NH3)6]SO4内界的配体中配位原子的VSEPR构型是_______ 。
②在[Ni(NH3)6]2+中H-N-H比NH3中H-N-H的键角_______ (选填“大”、“小”、“相等”或“无法判断”),原因是_______ 。
(3)镍白铜晶体中存在相互作用的微粒是_______ ,其作用是_______ 。
(4)某镍白铜合金的立方晶体结构如图所示:
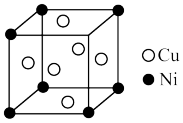
①晶胞中镍原子与铜原子的个数比为_______ 。
②若该合金的晶胞参数a pm,其密度为=_______ g/cm3。
(1)镍元素基态原子的价电于排布图为
(2)硫酸镍溶于氨水形成[Ni(NH3)6]SO4蓝色溶液。
①[Ni(NH3)6]SO4内界的配体中配位原子的VSEPR构型是
②在[Ni(NH3)6]2+中H-N-H比NH3中H-N-H的键角
(3)镍白铜晶体中存在相互作用的微粒是
(4)某镍白铜合金的立方晶体结构如图所示:

①晶胞中镍原子与铜原子的个数比为
②若该合金的晶胞参数a pm,其密度为=
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐1】三明清流“天芳悦潭”温泉富含珍稀“锗”元素。其中锗石含有人体所需的硒、锌、镍、钴、锰、镁、钙等30多种对人体有益的微量元素。回答下列问题:
(1)基态Ge原子价电子排布图为_______ 、属于_______ 区。
(2)锗与碳同族,性质和结构有一定的相似性,锗元素能形成无机化合物(如锗酸钠: ;二锗酸钠:
;二锗酸钠: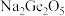 等),也能形成类似于烷烃的锗烷(
等),也能形成类似于烷烃的锗烷( )。
)。
① 中阴离子的空间结构是
中阴离子的空间结构是_______ 。
②推测1mol 中含有的σ键的数目是
中含有的σ键的数目是_______ (用 表示阿伏加德罗常数值)。
表示阿伏加德罗常数值)。
(3)利用离子液体[EMIM][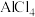 ]可电沉积还原金属Ge,其熔点只有7℃,其中
]可电沉积还原金属Ge,其熔点只有7℃,其中 结构如图所示。
结构如图所示。
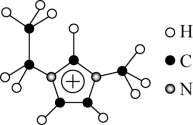
①该物质的晶体类型是_______ 。
② 离子中组成元素的电负性由小到大的顺序是
离子中组成元素的电负性由小到大的顺序是_______ 。
(4)独立的 分子中H−N−H的键角为107.3°,
分子中H−N−H的键角为107.3°, 离子中H−N−H的键角
离子中H−N−H的键角_______ 107.3°(填“大于”、“小于”或“等于”)。
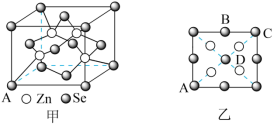
(5)硒化锌(ZnSe)是一种重要的半导体材料,其晶胞结构如图甲所示,已知晶胞边长为apm,该晶胞中两个Zn原子之间的间距是_______ ;乙图为甲图的俯视图,A点坐标为(0,0,0),B点坐标为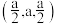 ,则D点坐标为
,则D点坐标为_______ ;若该晶胞密度为 ,则阿伏加德罗常数
,则阿伏加德罗常数 为
为_______ (只列出计算式)。
(1)基态Ge原子价电子排布图为
(2)锗与碳同族,性质和结构有一定的相似性,锗元素能形成无机化合物(如锗酸钠:
 ;二锗酸钠:
;二锗酸钠: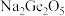 等),也能形成类似于烷烃的锗烷(
等),也能形成类似于烷烃的锗烷( )。
)。①
 中阴离子的空间结构是
中阴离子的空间结构是②推测1mol
 中含有的σ键的数目是
中含有的σ键的数目是 表示阿伏加德罗常数值)。
表示阿伏加德罗常数值)。(3)利用离子液体[EMIM][
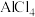 ]可电沉积还原金属Ge,其熔点只有7℃,其中
]可电沉积还原金属Ge,其熔点只有7℃,其中 结构如图所示。
结构如图所示。
①该物质的晶体类型是
②
 离子中组成元素的电负性由小到大的顺序是
离子中组成元素的电负性由小到大的顺序是(4)独立的
 分子中H−N−H的键角为107.3°,
分子中H−N−H的键角为107.3°, 离子中H−N−H的键角
离子中H−N−H的键角(5)硒化锌(ZnSe)是一种重要的半导体材料,其晶胞结构如图甲所示,已知晶胞边长为apm,该晶胞中两个Zn原子之间的间距是
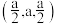 ,则D点坐标为
,则D点坐标为 ,则阿伏加德罗常数
,则阿伏加德罗常数 为
为
您最近一年使用:0次
【推荐2】W、X、Y、Z、N是原子序数依次增大的5种短周期元素,其元素性质或原子结构如下:
请完成下列空白:
(1)写出各元素的元素符号:W:___________ 、X:___________ 、Y:___________ 、Z:___________ 、N:___________ 。
(2)X、Y和Z三种元素的原子半径由大到小的顺序:___________ (请填元素符号)。
(3)X、Z和N三种元素的电负性由大到小的顺序:___________ (请填元素符号)。
(4)Y、Z和N三种元素的第一电离能由大到小的顺序:___________ (请填元素符号)。
| 元素 | 元素性质或原子结构 |
| W | 电子只有一种自旋取向 |
| X | 原子核外s能级上的电子总数与p能级上的电子总数相等,但第一电离能都低于同周期相邻元素 |
| Y | 原子核外s能级上的电子总数与p能级上的电子总数相等,但第一电离能都高于同周期相邻元素 |
| Z | 其价电子中,在不同形状的原子轨道中运动的电子数相等 |
| N | 只有一个不成对电子 |
(1)写出各元素的元素符号:W:
(2)X、Y和Z三种元素的原子半径由大到小的顺序:
(3)X、Z和N三种元素的电负性由大到小的顺序:
(4)Y、Z和N三种元素的第一电离能由大到小的顺序:
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐3】I.回答下列问题:
(1)下列原子或离子的核外电子排布正确的是___________ ,违反能量最低原理的是___________ ,违反洪特规则的是___________ ,违反泡利不相容原理的是___________ 。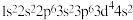 ⑤K:
⑤K: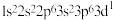 ⑥Mg:
⑥Mg:
(2)《中华本草》等中医典籍中,记载了炉甘石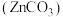 入药,可用于治疗皮肤炎症或表面创伤。Zn、C、O电负性由大至小的顺序是
入药,可用于治疗皮肤炎症或表面创伤。Zn、C、O电负性由大至小的顺序是___________ ,其阴离子的空间结构为___________ ,Zn位于元素周期表的___________ 区。
(3)基态锰原子有___________ 种空间运动状态的电子,锰有多种化合价,在+2、+3、+4、+5和+6中,最稳定的化合价是___________ 。
(4) 已知无水 固态时具有链状结构
固态时具有链状结构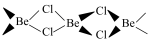 ,在二聚体分子(
,在二聚体分子(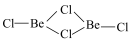 ),其中铍原子的杂化类型为
),其中铍原子的杂化类型为___________ 。
(1)下列原子或离子的核外电子排布正确的是
① :
: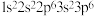 ②
② :
: ③P:
③P: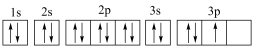
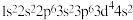 ⑤K:
⑤K: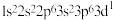 ⑥Mg:
⑥Mg:
⑦C: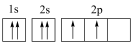
(2)《中华本草》等中医典籍中,记载了炉甘石
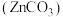 入药,可用于治疗皮肤炎症或表面创伤。Zn、C、O电负性由大至小的顺序是
入药,可用于治疗皮肤炎症或表面创伤。Zn、C、O电负性由大至小的顺序是(3)基态锰原子有
(4) 已知无水
 固态时具有链状结构
固态时具有链状结构 ,在二聚体分子(
,在二聚体分子( ),其中铍原子的杂化类型为
),其中铍原子的杂化类型为
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
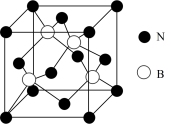
【推荐1】ⅢA、VA族元素组成的化合物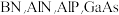 是人工合成的具有特殊功能的新材料,回答下列问题:
是人工合成的具有特殊功能的新材料,回答下列问题:
(1)基态B原子的电子排布式为___________ ;BN中B元素的化合价为___________ 。
(2)As基态原子的电子占据了___________ 个能层,最高能级的电子排布式为___________ ;和As位于同一周期,且未成对电子数也相同的元素还有___________ 种。
(3)元素周期表中与P紧邻的4种元素中电负性最大的是___________ (填元素符号):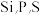 三种元素的第一电离能由大到小的顺序是
三种元素的第一电离能由大到小的顺序是___________ 。
(4)已知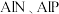 等半导体材料的晶体结构与单晶硅相似,则
等半导体材料的晶体结构与单晶硅相似,则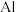 原子的杂化形式为
原子的杂化形式为___________ ;晶体结构中存在的化学键有___________ (填字母代号)。
A.离子键 B.σ键 C.π键 D.配位键
(5)立方氮化硼,其结构与金刚石相似,硬度与金刚石相当,晶胞边长为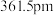 ,立方氮化硼的密度是
,立方氮化硼的密度是___________  (只要求列算式,不必计算出数值,阿伏加德罗常数为
(只要求列算式,不必计算出数值,阿伏加德罗常数为 )。
)。
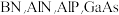 是人工合成的具有特殊功能的新材料,回答下列问题:
是人工合成的具有特殊功能的新材料,回答下列问题:(1)基态B原子的电子排布式为
(2)As基态原子的电子占据了
(3)元素周期表中与P紧邻的4种元素中电负性最大的是
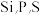 三种元素的第一电离能由大到小的顺序是
三种元素的第一电离能由大到小的顺序是(4)已知
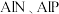 等半导体材料的晶体结构与单晶硅相似,则
等半导体材料的晶体结构与单晶硅相似,则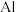 原子的杂化形式为
原子的杂化形式为A.离子键 B.σ键 C.π键 D.配位键
(5)立方氮化硼,其结构与金刚石相似,硬度与金刚石相当,晶胞边长为
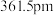 ,立方氮化硼的密度是
,立方氮化硼的密度是 (只要求列算式,不必计算出数值,阿伏加德罗常数为
(只要求列算式,不必计算出数值,阿伏加德罗常数为 )。
)。
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐2】N、P、As均为氮族元素,这些元素与人们的生活息息相关。回答下列问题:
(1)按电子排布N元素在周期表分区中属于_____ 区元素,基态N原子的未成对电子数目为____ 个。
(2)Si、P与S是同周期中相邻的元素,Si、P、S的电负性由大到小的顺序是____ ,第一电离能由大到小的顺序是_____ 。
(3)吡啶为含N有机物,这类物质是合成医药、农药的重要原料。下列吡啶类化合物A与Zn(CH3CH2)2(即ZnEt2)反应生成有机化合物B,B具有优异的催化性能。
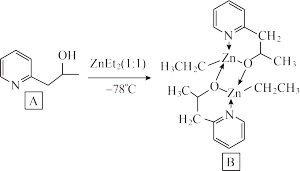
吡啶类化合物A中N原子的杂化类型是___ ,化合物A易溶于水,主要原因是_____ 。含Zn有机物B的分子结构中含_______ (填字母代号)。
A.离子键 B.配位键 C.π键 D.σ键 E.氢键
(4)N与金属可形成氮化物,如AlN的晶体结构如图1所示,某种氮化铁的结构如图2所示。
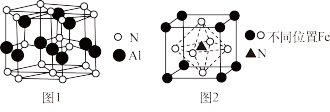
①AlN晶体结构单元中,含有的Al、N原子个数均是_______ ;
②若该氮化铁的晶胞边长为apm,阿伏加德罗常数的值为NA,则该氮化铁的晶体密度可表示为_______ g·cm−3。
(1)按电子排布N元素在周期表分区中属于
(2)Si、P与S是同周期中相邻的元素,Si、P、S的电负性由大到小的顺序是
(3)吡啶为含N有机物,这类物质是合成医药、农药的重要原料。下列吡啶类化合物A与Zn(CH3CH2)2(即ZnEt2)反应生成有机化合物B,B具有优异的催化性能。

吡啶类化合物A中N原子的杂化类型是
A.离子键 B.配位键 C.π键 D.σ键 E.氢键
(4)N与金属可形成氮化物,如AlN的晶体结构如图1所示,某种氮化铁的结构如图2所示。

①AlN晶体结构单元中,含有的Al、N原子个数均是
②若该氮化铁的晶胞边长为apm,阿伏加德罗常数的值为NA,则该氮化铁的晶体密度可表示为
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
【推荐3】2023年诺贝尔化学奖授予蒙吉·G·巴文迪等三位科学家,以表彰他们在发现和合成量子点方面所作出的贡献,碳量子点是一类具有显著荧光性能的零维碳纳米材料,其结构如图所示。回答下列问题:_______ 区,图中C的杂化方式为_______ 。
(2)碳量子点结构包含的元素中电负性由大到小排列为:_______ 。
(3)碳量子点水溶性_______ (选填“>”“<”“=”)石墨水溶性,理由是:_______ 。
(4)高压合成金刚石的原料是廉价的石墨,用高压釜持续施加高温高压并加入金属镍等金属催化剂,石墨可转化为金刚石。基态镍原子核外电子的空间运动状态有_______ 种,比较二者C-C共价键的键长:石墨_______ 金刚石(选填“>”“<”“=”)。
(5)氮化硼(BN)是一种性能优异、潜力巨大的新型材料,其中一种结构为立方氮化硼(如图),类似于金刚石。_______ ,则立方氮化硼晶体密度为_______ g·cm-3(列出计算式,阿伏加德罗常数的值为NA)。

(2)碳量子点结构包含的元素中电负性由大到小排列为:
(3)碳量子点水溶性
(4)高压合成金刚石的原料是廉价的石墨,用高压釜持续施加高温高压并加入金属镍等金属催化剂,石墨可转化为金刚石。基态镍原子核外电子的空间运动状态有
(5)氮化硼(BN)是一种性能优异、潜力巨大的新型材料,其中一种结构为立方氮化硼(如图),类似于金刚石。
您最近一年使用:0次



