东晋《华阳国志·南中志》卷四中已有关于白铜的记载,云南镍白铜(铜镍合金)闻名中外,曾主要用于造币,亦可用于制作仿银饰品。回答下列问题:
(1)镍元素基态原子的价电于排布图为_______ 。
(2)硫酸镍溶于氨水形成[Ni(NH3)6]SO4蓝色溶液。
①[Ni(NH3)6]SO4内界的配体中配位原子的VSEPR构型是_______ 。
②在[Ni(NH3)6]2+中H-N-H比NH3中H-N-H的键角_______ (选填“大”、“小”、“相等”或“无法判断”),原因是_______ 。
(3)镍白铜晶体中存在相互作用的微粒是_______ ,其作用是_______ 。
(4)某镍白铜合金的立方晶体结构如图所示:
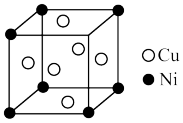
①晶胞中镍原子与铜原子的个数比为_______ 。
②若该合金的晶胞参数a pm,其密度为=_______ g/cm3。
(1)镍元素基态原子的价电于排布图为
(2)硫酸镍溶于氨水形成[Ni(NH3)6]SO4蓝色溶液。
①[Ni(NH3)6]SO4内界的配体中配位原子的VSEPR构型是
②在[Ni(NH3)6]2+中H-N-H比NH3中H-N-H的键角
(3)镍白铜晶体中存在相互作用的微粒是
(4)某镍白铜合金的立方晶体结构如图所示:

①晶胞中镍原子与铜原子的个数比为
②若该合金的晶胞参数a pm,其密度为=
更新时间:2022-10-26 12:58:57
|
相似题推荐
【推荐1】元素周期表前四周期的A、B、C、D、E五种元素,A元素的原子最外层电子排布式为ns1;B元素的原子价电子排布式为ns2np2;C元素位于第二周期且原子中p能级与s能级的电子总数相等;D元素原子的M能层的p能级中有3个未成对电子;E元素原子有5个未成对电子。
(1)写出下列元素的名称:
C___________ ;D_______ ;E_______ 。
(2)基态C原子的电子排布图为_____ 。
(3)当n=2时,B的最简单气态氢化物的电子式为_____ ,BC2分子的结构式为_____ ;当n=3时,B与C形成的化合物与氢氧化钠溶液反应的离子方程式是_________ 。
(4)若A元素的原子价电子排布式为2s1,B元素的原子价电子排布式为3s23p2,A、B、C、D四种元素的第一电离能由大到小的顺序是_____ (用元素符号表示)。
(5)E元素在元素周期表中的位置是______ ,其最高价氧化物的化学式是_____ 。
(1)写出下列元素的名称:
C
(2)基态C原子的电子排布图为
(3)当n=2时,B的最简单气态氢化物的电子式为
(4)若A元素的原子价电子排布式为2s1,B元素的原子价电子排布式为3s23p2,A、B、C、D四种元素的第一电离能由大到小的顺序是
(5)E元素在元素周期表中的位置是
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐2】有A、B、C、D四种短周期主族元素,它们的原子序数依次增大,其中A元素原子核外电子仅有一种原子轨道,且是宇宙中最丰富的元素,B元素原子的核外p电子数比s电子数少1,C为金属元素且原子核外p电子数和s电子数相等;D元素的原子核外所有p轨道全充满或半充满。
(1)写出四种元素的元素符号:A_____ ,B_____ ,C_____ ,D_____ 。
(2)写出C、D两种元素基态原子核外电子排布的轨道表示式。C_____ ,D_____ 。
(3)写出B、C两种元素单质在一定条件下反应的化学方程式:_____ 。
(4)写出B元素单质和氢化物的电子式,单质_____ ,氢化物_____ 。
(5)C元素位于第_____ 周期_____ 族。A、B、C、D四种元素原子半径由大到小顺序是_____ 。B、C离子半径大小是_____ 。
(1)写出四种元素的元素符号:A
(2)写出C、D两种元素基态原子核外电子排布的轨道表示式。C
(3)写出B、C两种元素单质在一定条件下反应的化学方程式:
(4)写出B元素单质和氢化物的电子式,单质
(5)C元素位于第
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐3】如图所示是s能级和p能级的原子轨道图:
(1)s电子的原子轨道呈___________ 形,每个s能级有___________ 个原子轨道;p电子的原子轨道呈___________ 形,每个p能级有___________ 个原子轨道。
(2)元素X的基态原子最外层电子排布式为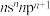 ,其p电子云在空间有3个互相
,其p电子云在空间有3个互相___________ (填“垂直”或“平行”)的伸展方向;元素X的名称是___________ ,它的最低价氢化物的电子式是___________ 。
(3)元素Y的基态原子最外层电子排布式为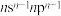 ,那么Y的元素符号应为
,那么Y的元素符号应为___________ ,其基态原子的轨道表示式为___________ 。

(1)s电子的原子轨道呈
(2)元素X的基态原子最外层电子排布式为
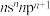 ,其p电子云在空间有3个互相
,其p电子云在空间有3个互相(3)元素Y的基态原子最外层电子排布式为
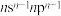 ,那么Y的元素符号应为
,那么Y的元素符号应为
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐1】回答下列问题。
(1)硼的研究在无机化学发展中占有独特的位置。硼元素有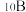 和
和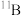 两种天然稳定的同位素,在基态
两种天然稳定的同位素,在基态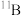 原子中,核外存在
原子中,核外存在___________ 对自旋相反的电子,有___________ 种不同空间运动状态的电子,根据对角线规则,硼元素许多性质与___________ 元素相似。
(2)在 分子中,
分子中, 的键角是
的键角是___________ 。
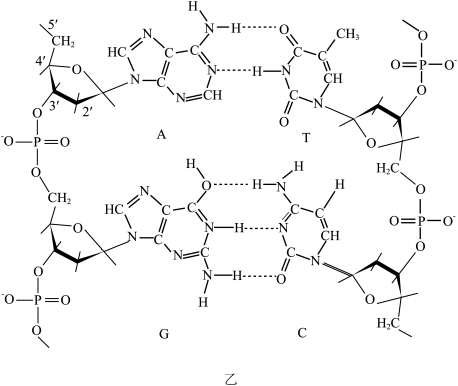
(3)O和S两种元素是自然界最常见的两种元素。均能与H形成 和
和 ,结构如图甲所示。请说明∠H—O—O(97°)略大于∠H-S-S(95°)的原因:
,结构如图甲所示。请说明∠H—O—O(97°)略大于∠H-S-S(95°)的原因:___________ 。___________ ;___________ 。
(1)硼的研究在无机化学发展中占有独特的位置。硼元素有
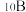 和
和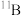 两种天然稳定的同位素,在基态
两种天然稳定的同位素,在基态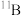 原子中,核外存在
原子中,核外存在(2)在
 分子中,
分子中, 的键角是
的键角是(3)O和S两种元素是自然界最常见的两种元素。均能与H形成
 和
和 ,结构如图甲所示。请说明∠H—O—O(97°)略大于∠H-S-S(95°)的原因:
,结构如图甲所示。请说明∠H—O—O(97°)略大于∠H-S-S(95°)的原因: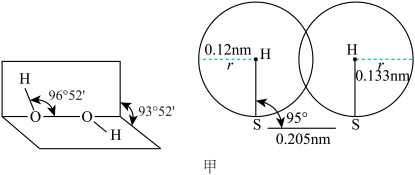
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
【推荐2】我国在新材料领域研究的重大突破,为“天宫”空间站的建设提供了坚实的物质基础。“天宫”空间站使用的材料中含有B、C、N、Ni、Cu等元素。回答下列问题:
(1)下列不同状态的硼中,失去一个电子需要吸收能量最多的是___________(填选项)
(2) 的VSEPR构型为
的VSEPR构型为___________ ,分子构型为___________
(3)镍能形成多种配合物,其中Ni(CO)4是无色挥发性液体,K2[Ni(CN)4]是红黄色单斜晶体。K2[Ni(CN)4]中的配位原子是:___________ ;K2[Ni(CN)4]的熔点高于Ni(CO)4的原因是___________ 。
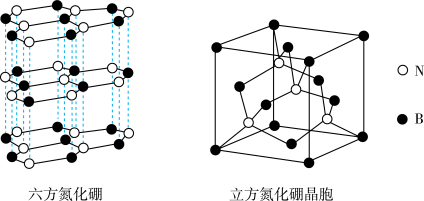
(4)氮化硼(BN)晶体存在如图所示的两种结构,六方氮化硼的结构与石墨类似,可做润滑剂;立方氮化硼的结构与金刚石类似,可作研磨剂。六方氮化硼的晶体类型为___________ ;立方氮化硼晶胞的密度为ρg∙cm-3,晶胞的边长为a cm。则阿伏加德罗常数的表达式为___________ 。
(1)下列不同状态的硼中,失去一个电子需要吸收能量最多的是___________(填选项)
A.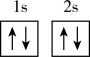 | B.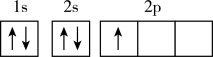 |
C.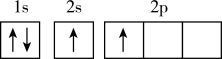 | D.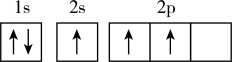 |
 的VSEPR构型为
的VSEPR构型为(3)镍能形成多种配合物,其中Ni(CO)4是无色挥发性液体,K2[Ni(CN)4]是红黄色单斜晶体。K2[Ni(CN)4]中的配位原子是:
(4)氮化硼(BN)晶体存在如图所示的两种结构,六方氮化硼的结构与石墨类似,可做润滑剂;立方氮化硼的结构与金刚石类似,可作研磨剂。六方氮化硼的晶体类型为

您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐3】铜是人类最早使用的金属之一,最近科学家发现Cu元素有很强的杀菌作用,还可代替 布线在硅芯片上。用黄铜矿(主要成分为
布线在硅芯片上。用黄铜矿(主要成分为 )生产粗铜,其反应原理如下:
)生产粗铜,其反应原理如下:
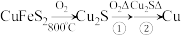
回答下列问题:
(1)基态 原子的价层电子排布式为
原子的价层电子排布式为___________ 。 的熔点
的熔点___________  的熔点(填写“<”、“>”或“=”)。
的熔点(填写“<”、“>”或“=”)。
(2)反应①、②中生成的气体 ,
, 分子的
分子的 模型为
模型为___________ (填名称)。
(3) 能与
能与 形成配位数为4的配合物,向
形成配位数为4的配合物,向 溶液中加入氨水,最终形成配合物
溶液中加入氨水,最终形成配合物 。请判断:
。请判断: 中存在的化学键的类型有
中存在的化学键的类型有___________ (填序号)。
a.离子键 b.金属键 c.配位键 d.非极性共价键 e.极性共价键
(4)如图是铜的一种氧化物晶体的晶胞结构。该化合物的化学式为___________ ,每个 原子周围与它最近且等距离的
原子周围与它最近且等距离的 原子有
原子有___________ 个,每个 原子周围与它最近且等距离的
原子周围与它最近且等距离的 原子有
原子有___________ 个。
 布线在硅芯片上。用黄铜矿(主要成分为
布线在硅芯片上。用黄铜矿(主要成分为 )生产粗铜,其反应原理如下:
)生产粗铜,其反应原理如下: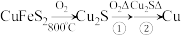
回答下列问题:
(1)基态
 原子的价层电子排布式为
原子的价层电子排布式为 的熔点
的熔点 的熔点(填写“<”、“>”或“=”)。
的熔点(填写“<”、“>”或“=”)。(2)反应①、②中生成的气体
 ,
, 分子的
分子的 模型为
模型为(3)
 能与
能与 形成配位数为4的配合物,向
形成配位数为4的配合物,向 溶液中加入氨水,最终形成配合物
溶液中加入氨水,最终形成配合物 。请判断:
。请判断: 中存在的化学键的类型有
中存在的化学键的类型有a.离子键 b.金属键 c.配位键 d.非极性共价键 e.极性共价键
(4)如图是铜的一种氧化物晶体的晶胞结构。该化合物的化学式为
 原子周围与它最近且等距离的
原子周围与它最近且等距离的 原子有
原子有 原子周围与它最近且等距离的
原子周围与它最近且等距离的 原子有
原子有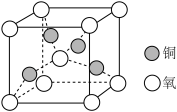
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
【推荐1】在不同温度下, 可与
可与 、
、 或
或 以配位键形成多种配合物。
以配位键形成多种配合物。 是一种微溶于冷水,易溶于热水的橙黄色晶体,实验室制备该配合物的过程可表示如下:
是一种微溶于冷水,易溶于热水的橙黄色晶体,实验室制备该配合物的过程可表示如下: 溶液为指示剂,用
溶液为指示剂,用 溶液滴定可测定
溶液滴定可测定 溶液中氯离子的含量。
溶液中氯离子的含量。
① 中含有的
中含有的 键的数目为
键的数目为_______ 。
②反应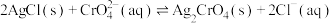 的平衡常数
的平衡常数
_______ 。(已知: ,
,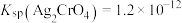 )
)
(2)“混合”反应物需降温到 以下,原因是
以下,原因是_______ 。
(3)制备 装置如图所示。加入催化剂活性炭加热至
装置如图所示。加入催化剂活性炭加热至 反应20min。
反应20min。_______ 。
②“转化”的化学方程式为_______ 。
(4)保持其它条件不变,改变反应温度, 的产率与温度变化如图所示。温度高于
的产率与温度变化如图所示。温度高于 时,
时, 产率下降的原因可能为
产率下降的原因可能为_______ 。 的实验方案:把反应后的混合物转移到烧杯中在冰水中快速冷却并过滤,
的实验方案:把反应后的混合物转移到烧杯中在冰水中快速冷却并过滤,_______ 。(实验中必须 使用的药品:浓盐酸、乙醇和水)
 可与
可与 、
、 或
或 以配位键形成多种配合物。
以配位键形成多种配合物。 是一种微溶于冷水,易溶于热水的橙黄色晶体,实验室制备该配合物的过程可表示如下:
是一种微溶于冷水,易溶于热水的橙黄色晶体,实验室制备该配合物的过程可表示如下: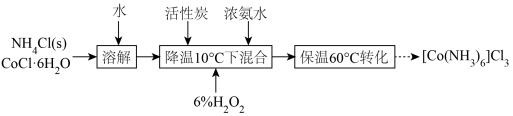
 溶液为指示剂,用
溶液为指示剂,用 溶液滴定可测定
溶液滴定可测定 溶液中氯离子的含量。
溶液中氯离子的含量。①
 中含有的
中含有的 键的数目为
键的数目为②反应
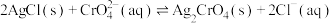 的平衡常数
的平衡常数
 ,
,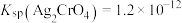 )
)(2)“混合”反应物需降温到
 以下,原因是
以下,原因是(3)制备
 装置如图所示。加入催化剂活性炭加热至
装置如图所示。加入催化剂活性炭加热至 反应20min。
反应20min。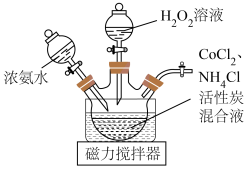
②“转化”的化学方程式为
(4)保持其它条件不变,改变反应温度,
 的产率与温度变化如图所示。温度高于
的产率与温度变化如图所示。温度高于 时,
时, 产率下降的原因可能为
产率下降的原因可能为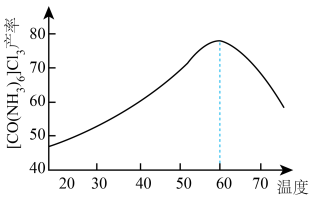
 的实验方案:把反应后的混合物转移到烧杯中在冰水中快速冷却并过滤,
的实验方案:把反应后的混合物转移到烧杯中在冰水中快速冷却并过滤,
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐2】完成下列问题
(1)基态铬原子的核外电子排布式为_______ ,有_______ 个未成对电子。
(2) 能形成配合物
能形成配合物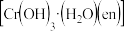 ,其中“en”代表
,其中“en”代表 。
。
①在该配合物中,提供孤电子对的原子是_______ (填元素符号)。
② “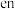 ”中采用
”中采用 杂化的原子是
杂化的原子是_______ (填元素符号)。
③在该配合物中,短周期元素按电负性由大到小的排列顺序为_______ (填元素符号)。
(3) 晶体的熔点为
晶体的熔点为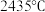 ,而
,而 晶体易升华,其主要原因是
晶体易升华,其主要原因是_______ 。
(4) 晶胞结构示意图。已知
晶胞结构示意图。已知 的摩尔质量为
的摩尔质量为 ,晶体密度为
,晶体密度为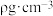 ,晶胞体积为
,晶胞体积为 。则:
。则:
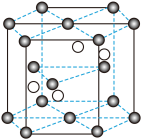
①晶胞结构示意图中的“小黑球”代表_______ (填“铬离子”或“氧离子”),1个晶胞中平均含有小黑球的个数是_______ 个。
②阿伏加德罗常数NA=_____ mol-1(用含 、
、 、
、 的代数式表示)。
的代数式表示)。
(1)基态铬原子的核外电子排布式为
(2)
 能形成配合物
能形成配合物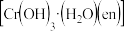 ,其中“en”代表
,其中“en”代表 。
。①在该配合物中,提供孤电子对的原子是
② “
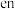 ”中采用
”中采用 杂化的原子是
杂化的原子是③在该配合物中,短周期元素按电负性由大到小的排列顺序为
(3)
 晶体的熔点为
晶体的熔点为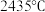 ,而
,而 晶体易升华,其主要原因是
晶体易升华,其主要原因是(4)
 晶胞结构示意图。已知
晶胞结构示意图。已知 的摩尔质量为
的摩尔质量为 ,晶体密度为
,晶体密度为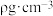 ,晶胞体积为
,晶胞体积为 。则:
。则:
①晶胞结构示意图中的“小黑球”代表
②阿伏加德罗常数NA=
 、
、 、
、 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
【推荐3】中国政府承诺:力争CO2的排放在2030年前实现“碳达峰”,2060年前实现“碳中和”,CO2的捕集与利用成为当前研究的热点。回答下面问题:
(1)写出CO2的电子式______ ,CO2分子属于______ (填“极性”或“非极性”)分子,其晶体俗名干冰,属于______ 晶体,其晶体内存在的微粒间相互作用有______ 。
(2)研究发现,在CO2合成甲醇(CH3OH)反应中,Co、Mn氧化物纳米粒子催化剂具有高活性,显示出良好的应用前景。Mn基态原子核外电子排布式为______ 。Co在周期表中属于______ 区元素。甲醇(CH3OH)能够与水任意比互溶,解释其原因是______ 。
(3)金属Zn属于金属晶体,其导电的原因是是______ 。已知金属Zn能溶于氨水,生成以氨为配体,配位数为4的配离子,Zn与氨水反应的离子方程式为______ 。
(4)CaF2的晶胞结构如图所示,X代表的离子是______ ;若该立方晶胞参数为apm,CaF2的摩尔质量用Mg/mol,阿伏伽德罗常数用NA来表示,则CaF2晶体的密度=______ g/cm3(写出表达式),阴阳离子的核间距最小为______ pm。

(1)写出CO2的电子式
(2)研究发现,在CO2合成甲醇(CH3OH)反应中,Co、Mn氧化物纳米粒子催化剂具有高活性,显示出良好的应用前景。Mn基态原子核外电子排布式为
(3)金属Zn属于金属晶体,其导电的原因是是
(4)CaF2的晶胞结构如图所示,X代表的离子是

您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐1】实验室用电石( )制乙炔时会产生
)制乙炔时会产生 和
和 杂质气体,可用
杂质气体,可用 溶液除去。
溶液除去。
(1) 的价电子排布图为
的价电子排布图为_______ 。
(2) 和
和 的沸点:
的沸点:
_______  (填“>”“<”或“=”),原因是
(填“>”“<”或“=”),原因是_______ 。
(3) 溶液中
溶液中 以
以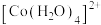 的形式存在,1.5mol
的形式存在,1.5mol 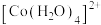 中σ键的数目为
中σ键的数目为_______ 。
(4)已知键角: ,原因是
,原因是_______ 。
(5)已知 晶体的晶胞结构与NaCl晶体的晶胞结构相似,但因
晶体的晶胞结构与NaCl晶体的晶胞结构相似,但因 晶体中有哑铃形的
晶体中有哑铃形的 存在而使晶胞沿一个方向拉长,晶胞参数分别为a nm、a nm、b nm,
存在而使晶胞沿一个方向拉长,晶胞参数分别为a nm、a nm、b nm, 为阿伏加德罗常数的值,则该晶体的密度是
为阿伏加德罗常数的值,则该晶体的密度是_______  (用含a、b、
(用含a、b、 的表达式表示)。
的表达式表示)。
 )制乙炔时会产生
)制乙炔时会产生 和
和 杂质气体,可用
杂质气体,可用 溶液除去。
溶液除去。(1)
 的价电子排布图为
的价电子排布图为(2)
 和
和 的沸点:
的沸点:
 (填“>”“<”或“=”),原因是
(填“>”“<”或“=”),原因是(3)
 溶液中
溶液中 以
以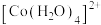 的形式存在,1.5mol
的形式存在,1.5mol 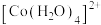 中σ键的数目为
中σ键的数目为(4)已知键角:
 ,原因是
,原因是(5)已知
 晶体的晶胞结构与NaCl晶体的晶胞结构相似,但因
晶体的晶胞结构与NaCl晶体的晶胞结构相似,但因 晶体中有哑铃形的
晶体中有哑铃形的 存在而使晶胞沿一个方向拉长,晶胞参数分别为a nm、a nm、b nm,
存在而使晶胞沿一个方向拉长,晶胞参数分别为a nm、a nm、b nm, 为阿伏加德罗常数的值,则该晶体的密度是
为阿伏加德罗常数的值,则该晶体的密度是 (用含a、b、
(用含a、b、 的表达式表示)。
的表达式表示)。
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
解题方法
【推荐2】用 、
、 可以制备含有
可以制备含有 的
的 悬浊液,该悬浊液可用于检验醛基,也可用于和葡萄糖反应制备纳米
悬浊液,该悬浊液可用于检验醛基,也可用于和葡萄糖反应制备纳米 。
。
(1)基态 的核外电子排布式为
的核外电子排布式为__________ 。
(2)与 互为等电子体的一种分子为
互为等电子体的一种分子为________ (填化学式)。
(3) 与
与 反应能生成
反应能生成 ,
, 中的配位原子为
中的配位原子为________ (填元素符号)。
(4)乙醛( )中碳原子的轨道杂化类型是
)中碳原子的轨道杂化类型是_________ ;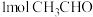 中含有
中含有 键的数目为
键的数目为________  。
。
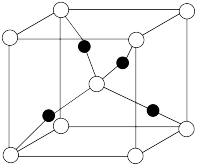
(5)一个 晶胞(见图)中,
晶胞(见图)中, 原子的数目为
原子的数目为________ 。
 、
、 可以制备含有
可以制备含有 的
的 悬浊液,该悬浊液可用于检验醛基,也可用于和葡萄糖反应制备纳米
悬浊液,该悬浊液可用于检验醛基,也可用于和葡萄糖反应制备纳米 。
。
(1)基态
 的核外电子排布式为
的核外电子排布式为(2)与
 互为等电子体的一种分子为
互为等电子体的一种分子为(3)
 与
与 反应能生成
反应能生成 ,
, 中的配位原子为
中的配位原子为(4)乙醛(
 )中碳原子的轨道杂化类型是
)中碳原子的轨道杂化类型是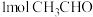 中含有
中含有 键的数目为
键的数目为 。
。(5)一个
 晶胞(见图)中,
晶胞(见图)中, 原子的数目为
原子的数目为
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
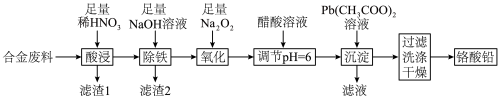
【推荐3】铬酸铅(PbCrO4)是黄色涂料“铬黄”的主要成分,实验室由某合金废料(主要成分为Fe、C、Cr2O3)制备PbCrO4的流程如图:
回答下列问题:
(1)基态82Pb2+的价层电子排布图为_______ 。
(2)“酸浸”时,加热可以加快反应速率,但温度不宜过高的原因是_______ (用化学方程式解释)。
(3)“滤渣2”中电负性最大的元素是_______ (填元素符号)。
(4)“氧化”时发生反应的离子方程式为_______ 。
(5)“调节pH=6”的目的是_______ 。
(6)二卤化铅(PbX2)是一类重要的含铅化合物,其熔点如下表所示:
①结合PbX2的熔点变化规律,可推断:依F、Cl、Br、I次序,PbX2中的化学键的离子性_______ (填“增强”“不变”或“减弱”,后同)、共价性_______ 。
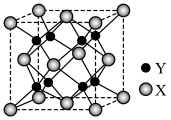
②PbF2的立方晶胞如图所示,其中X代表的离子是_______ (填离子符号);若该晶胞参数为anm,则正、负离子的最小核间距为_______ pm。
回答下列问题:
(1)基态82Pb2+的价层电子排布图为
(2)“酸浸”时,加热可以加快反应速率,但温度不宜过高的原因是
(3)“滤渣2”中电负性最大的元素是
(4)“氧化”时发生反应的离子方程式为
(5)“调节pH=6”的目的是
(6)二卤化铅(PbX2)是一类重要的含铅化合物,其熔点如下表所示:
| 二卤化铅 | PbF2 | PbCl2 | PbBr2 | PbI2 |
| 熔点/℃ | 824 | 501 | 373 | 402 |
②PbF2的立方晶胞如图所示,其中X代表的离子是
您最近一年使用:0次



