2023年诺贝尔化学奖授予蒙吉·G·巴文迪等三位科学家,以表彰他们在发现和合成量子点方面所作出的贡献,碳量子点是一类具有显著荧光性能的零维碳纳米材料,其结构如图所示。回答下列问题:_______ 区,图中C的杂化方式为_______ 。
(2)碳量子点结构包含的元素中电负性由大到小排列为:_______ 。
(3)碳量子点水溶性_______ (选填“>”“<”“=”)石墨水溶性,理由是:_______ 。
(4)高压合成金刚石的原料是廉价的石墨,用高压釜持续施加高温高压并加入金属镍等金属催化剂,石墨可转化为金刚石。基态镍原子核外电子的空间运动状态有_______ 种,比较二者C-C共价键的键长:石墨_______ 金刚石(选填“>”“<”“=”)。
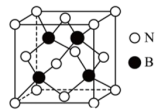
(5)氮化硼(BN)是一种性能优异、潜力巨大的新型材料,其中一种结构为立方氮化硼(如图),类似于金刚石。_______ ,则立方氮化硼晶体密度为_______ g·cm-3(列出计算式,阿伏加德罗常数的值为NA)。

(2)碳量子点结构包含的元素中电负性由大到小排列为:
(3)碳量子点水溶性
(4)高压合成金刚石的原料是廉价的石墨,用高压釜持续施加高温高压并加入金属镍等金属催化剂,石墨可转化为金刚石。基态镍原子核外电子的空间运动状态有
(5)氮化硼(BN)是一种性能优异、潜力巨大的新型材料,其中一种结构为立方氮化硼(如图),类似于金刚石。
更新时间:2024-04-28 08:17:11
|
相似题推荐
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐1】我国科学家是近成功合成了世界上首个五氮阴离子盐 (用R代表)。回答下列问题:
(用R代表)。回答下列问题:
(1)氮原子价层电子的轨道表达式(电子排布图)为_______ ,其能量最高的电子排布的轨道呈_______ 形。
(2)经X射线辐射测得化合物R的晶体结构,其局部结构如图所示。
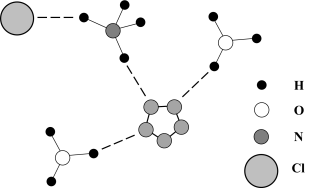
①从结构角度分析,R中两种阳离子的相同之处为_______ ,不同之处为_______ (填标号)
A.中心原子的杂化类型 B.中心原子的价层电子对数
C.立体结构 D.共价键类型
②R中阴离子 中的σ键总数为
中的σ键总数为_______ 个。分子中的大π键可用符号 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为
表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为 ),则
),则 中的大π键应表示为
中的大π键应表示为_______ 。
③比较键角: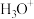
_______  ,并用物质结构的观点解释原因:
,并用物质结构的观点解释原因:_______ 。
④元素H、O、N的电负性由小到大的顺序_______ 。
 (用R代表)。回答下列问题:
(用R代表)。回答下列问题:(1)氮原子价层电子的轨道表达式(电子排布图)为
(2)经X射线辐射测得化合物R的晶体结构,其局部结构如图所示。

①从结构角度分析,R中两种阳离子的相同之处为
A.中心原子的杂化类型 B.中心原子的价层电子对数
C.立体结构 D.共价键类型
②R中阴离子
 中的σ键总数为
中的σ键总数为 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为
表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为 ),则
),则 中的大π键应表示为
中的大π键应表示为③比较键角:
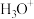
 ,并用物质结构的观点解释原因:
,并用物质结构的观点解释原因:④元素H、O、N的电负性由小到大的顺序
您最近半年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐2】A、B、C、D、E、F为前四周期元素且原子序数依次增大,其中基态A原子的电子分布在3个能级,且每个能级所含的电子数相同;C的原子核外最外层有 6 个运动状态不同的电子;D是短周期元素中电负性最小的元素;E的最高价氧化物的水化物酸性最强;基态F原子核外最外层只有一个电子,其余能层均充满电子。G元素与D元素同主族,且相差3个周期。
(1)下列物质的性质与氢键有关的是_______ 。
a.可燃冰的形成 b. A的氢化物的沸点 c. B的氢化物的热稳定性
(2)E的最高价含氧酸中 E 原子的杂化方式为_______ 。 基态 E 原子中,核外电子占据最高能级的电子云轮廓形状为_______ 。
(3)F原子的外围电子排布式为_______ 。
(4)已知元素 A、B形成的(AB)2分子中所有原子都满足8电子稳定结构,则其分子中σ键与π键数目之比为_______ 。
(5)通常情况下,D单质的熔沸点比G单质高,原因是_______ 。
(6)已知 DE 晶体的晶胞如图所示:
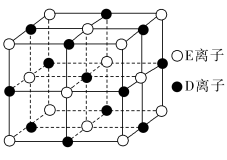
若将 DE 晶胞中的所有 E 离子去掉,并将 D 离子全部换为 A 原子,再在其中的 4 个“小立方体”中心各放置一个A 原子,且这 4 个“小立方体”不相邻。位于“小立方体”中的 A 原子与最近的 4 个 A 原子以单键相连,由此表示A的一种晶体的晶胞(已知 A−A 键的键长为a cm, NA表示阿伏加德罗常数),则该晶胞中含有_______ 个 A 原子,该晶体的密度是_______ g·cm-3(列式表示)。
(1)下列物质的性质与氢键有关的是
a.可燃冰的形成 b. A的氢化物的沸点 c. B的氢化物的热稳定性
(2)E的最高价含氧酸中 E 原子的杂化方式为
(3)F原子的外围电子排布式为
(4)已知元素 A、B形成的(AB)2分子中所有原子都满足8电子稳定结构,则其分子中σ键与π键数目之比为
(5)通常情况下,D单质的熔沸点比G单质高,原因是
(6)已知 DE 晶体的晶胞如图所示:

若将 DE 晶胞中的所有 E 离子去掉,并将 D 离子全部换为 A 原子,再在其中的 4 个“小立方体”中心各放置一个A 原子,且这 4 个“小立方体”不相邻。位于“小立方体”中的 A 原子与最近的 4 个 A 原子以单键相连,由此表示A的一种晶体的晶胞(已知 A−A 键的键长为a cm, NA表示阿伏加德罗常数),则该晶胞中含有
您最近半年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐3】硼的化合物在生产、生活和科研中应用广泛。回答下列问题:
(1)基态硼原子的电子排布图为:_____ ;B、N、H的电负性由大到小的顺序为_____ 。
(2)科学家合成了一种含硼阴离子[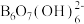 ],其结构如图1所示。其中硼原子的杂化方式为
],其结构如图1所示。其中硼原子的杂化方式为_______ ,该结构中共有_______ 种不同化学环境的氧原子。

图1
(3) 与
与 结合形成固态化合物
结合形成固态化合物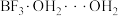 ,该物质在6.2℃时熔化电离出
,该物质在6.2℃时熔化电离出 和一种含硼阴离子
和一种含硼阴离子_______ (填离子符号); 空间构型为
空间构型为_______ 。
(1)基态硼原子的电子排布图为:
(2)科学家合成了一种含硼阴离子[
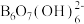 ],其结构如图1所示。其中硼原子的杂化方式为
],其结构如图1所示。其中硼原子的杂化方式为
图1
(3)
 与
与 结合形成固态化合物
结合形成固态化合物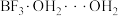 ,该物质在6.2℃时熔化电离出
,该物质在6.2℃时熔化电离出 和一种含硼阴离子
和一种含硼阴离子 空间构型为
空间构型为
您最近半年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐1】KZnF3被认为是良好的光学基质材料,可由K2CO3、ZnF2、NH4HF2制备。回答下列问题:
(1)基态F原子的价电子轨道表达式为_______ ;基态Zn原子核外占据最高能层电子的电子云轮廓图形状为_______ 。
(2)NH4HF2的组成元素的电负性由大到小的顺序为_______ (用元素符号表示);其中N原子的杂化方式为_______ ;HF能形成分子缔合体(HF)n的原因为_______ 。
(3)ZnF2具有金红石型四方结构,KZnF3具有钙钛矿型立方结构,两种晶体的晶胞结构如图所示:

①ZnF2和KZnF3晶体(晶胞顶点为K+ )中,Zn的配位数之比为_______ ;
②若NA表示阿伏加德罗常数的值,则ZnF2晶体的密度为_______ g/cm3(用含a、c、NA的代数式表示)。
(1)基态F原子的价电子轨道表达式为
(2)NH4HF2的组成元素的电负性由大到小的顺序为
(3)ZnF2具有金红石型四方结构,KZnF3具有钙钛矿型立方结构,两种晶体的晶胞结构如图所示:

①ZnF2和KZnF3晶体(晶胞顶点为K+ )中,Zn的配位数之比为
②若NA表示阿伏加德罗常数的值,则ZnF2晶体的密度为
您最近半年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐2】晶体的特殊性质是科学家不断研究和探索的新领域,根据你对晶体的认识,回答下列问题。
(1)一种发光二极管的半导体材料为GaAsxP1-x,该化合物中Ga、As、P的电负性从大到小的顺序为_______ 。
(2)下表列出了钠的卤化物和硅的卤化物的熔点:
从表中可以看出,钠的卤化物的熔点比相应的硅的卤化物的熔点高很多,请用所学知识简单解释:_______ 。
(3)磷化硼(BP)是受高度关注的耐磨材料,可作为金属表面的保护层,其结构与金刚石类似,晶胞结构如图所示。B的杂化类型为_______ 。磷化硼晶胞沿z轴在xy平面的投影图中,B原子构成的几何形状是_______ 。已知晶胞边长为458pm,假设 是阿伏加德罗常数的值,则磷化硼晶体的密度是
是阿伏加德罗常数的值,则磷化硼晶体的密度是_______ g•cm-3(列出计算式)。
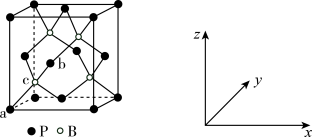
(4)原子坐标参数可表示晶胞内部各原子的相对位置。上图中原子坐标参数a为(0,0,0),b为( ,0,
,0, ),则c原子的坐标参数为
),则c原子的坐标参数为_______ 。
(1)一种发光二极管的半导体材料为GaAsxP1-x,该化合物中Ga、As、P的电负性从大到小的顺序为
(2)下表列出了钠的卤化物和硅的卤化物的熔点:
| NaX | NaF | NaCl | NaBr | NaI |
| 熔点/℃ | 995 | 801 | 775 | 651 |
| SiX4 | SiF4 | SiCl4 | SiBr4 | SiI4 |
| 熔点/℃ | -90.2 | -70.4 | 5.2 | 120.5 |
(3)磷化硼(BP)是受高度关注的耐磨材料,可作为金属表面的保护层,其结构与金刚石类似,晶胞结构如图所示。B的杂化类型为
 是阿伏加德罗常数的值,则磷化硼晶体的密度是
是阿伏加德罗常数的值,则磷化硼晶体的密度是
(4)原子坐标参数可表示晶胞内部各原子的相对位置。上图中原子坐标参数a为(0,0,0),b为(
 ,0,
,0, ),则c原子的坐标参数为
),则c原子的坐标参数为
您最近半年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐3】下图为元素周期表的一部分:

I.(1)元素③的基态原子轨道表示式为_________________ 。
(2)元素③④⑤的第一电离能由大到小的顺序为___________ (填元素符号)。
(3)以下组合的原子间反应最容易形成离子键的是_____ (选填A、B、C、D,下同)。
A.②和⑤ B.和⑤ C.⑤和⑥ D.⑥和⑧
(4)某些不同族元素的性质也有一定的相似性,如上表中元素⑦与元素②的单质及其化合物有相似的性质.写出元素②的最高价氧化物与NaOH溶液反应的离子方程式_________________________________ 。
II.(1)如图是部分元素原子的第一电离能I1随原子序数变化关系(其中12号至17号元素的有关数据缺失)。
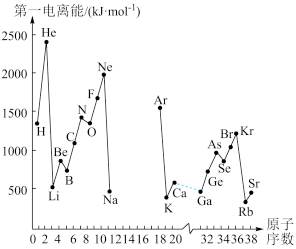
①根据同图示变化规律,可推测S的第一电离能的大小(最小)范围为___ < S <___ (填元素符号)
②图中第一电离能最小的元素在周期表中的位置____________________
(2)用In表示元素的第n电离能,则图中的a、b、c分别代表( )
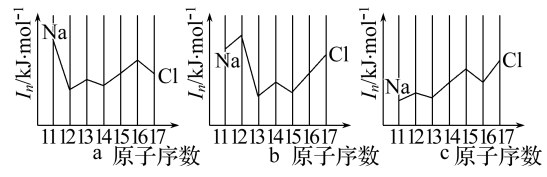
A.a为I1、b为I2、c为I3 B.a为I3、b为I2、c为I1
C.a为I2、b为I3、c为I1 D.a为I1、b为I3、c为I2
(3)铜、锌两种元素的第一电离能、第二电离能如表所示
铜的第一电离能(I1)小于锌的第一电离能,而铜的第二电离能(I2)却大于锌的第二电离能,其主要原因是______________________________________________________

I.(1)元素③的基态原子轨道表示式为
(2)元素③④⑤的第一电离能由大到小的顺序为
(3)以下组合的原子间反应最容易形成离子键的是
A.②和⑤ B.和⑤ C.⑤和⑥ D.⑥和⑧
(4)某些不同族元素的性质也有一定的相似性,如上表中元素⑦与元素②的单质及其化合物有相似的性质.写出元素②的最高价氧化物与NaOH溶液反应的离子方程式
II.(1)如图是部分元素原子的第一电离能I1随原子序数变化关系(其中12号至17号元素的有关数据缺失)。

①根据同图示变化规律,可推测S的第一电离能的大小(最小)范围为
②图中第一电离能最小的元素在周期表中的位置
(2)用In表示元素的第n电离能,则图中的a、b、c分别代表

A.a为I1、b为I2、c为I3 B.a为I3、b为I2、c为I1
C.a为I2、b为I3、c为I1 D.a为I1、b为I3、c为I2
(3)铜、锌两种元素的第一电离能、第二电离能如表所示
| 电离能/kJ/mol | I1 | I2 |
| Cu | 746 | 1958 |
| Zn | 906 | 1733 |
铜的第一电离能(I1)小于锌的第一电离能,而铜的第二电离能(I2)却大于锌的第二电离能,其主要原因是
您最近半年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐1】金属钛被誉为“二十一世纪金属”,有“生物金属,海洋金属,太空金属”的美称,具有广泛的应用前景。回答下列问题:
(1)钛原子核外电子有_____ 种空间运动状态;Ti2+电子占据的最高能层的电子排布式为______ 。
(2)磷酸钛铝锂可用作锂离子电池的正极材料,PO 的空间构型是
的空间构型是_____ ,第一电离能介于Al、P之间的第三周期元素为______ (填元素符号)。
(3)Ti(BH4)2是一种储氢材料,其中电负性最小的元素为______ ,B原子的杂化方式是_____ ,其中的 可由BH3和H-结合而成。
可由BH3和H-结合而成。 含有
含有______ 。(填序号)
①σ键 ②π键 ③氢键 ④配位键 ⑤离子键
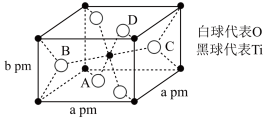
(4)TiO2在自然界中有三种同素异形态,即金红石型、锐钛型和斜钛型三种,其中金红石型是三种变体中最稳定的一种,其晶胞如图所示,该晶体的密度为_____ g•cm-3(设阿伏伽德罗常数的值为NA,用含a、b、NA的代数式表示)。
(1)钛原子核外电子有
(2)磷酸钛铝锂可用作锂离子电池的正极材料,PO
 的空间构型是
的空间构型是(3)Ti(BH4)2是一种储氢材料,其中电负性最小的元素为
 可由BH3和H-结合而成。
可由BH3和H-结合而成。 含有
含有①σ键 ②π键 ③氢键 ④配位键 ⑤离子键
(4)TiO2在自然界中有三种同素异形态,即金红石型、锐钛型和斜钛型三种,其中金红石型是三种变体中最稳定的一种,其晶胞如图所示,该晶体的密度为

您最近半年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐2】卤素单质及其化合物在科研和工农业生产中有着广泛的应用。回答下列问题:
(1)氟原子激发态的电子排布式有___________ (填标号)。
A.1s22s22p43s1 B.1s22s22p43d2 C.1s22s22p5
(2)基态Br原子核外电子占据最高能级的轨道形状为___________ 。
(3)X射线衍射测定等发现,I3AsF6中存在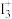 离子。
离子。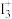 中心原子的杂化方式为
中心原子的杂化方式为___________ 。
(4)1-氯乙烯(C2H3Cl)分子中,C的一个___________ 杂化轨道与Cl的3px轨道形成C-Cl___________ 键,
(5)O、F、Cl电负性由大到小的顺序为___________ ,OF2分子的空间结构为___________ ;OF2的熔、沸点低于Cl2O,原因是___________ 。
(1)氟原子激发态的电子排布式有
A.1s22s22p43s1 B.1s22s22p43d2 C.1s22s22p5
(2)基态Br原子核外电子占据最高能级的轨道形状为
(3)X射线衍射测定等发现,I3AsF6中存在
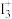 离子。
离子。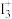 中心原子的杂化方式为
中心原子的杂化方式为(4)1-氯乙烯(C2H3Cl)分子中,C的一个
(5)O、F、Cl电负性由大到小的顺序为
您最近半年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
【推荐3】锑白( ,性质类似
,性质类似 )可用作白色颜料和阻燃剂。一种从含锑工业废渣(主要成分是
)可用作白色颜料和阻燃剂。一种从含锑工业废渣(主要成分是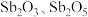 ,含有CuO、
,含有CuO、 和
和 等杂质)中制取
等杂质)中制取 的工业流程如下图所示:
的工业流程如下图所示:
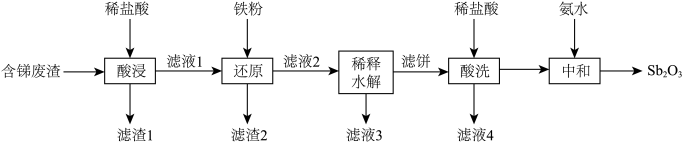
回答下列问题:
(1)锑元素原子序数为51,基态锑原子的价电子轨道表示式为___________ 。
(2)“还原”加入过量铁粉的目的是___________ (填序号)。
a.将 转化为
转化为 b.将
b.将 转化为
转化为 c.将铜离子转化为铜单质
c.将铜离子转化为铜单质
(3)“滤饼”的成分是SbOCl,“稀释水解”主要反应的离子方程式为___________ ;该操作中需要搅拌的原因是___________ 。
(4)“酸洗”后检验沉淀是否洗净的试剂是___________ (填名称)。
(5)“中和”时生成 的化学方程式为
的化学方程式为___________ ,“中和”时不宜将氨水换成氢氧化钠溶液,原因是___________ 。
(6)我国锑的蕴藏量占世界第一位,而锑的化合物也用途广泛。
氟锑酸化学式为 ,酸性比纯硫酸强
,酸性比纯硫酸强 倍,称为超强酸,其与HF作用生成
倍,称为超强酸,其与HF作用生成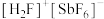 ,则其阳离子的空间结构为
,则其阳离子的空间结构为___________ ,阴离子中心原子的杂化方式合理的是___________ 。
a. b.
b. c.
c. d.
d.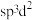
 ,性质类似
,性质类似 )可用作白色颜料和阻燃剂。一种从含锑工业废渣(主要成分是
)可用作白色颜料和阻燃剂。一种从含锑工业废渣(主要成分是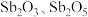 ,含有CuO、
,含有CuO、 和
和 等杂质)中制取
等杂质)中制取 的工业流程如下图所示:
的工业流程如下图所示:
回答下列问题:
(1)锑元素原子序数为51,基态锑原子的价电子轨道表示式为
(2)“还原”加入过量铁粉的目的是
a.将
 转化为
转化为 b.将
b.将 转化为
转化为 c.将铜离子转化为铜单质
c.将铜离子转化为铜单质(3)“滤饼”的成分是SbOCl,“稀释水解”主要反应的离子方程式为
(4)“酸洗”后检验沉淀是否洗净的试剂是
(5)“中和”时生成
 的化学方程式为
的化学方程式为(6)我国锑的蕴藏量占世界第一位,而锑的化合物也用途广泛。
氟锑酸化学式为
 ,酸性比纯硫酸强
,酸性比纯硫酸强 倍,称为超强酸,其与HF作用生成
倍,称为超强酸,其与HF作用生成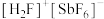 ,则其阳离子的空间结构为
,则其阳离子的空间结构为a.
 b.
b. c.
c. d.
d.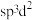
您最近半年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐1】Fe、Co、Ni是第四周期的重要的金属元素,回答下列问题:
(1)FeCoOx是一种新型光电催化剂,第四电离能大小关系是I4(Fe)_____ I4(Co)(填“>”“<”或“=”),原因是____________________ 。
(2)二茂铁是一种具有芳香族性质的有机过渡金属化合物。其在工业、农业、医药、航天、节能、环保等行业具有广泛的应用。环戊二烯可用于制备二茂铁。
①环戊二烯中碳原子的杂化方式为____________
②1mol环戊二烯中有__________ molσ键。
(3)①FeS2晶体的晶胞如图甲所示。已知其晶体密度为ρg·cm-3,阿伏加德罗常数的值为NA,晶胞边长__________ nm。
②该晶胞中Fe2+位于S 所形成的正八面体的体心,则正八面体的边长为
所形成的正八面体的体心,则正八面体的边长为______ nm
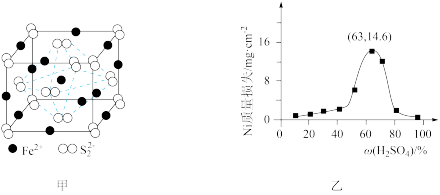
(4)基态Ni2+的价电子排布图为________ 。在一定温度下将Ni片与不同质量分数的硫酸反应,4h后的Ni的质量损失情况如图乙所示,发现当硫酸质量分数大于63%时Ni被腐蚀的速率逐渐降低,其可能原因为__________________ 。
(1)FeCoOx是一种新型光电催化剂,第四电离能大小关系是I4(Fe)
(2)二茂铁是一种具有芳香族性质的有机过渡金属化合物。其在工业、农业、医药、航天、节能、环保等行业具有广泛的应用。环戊二烯可用于制备二茂铁。
①环戊二烯中碳原子的杂化方式为
②1mol环戊二烯中有
(3)①FeS2晶体的晶胞如图甲所示。已知其晶体密度为ρg·cm-3,阿伏加德罗常数的值为NA,晶胞边长
②该晶胞中Fe2+位于S
 所形成的正八面体的体心,则正八面体的边长为
所形成的正八面体的体心,则正八面体的边长为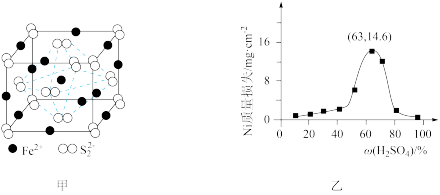
(4)基态Ni2+的价电子排布图为
您最近半年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐2】75号元素铼Re,熔点仅次于钨,是制造航空发动机的必需元素。地壳中铼的含量极低,多伴生于钼、铜、锌、铅等矿物中。回答下列问题:
(1)锰原子价层电子的轨道表示式为__ ,锰处于周期表的__ 区。
(2)与铼伴生的铜能形成多种配合物。如:醋酸二氨合铜(I)[Cu(NH3)2]Ac可用于吸收合成氨中对催化剂有害的CO气体:[Cu(NH3)2]Ac+CO+NH3 [Cu(NH3)3]Ac·CO。(Ac表示醋酸根)
[Cu(NH3)3]Ac·CO。(Ac表示醋酸根)
①与铜离子形成配合物的分子或离子应具备的结构特征是__ 。
②醋酸根中C原子的杂化类型为__ ,1mol配离子[Cu(NH3)2]+中含有σ键的数目为__ 。
③写出与NH3互为等电子体的一种离子的化学式__ 。
(3)锰与铼处于同一族,金属铼的熔点高于锰,原因是___ 。
(4)三氧化铼为立方晶胞,晶胞参数为apm,三氧化铼的摩尔质量为Mg/mol;铼原子占据顶点,氧原子占据所有棱心。则铼原子的配位数为__ ,铼原子填在了氧原子围成的空隙中___ (填“四面体”“立方体”或“八面体”),三氧化铼的密度为__ g/cm3。(用NA表示阿伏加 德罗常数的值)
(1)锰原子价层电子的轨道表示式为
(2)与铼伴生的铜能形成多种配合物。如:醋酸二氨合铜(I)[Cu(NH3)2]Ac可用于吸收合成氨中对催化剂有害的CO气体:[Cu(NH3)2]Ac+CO+NH3
 [Cu(NH3)3]Ac·CO。(Ac表示醋酸根)
[Cu(NH3)3]Ac·CO。(Ac表示醋酸根)①与铜离子形成配合物的分子或离子应具备的结构特征是
②醋酸根中C原子的杂化类型为
③写出与NH3互为等电子体的一种离子的化学式
(3)锰与铼处于同一族,金属铼的熔点高于锰,原因是
(4)三氧化铼为立方晶胞,晶胞参数为apm,三氧化铼的摩尔质量为Mg/mol;铼原子占据顶点,氧原子占据所有棱心。则铼原子的配位数为
您最近半年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐3】铁(Fe)、钴(Co)、铬(Ni)是第四周期第VⅢ族的元素,在化学上称为铁系元素,其化合物在生产生活中应用广泛。
(1)基态Co原子的核外电子排布式为___________ 。
(2)铁系元素能与CO形成 、
、 等金属羰基化合物。已知室温时
等金属羰基化合物。已知室温时 为浅黄色液体,沸点103℃,则
为浅黄色液体,沸点103℃,则 中含有的化学键类型包括___________。
中含有的化学键类型包括___________。
(3)以甲醇为溶剂, 可与色胺酮分子配位结合形成对DNA具有切割作用的色胺酮钴配合物(合成过程如下所示)。
可与色胺酮分子配位结合形成对DNA具有切割作用的色胺酮钴配合物(合成过程如下所示)。

①色胺酮分子中所含元素(C、N、O)第一电离能由小到大的顺序为___________ 。
②色氨酮分子中C原子的杂化类型为___________ 。
③X射线衍射分析显示色胺酮钴配合物晶胞中还含有一个CH3OH分子,CH3OH是通过___________ (填作用力)与色胺酮钴配合物相结合。
(4)Ge单晶具有金刚石型结构,其中Ge原子的杂化方式为___________ ,微粒之间存在的作用力是___________ 。
(5)晶胞有两个基本要素:
①原子坐标参数,表示晶胞内部各原子的相对位置。如图为Ge单晶的晶胞,其中原子坐标参数A为 ;B为
;B为 ;C为
;C为 。则D原子的坐标参数为
。则D原子的坐标参数为___________ 。
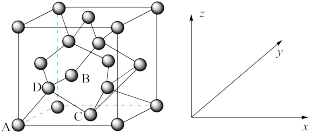
②晶胞参数,用于描述晶胞的大小和形状。已知Ge单晶的晶胞参数(棱长)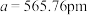 ,其密度为
,其密度为___________ g∙cm−3 (列出计算式即可,设NA为阿伏加德罗常数)。
(1)基态Co原子的核外电子排布式为
(2)铁系元素能与CO形成
 、
、 等金属羰基化合物。已知室温时
等金属羰基化合物。已知室温时 为浅黄色液体,沸点103℃,则
为浅黄色液体,沸点103℃,则 中含有的化学键类型包括___________。
中含有的化学键类型包括___________。| A.共价键 | B.离子键 | C.金属键 | D.配位键 |
 可与色胺酮分子配位结合形成对DNA具有切割作用的色胺酮钴配合物(合成过程如下所示)。
可与色胺酮分子配位结合形成对DNA具有切割作用的色胺酮钴配合物(合成过程如下所示)。
①色胺酮分子中所含元素(C、N、O)第一电离能由小到大的顺序为
②色氨酮分子中C原子的杂化类型为
③X射线衍射分析显示色胺酮钴配合物晶胞中还含有一个CH3OH分子,CH3OH是通过
(4)Ge单晶具有金刚石型结构,其中Ge原子的杂化方式为
(5)晶胞有两个基本要素:
①原子坐标参数,表示晶胞内部各原子的相对位置。如图为Ge单晶的晶胞,其中原子坐标参数A为
 ;B为
;B为 ;C为
;C为 。则D原子的坐标参数为
。则D原子的坐标参数为
②晶胞参数,用于描述晶胞的大小和形状。已知Ge单晶的晶胞参数(棱长)
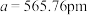 ,其密度为
,其密度为
您最近半年使用:0次



