(1)氟原子激发态的电子排布式有
A.1s22s22p43s1 B.1s22s22p43d2 C.1s22s22p5
(2)基态Br原子核外电子占据最高能级的轨道形状为
(3)X射线衍射测定等发现,I3AsF6中存在
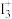 离子。
离子。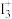 中心原子的杂化方式为
中心原子的杂化方式为(4)1-氯乙烯(C2H3Cl)分子中,C的一个
(5)O、F、Cl电负性由大到小的顺序为
相似题推荐
回答下列问题:
(1)R元素在元素周期表中的位置为
(2)元素的气态原子得到一个电子所放出的能量称为第一电子亲合能。气态原子结合电子越容易,电子亲合能越大。X和W的第一电子亲合能X
(3)X、Z、W的简单离子半径由大到小的顺序是
(4)Z单质与NaOH反应的离子反应方程式为
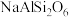 ,还含有其他多种金属阳离子。
,还含有其他多种金属阳离子。(1)
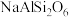 所含元素中,第一电离能最小的元素和电负性最大的元素组成的含有两种化学键的化合物的名称为:
所含元素中,第一电离能最小的元素和电负性最大的元素组成的含有两种化学键的化合物的名称为:(2)Al的电子排布式为
(3)配合物
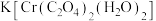 中的配体是:
中的配体是:(4)Ca、O、Cr可以形成一种具有特殊导电性的复合氧化物,晶胞结构如图所示,其中
 ,
, 采用面心立方最密堆积方式。
采用面心立方最密堆积方式。
①该晶体的化学式为:
②已知钙离子、氧离子半径分别为apm、bpm,该晶胞的参数(边长)为
(5)Ga可以形成
 等一系列配位数为6的配合物,向上述某物质的溶液中加入足量
等一系列配位数为6的配合物,向上述某物质的溶液中加入足量 溶液,有沉淀生成;过滤后,充分加热滤液有氨气逸出,且又有沉淀生成,两次沉淀的物质的量之比为1:2.则该溶液中溶质的化学式为
溶液,有沉淀生成;过滤后,充分加热滤液有氨气逸出,且又有沉淀生成,两次沉淀的物质的量之比为1:2.则该溶液中溶质的化学式为(1)A元素基态原子的最外层有2个未成对电子,次外层有2个电子,其元素符号为
(2)B元素的原子最外层电子排布式为
 ,其元素符号为
,其元素符号为(3)C元素基态的正三价离子的3d轨道为半充满(即有5个电子),其元素符号为
(4)D元素基态原子的M层全充满;N层没有成对电子,只有一个未成对电子。D的元素符号为
(5)E、F元素的基态原子都只有一个未成对电子;它们相互作用形成的离子的电子层结构相同,并且最高能级的电子对数等于其最高能层的电子层数。E、F的元素符号分别为
(1)微生物法脱硫
富含有机物的弱酸性废水在SBR细菌作用下产生
 、
、 等物质,可将废水中
等物质,可将废水中 还原为
还原为 ,同时用
,同时用 或
或 将
将 从水中吹出,再用碱液吸收。
从水中吹出,再用碱液吸收。①
 的空间构型为
的空间构型为②
 与
与 在SBR细菌作用下生成
在SBR细菌作用下生成 和
和 的离子方程式为
的离子方程式为③将
 从水中吹出时,用
从水中吹出时,用 比
比 效果更好,其原因是
效果更好,其原因是(2)吸收法脱硫
烟气中的
 可以用“亚硫酸铵吸收法”处理,发生的反应为
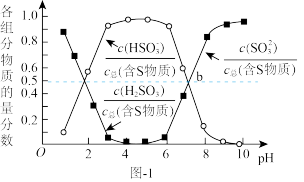
可以用“亚硫酸铵吸收法”处理,发生的反应为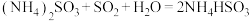 ,测得25℃时溶液pH与各组分物质的量分数的变化关系如图-1所示。b点时溶液
,测得25℃时溶液pH与各组分物质的量分数的变化关系如图-1所示。b点时溶液 ,则
,则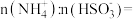
(3)电解法脱硫
用NaOH吸收后
 ,所得
,所得 溶液经电解后可制取
溶液经电解后可制取 溶液,反应装置如图-2所示。电解时每有1 mol
溶液,反应装置如图-2所示。电解时每有1 mol  生成有
生成有 透过质子交换膜。
透过质子交换膜。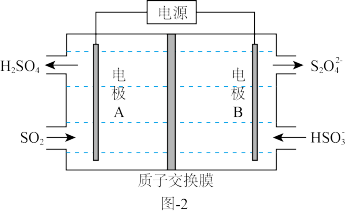
(4)还原法脱氮
用催化剂协同纳米零价铁去除水体中
 。其催化还原反应的过程如图-3所示。
。其催化还原反应的过程如图-3所示。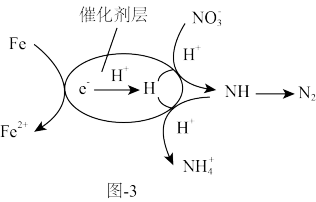
①该反应机理中生成
 的过程可描述为
的过程可描述为②过程中
 去除率及
去除率及 生成率如图-4所示,为有效降低水体中氮元素的含量,宜调整水体pH为4.2,当
生成率如图-4所示,为有效降低水体中氮元素的含量,宜调整水体pH为4.2,当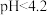 时,随pH减小,
时,随pH减小, 生成率逐渐降低的原因是
生成率逐渐降低的原因是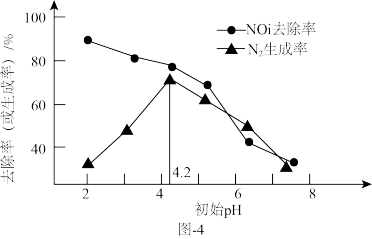
 。
。已知:①
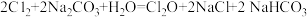 ;
;②
 ,反应温度为18~25℃;
,反应温度为18~25℃;③用水吸收
 (不含
(不含 )制得次氯酸溶液。
)制得次氯酸溶液。
(1)各装置的连接顺序为
(2)实验中控制氯气与空气体积比的方法是
(3)装置C应盛装
(4)产品浓度分析:取一定体积的E中溶液,加入
 溶液,充分反应。以淀粉溶液为指示剂,用标准
溶液,充分反应。以淀粉溶液为指示剂,用标准 溶液滴定,终点现象是
溶液滴定,终点现象是(5)HClO的VSEPR模型为
【推荐3】很长一段时间里,立方氮化硼被认为在自然界不存在,直至2009年,中国、美国、德国的科学家在中国青藏高原南部山区地下约306公里深处古海洋地壳的富铬岩内找到了这种矿物,其在大约1300°C、118430个大气压的条件下形成了晶体。该团队以中国科学家的名字将这种新矿物命名为青松矿(qingongite)。回答下列问题:
(1)基态B原子的电子排布式为
(2)以天然硼砂为原料,经如下流程可制得BF3和BN。
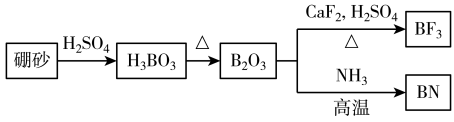
①在BF3分子中, B的杂化方式为
②H3BO3为一元酸,写出其在水溶液中的电离方程式
③BF3与NaF反应可制得NaBF4, BF 的立体构型为
的立体构型为
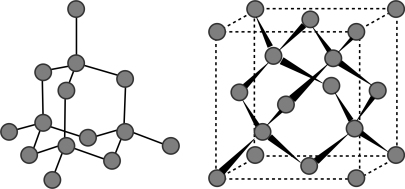
(3)立方氮化硼结构与金刚石类似( 金刚石的结构如图所示)。立方氮化硼的晶胞参数为361.5 pm。其中B-N键键长为
(1)磷酸根离子的空间构型为
(2)NH3分子中氮原子的轨道杂化类型是
(3)基态Fe2+与Fe3+离子中未成对的电子数之比为
 中与Fe2+配位的原子是
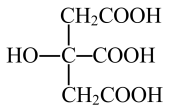
中与Fe2+配位的原子是(4)柠檬酸的结构简式如图。1 mol柠檬酸分子中碳原子与氧原子形成的σ键的数目为
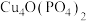 ,可通过下列反应制备:
,可通过下列反应制备: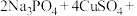
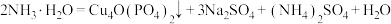 。
。(1)写出基态
 的电子排布式:
的电子排布式:(2)P、S元素第一电离能大小关系为
(3)氨基乙酸铜分子结构如图所示,碳原子的杂化方式为
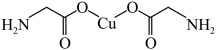
(4)在硫酸铜溶液中加入过量
 ,生成配合物
,生成配合物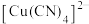 ,则
,则 该配合物含有
该配合物含有 键的数目为
键的数目为 表示阿伏加德罗常数的值)。
表示阿伏加德罗常数的值)。(5)晶体铜的晶胞结构如图甲所示,原子之间相对位置关系的平面图如图乙所示,铜原子的配位数为
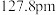 ,
, 表示阿伏加德罗常数的值,晶体铜的密度为
表示阿伏加德罗常数的值,晶体铜的密度为 (列出计算式即可)。
(列出计算式即可)。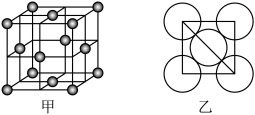
(1)下列有关微粒性质的排列顺序错误的是___________。
| A.元素的电负性:P<O<F | B.元素的第一电离能:C<N<O |
| C.离子半径:O2−>Na+>Mg2+ | D.原子的未成对电子数:Mn>Si>Cl |
(3)钌−多吡啶配合物具有丰富的光化学和光物理信息,结构简式如图所示。钌(II)的配位数是

(4)SO3的三聚体环状结构如图所示,该结构中S原子的杂化轨道类型为