次氯酸溶液是常用的消毒剂和漂白剂。将氯气和空气(不参与反应)按体积比1:3混合通入潮湿的碳酸钠中可以制得 。
。
已知:①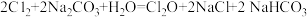 ;
;
② ,反应温度为18~25℃;
,反应温度为18~25℃;
③用水吸收 (不含
(不含 )制得次氯酸溶液。
)制得次氯酸溶液。

(1)各装置的连接顺序为___________ 。(每种装置只用一次)。
(2)实验中控制氯气与空气体积比的方法是___________ 。
(3)装置C应盛装___________ ,其主要作用是___________ 。
(4)产品浓度分析:取一定体积的E中溶液,加入___________ 以及一定量的稀 溶液,充分反应。以淀粉溶液为指示剂,用标准
溶液,充分反应。以淀粉溶液为指示剂,用标准 溶液滴定,终点现象是
溶液滴定,终点现象是___________ 。
(5)HClO的VSEPR模型为___________ ,其中氧原子的杂化方式为___________ ,其分子的空间结构为___________ 。
 。
。已知:①
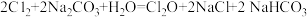 ;
;②
 ,反应温度为18~25℃;
,反应温度为18~25℃;③用水吸收
 (不含
(不含 )制得次氯酸溶液。
)制得次氯酸溶液。
(1)各装置的连接顺序为
(2)实验中控制氯气与空气体积比的方法是
(3)装置C应盛装
(4)产品浓度分析:取一定体积的E中溶液,加入
 溶液,充分反应。以淀粉溶液为指示剂,用标准
溶液,充分反应。以淀粉溶液为指示剂,用标准 溶液滴定,终点现象是
溶液滴定,终点现象是(5)HClO的VSEPR模型为
更新时间:2022-10-08 15:49:41
|
相似题推荐
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐1】I.回答下列问题:
(1)下列原子或离子的核外电子排布正确的是___________ ,违反能量最低原理的是___________ ,违反洪特规则的是___________ ,违反泡利不相容原理的是___________ 。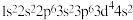 ⑤K:
⑤K: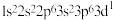 ⑥Mg:
⑥Mg:
(2)《中华本草》等中医典籍中,记载了炉甘石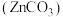 入药,可用于治疗皮肤炎症或表面创伤。Zn、C、O电负性由大至小的顺序是
入药,可用于治疗皮肤炎症或表面创伤。Zn、C、O电负性由大至小的顺序是___________ ,其阴离子的空间结构为___________ ,Zn位于元素周期表的___________ 区。
(3)基态锰原子有___________ 种空间运动状态的电子,锰有多种化合价,在+2、+3、+4、+5和+6中,最稳定的化合价是___________ 。
(4) 已知无水 固态时具有链状结构
固态时具有链状结构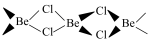 ,在二聚体分子(
,在二聚体分子(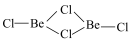 ),其中铍原子的杂化类型为
),其中铍原子的杂化类型为___________ 。
(1)下列原子或离子的核外电子排布正确的是
① :
: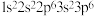 ②
② :
: ③P:
③P: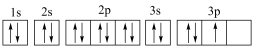
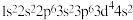 ⑤K:
⑤K: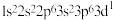 ⑥Mg:
⑥Mg:
⑦C: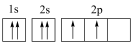
(2)《中华本草》等中医典籍中,记载了炉甘石
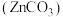 入药,可用于治疗皮肤炎症或表面创伤。Zn、C、O电负性由大至小的顺序是
入药,可用于治疗皮肤炎症或表面创伤。Zn、C、O电负性由大至小的顺序是(3)基态锰原子有
(4) 已知无水
 固态时具有链状结构
固态时具有链状结构 ,在二聚体分子(
,在二聚体分子( ),其中铍原子的杂化类型为
),其中铍原子的杂化类型为
您最近一年使用:0次
解答题-有机推断题
|
较易
(0.85)
名校
解题方法
【推荐2】I.乙烯是重要有机化工原料,以乙烯为原料合成部分化工产品的流程如下(部分反应条件略去)。
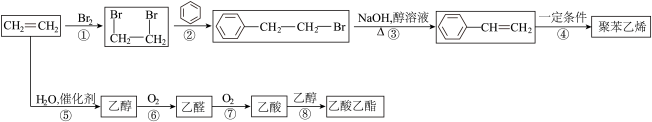
回答下列问题:
(1)乙酸的官能团的名称是___________ 。
(2)反应②的反应类型是___________ 。
(3)聚苯乙烯的结构简式为___________ 。
(4)反应⑧的化学方程式为___________ 。
Ⅱ.回答以下问题。
(5)基态Cu原子的核外电子排布式为___________ 。
(6)NH3的空间结构是___________ 。
(7)N和Cu元素形成的化合物的晶胞结构如图所示,该化合物的相对分子质量为M,NA为阿伏加德罗常数的值。若该晶胞的边长为apm,则该晶体的密度是___________ g·cm-3。
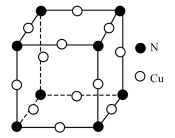

回答下列问题:
(1)乙酸的官能团的名称是
(2)反应②的反应类型是
(3)聚苯乙烯的结构简式为
(4)反应⑧的化学方程式为
Ⅱ.回答以下问题。
(5)基态Cu原子的核外电子排布式为
(6)NH3的空间结构是
(7)N和Cu元素形成的化合物的晶胞结构如图所示,该化合物的相对分子质量为M,NA为阿伏加德罗常数的值。若该晶胞的边长为apm,则该晶体的密度是

您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐3】填空。
(1)X、Y、Z、R代表四种短周期元素,X元素的基态原子电子排布式为1s1,Y元素的原子价电子排布为nsnnpn,Z元素位于第二周期且原子中p能级与所有s能级电子总数相等,R原子M电子层的p能级中有3个未成对电子。
①Z的基态原子的价电子排布式为_______ ;化合物X2Z分子的空间构型为_______ 形。
②Y2X2分子中,中心原子采用_______ 杂化,分子中σ键和π键个数之比为_______ ;按价层电子对互斥理论,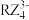 离子的VSEPR模型和立体构型均为
离子的VSEPR模型和立体构型均为_______ 形。
(2)金属氢化物是具有良好发展前景的储氢材料。
①LiH中,离子半径:Li+_______ H-(填“<”“>”或“=”)
②某储氢材料是短周期金属元素M的氢化物。M的部分电离能如下表所示,M的最高正价是_______ 。
③NaH具有NaCl型晶体结构,Na+的配位数为_______ ,Na+的堆积方式为_______ ,已知NaH晶体的晶胞参数;a=488pm,Na+半径为102pm,H-的半径为_______ cm。
(1)X、Y、Z、R代表四种短周期元素,X元素的基态原子电子排布式为1s1,Y元素的原子价电子排布为nsnnpn,Z元素位于第二周期且原子中p能级与所有s能级电子总数相等,R原子M电子层的p能级中有3个未成对电子。
①Z的基态原子的价电子排布式为
②Y2X2分子中,中心原子采用
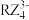 离子的VSEPR模型和立体构型均为
离子的VSEPR模型和立体构型均为(2)金属氢化物是具有良好发展前景的储氢材料。
①LiH中,离子半径:Li+
②某储氢材料是短周期金属元素M的氢化物。M的部分电离能如下表所示,M的最高正价是
| I₁/kJ·mol-1 | I₂/kJ·mol-1 | I₃/kJ·mol-1 | I₄/kJ·mol-1 | Is/kJ·mol-1 |
| 738 | 1451 | 7733 | 10540 | 13630 |
③NaH具有NaCl型晶体结构,Na+的配位数为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐1】铁及其化合物在生活中用途广泛,绿矾(FeSO4·7H2O)是一种常见的中草药成分,失水后可转为FeSO4·H2O,与FeS2可联合制备铁粉精(FexOy)和H2SO4。
i.FeSO4·H2O结构如图所示:

(1)Fe2+价层电子排布式为_________ 。
(2)比较 和
和 分子中的键角大小并给出相应解释:
分子中的键角大小并给出相应解释:_________ 。
(3) 与
与 和
和 之间的作用力分别为
之间的作用力分别为_________ 。
ii.实验室以 FeCl2溶液为原料制备高密度磁记录材料 Fe/Fe3O4复合物。
(4)在氩气气氛下,向装有50mL1mol•L−1FeCl2溶液的三颈烧瓶(装置如图)中逐滴加入 100mL14 mol∙L−1KOH溶液,用磁力搅拌器持续搅拌,在100℃下回流3h,得到成分为Fe和Fe3O4的黑色沉淀。
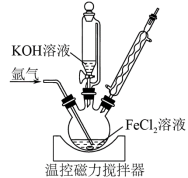
①三颈烧瓶发生反应的离子方程式为_________ 。
②检验反应是否进行完全的操作是_________ 。
(5)待三颈烧瓶中的混合物冷却后,过滤,再依次用沸水和乙醇洗涤,在40℃干燥后焙烧3h,得到Fe/Fe3O4复合物产品 3.24g。
①焙烧需在隔绝空气条件下进行,原因是_________ 。
②计算实验所得产品的产率_________ 。
i.FeSO4·H2O结构如图所示:

(1)Fe2+价层电子排布式为
(2)比较
 和
和 分子中的键角大小并给出相应解释:
分子中的键角大小并给出相应解释:(3)
 与
与 和
和 之间的作用力分别为
之间的作用力分别为ii.实验室以 FeCl2溶液为原料制备高密度磁记录材料 Fe/Fe3O4复合物。
(4)在氩气气氛下,向装有50mL1mol•L−1FeCl2溶液的三颈烧瓶(装置如图)中逐滴加入 100mL14 mol∙L−1KOH溶液,用磁力搅拌器持续搅拌,在100℃下回流3h,得到成分为Fe和Fe3O4的黑色沉淀。

①三颈烧瓶发生反应的离子方程式为
②检验反应是否进行完全的操作是
(5)待三颈烧瓶中的混合物冷却后,过滤,再依次用沸水和乙醇洗涤,在40℃干燥后焙烧3h,得到Fe/Fe3O4复合物产品 3.24g。
①焙烧需在隔绝空气条件下进行,原因是
②计算实验所得产品的产率
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐2】贫血的常用补铁剂.—葡萄糖酸亚铁[ ,易溶于水,
,易溶于水,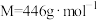 ]的合成前体是碳酸亚铁
]的合成前体是碳酸亚铁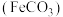 ,某实验小组用如图所示装置制备碳酸亚铁。
,某实验小组用如图所示装置制备碳酸亚铁。
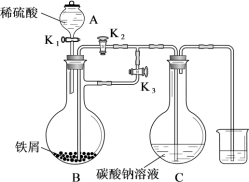
请回答下列问题:
(1)仪器A的名称为_______ ,仪器B中发生反应的离子方程式为_______ 。
(2)开始实验时,三个活塞的操作为先打开 和
和_______ (填“ ”或“
”或“ ”,下同),并关闭
”,下同),并关闭_______ ,这样操作的原因是_______ 。
(3)反应一段时间后,使蒸馏烧瓶中生成的硫酸亚铁溶液进入仪器C中的操作是_______ 。若碳酸亚铁置于空气中的时间过长,其表面呈红褐色,分析表面呈红褐色的原因:_______ 。(用化学方程式回答)
(4)以碳酸亚铁和葡萄糖酸为原料制备葡萄糖酸亚铁的反应方程式如下: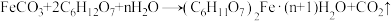 。为测定某
。为测定某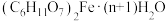 样品中n的值,现称取
样品中n的值,现称取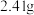 该晶体,在氢气气流中加热至完全分解,最终得到
该晶体,在氢气气流中加热至完全分解,最终得到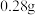 铁单质,则
铁单质,则
_______ 。
 ,易溶于水,
,易溶于水,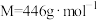 ]的合成前体是碳酸亚铁
]的合成前体是碳酸亚铁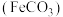 ,某实验小组用如图所示装置制备碳酸亚铁。
,某实验小组用如图所示装置制备碳酸亚铁。
请回答下列问题:
(1)仪器A的名称为
(2)开始实验时,三个活塞的操作为先打开
 和
和 ”或“
”或“ ”,下同),并关闭
”,下同),并关闭(3)反应一段时间后,使蒸馏烧瓶中生成的硫酸亚铁溶液进入仪器C中的操作是
(4)以碳酸亚铁和葡萄糖酸为原料制备葡萄糖酸亚铁的反应方程式如下:
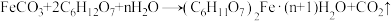 。为测定某
。为测定某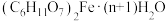 样品中n的值,现称取
样品中n的值,现称取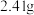 该晶体,在氢气气流中加热至完全分解,最终得到
该晶体,在氢气气流中加热至完全分解,最终得到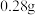 铁单质,则
铁单质,则
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
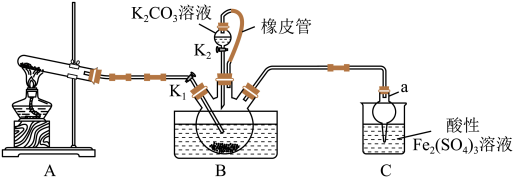
【推荐3】硫氰化钾(KSCN)是一种用途广泛的化工原料,常用于染料、药物的生产。实验小组设计如下实验装置模拟工业制备KSCN并进行相关探究实验。
已知:①CS2是一种不溶于水且密度大于水的非极性试剂。
②CS2+3NH3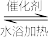 NH4SCN+NH4HS
NH4SCN+NH4HS
回答下列问题:
(1)SCN﹣的结构式为_______ 。
(2)装置A用于实验室制备氨气,反应的化学方程式为_______ 。
(3)装置B中,三颈烧瓶内盛放有CS2、水和固体催化剂,通入氨气的导管口需要插入CS2液体中,其目的是_______ (写两点)。
(4)待三颈烧瓶内液体不分层后,熄灭装置A处的酒精灯,关闭K1,移开水浴。将装置B继续加热至105℃,待NH4HS完全分解后(NH4HS NH3↑+H2S↑),打开K2,缓缓滴入适量的K2CO3溶液充分反应,(NH4)2CO3完全分解制得KSCN溶液。装置C中仪器a的名称是
NH3↑+H2S↑),打开K2,缓缓滴入适量的K2CO3溶液充分反应,(NH4)2CO3完全分解制得KSCN溶液。装置C中仪器a的名称是 _______ ,用离子方程式表示装置C处的烧杯中产生淡黄色浑浊的原因 _______ 。
(5)除去固体催化剂后,为使KSCN晶体充分析出并分离,采用的操作为减压蒸发、_______ 、过滤。

已知:①CS2是一种不溶于水且密度大于水的非极性试剂。
②CS2+3NH3
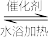 NH4SCN+NH4HS
NH4SCN+NH4HS回答下列问题:
(1)SCN﹣的结构式为
(2)装置A用于实验室制备氨气,反应的化学方程式为
(3)装置B中,三颈烧瓶内盛放有CS2、水和固体催化剂,通入氨气的导管口需要插入CS2液体中,其目的是
(4)待三颈烧瓶内液体不分层后,熄灭装置A处的酒精灯,关闭K1,移开水浴。将装置B继续加热至105℃,待NH4HS完全分解后(NH4HS
 NH3↑+H2S↑),打开K2,缓缓滴入适量的K2CO3溶液充分反应,(NH4)2CO3完全分解制得KSCN溶液。装置C中仪器a的名称是
NH3↑+H2S↑),打开K2,缓缓滴入适量的K2CO3溶液充分反应,(NH4)2CO3完全分解制得KSCN溶液。装置C中仪器a的名称是 (5)除去固体催化剂后,为使KSCN晶体充分析出并分离,采用的操作为减压蒸发、
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐1】医学上常将酸性高锰酸钾溶液和草酸溶液的反应用于测定血钙的含量。测定血钙的含量的方法是:取2mL血液用蒸馏水稀释后,向其中加入足量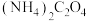 溶液,反应生成
溶液,反应生成 沉淀,将沉淀用稀硫酸溶解得到
沉淀,将沉淀用稀硫酸溶解得到 后,再用
后,再用 溶液滴定。回答下列问题:
溶液滴定。回答下列问题:
(1)用 溶液滴定待测液的反应原理为:
溶液滴定待测液的反应原理为:_______ (用离子方程式表示) 。该反应中的还原产物是_______ 。
(2)测定血钙的含量:
①稀硫酸溶解 沉淀的化学方程式是
沉淀的化学方程式是_______ 。
②溶解沉淀时_______ (能或不能)用稀盐酸,原因是_______ 。
③若滴定至终点时共消耗了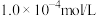 的
的 溶液20.00mL,则该血液中含钙
溶液20.00mL,则该血液中含钙_______ g/100mL
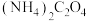 溶液,反应生成
溶液,反应生成 沉淀,将沉淀用稀硫酸溶解得到
沉淀,将沉淀用稀硫酸溶解得到 后,再用
后,再用 溶液滴定。回答下列问题:
溶液滴定。回答下列问题:(1)用
 溶液滴定待测液的反应原理为:
溶液滴定待测液的反应原理为:(2)测定血钙的含量:
①稀硫酸溶解
 沉淀的化学方程式是
沉淀的化学方程式是②溶解沉淀时
③若滴定至终点时共消耗了
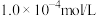 的
的 溶液20.00mL,则该血液中含钙
溶液20.00mL,则该血液中含钙
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
【推荐2】硫酸亚铁铵晶体[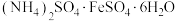 ]为浅蓝绿色,能溶于水、不溶于乙醇。在实验室中用铁屑来制备硫酸亚铁铵晶体的具体流程如下:
]为浅蓝绿色,能溶于水、不溶于乙醇。在实验室中用铁屑来制备硫酸亚铁铵晶体的具体流程如下:

回答下列问题:
(1)步骤①需要的玻璃仪器有烧杯、___________ 、___________ (填仪器名称)。
(2)制备硫酸亚铁过程加入炭黑的目的为___________ 。
(3)步骤②的具体操作为___________ 、___________ 、___________ 。
(4)“洗涤”包含水洗、醇洗,其中用乙醇洗涤的目的是___________ 。
(5)写出基态Fe原子的核外电子排布式:___________ 。
(6)称取16.0g制得的粗产品于100mL烧杯中,加入2mL3
 ,用少量水溶解,定容在100mL容量瓶中。准确移取20.00mL上述溶液于150mL锥形瓶中,加入5mL3
,用少量水溶解,定容在100mL容量瓶中。准确移取20.00mL上述溶液于150mL锥形瓶中,加入5mL3
 ,再用0.1
,再用0.1
 标准溶液滴定。平行滴定三次,平均消耗12.00mL
标准溶液滴定。平行滴定三次,平均消耗12.00mL 标准溶液,产品纯度为
标准溶液,产品纯度为___________ 。(写出计算过程,已知M[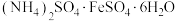 ]为392g/mol)
]为392g/mol)
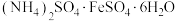 ]为浅蓝绿色,能溶于水、不溶于乙醇。在实验室中用铁屑来制备硫酸亚铁铵晶体的具体流程如下:
]为浅蓝绿色,能溶于水、不溶于乙醇。在实验室中用铁屑来制备硫酸亚铁铵晶体的具体流程如下:
回答下列问题:
(1)步骤①需要的玻璃仪器有烧杯、
(2)制备硫酸亚铁过程加入炭黑的目的为
(3)步骤②的具体操作为
(4)“洗涤”包含水洗、醇洗,其中用乙醇洗涤的目的是
(5)写出基态Fe原子的核外电子排布式:
(6)称取16.0g制得的粗产品于100mL烧杯中,加入2mL3

 ,用少量水溶解,定容在100mL容量瓶中。准确移取20.00mL上述溶液于150mL锥形瓶中,加入5mL3
,用少量水溶解,定容在100mL容量瓶中。准确移取20.00mL上述溶液于150mL锥形瓶中,加入5mL3
 ,再用0.1
,再用0.1
 标准溶液滴定。平行滴定三次,平均消耗12.00mL
标准溶液滴定。平行滴定三次,平均消耗12.00mL 标准溶液,产品纯度为
标准溶液,产品纯度为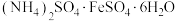 ]为392g/mol)
]为392g/mol)
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐3】草酸亚铁晶体(FeC2O4·xH2O)为淡黄色粉末,不溶于水,可作照相显影剂和用于制药工业。某化学兴趣小组对其定量探究,利用滴定实验测定x的值。
(1)滴定前,下列操作的正确顺序是_______ (填字母)。
a.用0.100 0 mol·L-1的酸性KMnO4溶液润洗滴定管;b.查漏、清洗;c.排尽滴定管尖嘴处的气泡并调整液面;d.盛装0.100 0 mol·L-1的酸性KMnO4溶液;e.记录初始读数为0.50 mL。
(2)称取n g样品,加入适量稀硫酸溶解,用准备的标准KMnO4溶液直接滴定,滴定终点时的现象为_______ 。
(3)终点读数为20.50 mL。结合上述实验数据求得x=_______ (用含n的代数式表示)。
(1)滴定前,下列操作的正确顺序是
a.用0.100 0 mol·L-1的酸性KMnO4溶液润洗滴定管;b.查漏、清洗;c.排尽滴定管尖嘴处的气泡并调整液面;d.盛装0.100 0 mol·L-1的酸性KMnO4溶液;e.记录初始读数为0.50 mL。
(2)称取n g样品,加入适量稀硫酸溶解,用准备的标准KMnO4溶液直接滴定,滴定终点时的现象为
(3)终点读数为20.50 mL。结合上述实验数据求得x=
您最近一年使用:0次



