工业上常用微生物法、吸收法、电解法、还原法等消除硫、氮等引起的污染。
(1)微生物法脱硫
富含有机物的弱酸性废水在SBR细菌作用下产生 、
、 等物质,可将废水中
等物质,可将废水中 还原为
还原为 ,同时用
,同时用 或
或 将
将 从水中吹出,再用碱液吸收。
从水中吹出,再用碱液吸收。
① 的空间构型为
的空间构型为_______ 。
② 与
与 在SBR细菌作用下生成
在SBR细菌作用下生成 和
和 的离子方程式为
的离子方程式为_______ 。
③将 从水中吹出时,用
从水中吹出时,用 比
比 效果更好,其原因是
效果更好,其原因是_______ 。
(2)吸收法脱硫
烟气中的 可以用“亚硫酸铵吸收法”处理,发生的反应为
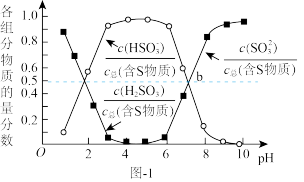
可以用“亚硫酸铵吸收法”处理,发生的反应为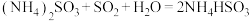 ,测得25℃时溶液pH与各组分物质的量分数的变化关系如图-1所示。b点时溶液
,测得25℃时溶液pH与各组分物质的量分数的变化关系如图-1所示。b点时溶液 ,则
,则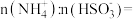
_______ 。
(3)电解法脱硫
用NaOH吸收后 ,所得
,所得 溶液经电解后可制取
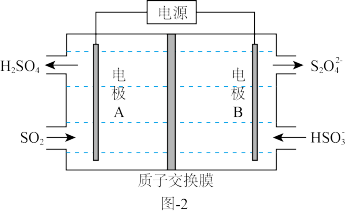
溶液经电解后可制取 溶液,反应装置如图-2所示。电解时每有1 mol
溶液,反应装置如图-2所示。电解时每有1 mol  生成有
生成有_______ mol  透过质子交换膜。
透过质子交换膜。
(4)还原法脱氮
用催化剂协同纳米零价铁去除水体中 。其催化还原反应的过程如图-3所示。
。其催化还原反应的过程如图-3所示。
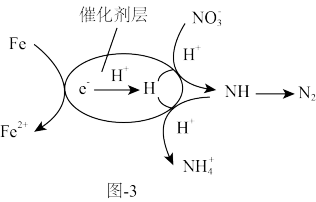
①该反应机理中生成 的过程可描述为
的过程可描述为_______ 。
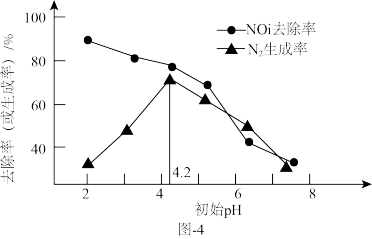
②过程中 去除率及
去除率及 生成率如图-4所示,为有效降低水体中氮元素的含量,宜调整水体pH为4.2,当
生成率如图-4所示,为有效降低水体中氮元素的含量,宜调整水体pH为4.2,当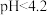 时,随pH减小,
时,随pH减小, 生成率逐渐降低的原因是
生成率逐渐降低的原因是_______ 。
(1)微生物法脱硫
富含有机物的弱酸性废水在SBR细菌作用下产生
 、
、 等物质,可将废水中
等物质,可将废水中 还原为
还原为 ,同时用
,同时用 或
或 将
将 从水中吹出,再用碱液吸收。
从水中吹出,再用碱液吸收。①
 的空间构型为
的空间构型为②
 与
与 在SBR细菌作用下生成
在SBR细菌作用下生成 和
和 的离子方程式为
的离子方程式为③将
 从水中吹出时,用
从水中吹出时,用 比
比 效果更好,其原因是
效果更好,其原因是(2)吸收法脱硫
烟气中的
 可以用“亚硫酸铵吸收法”处理,发生的反应为
可以用“亚硫酸铵吸收法”处理,发生的反应为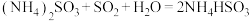 ,测得25℃时溶液pH与各组分物质的量分数的变化关系如图-1所示。b点时溶液
,测得25℃时溶液pH与各组分物质的量分数的变化关系如图-1所示。b点时溶液 ,则
,则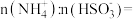

(3)电解法脱硫
用NaOH吸收后
 ,所得
,所得 溶液经电解后可制取
溶液经电解后可制取 溶液,反应装置如图-2所示。电解时每有1 mol
溶液,反应装置如图-2所示。电解时每有1 mol  生成有
生成有 透过质子交换膜。
透过质子交换膜。
(4)还原法脱氮
用催化剂协同纳米零价铁去除水体中
 。其催化还原反应的过程如图-3所示。
。其催化还原反应的过程如图-3所示。
①该反应机理中生成
 的过程可描述为
的过程可描述为②过程中
 去除率及
去除率及 生成率如图-4所示,为有效降低水体中氮元素的含量,宜调整水体pH为4.2,当
生成率如图-4所示,为有效降低水体中氮元素的含量,宜调整水体pH为4.2,当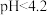 时,随pH减小,
时,随pH减小, 生成率逐渐降低的原因是
生成率逐渐降低的原因是
更新时间:2022-09-07 16:04:10
|
相似题推荐
解答题-工业流程题
|
较易
(0.85)
名校
解题方法
【推荐1】工业上从海水中获得纯净氯化钠溶液经过下列流程生产焦亚硫酸钠( ,能溶于水,在空气中容易被氧化),回答下列问题:
,能溶于水,在空气中容易被氧化),回答下列问题:
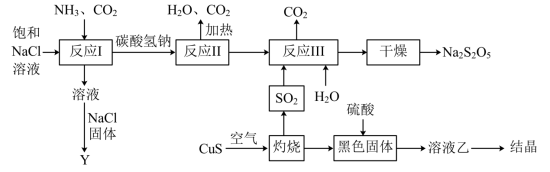
(1)反应I中应该先通入_______ ,反应I的离子方程式_______ 。
(2)从溶液乙中结晶得到纯净的CuSO4·5H2O具体操作是_______ 。
(3)该流程中,可以循环使用的是_______ 。
(4)灼烧的化学方程式为_______ 。
(5)已知 与稀硫酸反应生成
与稀硫酸反应生成 ,其离子方程式为
,其离子方程式为_______ 。焦亚硫酸钠常用作食物的抗氧化剂,在空气中容易被氧化而变质。要检验焦亚硫酸钠是否变质,具体的实验操作为_______ 。
 ,能溶于水,在空气中容易被氧化),回答下列问题:
,能溶于水,在空气中容易被氧化),回答下列问题:
(1)反应I中应该先通入
(2)从溶液乙中结晶得到纯净的CuSO4·5H2O具体操作是
(3)该流程中,可以循环使用的是
(4)灼烧的化学方程式为
(5)已知
 与稀硫酸反应生成
与稀硫酸反应生成 ,其离子方程式为
,其离子方程式为
您最近一年使用:0次
【推荐2】碱式硫酸铬[ ]主要用于鞣制皮革、作媒染剂及生产氢氧化铬和活性黑染料。以酸性含铬废液(主要含有
]主要用于鞣制皮革、作媒染剂及生产氢氧化铬和活性黑染料。以酸性含铬废液(主要含有 、
、 ,还含有少量
,还含有少量 、
、 、
、 )为原料制备碱式硫酸铬的工艺流程如图所示,回答下列问题:
)为原料制备碱式硫酸铬的工艺流程如图所示,回答下列问题:
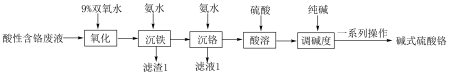
已知:常温下,部分金属阳离子开始沉淀和完全沉淀(离子浓度小于或等于 )时的pH如下表。
)时的pH如下表。
(1)Cr在元素周期表中的位置为_______ 。
(2)加入9%双氧水的作用是_______ (用离子方程式表示)。
(3)“沉铁”时调pH的范围为_______ ~_______ 。
(4)“沉铬”过程发生反应的离子方程式是_______ ,从滤液1中可回收一种氮肥,该物质是_______ (填化学式)。
(5)金属铬的晶胞结构如图,已知晶胞参数为anm。
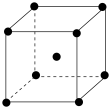
①该晶胞中含铬原子的个数为_______ 。
②铬原子的配位数为_______ 。
③铬原子之间的最短距离为_______ nm(用含a的代数式表示)。
 ]主要用于鞣制皮革、作媒染剂及生产氢氧化铬和活性黑染料。以酸性含铬废液(主要含有
]主要用于鞣制皮革、作媒染剂及生产氢氧化铬和活性黑染料。以酸性含铬废液(主要含有 、
、 ,还含有少量
,还含有少量 、
、 、
、 )为原料制备碱式硫酸铬的工艺流程如图所示,回答下列问题:
)为原料制备碱式硫酸铬的工艺流程如图所示,回答下列问题:
已知:常温下,部分金属阳离子开始沉淀和完全沉淀(离子浓度小于或等于
 )时的pH如下表。
)时的pH如下表。| 离子 |  |  |  |
| 开始沉淀的pH | 7.6 | 1.9 | 4.4 |
| 完全沉淀的pH | 9.6 | 3.1 | 5.6 |
(1)Cr在元素周期表中的位置为
(2)加入9%双氧水的作用是
(3)“沉铁”时调pH的范围为
(4)“沉铬”过程发生反应的离子方程式是
(5)金属铬的晶胞结构如图,已知晶胞参数为anm。

①该晶胞中含铬原子的个数为
②铬原子的配位数为
③铬原子之间的最短距离为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐3】I.为比较 和
和 对
对 分解的催化效果,某化学研究小组的同学分别设计了如图甲、乙所示的实验。请回答相关问题:
分解的催化效果,某化学研究小组的同学分别设计了如图甲、乙所示的实验。请回答相关问题:
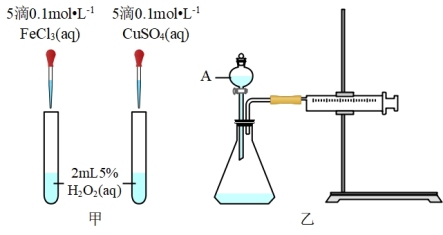
(1)定性分析:如图甲可通过观察_______ 的快慢,定性比较得出结论。有同学提出将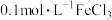 改为
改为_______ 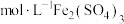 更为合理,其理由是
更为合理,其理由是_______ 。
(2)定量分析:如图乙所示,实验时均以生成 气体为准,其他可能影响实验的因素均已忽略。实验中需要测量的数据是
气体为准,其他可能影响实验的因素均已忽略。实验中需要测量的数据是_______ 。
(3)查阅资料得知:将作为催化剂的 溶液加入
溶液加入 溶液后,溶液中会发生两个氧化还原反应,且两个反应中
溶液后,溶液中会发生两个氧化还原反应,且两个反应中 均参加了反应,试从催化剂的角度分析,这两个氧化还原反应的离子方程式分别是
均参加了反应,试从催化剂的角度分析,这两个氧化还原反应的离子方程式分别是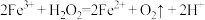 和
和_______ 。
Ⅱ.欲用如图所示实验来证明是 分解反应的催化剂。
分解反应的催化剂。
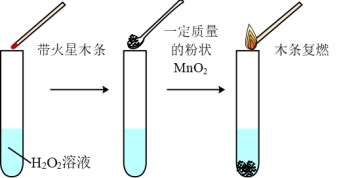
(4)该实验不能达到目的,若想证明 是催化剂还需要确认
是催化剂还需要确认_______ 。
(5)写出 在二氧化锰作用下发生反应的化学方程式:
在二氧化锰作用下发生反应的化学方程式:_______ 。
 和
和 对
对 分解的催化效果,某化学研究小组的同学分别设计了如图甲、乙所示的实验。请回答相关问题:
分解的催化效果,某化学研究小组的同学分别设计了如图甲、乙所示的实验。请回答相关问题:
(1)定性分析:如图甲可通过观察
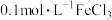 改为
改为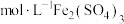 更为合理,其理由是
更为合理,其理由是(2)定量分析:如图乙所示,实验时均以生成
 气体为准,其他可能影响实验的因素均已忽略。实验中需要测量的数据是
气体为准,其他可能影响实验的因素均已忽略。实验中需要测量的数据是(3)查阅资料得知:将作为催化剂的
 溶液加入
溶液加入 溶液后,溶液中会发生两个氧化还原反应,且两个反应中
溶液后,溶液中会发生两个氧化还原反应,且两个反应中 均参加了反应,试从催化剂的角度分析,这两个氧化还原反应的离子方程式分别是
均参加了反应,试从催化剂的角度分析,这两个氧化还原反应的离子方程式分别是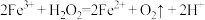 和
和Ⅱ.欲用如图所示实验来证明是
 分解反应的催化剂。
分解反应的催化剂。
(4)该实验不能达到目的,若想证明
 是催化剂还需要确认
是催化剂还需要确认(5)写出
 在二氧化锰作用下发生反应的化学方程式:
在二氧化锰作用下发生反应的化学方程式:
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
解题方法
【推荐1】 、NO是大气污染物。吸收
、NO是大气污染物。吸收 和NO,获得
和NO,获得 和
和 产品的流程图如下(Ce为铈元素):
产品的流程图如下(Ce为铈元素):

(1)含硫各微粒( 、
、 和
和 )存在于
)存在于 与NaOH溶液反应后的溶液中,它们的物质的量分数X(i)与溶液pH的关系如下图所示。
与NaOH溶液反应后的溶液中,它们的物质的量分数X(i)与溶液pH的关系如下图所示。
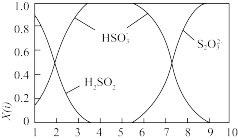
①下列说法正确的是_______ (填字母序号)。
a.pH=8时,溶液中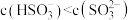
b.pH=7时,溶液中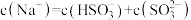
c.为获得尽可能纯的 ,可将溶液的pH控制在4~5左右
,可将溶液的pH控制在4~5左右
②已知 溶液显酸性,用化学平衡原理解释并写出相应的离子反应方程式:
溶液显酸性,用化学平衡原理解释并写出相应的离子反应方程式:_______ 。
(2)装置Ⅱ中,酸性条件下,NO被 氧化的产物主要是
氧化的产物主要是 、
、 ,写出生成
,写出生成 的离子方程式
的离子方程式_______ 。
(3)装置Ⅲ的作用之一是再生 ,其原理如图所示。
,其原理如图所示。
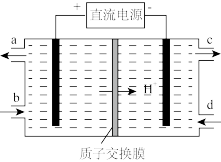
①生成 的电极反应式为
的电极反应式为_______ 。
②生成 从电解槽的
从电解槽的_______ (填字母序号)口流出。
 、NO是大气污染物。吸收
、NO是大气污染物。吸收 和NO,获得
和NO,获得 和
和 产品的流程图如下(Ce为铈元素):
产品的流程图如下(Ce为铈元素):
(1)含硫各微粒(
 、
、 和
和 )存在于
)存在于 与NaOH溶液反应后的溶液中,它们的物质的量分数X(i)与溶液pH的关系如下图所示。
与NaOH溶液反应后的溶液中,它们的物质的量分数X(i)与溶液pH的关系如下图所示。
①下列说法正确的是
a.pH=8时,溶液中
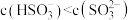
b.pH=7时,溶液中
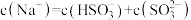
c.为获得尽可能纯的
 ,可将溶液的pH控制在4~5左右
,可将溶液的pH控制在4~5左右②已知
 溶液显酸性,用化学平衡原理解释并写出相应的离子反应方程式:
溶液显酸性,用化学平衡原理解释并写出相应的离子反应方程式:(2)装置Ⅱ中,酸性条件下,NO被
 氧化的产物主要是
氧化的产物主要是 、
、 ,写出生成
,写出生成 的离子方程式
的离子方程式(3)装置Ⅲ的作用之一是再生
 ,其原理如图所示。
,其原理如图所示。
①生成
 的电极反应式为
的电极反应式为②生成
 从电解槽的
从电解槽的
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
名校
【推荐2】Ⅰ. 在染料、造纸、制革、化学合成等工业中作为还原剂,在酿造、饮料行业中用作杀菌剂,还可用于生产糖精、香料等。其水溶液中含硫微粒随pH的分布曲线如图所示。
在染料、造纸、制革、化学合成等工业中作为还原剂,在酿造、饮料行业中用作杀菌剂,还可用于生产糖精、香料等。其水溶液中含硫微粒随pH的分布曲线如图所示。
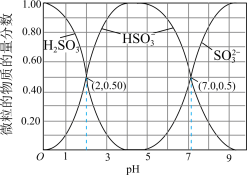
请回答以下问题:
(1)下列说法正确的是_______。
(2)若向 溶液中滴入NaOH溶液使pH恰好为7,此时测得
溶液中滴入NaOH溶液使pH恰好为7,此时测得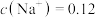 mol∙L−1,则溶液中
mol∙L−1,则溶液中
_______ mol∙L−1;
(3)已知几种酸的Ka如下表所示,下列化学方程式正确的是_______。
Ⅱ.工业上可用纯碱吸收二氧化硫法制备 ,流程如下图所示。
,流程如下图所示。
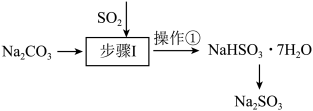
(4)步骤I中边搅拌边向 溶液中通入
溶液中通入 制备
制备 溶液,结合
溶液,结合 的分布系数图,确定停止通入
的分布系数图,确定停止通入 的最佳pH范围是
的最佳pH范围是_______ ,操作①的名称为_______ ;
(5)某小组同学用0.1000 mol∙L−1的酸性 溶液测定产品中
溶液测定产品中 的含量,具体流程:
的含量,具体流程:
①称量1 g样品,溶解,配置成250 mL的溶液;
②用滴定管量取25.00 mL样品溶液于锥形瓶中,用酸性 溶液滴定;
溶液滴定;
③消耗 溶液体积为20.00 mL;
溶液体积为20.00 mL;
试计算样品中 的纯度
的纯度_______ 。
(6)连二亚硫酸钠( )俗称保险粉,是一种强还原剂。工业常用惰性电极电解酸性亚硫酸氢钠溶液制备连二亚硫酸钠,原理及装置如图所示,a电极反应为
)俗称保险粉,是一种强还原剂。工业常用惰性电极电解酸性亚硫酸氢钠溶液制备连二亚硫酸钠,原理及装置如图所示,a电极反应为_______ 。

 在染料、造纸、制革、化学合成等工业中作为还原剂,在酿造、饮料行业中用作杀菌剂,还可用于生产糖精、香料等。其水溶液中含硫微粒随pH的分布曲线如图所示。
在染料、造纸、制革、化学合成等工业中作为还原剂,在酿造、饮料行业中用作杀菌剂,还可用于生产糖精、香料等。其水溶液中含硫微粒随pH的分布曲线如图所示。
请回答以下问题:
(1)下列说法正确的是_______。
A. 溶液显碱性 溶液显碱性 |
B. 时,溶液中 时,溶液中 |
C. 溶液中 溶液中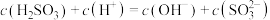 |
D. 溶液中 溶液中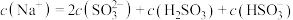 |
 溶液中滴入NaOH溶液使pH恰好为7,此时测得
溶液中滴入NaOH溶液使pH恰好为7,此时测得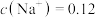 mol∙L−1,则溶液中
mol∙L−1,则溶液中
(3)已知几种酸的Ka如下表所示,下列化学方程式正确的是_______。
| 碳酸 | 次氯酸 | 醋酸 |
 |  | 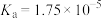 |
 |
A.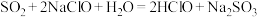 |
B.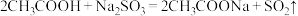 |
C. |
D. |
Ⅱ.工业上可用纯碱吸收二氧化硫法制备
 ,流程如下图所示。
,流程如下图所示。
(4)步骤I中边搅拌边向
 溶液中通入
溶液中通入 制备
制备 溶液,结合
溶液,结合 的分布系数图,确定停止通入
的分布系数图,确定停止通入 的最佳pH范围是
的最佳pH范围是(5)某小组同学用0.1000 mol∙L−1的酸性
 溶液测定产品中
溶液测定产品中 的含量,具体流程:
的含量,具体流程:①称量1 g样品,溶解,配置成250 mL的溶液;
②用滴定管量取25.00 mL样品溶液于锥形瓶中,用酸性
 溶液滴定;
溶液滴定;③消耗
 溶液体积为20.00 mL;
溶液体积为20.00 mL;试计算样品中
 的纯度
的纯度(6)连二亚硫酸钠(
 )俗称保险粉,是一种强还原剂。工业常用惰性电极电解酸性亚硫酸氢钠溶液制备连二亚硫酸钠,原理及装置如图所示,a电极反应为
)俗称保险粉,是一种强还原剂。工业常用惰性电极电解酸性亚硫酸氢钠溶液制备连二亚硫酸钠,原理及装置如图所示,a电极反应为
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
【推荐3】Ⅰ.柠檬酸(俗称枸橼酸,分子式为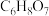 )是一种重要的有机弱酸,易溶于水的无色晶体,被广泛用作酸度调节剂、防腐剂和化工原料等。其结构简式和各级电离平衡常数如下表。
)是一种重要的有机弱酸,易溶于水的无色晶体,被广泛用作酸度调节剂、防腐剂和化工原料等。其结构简式和各级电离平衡常数如下表。
(1)关于柠檬酸分子说法正确的是___________。
(2)某泡腾片是以柠檬酸和碳酸氢钠泡腾崩解剂。将其置入水中,即刻发生泡腾反应,生成并释放大量气体。解释上述泡腾片只有加入水中才会产生气体的原因__________ 。
Ⅱ.用 溶液滴定等浓度的柠檬酸溶液,滴定曲线如下图所示。
溶液滴定等浓度的柠檬酸溶液,滴定曲线如下图所示。
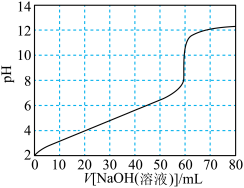
(3)上述滴定时所用的指示剂为___________ (选填“甲基橙试液”或“酚酞试液”)。理由是___________ 。
(4)已知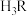 表示柠檬酸。在上述滴定过程中,各微粒浓度大小关系正确是___________。(不定项)
表示柠檬酸。在上述滴定过程中,各微粒浓度大小关系正确是___________。(不定项)
Ⅲ.以柠檬酸、硫酸亚铁、氨水等为原料制备一种食品添加剂—柠檬酸铁铵[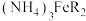 ]的流程如下所示:
]的流程如下所示:
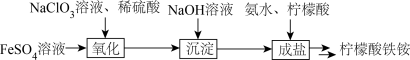
(5)用单线桥法表示“氧化”步骤中反应的电子转移方向和数目__________ 。
(6)柠檬酸铁铵化学式中R表示的是___________。
(7)欲检验 溶液是否被完全氧化,简述实验方法(包括试剂、步骤、现象等)
溶液是否被完全氧化,简述实验方法(包括试剂、步骤、现象等) ___________ 。
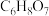 )是一种重要的有机弱酸,易溶于水的无色晶体,被广泛用作酸度调节剂、防腐剂和化工原料等。其结构简式和各级电离平衡常数如下表。
)是一种重要的有机弱酸,易溶于水的无色晶体,被广泛用作酸度调节剂、防腐剂和化工原料等。其结构简式和各级电离平衡常数如下表。| 结构简式 |  |  | 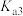 |
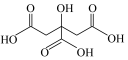 |  | 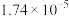 | 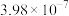 |
(1)关于柠檬酸分子说法正确的是___________。
A.分子中含有3个 键 键 | B.分子中含有13个 键 键 |
| C.分子中含有手性碳原子 | D.不能形成分子内氢键 |
(2)某泡腾片是以柠檬酸和碳酸氢钠泡腾崩解剂。将其置入水中,即刻发生泡腾反应,生成并释放大量气体。解释上述泡腾片只有加入水中才会产生气体的原因
Ⅱ.用
 溶液滴定等浓度的柠檬酸溶液,滴定曲线如下图所示。
溶液滴定等浓度的柠檬酸溶液,滴定曲线如下图所示。
(3)上述滴定时所用的指示剂为
(4)已知
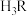 表示柠檬酸。在上述滴定过程中,各微粒浓度大小关系正确是___________。(不定项)
表示柠檬酸。在上述滴定过程中,各微粒浓度大小关系正确是___________。(不定项)A.V=0时,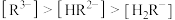 |
B.V=20时,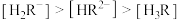 |
C.V=40时, |
D.V=60时,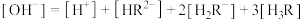 |
Ⅲ.以柠檬酸、硫酸亚铁、氨水等为原料制备一种食品添加剂—柠檬酸铁铵[
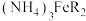 ]的流程如下所示:
]的流程如下所示:
(5)用单线桥法表示“氧化”步骤中反应的电子转移方向和数目
(6)柠檬酸铁铵化学式中R表示的是___________。
A.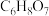 | B. | C. | D. |
(7)欲检验
 溶液是否被完全氧化,简述实验方法(包括试剂、步骤、现象等)
溶液是否被完全氧化,简述实验方法(包括试剂、步骤、现象等)
您最近一年使用:0次
【推荐1】根据元素周期表中完整周期元素的性质,填写下列空白。
(1)第四周期元素中未成对电子数最多的元素符号是___________ ,其基态原子的简化电子排布式为___________ ,原子中所有电子占有___________ 个轨道,核外共有___________ 个不同运动状态的电子。
(2)杀虫剂 中阴离子的空间构型为
中阴离子的空间构型为___________ , 原子采取
原子采取___________ 杂化。
(3)用惰性电极电解第三周期原子半径最大的元素的氯化物的水溶液,其阳极反应的电极方程式为___________ 。电解一段时间后,阴极区
___________ (填“增大”、“减小”或“不变”)。
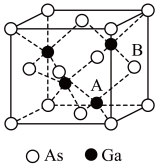
(4)原子晶体 的晶胞参数
的晶胞参数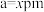 ,它的晶胞结构如图所示。该晶胞内部存在的共价键数为
,它的晶胞结构如图所示。该晶胞内部存在的共价键数为___________ ;该晶胞的密度为___________  。(阿伏加德罗常数用
。(阿伏加德罗常数用 表示,已知Ga:70As:75)。
表示,已知Ga:70As:75)。
(1)第四周期元素中未成对电子数最多的元素符号是
(2)杀虫剂
 中阴离子的空间构型为
中阴离子的空间构型为 原子采取
原子采取(3)用惰性电极电解第三周期原子半径最大的元素的氯化物的水溶液,其阳极反应的电极方程式为

(4)原子晶体
 的晶胞参数
的晶胞参数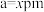 ,它的晶胞结构如图所示。该晶胞内部存在的共价键数为
,它的晶胞结构如图所示。该晶胞内部存在的共价键数为 。(阿伏加德罗常数用
。(阿伏加德罗常数用 表示,已知Ga:70As:75)。
表示,已知Ga:70As:75)。
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
名校
【推荐2】随着人类社会的发展,氮氧化物的排做导致一系列环境问题。
(1)NO加速臭氧层被破坏,其反应过程如图所示:
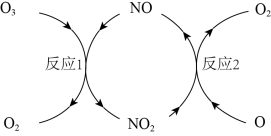
①NO的作用是___________ 。
②反应O3(g) + O(g) == 2O2(g) △H= -143 kJ/mol
反应1: O3(g)+ NO(g)==NO2(g) + O2(g) △H1= -200.2 kJ/mol
反应2:热化学方程式为___________________ 。
(2)通过NOx,传感器可监测NOx的含量,其工作原理示意图如下:

①Pt电极上发生的是___ 反应(填氧化或还原)。
②写出NiO电极的电极反应式:____________ 。
(3)电解NO制备NH4NO3,是处理氨氧化物的排放的方法之一,其工作原理如图所示:
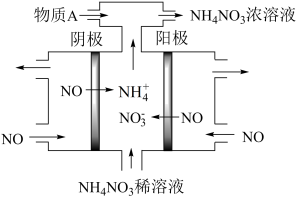
①阴极的电极反应式:______________
②为使电解产物全部转化为NH4NO3需补充物质A______ , 说明理由: ______ 。
(1)NO加速臭氧层被破坏,其反应过程如图所示:

①NO的作用是
②反应O3(g) + O(g) == 2O2(g) △H= -143 kJ/mol
反应1: O3(g)+ NO(g)==NO2(g) + O2(g) △H1= -200.2 kJ/mol
反应2:热化学方程式为
(2)通过NOx,传感器可监测NOx的含量,其工作原理示意图如下:

①Pt电极上发生的是
②写出NiO电极的电极反应式:
(3)电解NO制备NH4NO3,是处理氨氧化物的排放的方法之一,其工作原理如图所示:

①阴极的电极反应式:
②为使电解产物全部转化为NH4NO3需补充物质A
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
解题方法
【推荐3】CuCl2溶液中的铜主要以Cu (H2O)42+、CuCl42-形式存在,它们间有如下转化关系:Cu (H2O)42+(蓝色)+4Cl- CuCl42-(黄色)+4H2O;电解不同浓度的CuCl2溶液,均可看做Cu2+、Cl-直接放电。下图为电解浓度较大CuCl2溶液的装置,实验开始后,观察到丙中的KI-淀粉溶液慢慢变蓝。回答下列问题:
CuCl42-(黄色)+4H2O;电解不同浓度的CuCl2溶液,均可看做Cu2+、Cl-直接放电。下图为电解浓度较大CuCl2溶液的装置,实验开始后,观察到丙中的KI-淀粉溶液慢慢变蓝。回答下列问题:
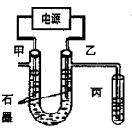
(1)甲电极的电极反应式为_________________ 。
(2)丙中溶液变蓝是乙电极产物与KI反应导致的,该反应的化学方程式为_________________ 。
(3)随电解的不断进行,U型管中溶液的颜色变化为__________ ;
A.由黄色变为浅蓝色 B.由蓝色变为浅黄色
溶液颜色变化的原因是_________________ 。
(4)当电解到一定程度,甲电极附近出现蓝色Cu(OH)2絮状物。经测,甲电极附近溶液的pH=a,此时甲电极附近c(Cu2+)=________ mol·L-1。(已知:Cu(OH)2的Ksp=2.2*10-20)。
 CuCl42-(黄色)+4H2O;电解不同浓度的CuCl2溶液,均可看做Cu2+、Cl-直接放电。下图为电解浓度较大CuCl2溶液的装置,实验开始后,观察到丙中的KI-淀粉溶液慢慢变蓝。回答下列问题:
CuCl42-(黄色)+4H2O;电解不同浓度的CuCl2溶液,均可看做Cu2+、Cl-直接放电。下图为电解浓度较大CuCl2溶液的装置,实验开始后,观察到丙中的KI-淀粉溶液慢慢变蓝。回答下列问题:
(1)甲电极的电极反应式为
(2)丙中溶液变蓝是乙电极产物与KI反应导致的,该反应的化学方程式为
(3)随电解的不断进行,U型管中溶液的颜色变化为
A.由黄色变为浅蓝色 B.由蓝色变为浅黄色
溶液颜色变化的原因是
(4)当电解到一定程度,甲电极附近出现蓝色Cu(OH)2絮状物。经测,甲电极附近溶液的pH=a,此时甲电极附近c(Cu2+)=
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
【推荐1】C、N、Si、Ni等元素在新型材料的研制中有着重要应用,请回答下列问题:
(1)Ni元素的价层电子排布式为______ ,C、N、Si的第一电离能由大到小的顺序为______ 。
(2)研究发现, 固体由
固体由 和
和 两种离子组成,
两种离子组成, 空间构型为
空间构型为______ ; 和
和 二者相比较,
二者相比较, 键角更大,原因是
键角更大,原因是______ 。
(3)碳的一种同素异形体——石墨,其晶体片层结构俯视图如下A,晶胞结构如B,其中图A中的虚线表示的平行四边形即图B中的底面。石墨晶胞含碳原子个数为______ 。已知石墨的密度为 ,C—C键键长为a cm,阿伏加德罗常数的值为
,C—C键键长为a cm,阿伏加德罗常数的值为 ,石墨晶体的层间距为d cm,计算d为
,石墨晶体的层间距为d cm,计算d为______ cm。

(1)Ni元素的价层电子排布式为
(2)研究发现,
 固体由
固体由 和
和 两种离子组成,
两种离子组成, 空间构型为
空间构型为 和
和 二者相比较,
二者相比较, 键角更大,原因是
键角更大,原因是(3)碳的一种同素异形体——石墨,其晶体片层结构俯视图如下A,晶胞结构如B,其中图A中的虚线表示的平行四边形即图B中的底面。石墨晶胞含碳原子个数为
 ,C—C键键长为a cm,阿伏加德罗常数的值为
,C—C键键长为a cm,阿伏加德罗常数的值为 ,石墨晶体的层间距为d cm,计算d为
,石墨晶体的层间距为d cm,计算d为
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐2】氨化硼(BN)是一种重要的功能陶瓷材料。以天然硼砂为原料,经过一系列反应可以得到BF3和BN,流程如图所示。
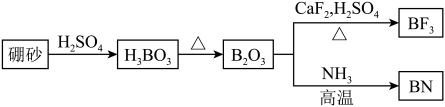
回答下列问题:
(1)BF3分子为____ (填“极性”或“非极性”)分子,该分子中F-B-F键角是____ 。
(2)BF3和过量NaF作用可生成NaBF4,BF 的空间结构为
的空间结构为____ ,NaBF4中____ (填“含有”或“不含”)配位键。
(3)六方氮化硼具有的平面层状结构如图所示,层内B原子与N原子之间的化学键为____ 共价键(填“极性”或“非极性”),B、N原子的杂化形式分别是____ 、____ 。

(4)BF3的沸点低于BCl3,原因是____ 。

回答下列问题:
(1)BF3分子为
(2)BF3和过量NaF作用可生成NaBF4,BF
 的空间结构为
的空间结构为(3)六方氮化硼具有的平面层状结构如图所示,层内B原子与N原子之间的化学键为

(4)BF3的沸点低于BCl3,原因是
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐3】已知:A、B、C、D、E、F六种元素,原子序数依次增大。A原子核外有两种形状的电子云,两种形状的电子云轨道上电子数相等;B是短周期中原子半径最大的元素;C元素3p能级半充满;E是所在周期电负性最大的元素;F是第四周期未成对电子最多的元素。试回答下列有关的问题。
(1)写出F元素的电子排布式:________ 。
(2)已知A元素的一种氢化物分子中含四个原子,则在该化合物的分子中A原子的杂化轨道类型为________ 。
(3)已知C、E两种元素形成的化合物通常有CE3、CE5两种。这两种化合物中一种为非极性分子,一种为极性分子,属于极性分子的化合物的分子空间构型是_________ 。
(4)B、C、D、E的第一电离能由大到小的顺序是________ (写元素符号)。四种元素最高价氧化物的水化物形成的溶液,物质的量浓度相同时,pH由大到小的顺序是________ (写化学式)。
(5)由B、E两元素形成的化合物组成的晶体中,阴、阳离子都具有球型对称结构,它们都可以看做刚性圆球,并彼此“相切”。如图所示为B、E形成化合物的晶胞结构图以及晶胞的剖面图:晶胞中距离一个B+最近的B+有________ 个;B+的配位数是________ 。
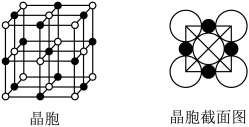
(1)写出F元素的电子排布式:
(2)已知A元素的一种氢化物分子中含四个原子,则在该化合物的分子中A原子的杂化轨道类型为
(3)已知C、E两种元素形成的化合物通常有CE3、CE5两种。这两种化合物中一种为非极性分子,一种为极性分子,属于极性分子的化合物的分子空间构型是
(4)B、C、D、E的第一电离能由大到小的顺序是
(5)由B、E两元素形成的化合物组成的晶体中,阴、阳离子都具有球型对称结构,它们都可以看做刚性圆球,并彼此“相切”。如图所示为B、E形成化合物的晶胞结构图以及晶胞的剖面图:晶胞中距离一个B+最近的B+有

您最近一年使用:0次



