已知:A、B、C、D、E、F六种元素,原子序数依次增大。A原子核外有两种形状的电子云,两种形状的电子云轨道上电子数相等;B是短周期中原子半径最大的元素;C元素3p能级半充满;E是所在周期电负性最大的元素;F是第四周期未成对电子最多的元素。试回答下列有关的问题。
(1)写出F元素的电子排布式:________ 。
(2)已知A元素的一种氢化物分子中含四个原子,则在该化合物的分子中A原子的杂化轨道类型为________ 。
(3)已知C、E两种元素形成的化合物通常有CE3、CE5两种。这两种化合物中一种为非极性分子,一种为极性分子,属于极性分子的化合物的分子空间构型是_________ 。
(4)B、C、D、E的第一电离能由大到小的顺序是________ (写元素符号)。四种元素最高价氧化物的水化物形成的溶液,物质的量浓度相同时,pH由大到小的顺序是________ (写化学式)。
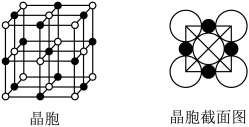
(5)由B、E两元素形成的化合物组成的晶体中,阴、阳离子都具有球型对称结构,它们都可以看做刚性圆球,并彼此“相切”。如图所示为B、E形成化合物的晶胞结构图以及晶胞的剖面图:晶胞中距离一个B+最近的B+有________ 个;B+的配位数是________ 。
(1)写出F元素的电子排布式:
(2)已知A元素的一种氢化物分子中含四个原子,则在该化合物的分子中A原子的杂化轨道类型为
(3)已知C、E两种元素形成的化合物通常有CE3、CE5两种。这两种化合物中一种为非极性分子,一种为极性分子,属于极性分子的化合物的分子空间构型是
(4)B、C、D、E的第一电离能由大到小的顺序是
(5)由B、E两元素形成的化合物组成的晶体中,阴、阳离子都具有球型对称结构,它们都可以看做刚性圆球,并彼此“相切”。如图所示为B、E形成化合物的晶胞结构图以及晶胞的剖面图:晶胞中距离一个B+最近的B+有

更新时间:2023-10-13 12:45:52
|
相似题推荐
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐1】已知短周期元素X、Y、Z、W、Q和R在周期表中的相对位置如图所示,X能与W形成两种常见的离子化合物,阴阳离子个数比均为1∶2。回答下列问题:
(1)化合物XR的电子式为____ 。
(2)基态W原子的最外层有____ 个未成对电子。
(3)Z单质与Q的最高价氧化物对应水化物的浓溶液在加热条件下反应的化学方程式为____ 。
(4)Y在Z的最高价氧化物中燃烧的化学方程式为____ 。
| Z | W | |||||
| X | Y | Q | R |
(2)基态W原子的最外层有
(3)Z单质与Q的最高价氧化物对应水化物的浓溶液在加热条件下反应的化学方程式为
(4)Y在Z的最高价氧化物中燃烧的化学方程式为
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
【推荐2】配合物在许多尖端领域如激光材料、超导材料、抗癌药物、催化剂、自组装超分子等方面有广泛的应用。回答下列问题:
(1)Ni与CO形成的配合物Ni(CO)4为无色液体,易溶于CCl4、CS2等有机溶剂。碳原子的核外电子排布式为___________ 。CO的结构式为C≡O,则Ni(CO)4分子中σ键与π键个数之比为___________ 。
(2)胆矾溶于水后可得蓝色的水合铜离子,其中 的配位数是
的配位数是___________ 。胆矾晶体的结构如下图所示,其存在的化学键有___________ (填字母)。

A.离子键 B.极性键 C.范德华力 D.氢键 E.配位键
(3)金属Ni可以与Mg、C形成一种新型超导体,它的临界温度为8K,由C、Mg、Ni形成的某物质的晶胞为正六面体,结构如图所示。
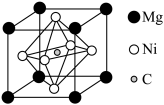
①该物质的化学式为___________ 。
②每个Mg原子距离最近的Ni原子的个数是___________ 。
③若用NA表示阿伏伽德罗常数的值,如果晶体的密度为ρg/cm3,则该晶胞的体积为___________ nm3(用含ρ、NA的代数式表示)。
(1)Ni与CO形成的配合物Ni(CO)4为无色液体,易溶于CCl4、CS2等有机溶剂。碳原子的核外电子排布式为
(2)胆矾溶于水后可得蓝色的水合铜离子,其中
 的配位数是
的配位数是
A.离子键 B.极性键 C.范德华力 D.氢键 E.配位键
(3)金属Ni可以与Mg、C形成一种新型超导体,它的临界温度为8K,由C、Mg、Ni形成的某物质的晶胞为正六面体,结构如图所示。

①该物质的化学式为
②每个Mg原子距离最近的Ni原子的个数是
③若用NA表示阿伏伽德罗常数的值,如果晶体的密度为ρg/cm3,则该晶胞的体积为
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐3】在制取合成氨原料气的过程中,常混有一些杂质,如CO会使催化剂中毒。除去CO的化学方程式为(HAc表示醋酸):Cu(NH3)2Ac+CO+NH3=Cu(NH3)3(CO)Ac。请回答下列问题:
(1)C、N、O的电负性由大到小的顺序为________ 。
(2)写出Cu的核外电子排布式________ 。
(3)化合物Cu(NH3)3(CO)Ac中,金属元素的化合价为________ 。
(4)在一定条件下NH3和CO2能合成尿素CO(NH2)2,尿素中C原子轨道的杂化类型为________ ;1mol尿素分子中,σ 键的数目为________ 。
(1)C、N、O的电负性由大到小的顺序为
(2)写出Cu的核外电子排布式
(3)化合物Cu(NH3)3(CO)Ac中,金属元素的化合价为
(4)在一定条件下NH3和CO2能合成尿素CO(NH2)2,尿素中C原子轨道的杂化类型为
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐1】制备 的实验操作如下:向盛有硫酸铜水溶液的试管中加入氨水,首先形成蓝色沉淀,继续添加氨水,沉淀溶解,得到深蓝色的透明溶液;若加入极性较小的溶剂(如乙醇),将析出深蓝色的晶体。回答以下问题:
的实验操作如下:向盛有硫酸铜水溶液的试管中加入氨水,首先形成蓝色沉淀,继续添加氨水,沉淀溶解,得到深蓝色的透明溶液;若加入极性较小的溶剂(如乙醇),将析出深蓝色的晶体。回答以下问题:
(1)“沉淀溶解”时发生反应的离子方程式为_______
(2)基态 价层电子排布式为
价层电子排布式为_______ 。
(3)N、O、S三种元素的第一电离能由大到小的顺序为_______ 。
(4)沸点: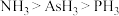 ,原因为
,原因为_______ 。
(5)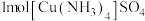 含有σ键的数目为
含有σ键的数目为_______ 。
(6)写出一种与 互为等电子体的分子的化学式
互为等电子体的分子的化学式_______ 。
(7)S与 形成的某化合物晶体的晶胞(实心点表示
形成的某化合物晶体的晶胞(实心点表示 ,空心点表示S)如图所示:
,空心点表示S)如图所示:
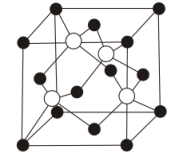
①该化合物的化学式为_______ 。
②已知该晶胞的晶胞参数为 ,阿伏加德罗常数为NA,则该晶胞的密度为
,阿伏加德罗常数为NA,则该晶胞的密度为_____  。
。
 的实验操作如下:向盛有硫酸铜水溶液的试管中加入氨水,首先形成蓝色沉淀,继续添加氨水,沉淀溶解,得到深蓝色的透明溶液;若加入极性较小的溶剂(如乙醇),将析出深蓝色的晶体。回答以下问题:
的实验操作如下:向盛有硫酸铜水溶液的试管中加入氨水,首先形成蓝色沉淀,继续添加氨水,沉淀溶解,得到深蓝色的透明溶液;若加入极性较小的溶剂(如乙醇),将析出深蓝色的晶体。回答以下问题:(1)“沉淀溶解”时发生反应的离子方程式为
(2)基态
 价层电子排布式为
价层电子排布式为(3)N、O、S三种元素的第一电离能由大到小的顺序为
(4)沸点:
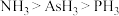 ,原因为
,原因为(5)
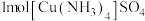 含有σ键的数目为
含有σ键的数目为(6)写出一种与
 互为等电子体的分子的化学式
互为等电子体的分子的化学式(7)S与
 形成的某化合物晶体的晶胞(实心点表示
形成的某化合物晶体的晶胞(实心点表示 ,空心点表示S)如图所示:
,空心点表示S)如图所示:
①该化合物的化学式为
②已知该晶胞的晶胞参数为
 ,阿伏加德罗常数为NA,则该晶胞的密度为
,阿伏加德罗常数为NA,则该晶胞的密度为 。
。
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐2】氮族元素包括氮(N)、磷(P)、砷(As)、锑(Sb)、铋(Bi),在性质上表现出从典型的非金属元素到典型的金属元素的过渡。回答下列问题:
(1)①基态N原子含有___________ 种不同能量的电子。
② 、
、 、
、 、
、 中,中心原子与
中,中心原子与 中N原子杂化类型相同的为
中N原子杂化类型相同的为___________ (填化学式,下同),微粒的空间结构相同的为___________ 和___________ ;键角:
___________  (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
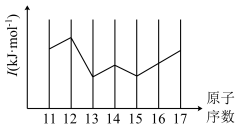
(2)第三周期主族元素某一级电离能如图所示,该电离能是第___________ (填“一”“二”或“三”)电离能,其中P的该级电离能比Si小的原因为___________ 。
(3) 和
和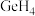 的沸点如下表:
的沸点如下表:
 的沸点比
的沸点比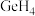 的沸点高的主要原因为
的沸点高的主要原因为___________ 。
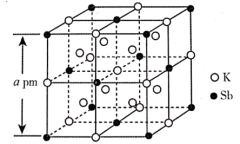
(4)锑钾(Sb-K)合金的立方晶胞结构如图所示,晶胞中锑原子与钾原子的数量比为___________ 。若该合金的密度为 ,该合金的摩尔质量为
,该合金的摩尔质量为___________  (
( 表示阿伏加德罗常数的值,用含
表示阿伏加德罗常数的值,用含 、a、
、a、 的式子表示)。
的式子表示)。
(1)①基态N原子含有
②
 、
、 、
、 、
、 中,中心原子与
中,中心原子与 中N原子杂化类型相同的为
中N原子杂化类型相同的为
 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。(2)第三周期主族元素某一级电离能如图所示,该电离能是第

(3)
 和
和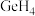 的沸点如下表:
的沸点如下表:| 物质 |  | 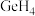 |
| 沸点 | -62℃ | -90℃ |
 的沸点比
的沸点比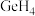 的沸点高的主要原因为
的沸点高的主要原因为(4)锑钾(Sb-K)合金的立方晶胞结构如图所示,晶胞中锑原子与钾原子的数量比为
 ,该合金的摩尔质量为
,该合金的摩尔质量为 (
( 表示阿伏加德罗常数的值,用含
表示阿伏加德罗常数的值,用含 、a、
、a、 的式子表示)。
的式子表示)。
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐3】Mn、Fe、Se等元素对人体生命活动非常重要,例如Se参与合成人体内多种含硒酶和含硒
蛋白,具有多种生物功能。请结合图示回答下列问题。
(1)锰和铁同周期且相邻,现有几种锰、铁元素的相应状态,①锰: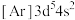 、②铁:
、②铁: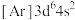 、③锰:
、③锰: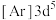 、④铁:
、④铁: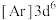 ,失去1个电子需要的能量由大到小排序是___________(填字母)。
,失去1个电子需要的能量由大到小排序是___________(填字母)。
(2)硒代半胱氨酸是第21个组成人体蛋白质的氨基酸,分子式为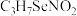 ,其结构简式如图所示。
,其结构简式如图所示。
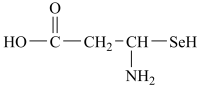
①其中杂化方式为 和
和 的碳原子个数比为
的碳原子个数比为___________ 。
②下列说法正确的是:___________ 。
A.C、N、O三种元素第一电离能从大到小的顺序是
B.硒代半胱氨酸分子中存在的化学键类型包括极性键、非极性键、氢键
C.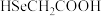 比
比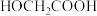 酸性弱
酸性弱
D.一个硒代半胱氨酸分子中σ键和π键的比例为
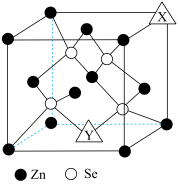
(3)硒化锌是一种化学惰性材料,具有纯度高,环境适应能力强,易于加工等特点,是良好的聚焦镜基材。下图所示是硒化锌晶胞结构(类似金刚石晶胞),从晶胞基本定义可知X、Y均为_______ (填元素符号),距离Se最近的Zn有________ 个,已知晶胞参数为anm,则硒化锌密度为________ 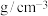 。
。
蛋白,具有多种生物功能。请结合图示回答下列问题。
(1)锰和铁同周期且相邻,现有几种锰、铁元素的相应状态,①锰:
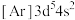 、②铁:
、②铁: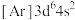 、③锰:
、③锰: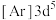 、④铁:
、④铁: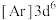 ,失去1个电子需要的能量由大到小排序是___________(填字母)。
,失去1个电子需要的能量由大到小排序是___________(填字母)。| A.①②③④ | B.④③②① | C.③④②① | D.④②③① |
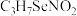 ,其结构简式如图所示。
,其结构简式如图所示。
①其中杂化方式为
 和
和 的碳原子个数比为
的碳原子个数比为②下列说法正确的是:
A.C、N、O三种元素第一电离能从大到小的顺序是

B.硒代半胱氨酸分子中存在的化学键类型包括极性键、非极性键、氢键
C.
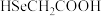 比
比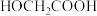 酸性弱
酸性弱D.一个硒代半胱氨酸分子中σ键和π键的比例为

(3)硒化锌是一种化学惰性材料,具有纯度高,环境适应能力强,易于加工等特点,是良好的聚焦镜基材。下图所示是硒化锌晶胞结构(类似金刚石晶胞),从晶胞基本定义可知X、Y均为
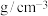 。
。
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
【推荐1】完成下列问题。
Ⅰ.短周期元素D、E、X、Y、Z原子序数逐渐增大,它们的最简单氢化物分子空间结构依次是正四面体形、三角锥形、正四面体形、V形、直线形。回答下列问题:
(1)HZO分子的中心原子价层电子对数的计算式为___________ ,该分子的空间结构为___________ 。
(2)Y的价层电子排布式为_________ ,Y的最高价氧化物的VSEPR模型为________ 。
(3)D、E的最简单氢化物的分子空间结构分别是正四面体形与三角锥形,这是因为_______ 。
a.两种分子的中心原子的价层电子对数不同
b.D、E的非金属性不同
c.E的氢化物分子中有一个孤电子对,而D的氢化物分子中没有
Ⅱ.有A、B、C、D、E、F六种主族元素,有关信息如下:
①短周期元素C原子的价电子排布式为ns2np2,E的单质可在空气中燃烧;
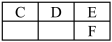
②如图是元素周期表中主族元素的一部分:
③A、B同周期,其电离能数据如下(单位:kJ·mol-1):
试回答下列问题:
(4)F原子的核外电子排布式为___________ 。
(5)C、D、E元素的电负性相对大小为___________ (用元素符号表示)。
(6)化合价是元素的一种性质,由A、B的电离能数据判断下列说法正确的是______ (填字母)。
a.A通常显+1价,B通常显+4价
b.B元素的第一电离能较小,其活泼性比A强
c.A、B的单质分别与盐酸反应放出等量氢气时,消耗单质的物质的量之比为3∶2
Ⅰ.短周期元素D、E、X、Y、Z原子序数逐渐增大,它们的最简单氢化物分子空间结构依次是正四面体形、三角锥形、正四面体形、V形、直线形。回答下列问题:
(1)HZO分子的中心原子价层电子对数的计算式为
(2)Y的价层电子排布式为
(3)D、E的最简单氢化物的分子空间结构分别是正四面体形与三角锥形,这是因为
a.两种分子的中心原子的价层电子对数不同
b.D、E的非金属性不同
c.E的氢化物分子中有一个孤电子对,而D的氢化物分子中没有
Ⅱ.有A、B、C、D、E、F六种主族元素,有关信息如下:
①短周期元素C原子的价电子排布式为ns2np2,E的单质可在空气中燃烧;
②如图是元素周期表中主族元素的一部分:

③A、B同周期,其电离能数据如下(单位:kJ·mol-1):
| I1 | I2 | I3 | I4 | |
| A | 738 | 1 451 | 7 733 | 10 540 |
| B | 578 | 1 817 | 2 745 | 11 575 |
(4)F原子的核外电子排布式为
(5)C、D、E元素的电负性相对大小为
(6)化合价是元素的一种性质,由A、B的电离能数据判断下列说法正确的是
a.A通常显+1价,B通常显+4价
b.B元素的第一电离能较小,其活泼性比A强
c.A、B的单质分别与盐酸反应放出等量氢气时,消耗单质的物质的量之比为3∶2
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐2】硒(Se)是人体必需微量元素之一,含硒化合物在材料和药物领域具有重要应用。自我国科学家发现聚集诱导发光(AIE)效应以来,AIE在发光材料、生物医学等领域引起广泛关注。一种含Se的新型AIE分子N的合成路线如下:
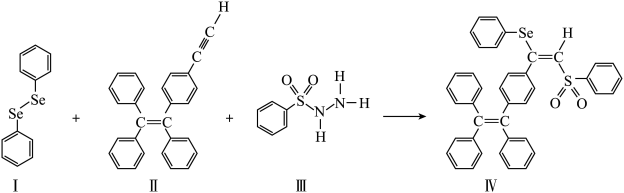
(1)H2Se的沸点低于H2O,其原因是___________ 。
(2)关于I~Ⅲ三种反应物,下列说法正确的有___________ 。
A. I中仅有σ键 B. I中的 Se-Se为非极性共价键
C. Ⅱ易溶于水 D. Ⅱ中原子的杂化轨道类型只有sp与sp2
E. I~Ⅲ含有的元素中,O电负性最大
(3)Ⅳ中具有孤电子对的原子有___________ 。
(4)研究发现,给小鼠喂食适量硒酸钠(Na2SeO4)可减轻重金属铊引起的中毒。 的空间结构为
的空间结构为___________ 。
(5)吡啶(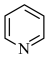 )替代苯也可形成类似的笼形包合物。已知吡啶中含有与苯类似的
)替代苯也可形成类似的笼形包合物。已知吡啶中含有与苯类似的 大
大 键,则吡啶中N原子的价层孤电子对占据___________(填标号)。
键,则吡啶中N原子的价层孤电子对占据___________(填标号)。
(6)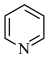 、
、 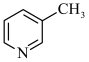 、
、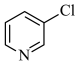 的碱性随N原子电子云密度的增大而增强,其中碱性最弱的是
的碱性随N原子电子云密度的增大而增强,其中碱性最弱的是___________ 。

(1)H2Se的沸点低于H2O,其原因是
(2)关于I~Ⅲ三种反应物,下列说法正确的有
A. I中仅有σ键 B. I中的 Se-Se为非极性共价键
C. Ⅱ易溶于水 D. Ⅱ中原子的杂化轨道类型只有sp与sp2
E. I~Ⅲ含有的元素中,O电负性最大
(3)Ⅳ中具有孤电子对的原子有
(4)研究发现,给小鼠喂食适量硒酸钠(Na2SeO4)可减轻重金属铊引起的中毒。
 的空间结构为
的空间结构为(5)吡啶(
 )替代苯也可形成类似的笼形包合物。已知吡啶中含有与苯类似的
)替代苯也可形成类似的笼形包合物。已知吡啶中含有与苯类似的 大
大 键,则吡啶中N原子的价层孤电子对占据___________(填标号)。
键,则吡啶中N原子的价层孤电子对占据___________(填标号)。| A.2s轨道 | B.2p轨道 | C.sp杂化轨道 | D.sp2杂化轨道 |
(6)
 、
、  、
、 的碱性随N原子电子云密度的增大而增强,其中碱性最弱的是
的碱性随N原子电子云密度的增大而增强,其中碱性最弱的是
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐3】氨化硼(BN)是一种重要的功能陶瓷材料。以天然硼砂为原料,经过一系列反应可以得到BF3和BN,流程如图所示。
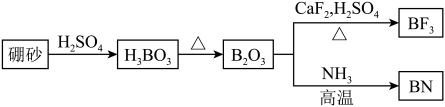
回答下列问题:
(1)BF3分子为____ (填“极性”或“非极性”)分子,该分子中F-B-F键角是____ 。
(2)BF3和过量NaF作用可生成NaBF4,BF 的空间结构为
的空间结构为____ ,NaBF4中____ (填“含有”或“不含”)配位键。
(3)六方氮化硼具有的平面层状结构如图所示,层内B原子与N原子之间的化学键为____ 共价键(填“极性”或“非极性”),B、N原子的杂化形式分别是____ 、____ 。

(4)BF3的沸点低于BCl3,原因是____ 。

回答下列问题:
(1)BF3分子为
(2)BF3和过量NaF作用可生成NaBF4,BF
 的空间结构为
的空间结构为(3)六方氮化硼具有的平面层状结构如图所示,层内B原子与N原子之间的化学键为

(4)BF3的沸点低于BCl3,原因是
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐1】(乙酸锰可用于制造钠离子电池的负极材料。可用如下反应制得乙酸锰:4Mn(NO3)2•6H2O+26(CH3CO)2O=4(CH3COO)3Mn+8HNO2+3O2↑+40CH3COOH
(1)Mn3+基态核外电子排布式为___ 。
(2)NO3-中氮原子轨道的杂化类型是___ 。
(3)与HNO2互为等电子体的一种阴离子的化学式为___ 。
(4)配合物[Mn(CH3OH)6]2+中配位原子是___ 。
(5)CH3COOH能与H2O任意比混溶的原因,除它们都是极性分子外还有___ 。
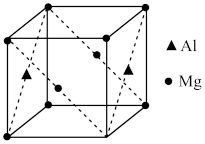
(6)镁铝合金经过高温淬火获得一种储钠材料,其晶胞为立方结构(如图所示),图中原子位于顶点或面心。该晶体中每个铝原子周围距离最近的镁原子数目为___ 。
(1)Mn3+基态核外电子排布式为
(2)NO3-中氮原子轨道的杂化类型是
(3)与HNO2互为等电子体的一种阴离子的化学式为
(4)配合物[Mn(CH3OH)6]2+中配位原子是
(5)CH3COOH能与H2O任意比混溶的原因,除它们都是极性分子外还有
(6)镁铝合金经过高温淬火获得一种储钠材料,其晶胞为立方结构(如图所示),图中原子位于顶点或面心。该晶体中每个铝原子周围距离最近的镁原子数目为

您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐2】锗(Ge)是典型的半导体元素,在电子、材料等领域应用广泛。回答下列问题:
(1)基态Ge原子的电子排布式为_______ ,有_______ 个未成对电子。
(2)比较下列锗卤化物的熔点和沸点,分析其变化规律及原因:_______ 。
(3)Ge单晶具有金刚石型结构,其中Ge原子的杂化方式为_______ ,微粒之间存在的作用力是_______ 。
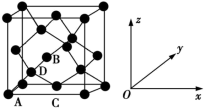
(4)原子坐标参数,表示晶胞内部各原子的相对位置。如图为Ge单晶的晶胞,其中原子坐标参数A为(0,0,0);B为( ,0,
,0, );C为(
);C为( ,
, ,0);则D原子的坐标参数为
,0);则D原子的坐标参数为_______ 。
(1)基态Ge原子的电子排布式为
(2)比较下列锗卤化物的熔点和沸点,分析其变化规律及原因:
| GeCl4 | GeBr4 | GeI4 | |
| 熔点/℃ | -49.5 | 26 | 146 |
| 沸点/℃ | 83.1 | 186 | 约400 |
(4)原子坐标参数,表示晶胞内部各原子的相对位置。如图为Ge单晶的晶胞,其中原子坐标参数A为(0,0,0);B为(
 ,0,
,0, );C为(
);C为( ,
, ,0);则D原子的坐标参数为
,0);则D原子的坐标参数为
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐3】理论计算预测,由汞(Hg)、锗(Ge)、锑(Sb)形成的一种新物质X为潜在的拓扑绝缘体材料。X的晶体可视为Ge晶体(晶胞如图a所示)中部分Ge原子被Hg和Sb取代后形成。
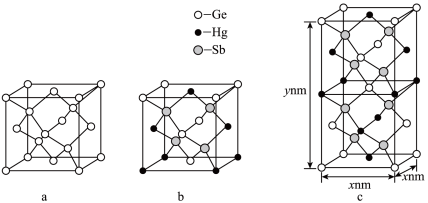
(1)图b为Ge晶胞中部分Ge原子被Hg和Sb取代后形成的一种单元结构,它不是晶胞单元,理由是______________________ 。
(2)图c为X的晶胞,X的晶体中与Hg距离最近的Sb的数目为________ ;该晶胞中粒子个数比Hg∶Ge∶Sb=________ 。
(3)设X的最简式的式量为Mr,则X晶体的密度为____________ g·cm-3(列出算式)。

(1)图b为Ge晶胞中部分Ge原子被Hg和Sb取代后形成的一种单元结构,它不是晶胞单元,理由是
(2)图c为X的晶胞,X的晶体中与Hg距离最近的Sb的数目为
(3)设X的最简式的式量为Mr,则X晶体的密度为
您最近一年使用:0次



