制备 的实验操作如下:向盛有硫酸铜水溶液的试管中加入氨水,首先形成蓝色沉淀,继续添加氨水,沉淀溶解,得到深蓝色的透明溶液;若加入极性较小的溶剂(如乙醇),将析出深蓝色的晶体。回答以下问题:
的实验操作如下:向盛有硫酸铜水溶液的试管中加入氨水,首先形成蓝色沉淀,继续添加氨水,沉淀溶解,得到深蓝色的透明溶液;若加入极性较小的溶剂(如乙醇),将析出深蓝色的晶体。回答以下问题:
(1)“沉淀溶解”时发生反应的离子方程式为_______
(2)基态 价层电子排布式为
价层电子排布式为_______ 。
(3)N、O、S三种元素的第一电离能由大到小的顺序为_______ 。
(4)沸点: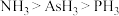 ,原因为
,原因为_______ 。
(5)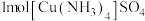 含有σ键的数目为
含有σ键的数目为_______ 。
(6)写出一种与 互为等电子体的分子的化学式
互为等电子体的分子的化学式_______ 。
(7)S与 形成的某化合物晶体的晶胞(实心点表示
形成的某化合物晶体的晶胞(实心点表示 ,空心点表示S)如图所示:
,空心点表示S)如图所示:
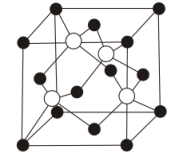
①该化合物的化学式为_______ 。
②已知该晶胞的晶胞参数为 ,阿伏加德罗常数为NA,则该晶胞的密度为
,阿伏加德罗常数为NA,则该晶胞的密度为_____  。
。
 的实验操作如下:向盛有硫酸铜水溶液的试管中加入氨水,首先形成蓝色沉淀,继续添加氨水,沉淀溶解,得到深蓝色的透明溶液;若加入极性较小的溶剂(如乙醇),将析出深蓝色的晶体。回答以下问题:
的实验操作如下:向盛有硫酸铜水溶液的试管中加入氨水,首先形成蓝色沉淀,继续添加氨水,沉淀溶解,得到深蓝色的透明溶液;若加入极性较小的溶剂(如乙醇),将析出深蓝色的晶体。回答以下问题:(1)“沉淀溶解”时发生反应的离子方程式为
(2)基态
 价层电子排布式为
价层电子排布式为(3)N、O、S三种元素的第一电离能由大到小的顺序为
(4)沸点:
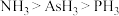 ,原因为
,原因为(5)
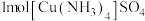 含有σ键的数目为
含有σ键的数目为(6)写出一种与
 互为等电子体的分子的化学式
互为等电子体的分子的化学式(7)S与
 形成的某化合物晶体的晶胞(实心点表示
形成的某化合物晶体的晶胞(实心点表示 ,空心点表示S)如图所示:
,空心点表示S)如图所示:
①该化合物的化学式为
②已知该晶胞的晶胞参数为
 ,阿伏加德罗常数为NA,则该晶胞的密度为
,阿伏加德罗常数为NA,则该晶胞的密度为 。
。
2022·湖南怀化·一模 查看更多[3]
更新时间:2022-05-14 21:51:03
|
相似题推荐
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐1】硼单质及其化合物有重要的应用。阅读下列材料,回答问题:
硼晶体熔点为2076℃。乙硼烷(B2H6)具有还原性,易水解生成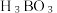 (一元弱酸);乙硼烷可与
(一元弱酸);乙硼烷可与 反应生成氨硼烷(
反应生成氨硼烷( ,其在一定条件下可以脱氢,最终得到氮化硼;乙硼烷也可与NaH反应生成
,其在一定条件下可以脱氢,最终得到氮化硼;乙硼烷也可与NaH反应生成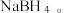
(1)下列说法正确的是_______(填字母)。
(2)根据对角线规则,B的一些化学性质与元素_______ 的相似;B 的空间结构是
的空间结构是_______ 。
(3)硼酸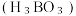 是一种片层状结构的白色晶体(如图),有油腻感,可做润滑剂。
是一种片层状结构的白色晶体(如图),有油腻感,可做润滑剂。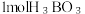 晶体中含有
晶体中含有_______ mol氢键;加热时,硼酸在水中溶解度增大,从结构角度分析,可能的原因为_______ 。
②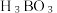 与NaOH溶液反应可以制备硼砂
与NaOH溶液反应可以制备硼砂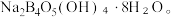 常温下,
常温下, 可以水解生成等物质的量浓度的
可以水解生成等物质的量浓度的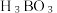 和
和 该水解反应的离子方程式为
该水解反应的离子方程式为_______ 。
(4)氮化硼(BN)晶体有多种相结构。一种立方BN晶体与金刚石结构相似,其晶胞结构如图: 则晶胞中含有BN的个数为
则晶胞中含有BN的个数为_______ (列出计算式,阿伏加德罗常数的数值为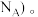
硼晶体熔点为2076℃。乙硼烷(B2H6)具有还原性,易水解生成
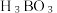 (一元弱酸);乙硼烷可与
(一元弱酸);乙硼烷可与 反应生成氨硼烷(
反应生成氨硼烷( ,其在一定条件下可以脱氢,最终得到氮化硼;乙硼烷也可与NaH反应生成
,其在一定条件下可以脱氢,最终得到氮化硼;乙硼烷也可与NaH反应生成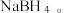
(1)下列说法正确的是_______(填字母)。
| A.元素的电负性大小顺序是O>N>B>H |
B.乙硼烷水解方程式为 |
| C.氨硼烷分子中N提供孤电子对,B提供空轨道形成配位键 |
D.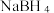 晶体中存在的相互作用有离子键、共价键、氢键 晶体中存在的相互作用有离子键、共价键、氢键 |
 的空间结构是
的空间结构是(3)硼酸
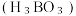 是一种片层状结构的白色晶体(如图),有油腻感,可做润滑剂。
是一种片层状结构的白色晶体(如图),有油腻感,可做润滑剂。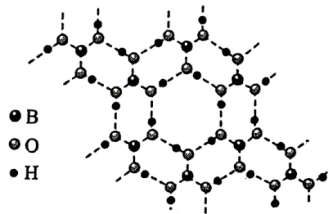
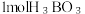 晶体中含有
晶体中含有②
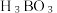 与NaOH溶液反应可以制备硼砂
与NaOH溶液反应可以制备硼砂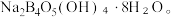 常温下,
常温下, 可以水解生成等物质的量浓度的
可以水解生成等物质的量浓度的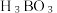 和
和 该水解反应的离子方程式为
该水解反应的离子方程式为(4)氮化硼(BN)晶体有多种相结构。一种立方BN晶体与金刚石结构相似,其晶胞结构如图:
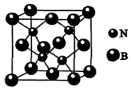
 则晶胞中含有BN的个数为
则晶胞中含有BN的个数为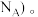
您最近一年使用:0次
【推荐2】氰化钾是一种剧毒物质,贮存和使用时必须注意安全。已知: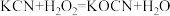 。回答下列问题:
。回答下列问题:
(1) 中所含三种元素的第一电离能从大到小的顺序为
中所含三种元素的第一电离能从大到小的顺序为___________ (用元素符号表示,下同),电负性从大到小的顺序为___________
(2)与 互为等电子体的分子为
互为等电子体的分子为___________ (任举一例)。
(3)试比较下列含氧酸的酸性强弱(填“>”、“<”或“=”):HClO4___________ HClO2,H2SO3___________ H2SO4
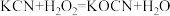 。回答下列问题:
。回答下列问题:(1)
 中所含三种元素的第一电离能从大到小的顺序为
中所含三种元素的第一电离能从大到小的顺序为(2)与
 互为等电子体的分子为
互为等电子体的分子为(3)试比较下列含氧酸的酸性强弱(填“>”、“<”或“=”):HClO4
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐3】镁、铝、硅、银、铁的单质及其化合物在建筑业、飞机制造业、电子工业和石油化工等方面应用广泛。回答下列问题:
(1)Fe3+价层电子的轨道表达式(电子排布图)为__ 。
(2)硅能形成多种化合物(如SiH4、Si2H4等),SiH4的中心原子的杂化轨道类型为__ ,其分子的立体构型为__ ,键角为__ ;Si2H4分子中含有的σ键和π键的数目之比为__ 。
(3)Mg、Al的第一电离能:Mg__ Al(填“>”或“<”)。
(4)Ca和Fe属于同一周期,且核外最外层电子构型相同,但金属Ca的熔点、沸点等都比金属Fe低,原因是__ 。
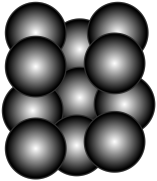
(5)Ag晶体的堆积方式为面心立方最密堆积(如图所示),晶胞中Ag原子的配位数为__ ;设Ag原子半径为rcm,阿伏加 德罗常数的值用NA表示,则Ag晶体的密度为__ g·cm-3(写出表达式)。
(1)Fe3+价层电子的轨道表达式(电子排布图)为
(2)硅能形成多种化合物(如SiH4、Si2H4等),SiH4的中心原子的杂化轨道类型为
(3)Mg、Al的第一电离能:Mg
(4)Ca和Fe属于同一周期,且核外最外层电子构型相同,但金属Ca的熔点、沸点等都比金属Fe低,原因是
(5)Ag晶体的堆积方式为面心立方最密堆积(如图所示),晶胞中Ag原子的配位数为

您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐1】A、B、C、D、E为短周期元素且它们的原子序数依次增大,A的核外电子总数与其周期数相同;其中D原子的L电子层中,成对电子与未成对电子占据的轨道数相同,并且无空轨道;B原子的L电子层中未成对电子数与D相同,但还有空轨道;D与E同族。请回答下列问题:
(1)A与B形成的共价化合物中既含有σ键,又含π键的化合物是___________ (任写一种)。
(2)C的简单氢化物的电子式为___________ 。
(3)B的氢化物中空间结构为正四面体形的是___________ (填名称),键角为___________ ,中心原子的杂化方式为___________ 杂化。
(4)A与B形成B2A2分子,其分子中σ键和π键的数目之比为___________ 。
(5)基态原子第一电离能:C___________ (填“>”“<”或“=”)E.
(6)离子CD3-的中心原子的价层电子对数为___________ 。
(1)A与B形成的共价化合物中既含有σ键,又含π键的化合物是
(2)C的简单氢化物的电子式为
(3)B的氢化物中空间结构为正四面体形的是
(4)A与B形成B2A2分子,其分子中σ键和π键的数目之比为
(5)基态原子第一电离能:C
(6)离子CD3-的中心原子的价层电子对数为
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
【推荐2】回答下列问题
(1)有A、B、C、D、E五种元素,它们的核电荷数依次增大,A是元素周期表中原子半径最小的一种元素,B、C、D、E是连继相邻的四种元素,且均比A多一个电子层,其中E是元素周期表中非金属性最强的一种元素,按要求完成下列问题:
①这几种元素中电负性最大的是_______ (填元素符号,下同);
②B、C、D、E的第一电离能由小到大的顺序是_______ ;
③C的最高价氧化物对应的水化物和C的最低价氢物形成的化合物的化学式是_______ 。
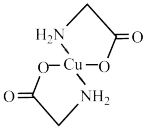
(2)太阳能的开发利用在新能源研究中占据重要地位,单晶硅太阳能电池片在加工时,一般掺杂微量的铜、铁、钴、硼、镓、硒等。其中某种重要的含铜的化合物结构如图。请回答下列问题:
①硅原子电子占据的最高能级电子云形状为_______ ;
②Fe3+的价电子排布图为_______ ;
③铜位于周期表中_______ 区,铜原子的电子排布式为_______ 。试从核外电子排布角度比较,高温下Cu2O和CuO的稳定性更高的原因是_______ 。
(1)有A、B、C、D、E五种元素,它们的核电荷数依次增大,A是元素周期表中原子半径最小的一种元素,B、C、D、E是连继相邻的四种元素,且均比A多一个电子层,其中E是元素周期表中非金属性最强的一种元素,按要求完成下列问题:
①这几种元素中电负性最大的是
②B、C、D、E的第一电离能由小到大的顺序是
③C的最高价氧化物对应的水化物和C的最低价氢物形成的化合物的化学式是
(2)太阳能的开发利用在新能源研究中占据重要地位,单晶硅太阳能电池片在加工时,一般掺杂微量的铜、铁、钴、硼、镓、硒等。其中某种重要的含铜的化合物结构如图。请回答下列问题:

①硅原子电子占据的最高能级电子云形状为
②Fe3+的价电子排布图为
③铜位于周期表中
您最近一年使用:0次
【推荐3】现有位于元素周期表前四周期的A、B、C、D、E、F、G七种非零族元素,它们的原子序数依次增大。请根据下列相关信息,回答有关问题。
(1)由A、C形成的18电子分子的电子式为___________ 。
(2)D元素的基态原子核外共有________ 种不同空间运动状态的电子,B元素基态原子中能量最高的电子所占据的原子轨道呈________ 形。B、C、D三种元素电负性由大到小的顺序为________ (填元素符号)。
(3)某同学推断E元素基态原子的核外电子轨道表示式为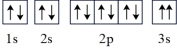 。该同学所画的电子轨道表示式违背了
。该同学所画的电子轨道表示式违背了______ ,该元素的第三电离能I3远远大于其第二电离能I2,其原因是_______ 。
(4)D、E、F三种元素的简单离子半径由大到小的顺序是________ (用离子符号表示)。
(5)检验G元素的方法是______ ,请用原子结构的知识解释其原理:_______ 。
| A | 在周期表的所有元素中原子半径最小 |
| B | 基态原子中有两个未成对电子 |
| C | 基态原子在同周期中未成对电子数最多 |
| D | 基态原子中有两个未成对电子 |
| E | 基态原子中没有未成对电子 |
| F | 同周期元素中电负性最大 |
| G | 同周期元素中第一电离能最小 |
(2)D元素的基态原子核外共有
(3)某同学推断E元素基态原子的核外电子轨道表示式为
 。该同学所画的电子轨道表示式违背了
。该同学所画的电子轨道表示式违背了(4)D、E、F三种元素的简单离子半径由大到小的顺序是
(5)检验G元素的方法是
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐1】钛被誉为“21世纪的金属”,可呈现多种化合价,其中以+4价的Ti最为稳定。回答下列问题:
(1)基态Ti原子的价电子排布图为___________ 。
(2)已知电离能:I2(Ti)=1310 kJ·mol-1,I2(K)=3051 kJ·mol-1,I2(Ti)<I2(K),其原因为___________ 。
(3)钛某配合物可用于催化环烯烃聚合,其结构如图所示:
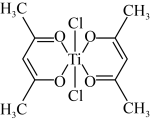
①钛的配位数为___________ ,碳原子的杂化类型___________ 。
②该配合物中存在的化学键有___________ (填字母代号)。
A.离子键 B.配位键 C.金属键 D.共价键 E。氢键
(4)钙钛矿(CaTiO3)是工业获取钛的重要原料。CaTiO3晶胞如下图,边长为a=0.266nm,晶胞中Ti、Ca、O分别处于顶角、体心、面心位置。Ti与O间的最短距离为___________ nm(已知 =1.414),与Ti紧邻的O个数为
=1.414),与Ti紧邻的O个数为___________ 。
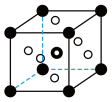
(5)在CaTiO3晶胞结构的另一种表示中,Ca处于各顶角位置,则Ti处于___________ 位置,O处于___________ 位置。
(1)基态Ti原子的价电子排布图为
(2)已知电离能:I2(Ti)=1310 kJ·mol-1,I2(K)=3051 kJ·mol-1,I2(Ti)<I2(K),其原因为
(3)钛某配合物可用于催化环烯烃聚合,其结构如图所示:

①钛的配位数为
②该配合物中存在的化学键有
A.离子键 B.配位键 C.金属键 D.共价键 E。氢键
(4)钙钛矿(CaTiO3)是工业获取钛的重要原料。CaTiO3晶胞如下图,边长为a=0.266nm,晶胞中Ti、Ca、O分别处于顶角、体心、面心位置。Ti与O间的最短距离为
 =1.414),与Ti紧邻的O个数为
=1.414),与Ti紧邻的O个数为
(5)在CaTiO3晶胞结构的另一种表示中,Ca处于各顶角位置,则Ti处于
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐2】(乙酸锰可用于制造钠离子电池的负极材料。可用如下反应制得乙酸锰:4Mn(NO3)2•6H2O+26(CH3CO)2O=4(CH3COO)3Mn+8HNO2+3O2↑+40CH3COOH
(1)Mn3+基态核外电子排布式为___ 。
(2)NO3-中氮原子轨道的杂化类型是___ 。
(3)与HNO2互为等电子体的一种阴离子的化学式为___ 。
(4)配合物[Mn(CH3OH)6]2+中配位原子是___ 。
(5)CH3COOH能与H2O任意比混溶的原因,除它们都是极性分子外还有___ 。
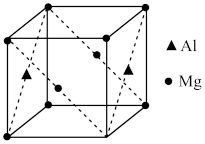
(6)镁铝合金经过高温淬火获得一种储钠材料,其晶胞为立方结构(如图所示),图中原子位于顶点或面心。该晶体中每个铝原子周围距离最近的镁原子数目为___ 。
(1)Mn3+基态核外电子排布式为
(2)NO3-中氮原子轨道的杂化类型是
(3)与HNO2互为等电子体的一种阴离子的化学式为
(4)配合物[Mn(CH3OH)6]2+中配位原子是
(5)CH3COOH能与H2O任意比混溶的原因,除它们都是极性分子外还有
(6)镁铝合金经过高温淬火获得一种储钠材料,其晶胞为立方结构(如图所示),图中原子位于顶点或面心。该晶体中每个铝原子周围距离最近的镁原子数目为

您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐3】氮元素与氢元素能形成多种化合物,在工业、农业和国防等方面用途非常广泛,例如:氨气、肼(N2H4)、叠氮酸(HN3)……等,请回答下列问题:
(1)N位于周期表中____ 区,基态N原子的价电子排布式为____ 。
(2)N2H4分子的电子式为____ ,其中N采取____ 杂化。
(3)叠氮酸(HN3)是一种弱酸,可部分电离出H+和N 。请写出一种与N
。请写出一种与N 互为等电子体的分子的化学式
互为等电子体的分子的化学式____ ;叠氮化物易与过渡金属元素形成配合物,如:[Fe(N3)(NH3)5]SO4,在该配合物中Fe的配位数为____ ,SO 的立体构型为
的立体构型为____ 。
(4)已知Zn2+能与氨分子形成配离子[Zn(NH3)4]2+,1mol该离子含有σ键的数目为____ 。
(5)氮与铝形成的某种晶体的晶胞如图所示。
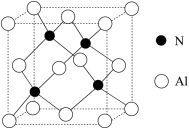
①该晶体的化学式为____ 。
②已知该晶体的密度为dg·cm−3,N和Al的半径分别为apm和bpm,阿伏加德罗常数值为NA。用含a、b、d和NA的式子表示该晶体中原子的空间利用率____ (用含a、b、d和NA的式子表示)。
(1)N位于周期表中
(2)N2H4分子的电子式为
(3)叠氮酸(HN3)是一种弱酸,可部分电离出H+和N
 。请写出一种与N
。请写出一种与N 互为等电子体的分子的化学式
互为等电子体的分子的化学式 的立体构型为
的立体构型为(4)已知Zn2+能与氨分子形成配离子[Zn(NH3)4]2+,1mol该离子含有σ键的数目为
(5)氮与铝形成的某种晶体的晶胞如图所示。

①该晶体的化学式为
②已知该晶体的密度为dg·cm−3,N和Al的半径分别为apm和bpm,阿伏加德罗常数值为NA。用含a、b、d和NA的式子表示该晶体中原子的空间利用率
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐1】2020年2月15日,由国家科研攻关组的主要成员单位的专家组共同研判磷酸氯喹在细胞水平上能
有效抑制新型冠状病毒(2019-nCoV)的感染。
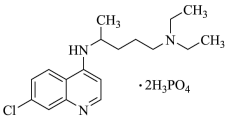
(1)已知磷酸氯喹的结构如图所示,则所含C、N、O三种元素第一电离能由大到小的顺序为_______________ 。P原子核外价层电子排布式为________ ,其核外电子有____ 个空间运动状态。
(2)磷酸氯喹中N原子的杂化方式为_________ ,NH3是一种极易溶于水的气体,其沸点比AsH3的沸点高,其原因是_______________________ 。
(3)H3PO4中PO43- 的空间构型为________________ 。
(4)磷化镓是一种由ⅢA族元素镓(Ga)与VA族元素磷(P)人工合成的Ⅲ—V族化合物半导体材料。晶胞结构可看作金刚石晶胞内部的碳原子被P原子代替,顶点和面心的碳原子被Ga原子代替。
①磷化镓晶体中含有的化学键类型为__________ (填选项字母)
A.离子键 B.配位键 C.σ键 D.π键 E.极性键 F.非极性键
②以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标。若沿y轴投影的晶胞中所有原子的分布图如图,则原子2的分数坐标为______________ 。
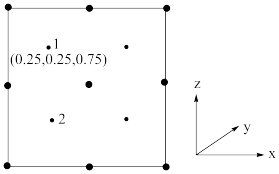
③若磷化镓的晶体密度为ρ g·cm-3,阿伏加 德罗常数的值为NA,则晶胞中Ga和P原子的最近距离为___________ pm。
有效抑制新型冠状病毒(2019-nCoV)的感染。

(1)已知磷酸氯喹的结构如图所示,则所含C、N、O三种元素第一电离能由大到小的顺序为
(2)磷酸氯喹中N原子的杂化方式为
(3)H3PO4中PO43- 的空间构型为
(4)磷化镓是一种由ⅢA族元素镓(Ga)与VA族元素磷(P)人工合成的Ⅲ—V族化合物半导体材料。晶胞结构可看作金刚石晶胞内部的碳原子被P原子代替,顶点和面心的碳原子被Ga原子代替。
①磷化镓晶体中含有的化学键类型为
A.离子键 B.配位键 C.σ键 D.π键 E.极性键 F.非极性键
②以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标。若沿y轴投影的晶胞中所有原子的分布图如图,则原子2的分数坐标为

③若磷化镓的晶体密度为ρ g·cm-3,阿伏加 德罗常数的值为NA,则晶胞中Ga和P原子的最近距离为
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐2】Na2FeO4、Li4YiO12和LiFePO4均可用作电极材料。请回答下列问题:
⑴基态Fe3+的价层电子轨道表达式为________ ;同周期元素中,基态原子的未成对电子数与基态Fe3+相同的元素为________ 。
⑵PO43-的空间构型为________ ,其中P原子的杂化方式为________ ;写出一种与PO43-互为等电子体且中心原子与P不同主族的阴离子:________ (填离子符号)。
⑶[Ti(H2O)6]Cl3为紫色晶体,其中1mol阳离子中所含δ键的数目为________ ;配位键中提供孤电子对的原子为________ (填元素符号)。
⑷已知物质间的转化关系如图甲所示,其中a、c均大于0。
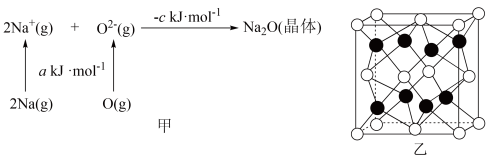
①基态Na原子的第一电离能可表示为________ 。
②相同条件下,Li2O的晶格能________ (填“>”“<”或“=”)ckJ∙mol-1,原因为________________________________ 。
③Na2O的立方晶胞结构如图乙所示。若紧邻的两个Na+之间的距离为d pm,阿伏加 德罗常数的值为NA,晶体的密度为ρ g∙cm-3,则Na的摩尔质量可表示为_______ g∙mol-1(用含有d、ρ、NA的代数式表示)。
⑴基态Fe3+的价层电子轨道表达式为
⑵PO43-的空间构型为
⑶[Ti(H2O)6]Cl3为紫色晶体,其中1mol阳离子中所含δ键的数目为
⑷已知物质间的转化关系如图甲所示,其中a、c均大于0。

①基态Na原子的第一电离能可表示为
②相同条件下,Li2O的晶格能
③Na2O的立方晶胞结构如图乙所示。若紧邻的两个Na+之间的距离为d pm,阿伏加 德罗常数的值为NA,晶体的密度为ρ g∙cm-3,则Na的摩尔质量可表示为
您最近一年使用:0次
【推荐3】A、B、C、D、E、F、G是前四周期元素,原子序数依次增大,根据表中提供的有关信息,回答问题:
(1)E元素在周期表中的位置是______ ,F元素原子最外层电子排布式为_____ ,BD2的空间构型为_____ 。
(2)由D、E、F三种元素形成的一种常见物质的水溶液显碱性,用离子方程式表示其显碱性的原因:_____ 。
(3)氢化物稳定性:B___ D;最高价氧化物对应的水化物酸性:C____ F(选填“<”或“>”)。
(4)每个B2A4分子中含有___ 个σ键,___ 个π键。
(5)G和A可形成化学式为GA的一种晶体,晶胞结构如图所示。若该晶胞的边长为acm,阿伏加德罗常数的值为NA,GA的密度为______ g·cm-3(用含a和NA的式子表示)。
| 元素 | 相关信息 |
| A | 所有单质中密度最小 |
| B | 形成化合物种类最多的元素 |
| D | 基态原子中只有3个能级,有2个未成对电子 |
| E | 短周期中原子半径最大 |
| F | 第三周期中电负性最大的元素 |
| G | 最外层只有一个电子,内层填满电子 |
(2)由D、E、F三种元素形成的一种常见物质的水溶液显碱性,用离子方程式表示其显碱性的原因:
(3)氢化物稳定性:B
(4)每个B2A4分子中含有
(5)G和A可形成化学式为GA的一种晶体,晶胞结构如图所示。若该晶胞的边长为acm,阿伏加德罗常数的值为NA,GA的密度为

您最近一年使用:0次



