已知短周期元素X、Y、Z、W、Q和R在周期表中的相对位置如图所示,X能与W形成两种常见的离子化合物,阴阳离子个数比均为1∶2。回答下列问题:
(1)化合物XR的电子式为____ 。
(2)基态W原子的最外层有____ 个未成对电子。
(3)Z单质与Q的最高价氧化物对应水化物的浓溶液在加热条件下反应的化学方程式为____ 。
(4)Y在Z的最高价氧化物中燃烧的化学方程式为____ 。
| Z | W | |||||
| X | Y | Q | R |
(2)基态W原子的最外层有
(3)Z单质与Q的最高价氧化物对应水化物的浓溶液在加热条件下反应的化学方程式为
(4)Y在Z的最高价氧化物中燃烧的化学方程式为
更新时间:2022-08-22 13:51:09
|
相似题推荐
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐1】A、B、C、D、E、F、G的原子序数依次增大的元素,A、D元素的原子最外层电子数相同,A元素的一种原子没有中子;B的一种同位素可用于考古断代;C是地壳中含量最多的一种元素;D元素的阳离子电子层结构与氖原子相同;E的最外层电子数是电子层数的2倍;F的单质具有强氧化性。G是用途最广泛的金属元素,它的单质能被磁铁所吸引;试回答以下问题:
(1)E的原子结构示意图:______ 。
(2)D单质与C单质在加热条件下反应产物的电子式________ ,该物质与A2C反应的离子方程式______ 。
(3)化合物甲、乙由A、B、C、D中的三种或四种组成的常见物质,且甲、乙的水溶液均呈碱性。则甲、乙反应的化学方程式为______ 。
(4)用电子式写出A2C的形成过程________ 。
(1)E的原子结构示意图:
(2)D单质与C单质在加热条件下反应产物的电子式
(3)化合物甲、乙由A、B、C、D中的三种或四种组成的常见物质,且甲、乙的水溶液均呈碱性。则甲、乙反应的化学方程式为
(4)用电子式写出A2C的形成过程
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐2】下表是元素周期表的一部分,回答下列有关问题:
(1)h的原子结构示意图是_______ 。
(2)c、d、e的简单离子半径由大到小的顺序是_______ (填离子符号)。
(3)d、f、g的气态氢化物的稳定性由强到弱的顺序_______ (填化学式)。
(4)a、c和e三种元素形成化合物含_______ (填化学键类型),它的电子式为_______ 。
(5)用电子式表示由a、g两元素组成的化合物的形成过程:_______ 。
| 周期 | IA | |||||||
| 1 | a | IIA | IIIA | IVA | VA | VIA | VIIA | |
| 2 | b | c | d | |||||
| 3 | e | f | g | |||||
| 4 | h |
(2)c、d、e的简单离子半径由大到小的顺序是
(3)d、f、g的气态氢化物的稳定性由强到弱的顺序
(4)a、c和e三种元素形成化合物含
(5)用电子式表示由a、g两元素组成的化合物的形成过程:
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
【推荐3】下表为元素周期表的一部分,表中所列的字母分别代表一种化学元素。
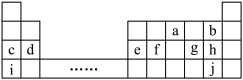
(1)元素a、b、c对应原子半径由大到小的顺序是_______ (用对应元素符号表示,下同)。
元素a、b、c对应简单离子中,半径最小的是_______ (用对应离子符号)。
(2)写出由上述元素形成的最高价氧化物对应水化物酸性最强的酸和最高价氧化物对应水化物碱性最强的碱反应的化学方程式:_______ 。
(3)上述元素中最高正化合价与最低负化合价绝对值相等的元素是_______ 。
(4)g的简单氢化物的电子式为_______ 。
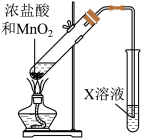
(5)用如图所示装置可以比较h和j的单质氧化性强弱,则X可以是_______ (填化学式)。

(1)元素a、b、c对应原子半径由大到小的顺序是
元素a、b、c对应简单离子中,半径最小的是
(2)写出由上述元素形成的最高价氧化物对应水化物酸性最强的酸和最高价氧化物对应水化物碱性最强的碱反应的化学方程式:
(3)上述元素中最高正化合价与最低负化合价绝对值相等的元素是
(4)g的简单氢化物的电子式为
(5)用如图所示装置可以比较h和j的单质氧化性强弱,则X可以是

您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐1】下表显示了碳元素(C)和①~⑥6种短周期元素在周期表中的位置:
回答下列问题:
(1)①的单质的分子式为__________ 。
(2)②的原子结构示意图为__________ 。
(3)按①→②→③的顺序,其简单氢化物的稳定性逐渐__________ (填“增强”或“减弱”)。
(4)④为稀有气体元素,它的化学性质__________ (填“活泼”或“不活泼”)。
(5)⑤和⑥的单质在加热的条件下剧烈反应,写出该反应的化学方程式__________ 。
周期 | 族 | |||||||
ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
2 | C | ① | ② | ③ | ④ | |||
3 | ⑤ | ⑥ | ||||||
(1)①的单质的分子式为
(2)②的原子结构示意图为
(3)按①→②→③的顺序,其简单氢化物的稳定性逐渐
(4)④为稀有气体元素,它的化学性质
(5)⑤和⑥的单质在加热的条件下剧烈反应,写出该反应的化学方程式
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐2】X、Y、Z、W是元素周期表中原子序数依次增大的四种短周期元素,其相关信息如表:
(1)X和W的元素符号分别为___ 、___ 。
(2)X与Y形成的原子个数比为2∶1的化合物中,Y原子最外层为8电子结构,请写出该化合物的电子式___ ,工业合成Y的氢化物的化学方程式为___ 。
(3)X和Z组成的化合物中,既含有极性共价键又含有非极性共价键的是___ 。此化合物还可将碱性工业废水中的CN-氧化为碳酸盐和氨,相应的离子方程式为___ 。
| 元素 | 相关信息 |
| X | X的单质为密度最小的气体 |
| Y | Y的氢化物的水溶液呈碱性 |
| Z | Z是地壳中含量最高的元素 |
| W | W的一种核素的质量数为35,中子数为18 |
(2)X与Y形成的原子个数比为2∶1的化合物中,Y原子最外层为8电子结构,请写出该化合物的电子式
(3)X和Z组成的化合物中,既含有极性共价键又含有非极性共价键的是
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
【推荐3】如图是元素周期表的一部分,其中每个字母代表对应的一种元素。
请按要求回答下列问题:
(1)写出D与E按 的原子个数比形成的化合物与水反应的离子方程式:
的原子个数比形成的化合物与水反应的离子方程式:___________ ,F的原子结构示意图为___________ 。
(2)B在周期表中的位置为___________ ,A、C、F三种元素形成的化合物CA4F中阳离子的检验方法为:取少量待测液,___________ 。
(3)化合物甲由A、B、D、E四种元素组成,俗称小苏打,乙由A、D、E三种元素组成,则甲、乙反应的离子方程式为___________ 。
(4)C、D、E的原子半径由大到小的顺序是___________ (用元素符号表示)。
(5)B的非金属性___________ 于C(填“强”或“弱”),并用化学方程式证明上述结论___________ 。
| A | |||||||||||||
| B | C | D | |||||||||||
| E | F |
(1)写出D与E按
 的原子个数比形成的化合物与水反应的离子方程式:
的原子个数比形成的化合物与水反应的离子方程式:(2)B在周期表中的位置为
(3)化合物甲由A、B、D、E四种元素组成,俗称小苏打,乙由A、D、E三种元素组成,则甲、乙反应的离子方程式为
(4)C、D、E的原子半径由大到小的顺序是
(5)B的非金属性
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐1】下表是元素周期表的一部分,针对表中的①~⑩种元素,填写下列空白(填写序号不得分):
(1)比较①与⑤的最高价氧化物对应的水化物,_____ 的酸性强(填化学式 )
(2)工业上制取②的氢化物的化学方程式 _____ ;②的氢化物与②的最高价氧化物的水化物反应所得的产物化学式 为____ 。
(3)②可以形成多种氧化物,其中一种是红棕色气体,试用方程式说明该气体不宜采用排水法收集的原因_____ (用化学方程式 表示)
(4)比较③与⑥的氢化物,____ 更稳定,_____ 沸点更高(填化学式 )
(5)⑦元素和⑨元素它们可以形成__ (填离子或共价)化合物,用电子式表示其形成过程__ 。
族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0族 |
| 二 | ① | ② | ③ | ④ | ||||
| 三 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
| 四 | ⑨ | ⑩ |
(2)工业上制取②的氢化物的
(3)②可以形成多种氧化物,其中一种是红棕色气体,试用方程式说明该气体不宜采用排水法收集的原因
(4)比较③与⑥的氢化物,
(5)⑦元素和⑨元素它们可以形成
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐2】A、B、D、E、F、G为短周期元素,且原子序数依次递增。A、F同主族,E、G同主族。A与其他非金属元素化合时易形成共价键,F与具他非金属元素化合时易形成离子键,且F+与E2-核外电子排布相同。由以上元素组成的物质BE和 具有相同的电子数。请回答以下问题:
具有相同的电子数。请回答以下问题:
(1)G位于第______ 周期第______ 族。
(2)用电子式表示 :
:_________ 。
(3)由A、E、F三种元素形成的化合物的化学式为_______ ,含有的化学键有______ (填“离子键”“极性键”或“非极性键”)。
(4)写出A与B形成的10电子分子的结构式是______ 。
(5) 与
与 的沸点:
的沸点:
____  的沸点(填“高于”或“低于”)
的沸点(填“高于”或“低于”)
 具有相同的电子数。请回答以下问题:
具有相同的电子数。请回答以下问题:(1)G位于第
(2)用电子式表示
 :
:(3)由A、E、F三种元素形成的化合物的化学式为
(4)写出A与B形成的10电子分子的结构式是
(5)
 与
与 的沸点:
的沸点:
 的沸点(填“高于”或“低于”)
的沸点(填“高于”或“低于”)
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
【推荐3】已知a、b、d、e、 f、g、 h为原子序数依次增大的六种短周期主族元素, 非金属元素a最外层电子数与其周期数相同,b原子的最外层电子数是其所在周期数的2倍。d的一种单质可杀菌消毒,g的最高正价与最低负价代数和为4, f的最高价氧化物可分别与e和h的最高价氧化物的水化物反应,a单质在h单质中燃烧,产物溶于水得到一种强酸甲。请用化学用语回答下列问题:
(1)f在元素周期表中的位置___ 画出与h同族的第四周期元素的原子结构示意图____________ 。
(2)d、e、f、h的简单离子的半径由大到小的顺序_________ 。
(3)下列说法正确的是 。
(4)设计一个简单的实验证明d和g的非金属性强弱: _________ (用化学方程式表示)。
(5)为降低水源中NO 对人体的危害,可在强碱性条件下用f的单质将溶液中的NO
对人体的危害,可在强碱性条件下用f的单质将溶液中的NO 还原为N2,该反应的离子方程式为
还原为N2,该反应的离子方程式为______________ 。
(6)将e和f单质各1mol投入足量水中,充分反应后,所得溶液体积为500mL,则该过程可得标况下气体体积_______ L。最终获得溶液的物质的量浓度为_____ mol∙L−1。
(1)f在元素周期表中的位置
(2)d、e、f、h的简单离子的半径由大到小的顺序
(3)下列说法正确的是 。
| A.氢化物的稳定性d>b |
| B.含氧酸的酸性h>g>b>f |
| C.bg2中b为+4价;g为−2价可说明g的非金属性强于b |
| D.g阴离子能与Fe3+反应而h的阴离子不能,可说明g的非金属性弱于h |
(5)为降低水源中NO
 对人体的危害,可在强碱性条件下用f的单质将溶液中的NO
对人体的危害,可在强碱性条件下用f的单质将溶液中的NO 还原为N2,该反应的离子方程式为
还原为N2,该反应的离子方程式为(6)将e和f单质各1mol投入足量水中,充分反应后,所得溶液体积为500mL,则该过程可得标况下气体体积
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
解题方法
【推荐1】含铜丰富的自然资源黄铜矿( )冶炼铜的工艺流程如下:
)冶炼铜的工艺流程如下:
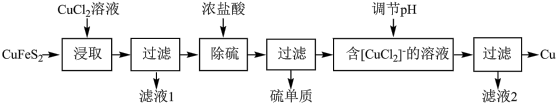
已知:
(1)在元素周期表中,Cu价层电子排布为____ 。
(2)为提高“浸取”时的反应速率,通常可采用的措施有________ (答一条即可)。
(3)“除硫”时加入浓盐酸发生反应的离子方程式为_______ 。
(4)调节溶液的pH后,除生成Cu外,还能产生一种金属离子,此金属离子是______ 。(填离子符号)
(5)“滤液2”中可以循环使用的物质为HCl、_______ ,为保持流程持续循环,每生成1molCu,理论上需补充 的物质的量为
的物质的量为___ 。
(6)冶炼工艺还可以将精选后的黄铜矿砂与空气在高温下煅烧,使其转变为铜,发生的反应为
 、
、 。此工艺与前一工艺相比主要缺点有
。此工艺与前一工艺相比主要缺点有______________________________ (任答一点)。
 )冶炼铜的工艺流程如下:
)冶炼铜的工艺流程如下:
已知:

(1)在元素周期表中,Cu价层电子排布为
(2)为提高“浸取”时的反应速率,通常可采用的措施有
(3)“除硫”时加入浓盐酸发生反应的离子方程式为
(4)调节溶液的pH后,除生成Cu外,还能产生一种金属离子,此金属离子是
(5)“滤液2”中可以循环使用的物质为HCl、
 的物质的量为
的物质的量为(6)冶炼工艺还可以将精选后的黄铜矿砂与空气在高温下煅烧,使其转变为铜,发生的反应为

 、
、 。此工艺与前一工艺相比主要缺点有
。此工艺与前一工艺相比主要缺点有
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
【推荐2】碳、硅、铁、铜、铝、钛是重要的材料元素。请回答下列有关问题:
(1)上述元素中属于主族元素的是___________ (填写元素符号,下同),在元素周期表d区的元素是___________ 。
(2)原子核外电子含有四个电子层的元素是___________ ,基态原子的原子轨道中未成对电子数最多的是___________ 。
(3)基态钛原子价电子的轨道表示式为___________ 。
(4)基态铜原子的价电子排布式为3d104s1,由此可判断铜在元素周期表中位于第___________ 周期___________ 族。
(1)上述元素中属于主族元素的是
(2)原子核外电子含有四个电子层的元素是
(3)基态钛原子价电子的轨道表示式为
(4)基态铜原子的价电子排布式为3d104s1,由此可判断铜在元素周期表中位于第
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
【推荐3】中国科学家参与的国际阿伏加德罗组织以高纯单晶28Si为样品高精度地测定了NA。
Ⅰ.高纯单晶28Si的制备流程如下___________ 。
(2)SiF4分子的空间构型是___________ 。
(3)写出反应②的化学方程式___________ 。
(4)③中发生分解反应,判断SiH4的分解温度___________ (填“大于”或“小于”)CH4的分解温度,理由是___________ 。
Ⅱ.NA的测定
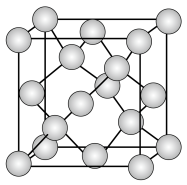
(5)单晶硅的晶胞结构如图所示,X射线衍射测定其边长为a cm。___________ 。
Ⅰ.高纯单晶28Si的制备流程如下

(2)SiF4分子的空间构型是
(3)写出反应②的化学方程式
(4)③中发生分解反应,判断SiH4的分解温度
Ⅱ.NA的测定
(5)单晶硅的晶胞结构如图所示,X射线衍射测定其边长为a cm。
您最近一年使用:0次



