我国科学家是近成功合成了世界上首个五氮阴离子盐 (用R代表)。回答下列问题:
(用R代表)。回答下列问题:
(1)氮原子价层电子的轨道表达式(电子排布图)为_______ ,其能量最高的电子排布的轨道呈_______ 形。
(2)经X射线辐射测得化合物R的晶体结构,其局部结构如图所示。
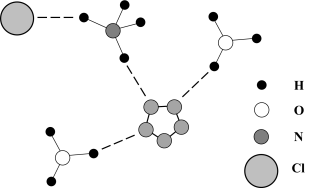
①从结构角度分析,R中两种阳离子的相同之处为_______ ,不同之处为_______ (填标号)
A.中心原子的杂化类型 B.中心原子的价层电子对数
C.立体结构 D.共价键类型
②R中阴离子 中的σ键总数为
中的σ键总数为_______ 个。分子中的大π键可用符号 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为
表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为 ),则
),则 中的大π键应表示为
中的大π键应表示为_______ 。
③比较键角: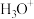
_______  ,并用物质结构的观点解释原因:
,并用物质结构的观点解释原因:_______ 。
④元素H、O、N的电负性由小到大的顺序_______ 。
 (用R代表)。回答下列问题:
(用R代表)。回答下列问题:(1)氮原子价层电子的轨道表达式(电子排布图)为
(2)经X射线辐射测得化合物R的晶体结构,其局部结构如图所示。

①从结构角度分析,R中两种阳离子的相同之处为
A.中心原子的杂化类型 B.中心原子的价层电子对数
C.立体结构 D.共价键类型
②R中阴离子
 中的σ键总数为
中的σ键总数为 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为
表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为 ),则
),则 中的大π键应表示为
中的大π键应表示为③比较键角:
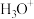
 ,并用物质结构的观点解释原因:
,并用物质结构的观点解释原因:④元素H、O、N的电负性由小到大的顺序
更新时间:2022-04-07 23:14:44
|
相似题推荐
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐1】Li是最轻的固体金属,采用Li作为负极材料的电池具有小而轻、能量密度大等优良性能,得到广泛应用。回答下列问题:
(1)下列Li原子电子排布图表示的状态中,能量最低和最高的分别为___ 、___ (填标号)。
A.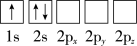
B.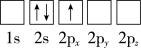
C.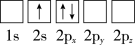
D.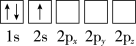
(2)Li+与H−具有相同的电子构型,r(Li+)小于r(H−),原因是___ 。
(3)LiAlH4是有机合成中常用的还原剂,LiAlH4中的阴离子(AlH )空间构型是
)空间构型是___ 、中心原子的杂化形式为___ 。
(4)Li2O是离子晶体,其晶格能可通过如图的Born−Haber循环计算得到。
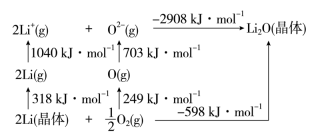
可知,Li原子的第一电离能为___ kJ·mol−1,O=O键键能为___ kJ·mol−1。
(1)下列Li原子电子排布图表示的状态中,能量最低和最高的分别为
A.

B.

C.

D.

(2)Li+与H−具有相同的电子构型,r(Li+)小于r(H−),原因是
(3)LiAlH4是有机合成中常用的还原剂,LiAlH4中的阴离子(AlH
 )空间构型是
)空间构型是(4)Li2O是离子晶体,其晶格能可通过如图的Born−Haber循环计算得到。
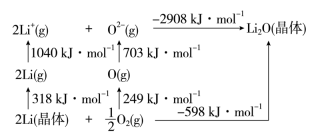
可知,Li原子的第一电离能为
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐2】碳元素在自然界中分布很广,是存在形式最复杂的元素。实验室可用邻二氮菲(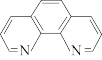 )与
)与 形成的红色配合物(如下图)测定铁的含量。
形成的红色配合物(如下图)测定铁的含量。
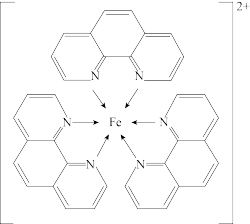
回答下列问题:
(1)基态Fe原子的价层电子排布式为_______ 。
(2)红色配合物中非金属元素的电负性从大到小的顺序为_______ 。
(3)邻二氮菲分子中C、N两种元素原子的杂化方式分别为_______ 、_______ 。
(4)红色配合物的中心原子的配位数为_______ 。
(5)红色配合物中不存在的作用力有_______ 。
A.σ键 B.π键 C.离子键 D.氢键 E.配位键
(6)上世纪末,科学家合成了硬度超过金刚石的 晶体,该晶体的硬度比金刚石大的原因是
晶体,该晶体的硬度比金刚石大的原因是_______ 。
(7)碳化硅俗称金刚砂,也是一种硬度很大的固体,其晶胞结构如下图所示,Si原子的配位数是_______ 。已知相邻的碳硅原子的核间距为dpm,阿伏加德罗常数数值为 ,该晶体的密度为
,该晶体的密度为_______  (列出计算式)。
(列出计算式)。

 )与
)与 形成的红色配合物(如下图)测定铁的含量。
形成的红色配合物(如下图)测定铁的含量。
回答下列问题:
(1)基态Fe原子的价层电子排布式为
(2)红色配合物中非金属元素的电负性从大到小的顺序为
(3)邻二氮菲分子中C、N两种元素原子的杂化方式分别为
(4)红色配合物的中心原子的配位数为
(5)红色配合物中不存在的作用力有
A.σ键 B.π键 C.离子键 D.氢键 E.配位键
(6)上世纪末,科学家合成了硬度超过金刚石的
 晶体,该晶体的硬度比金刚石大的原因是
晶体,该晶体的硬度比金刚石大的原因是(7)碳化硅俗称金刚砂,也是一种硬度很大的固体,其晶胞结构如下图所示,Si原子的配位数是
 ,该晶体的密度为
,该晶体的密度为 (列出计算式)。
(列出计算式)。
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐3】制备 的实验操作如下:向盛有硫酸铜水溶液的试管中加入氨水,首先形成蓝色沉淀,继续添加氨水,沉淀溶解,得到深蓝色的透明溶液;若加入极性较小的溶剂(如乙醇),将析出深蓝色的晶体。回答以下问题:
的实验操作如下:向盛有硫酸铜水溶液的试管中加入氨水,首先形成蓝色沉淀,继续添加氨水,沉淀溶解,得到深蓝色的透明溶液;若加入极性较小的溶剂(如乙醇),将析出深蓝色的晶体。回答以下问题:
(1)“沉淀溶解”时发生反应的离子方程式为_______
(2)基态 价层电子排布式为
价层电子排布式为_______ 。
(3)N、O、S三种元素的第一电离能由大到小的顺序为_______ 。
(4)沸点: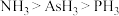 ,原因为
,原因为_______ 。
(5)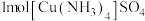 含有σ键的数目为
含有σ键的数目为_______ 。
(6)写出一种与 互为等电子体的分子的化学式
互为等电子体的分子的化学式_______ 。
(7)S与 形成的某化合物晶体的晶胞(实心点表示
形成的某化合物晶体的晶胞(实心点表示 ,空心点表示S)如图所示:
,空心点表示S)如图所示:
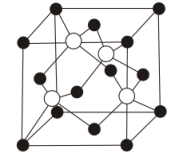
①该化合物的化学式为_______ 。
②已知该晶胞的晶胞参数为 ,阿伏加德罗常数为NA,则该晶胞的密度为
,阿伏加德罗常数为NA,则该晶胞的密度为_____  。
。
 的实验操作如下:向盛有硫酸铜水溶液的试管中加入氨水,首先形成蓝色沉淀,继续添加氨水,沉淀溶解,得到深蓝色的透明溶液;若加入极性较小的溶剂(如乙醇),将析出深蓝色的晶体。回答以下问题:
的实验操作如下:向盛有硫酸铜水溶液的试管中加入氨水,首先形成蓝色沉淀,继续添加氨水,沉淀溶解,得到深蓝色的透明溶液;若加入极性较小的溶剂(如乙醇),将析出深蓝色的晶体。回答以下问题:(1)“沉淀溶解”时发生反应的离子方程式为
(2)基态
 价层电子排布式为
价层电子排布式为(3)N、O、S三种元素的第一电离能由大到小的顺序为
(4)沸点:
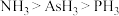 ,原因为
,原因为(5)
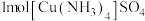 含有σ键的数目为
含有σ键的数目为(6)写出一种与
 互为等电子体的分子的化学式
互为等电子体的分子的化学式(7)S与
 形成的某化合物晶体的晶胞(实心点表示
形成的某化合物晶体的晶胞(实心点表示 ,空心点表示S)如图所示:
,空心点表示S)如图所示:
①该化合物的化学式为
②已知该晶胞的晶胞参数为
 ,阿伏加德罗常数为NA,则该晶胞的密度为
,阿伏加德罗常数为NA,则该晶胞的密度为 。
。
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
【推荐1】Ⅰ.已知元素M是组成物质 NH4Al(SO4)2的其中一种元素。元素M的气态原子逐个失去第1个至第4个电子所需能量(即电离能,用符号I1至I4表示)如表所示:
(1)元素M是_______ (填元素符号)。
(2)NH4Al(SO4)2中,电负性最大的元素是_______ (填元素符号),S的_______ 杂化轨道与O的2p轨道形成_______ 键。
Ⅱ.如图所示为高温超导领域里的一种化合物-钙钛矿晶体结构,该结构是具有代表性的最小重复单位。
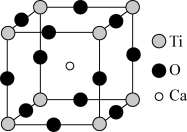
(3)在该物质的晶体结构中,每个钛离子周围与它最接近且距离相等的氧离子、钙离子各有_______ 个、_______ 个。
(4)该晶体结构中,氧、钛、钙的离子个数比是_______
(5)若钙、钛、氧三种元素的相对质量分别为a、b、c,晶体结构图中正方体边长(钛离子之间的距离)为d nm(1 nm=10-9 m),则该晶体的密度为_______ g/cm3。
| I1 | I2 | I3 | I4 | |
| 电离能(kJ·mol-1) | 578 | 1817 | 2745 | 11578 |
(2)NH4Al(SO4)2中,电负性最大的元素是
Ⅱ.如图所示为高温超导领域里的一种化合物-钙钛矿晶体结构,该结构是具有代表性的最小重复单位。

(3)在该物质的晶体结构中,每个钛离子周围与它最接近且距离相等的氧离子、钙离子各有
(4)该晶体结构中,氧、钛、钙的离子个数比是
(5)若钙、钛、氧三种元素的相对质量分别为a、b、c,晶体结构图中正方体边长(钛离子之间的距离)为d nm(1 nm=10-9 m),则该晶体的密度为
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐2】我国可燃冰资源一直被视为能源领域的宝藏,可燃冰被寄予厚望成为替代传统石油和天然气的清洁能源。回答下列问题:
(1)一定条件下, 、
、 都能与
都能与 形成笼状结构(如图所示)的水合物晶体,其相关参数见下表。
形成笼状结构(如图所示)的水合物晶体,其相关参数见下表。 与
与 形成的水合物晶体俗称“可燃冰”。
形成的水合物晶体俗称“可燃冰”。
 和
和 所含的三种元素电负性从大到小的顺序为
所含的三种元素电负性从大到小的顺序为___________ ;碳原子的最高能级的符号是___________ ,其电子云形状是___________ 。
(2) 分子的空间结构为
分子的空间结构为___________ 。相同条件下 与
与 在水中的溶解度较大的是
在水中的溶解度较大的是 ,理由是
,理由是___________ 。
(3)“可燃冰”中分子间存在的两种作用力是___________ 。
(4)下列关于 和
和 的说法正确的是___________(填标号)。
的说法正确的是___________(填标号)。
(5)为开采深海海底的“可燃冰”,有科学家提出用 置换
置换 的设想。已知上图中笼状结构的空腔直径为0.586nm,根据上述图表,从物质结构及性质的角度分析,该设想的依据是
的设想。已知上图中笼状结构的空腔直径为0.586nm,根据上述图表,从物质结构及性质的角度分析,该设想的依据是___________ 。
(1)一定条件下,
 、
、 都能与
都能与 形成笼状结构(如图所示)的水合物晶体,其相关参数见下表。
形成笼状结构(如图所示)的水合物晶体,其相关参数见下表。 与
与 形成的水合物晶体俗称“可燃冰”。
形成的水合物晶体俗称“可燃冰”。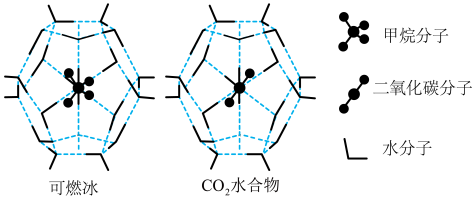
| 参数分子 | 分子直径/nm | 分子与 的结合能E/(kJ·mol 的结合能E/(kJ·mol ) ) |
 | 0.436 | 16.40 |
 | 0.512 | 29.91 |
 和
和 所含的三种元素电负性从大到小的顺序为
所含的三种元素电负性从大到小的顺序为(2)
 分子的空间结构为
分子的空间结构为 与
与 在水中的溶解度较大的是
在水中的溶解度较大的是 ,理由是
,理由是(3)“可燃冰”中分子间存在的两种作用力是
(4)下列关于
 和
和 的说法正确的是___________(填标号)。
的说法正确的是___________(填标号)。A. 分子中含有2个σ键和2个π键 分子中含有2个σ键和2个π键 |
B. 分子中含有极性共价键,是极性分子 分子中含有极性共价键,是极性分子 |
C.因为碳氢键键能小于碳氧键,所以 的熔点低于 的熔点低于 |
D. 和 和 分子中碳原子的杂化类型分别是 分子中碳原子的杂化类型分别是 和sp 和sp |
(5)为开采深海海底的“可燃冰”,有科学家提出用
 置换
置换 的设想。已知上图中笼状结构的空腔直径为0.586nm,根据上述图表,从物质结构及性质的角度分析,该设想的依据是
的设想。已知上图中笼状结构的空腔直径为0.586nm,根据上述图表,从物质结构及性质的角度分析,该设想的依据是
您最近一年使用:0次
【推荐3】钙钛矿型化合物是一类可用于生产太阳能电池、传感器、固体电阻器等的功能材料,如图所示为钙钛矿晶体结构,该结构是其晶体中具有代表性的最小重复单位。
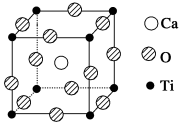
回答下列问题:
(1)在该物质的晶体结构中,每个钛离子周围与它最接近且距离相等的钛离子、钙离子各有___________ 个、___________ 个。该物质的化学式可表示为___________ 。
(2)Ti的四卤化物熔点如下表所示,TiF4熔点高于其他三种卤化物,自TiCl4至TiI4熔点依次升高,原因是___________ 。
(3)钙钛矿的组成元素中电负性大小顺序是___________ ;金属离子与氧离子间的作用力为___________ 。

回答下列问题:
(1)在该物质的晶体结构中,每个钛离子周围与它最接近且距离相等的钛离子、钙离子各有
(2)Ti的四卤化物熔点如下表所示,TiF4熔点高于其他三种卤化物,自TiCl4至TiI4熔点依次升高,原因是
化合物 | TiF4 | TiCl4 | TiBr4 | TiI4 |
熔点/℃ | 377 | -24.12 | 38.3 | 155 |
(3)钙钛矿的组成元素中电负性大小顺序是
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐1】已知  和
和 可以形成
可以形成  和
和  两种化合物,试根据有关信息完成下列问题:
两种化合物,试根据有关信息完成下列问题:
① 内的
内的  水分子间的范德华力和氢键,从强到弱依次为
水分子间的范德华力和氢键,从强到弱依次为___________ ;
②用球棍模型表示的水分子结构是 ; 可与
可与  形成
形成 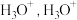 中的
中的 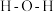 键角比
键角比  的键角
的键角___________ 。(填“大”或“小”)
(2)已知 分子的结构如图所示:
分子的结构如图所示: 分子不是直线形的,两个氢原子犹如在半展开的书的两面上,两个氧原子在书脊位置上,书页夹角
分子不是直线形的,两个氢原子犹如在半展开的书的两面上,两个氧原子在书脊位置上,书页夹角 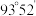 ,而两个
,而两个  键与
键与  键的夹角均为
键的夹角均为 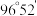 。
。
请回答下列问题:
① 子的电子式是
子的电子式是___________ ,结构式是___________ 。
② 分子是含有
分子是含有___________ 键和___________ 键的___________ (填“极性”或“非极性”)分子。
③ 能与水混溶,却不溶于
能与水混溶,却不溶于  试剂,请予以解释:
试剂,请予以解释:___________ 。
 和
和 可以形成
可以形成  和
和  两种化合物,试根据有关信息完成下列问题:
两种化合物,试根据有关信息完成下列问题: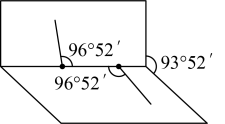
①
 内的
内的 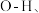 水分子间的范德华力和氢键,从强到弱依次为
水分子间的范德华力和氢键,从强到弱依次为②用球棍模型表示的水分子结构是 ;
A. 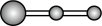 B.
B. 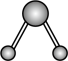 C.
C.  D.
D.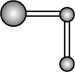
 可与
可与  形成
形成 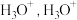 中的
中的 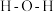 键角比
键角比  的键角
的键角(2)已知
 分子的结构如图所示:
分子的结构如图所示: 分子不是直线形的,两个氢原子犹如在半展开的书的两面上,两个氧原子在书脊位置上,书页夹角
分子不是直线形的,两个氢原子犹如在半展开的书的两面上,两个氧原子在书脊位置上,书页夹角 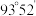 ,而两个
,而两个  键与
键与  键的夹角均为
键的夹角均为 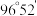 。
。请回答下列问题:
①
 子的电子式是
子的电子式是②
 分子是含有
分子是含有③
 能与水混溶,却不溶于
能与水混溶,却不溶于  试剂,请予以解释:
试剂,请予以解释:
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐2】明代科学家宋应星在《天工开物》中写道:“凡玉入中国,贵者尽出于田葱岭”。和田玉的主要化学成分是含水的钙镁硅酸盐。回答下列问题:
(1)元素镁能形成很多简单微粒,下面是镁原子形成的微粒的电子排布式,其中再电离出一个电子所需能量最大的是______ (填标号),当从C状态变到B状态,形成的是______ 光谱(选填“发射”或“吸收”)。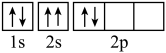 ,该电子排布图违背了
,该电子排布图违背了______ 。
(3)元素钙、镁和氯三种元素形成的最高价氧化物的水化物中,碱性最强的是______ (填化学式,下同),酸性最强的是______ 。
(4) 中中心原子Si的杂化类型是
中中心原子Si的杂化类型是______ ,离子空间结构为______ 。
(5)在 中不存在的化学键类型有
中不存在的化学键类型有______ 。
A.非极性共价键 B.极性共价键 C. 键 D.
键 D. 键
键
碳酸( )的酸性比硅酸(
)的酸性比硅酸( )
)______ (填“强”或“弱”),用离子方程式证明______ 。
(6)羧基( )能电离出
)能电离出 ,使溶液呈现酸性,已知
,使溶液呈现酸性,已知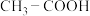 的酸性小于
的酸性小于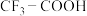 ,则推电子能力较强的是
,则推电子能力较强的是______ (填“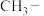 ”或“
”或“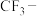 ”)
”)
(1)元素镁能形成很多简单微粒,下面是镁原子形成的微粒的电子排布式,其中再电离出一个电子所需能量最大的是
A. 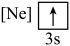 B.
B.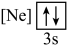 C.
C. 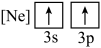 D.
D.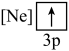
 ,该电子排布图违背了
,该电子排布图违背了(3)元素钙、镁和氯三种元素形成的最高价氧化物的水化物中,碱性最强的是
(4)
 中中心原子Si的杂化类型是
中中心原子Si的杂化类型是(5)在
 中不存在的化学键类型有
中不存在的化学键类型有A.非极性共价键 B.极性共价键 C.
 键 D.
键 D. 键
键碳酸(
 )的酸性比硅酸(
)的酸性比硅酸( )
)(6)羧基(
 )能电离出
)能电离出 ,使溶液呈现酸性,已知
,使溶液呈现酸性,已知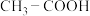 的酸性小于
的酸性小于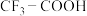 ,则推电子能力较强的是
,则推电子能力较强的是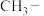 ”或“
”或“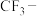 ”)
”)
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
【推荐3】电气石是一种具有保健作用的天然石材,其中含有的主要元素为 等元素。
等元素。
(1)上述元素中,原子半径最小的是_______ (用元素符号表示),与硫同周期的元素中简单离子半径最小的是_______ (用离子符号表示);
(2)用轨道表示式表示氧元素原子核外电子的运动状态_______ ;氧元素原子核外有_______ 种不同能量的电子;
(3) 分子中
分子中 为
为_______ 杂化,键角等于_______ ,可以判断出 分子为
分子为_______ 分子(选填“极性”或“非极性”); 晶体的熔点比
晶体的熔点比 晶体
晶体_______ (选填“高”、“低”),原因为_______ 。
 等元素。
等元素。(1)上述元素中,原子半径最小的是
(2)用轨道表示式表示氧元素原子核外电子的运动状态
(3)
 分子中
分子中 为
为 分子为
分子为 晶体的熔点比
晶体的熔点比 晶体
晶体
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐1】Fe、Co、Ni是几种重要的金属元素。请回答下列问题。
(1)基态Co原子的价电子轨道表示式为___________ 。
(2) 常温下为无色液体,沸点为42.1℃,熔点为-19.3℃,难溶于水,易溶于有机溶剂。推测
常温下为无色液体,沸点为42.1℃,熔点为-19.3℃,难溶于水,易溶于有机溶剂。推测 是
是___________ 分子(填“极性”或“非极性”)。
(3)实验室常用KSCN溶液或苯酚(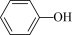 )检验
)检验 。第一电离能:N
。第一电离能:N___________ O(填“>”或“<”),KSCN的配位原子有___________ 。苯酚中碳原子和氧原子的杂化类型分别为___________ ;___________ 。
(4)配位化合物 中心原子Co的配位数为
中心原子Co的配位数为___________ ,配体为___________ 。
(5)ZnS在荧光体、光导体材料、涂料、颜料等行业中应用广泛。立方ZnS晶体结构如下图所示,S原子的配位数是___________ ,其晶胞边长为540.0pm,密度为___________ (列式并计算)。Zn:65 S:32
(1)基态Co原子的价电子轨道表示式为
(2)
 常温下为无色液体,沸点为42.1℃,熔点为-19.3℃,难溶于水,易溶于有机溶剂。推测
常温下为无色液体,沸点为42.1℃,熔点为-19.3℃,难溶于水,易溶于有机溶剂。推测 是
是(3)实验室常用KSCN溶液或苯酚(
 )检验
)检验 。第一电离能:N
。第一电离能:N(4)配位化合物
 中心原子Co的配位数为
中心原子Co的配位数为(5)ZnS在荧光体、光导体材料、涂料、颜料等行业中应用广泛。立方ZnS晶体结构如下图所示,S原子的配位数是
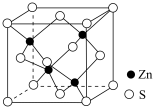
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
【推荐2】【化学——选修3:物质结构与性质】
铁是最常见的金属材料。铁能形成 [Fe(H2NCONH2)6](NO3)3[三硝酸六尿素合铁(Ⅲ)]和Fe(CO)x等多种配合物。
(1)基态Fe3+的M层电子排布式为______________ ;
(2)尿素(H2NCONH2)分子中C、N原子的杂化方式分别是__________ 、__________ ;
(3)配合物Fe(CO)x的中心原子价电子数与配体提供电子数之和为18,则x=__ 。 Fe(CO)x常温下呈液态,熔点为﹣20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断Fe(CO)x晶体属于________ (填晶体类型)。
(4)常温条件下,铁的晶体采用如图所示的堆积方式。则这种堆积模型的配位数为_______ ,如果铁的原子半径为a cm,阿伏加德常数的值为NA,则此种铁单质的密度表达式为_______ g/cm3。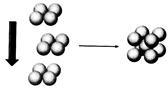
铁是最常见的金属材料。铁能形成 [Fe(H2NCONH2)6](NO3)3[三硝酸六尿素合铁(Ⅲ)]和Fe(CO)x等多种配合物。
(1)基态Fe3+的M层电子排布式为
(2)尿素(H2NCONH2)分子中C、N原子的杂化方式分别是
(3)配合物Fe(CO)x的中心原子价电子数与配体提供电子数之和为18,则x=
(4)常温条件下,铁的晶体采用如图所示的堆积方式。则这种堆积模型的配位数为

您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
【推荐3】超分子笼PPC-2封装钌(Ru)纳米颗粒形成一种高效催化剂。PPC-2是由A、B、C三个组件拼装而成的正八面体超分子笼,结构示意如图。
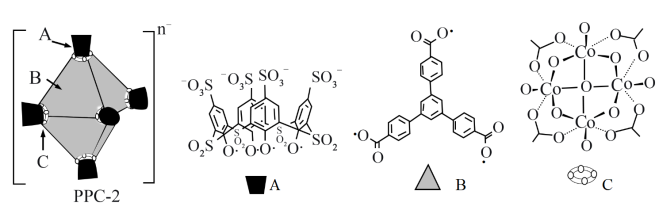
注:C组件中浅色原子由其他邻近组件提供。
(1)基态Co原子的价电子排布式为_______ 。
(2)组件A中所含四种元素的电负性由小到大的顺序为_______ 。
(3)组件B中碳原子的杂化类型为_______ 。
(4)组件C中Co原子位于相邻O原子构成的_______ 空隙中(填“四面体”或“八面体”)。
(5)每个组件C带一个单位负电荷,综合各组件所带电荷,计算PPC-2中n=_______ 。
(6)钌纳米颗粒进入PPC-2超分子笼后,钌晶体从六方堆积转化为面心立方堆积(晶胞参数为a pm)。超分子笼内钌晶体密度为_______ g·cm-3(用含a、NA的代数式表示)。

注:C组件中浅色原子由其他邻近组件提供。
(1)基态Co原子的价电子排布式为
(2)组件A中所含四种元素的电负性由小到大的顺序为
(3)组件B中碳原子的杂化类型为
(4)组件C中Co原子位于相邻O原子构成的
(5)每个组件C带一个单位负电荷,综合各组件所带电荷,计算PPC-2中n=
(6)钌纳米颗粒进入PPC-2超分子笼后,钌晶体从六方堆积转化为面心立方堆积(晶胞参数为a pm)。超分子笼内钌晶体密度为
您最近一年使用:0次



