电气石是一种具有保健作用的天然石材,其中含有的主要元素为 等元素。
等元素。
(1)上述元素中,原子半径最小的是_______ (用元素符号表示),与硫同周期的元素中简单离子半径最小的是_______ (用离子符号表示);
(2)用轨道表示式表示氧元素原子核外电子的运动状态_______ ;氧元素原子核外有_______ 种不同能量的电子;
(3) 分子中
分子中 为
为_______ 杂化,键角等于_______ ,可以判断出 分子为
分子为_______ 分子(选填“极性”或“非极性”); 晶体的熔点比
晶体的熔点比 晶体
晶体_______ (选填“高”、“低”),原因为_______ 。
 等元素。
等元素。(1)上述元素中,原子半径最小的是
(2)用轨道表示式表示氧元素原子核外电子的运动状态
(3)
 分子中
分子中 为
为 分子为
分子为 晶体的熔点比
晶体的熔点比 晶体
晶体
更新时间:2023-12-18 10:42:00
|
相似题推荐
解答题-无机推断题
|
较易
(0.85)
名校
【推荐1】门捷列夫是俄国科学家,他发明的元素周期表是化学领域的重要里程碑。周期表的发明帮助人们更好地理解元素性质和变化规律,推动了化学和其他学科的发展。门捷列夫被誉为“现代化学之父”。
(1)②的元素符号是:___________ ;①的最高价氧化物对应的水合物化学式是___________ 。
(2)磷元素在周期表中的位置是:___________ 周期___________ 族。写出④的最高价氧化物对应水合物和⑧的最高价氧化物对应水合物相互反应的化学方程式___________ 。
(3)③、④两种元素的简单离子半径大小关系:___________ (填离子符号)
(4)④、⑤和⑥中,金属性最强的元素是___________ (填元素符号);③和⑧两种元素形成的气态氢化物稳定性强的是:___________ (填化学式);④、⑤、⑥、⑦、⑧元素最高价氧化物形成的水化物中酸性最强的是___________ (填化学式)。
(5)Cl元素比S元素的非金属性强,是因为从结构层面看来,Cl原子和S原子___________ 相同,而Cl原子的核电荷数比S原子___________ ,所以,原子核对电子的吸引作用更___________ 。能证明这一事实的化学反应为___________ (请写出化学方程式)。
| 族 周期 | IA | 0 | |||||||
| 1 | IIA | IIIA | IVA | VA | VIA | VIIA | |||
| 2 | ① | ② | ③ | ||||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||||
(2)磷元素在周期表中的位置是:
(3)③、④两种元素的简单离子半径大小关系:
(4)④、⑤和⑥中,金属性最强的元素是
(5)Cl元素比S元素的非金属性强,是因为从结构层面看来,Cl原子和S原子
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐2】元素①~⑧在元素周期表中的位置如下,回答有关问题:
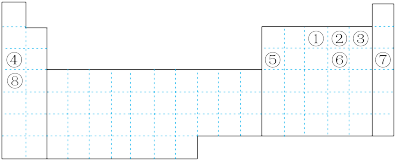
(1)画出⑥的离子结构示意图___________________ 。
(2)在②、③、④、⑤四种元素中,其简单离子半径按由大到小的排列顺序为________________ 【示例:用r(A2-)>r(B-)的形式表示】。
(3)元素②、③氢化物的稳定性由强到弱的顺序为(填化学式)____________________________ 。
(4)与③同一主族并且在短周期的元素的某种含氧酸可以消毒杀菌,写出该物质的电子式___________ 。
(5)比较①与其同族短周期元素的氢化物的熔沸点高低,并说明理由____________________________ 。

(1)画出⑥的离子结构示意图
(2)在②、③、④、⑤四种元素中,其简单离子半径按由大到小的排列顺序为
(3)元素②、③氢化物的稳定性由强到弱的顺序为(填化学式)
(4)与③同一主族并且在短周期的元素的某种含氧酸可以消毒杀菌,写出该物质的电子式
(5)比较①与其同族短周期元素的氢化物的熔沸点高低,并说明理由
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐3】如图所示是部分短周期元素原子半径与原子序数的关系,回答下列问题:
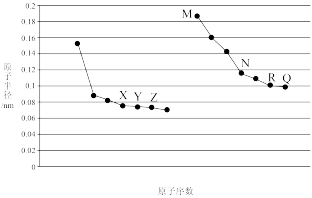
(1)X在周期表中的位置是_______ 。
(2)X、Q的最高价氧化物对应的水化物中,酸性较强的物质是_______ 。(填化学式)。
(3)用电子式表示化合物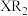 的形成过程
的形成过程_______ 。
(4)请写出实验室制备Y的气态氢化物的化学方程式_______ 。
(5)写出 的结构式
的结构式_______ 。
(6)均含有M、Z、R和H四种元素的两种化合物反应的化学方程式为_______ 。

(1)X在周期表中的位置是
(2)X、Q的最高价氧化物对应的水化物中,酸性较强的物质是
(3)用电子式表示化合物
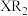 的形成过程
的形成过程(4)请写出实验室制备Y的气态氢化物的化学方程式
(5)写出
 的结构式
的结构式(6)均含有M、Z、R和H四种元素的两种化合物反应的化学方程式为
您最近一年使用:0次
【推荐1】法国一家公司研发出一种比锂电池成本更低、寿命更长、充电速度更快的钠离子电池,该电池的负极材料为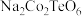 (制备原料为
(制备原料为 、
、 和
和 ),电解液为
),电解液为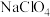 的碳酸丙烯酯溶液。回答下列问题:
的碳酸丙烯酯溶液。回答下列问题:
(1)基态Na原子中,核外电子占据的原子轨道总数为_______ ,Te属于元素周期表中_______ 区元素,其基态原子的价电子排布式为_______ 。
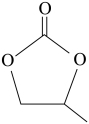
(2) 的空间结构为
的空间结构为_______ ,碳酸丙烯酯的结构简式如图所示,其中碳原子的杂化轨道类型为_______ ,1mol碳酸丙烯酯中 键的数目为
键的数目为_______ 。
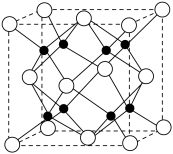
(3)Na和O形成的离子化合物的晶胞结构如图所示,晶胞中O的配位数为_______ ,该晶胞的密度为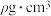 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则Na与O之间的最短距离为
,则Na与O之间的最短距离为_______ cm(用含有 、
、 的代数式表示)。
的代数式表示)。
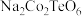 (制备原料为
(制备原料为 、
、 和
和 ),电解液为
),电解液为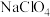 的碳酸丙烯酯溶液。回答下列问题:
的碳酸丙烯酯溶液。回答下列问题:(1)基态Na原子中,核外电子占据的原子轨道总数为
(2)
 的空间结构为
的空间结构为 键的数目为
键的数目为
(3)Na和O形成的离子化合物的晶胞结构如图所示,晶胞中O的配位数为
 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则Na与O之间的最短距离为
,则Na与O之间的最短距离为 、
、 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐2】以CuSO4、NaOH和抗坏血酸为原料,可制备Cu₂O。_____ 。
(2) 的空间构型为
的空间构型为_____ (用文字描述);Cu2+与OH−反应能生成[Cu(OH)4]2−,[Cu(OH)4]2−中的配位原子为_____ (填元素符号)。
(3)抗坏血酸的分子结构如图1所示,分子中碳原子的轨道杂化类型为_____ ;推测抗坏血酸在水中的溶解性:_____ (填“难溶于水”或“易溶于水”)。
(4)一个Cu2O晶胞(见图2)中,Cu原子的数目为_____ 。


(2)
 的空间构型为
的空间构型为(3)抗坏血酸的分子结构如图1所示,分子中碳原子的轨道杂化类型为
(4)一个Cu2O晶胞(见图2)中,Cu原子的数目为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐3】X、Y、Z三种元素的结构信息如表所示。请根据信息回答下列问题:
(1)基态X原子中,核外电子占据最高能层的符号是_______ ,占据该能层电子的电子云轮廓图形状为_______ 。
(2)元素W与X处于同一周期,其基态原子中未成对电子数是核外电子总数的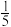 ,W的元素符号为
,W的元素符号为________ 。
(3)在第三周期中,第一电离能比Y大的主族元素有_________ (填元素符号)。
(4)YZ3分子中,Y原子的杂化轨道类型是________ ,其分子的立体构型为__________ 。
(5)Z的氢化物(H2Z)的稳定性高于Y的氢化物(H2Y),其原因是_________ 。
(6)H2Z在特定条件下得到一个H+形成H3Z+,从结构角度对上述过程分析错误的是________
| 元素 | 结构信息 |
| X | 位于第四周期,其基态原子的内层轨道全部排满电子,且最外层电子数为2 |
| Y | 基态原子的3p轨道上有4个电子 |
| Z | 元素Z的原子最外层电子数是其内层的3倍 |
(2)元素W与X处于同一周期,其基态原子中未成对电子数是核外电子总数的
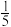 ,W的元素符号为
,W的元素符号为(3)在第三周期中,第一电离能比Y大的主族元素有
(4)YZ3分子中,Y原子的杂化轨道类型是
(5)Z的氢化物(H2Z)的稳定性高于Y的氢化物(H2Y),其原因是
(6)H2Z在特定条件下得到一个H+形成H3Z+,从结构角度对上述过程分析错误的是________
| A.中心原子的杂化轨道类型发生了改变 |
| B.中心原子的价层电子对数发生了改变 |
| C.微粒的立体结构发生了改变 |
| D.微粒中键角发生了改变 |
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐1】根据已学知识,请回答下列问题:
(1)最外层电子排布为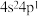 的基态原子的核电荷数为
的基态原子的核电荷数为_______ 。
(2)某元素被科学家称之为人体微量元素中的“防癌之王”,其基态原子的外围电子排布式为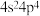 ,该元素的名称是
,该元素的名称是_______
(3)基态Fe原子中,电子填充的能量最高的能级符号为_______ ;基态N原子的轨道表示为_______ 。
(4)已知熔融的 不导电,则
不导电,则 属于
属于_______ 晶体,中心原子的杂化类型为_______ 。
(5)氨水中存在_______ 种氢键,任写其中的一种_______ 。
(6)As的电子排布简式为:[Ar]_______ ;它有两种含氧酸: 和
和 ,其中酸性较强的是
,其中酸性较强的是_______ 。
(7) 的一种配离子
的一种配离子 中,
中, 的配位数是
的配位数是_______ 。配体 中心原子的杂化类型为
中心原子的杂化类型为_______ 。CoO的熔点是1935℃,CoS的熔点是1135℃,试分析CoO的熔点较高的原因_______
(1)最外层电子排布为
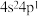 的基态原子的核电荷数为
的基态原子的核电荷数为(2)某元素被科学家称之为人体微量元素中的“防癌之王”,其基态原子的外围电子排布式为
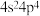 ,该元素的名称是
,该元素的名称是(3)基态Fe原子中,电子填充的能量最高的能级符号为
(4)已知熔融的
 不导电,则
不导电,则 属于
属于(5)氨水中存在
(6)As的电子排布简式为:[Ar]
 和
和 ,其中酸性较强的是
,其中酸性较强的是(7)
 的一种配离子
的一种配离子 中,
中, 的配位数是
的配位数是 中心原子的杂化类型为
中心原子的杂化类型为
您最近一年使用:0次
【推荐2】研究发现,在CO2低压合成甲醇反应CO23H2CH3OHH2O中,Co氧化物负载的Mn氧化物纳米粒子催化剂具有高活性,显示出良好的应用前景。回答下列问题:
(1)Co基态原子核外电子排布式为________ 。元素Mn与O中,第一电离能较大的是________ ,基态原子核外未成对电子数较多的是________ 。
(2)CO2和CH3OH分子中C原子的杂化形式分别为________ 和________ 。
(3)比较CO2和H2O沸点________ ,原因是________ 。
(4)MnNO3中的化学键除了σ键外,还存在________ 。
(1)Co基态原子核外电子排布式为
(2)CO2和CH3OH分子中C原子的杂化形式分别为
(3)比较CO2和H2O沸点
(4)MnNO3中的化学键除了σ键外,还存在
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
【推荐3】KI或 可作为食盐的加碘剂,起到预防大脖子病的作用。
可作为食盐的加碘剂,起到预防大脖子病的作用。
(1)基态Ⅰ原子的价层电子排布式为___________ 。
(2)对含 较多的食盐,可选用KI作为加碘剂。
较多的食盐,可选用KI作为加碘剂。 可用
可用 检验,
检验, 的配位数为
的配位数为___________ ,配体中的C杂化方式为___________ ;
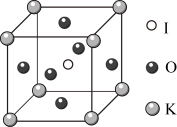
(3) 晶体的晶胞结构如图所示,边长为anm(
晶体的晶胞结构如图所示,边长为anm(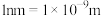 ),晶胞中K、I、O分别处于顶角、体心、面心位置。
),晶胞中K、I、O分别处于顶角、体心、面心位置。
① 的空间结构为
的空间结构为___________ 。
②与K紧邻的O的个数为___________ ,在 晶胞结构的另一种表示中,I处于各顶角的位置,则O处于
晶胞结构的另一种表示中,I处于各顶角的位置,则O处于___________ 位置。
③已知阿伏加德罗常数的值为 ,则
,则 的密度为
的密度为___________ (列式表示) 。
。
 可作为食盐的加碘剂,起到预防大脖子病的作用。
可作为食盐的加碘剂,起到预防大脖子病的作用。(1)基态Ⅰ原子的价层电子排布式为
(2)对含
 较多的食盐,可选用KI作为加碘剂。
较多的食盐,可选用KI作为加碘剂。 可用
可用 检验,
检验, 的配位数为
的配位数为(3)
 晶体的晶胞结构如图所示,边长为anm(
晶体的晶胞结构如图所示,边长为anm(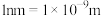 ),晶胞中K、I、O分别处于顶角、体心、面心位置。
),晶胞中K、I、O分别处于顶角、体心、面心位置。
①
 的空间结构为
的空间结构为②与K紧邻的O的个数为
 晶胞结构的另一种表示中,I处于各顶角的位置,则O处于
晶胞结构的另一种表示中,I处于各顶角的位置,则O处于③已知阿伏加德罗常数的值为
 ,则
,则 的密度为
的密度为 。
。
您最近一年使用:0次



