钙钛矿型化合物是一类可用于生产太阳能电池、传感器、固体电阻器等的功能材料,如图所示为钙钛矿晶体结构,该结构是其晶体中具有代表性的最小重复单位。
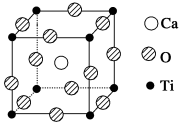
回答下列问题:
(1)在该物质的晶体结构中,每个钛离子周围与它最接近且距离相等的钛离子、钙离子各有___________ 个、___________ 个。该物质的化学式可表示为___________ 。
(2)Ti的四卤化物熔点如下表所示,TiF4熔点高于其他三种卤化物,自TiCl4至TiI4熔点依次升高,原因是___________ 。
(3)钙钛矿的组成元素中电负性大小顺序是___________ ;金属离子与氧离子间的作用力为___________ 。

回答下列问题:
(1)在该物质的晶体结构中,每个钛离子周围与它最接近且距离相等的钛离子、钙离子各有
(2)Ti的四卤化物熔点如下表所示,TiF4熔点高于其他三种卤化物,自TiCl4至TiI4熔点依次升高,原因是
化合物 | TiF4 | TiCl4 | TiBr4 | TiI4 |
熔点/℃ | 377 | -24.12 | 38.3 | 155 |
(3)钙钛矿的组成元素中电负性大小顺序是
更新时间:2021-07-04 07:23:18
|
相似题推荐
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐1】葡萄糖酸锌{ }用于治疗缺锌引起的营养不良、厌食症、异食癖、口腔溃疡、痤疮、儿童生长发育迟缓等,可用葡萄糖酸和碳酸锌反应制得。
}用于治疗缺锌引起的营养不良、厌食症、异食癖、口腔溃疡、痤疮、儿童生长发育迟缓等,可用葡萄糖酸和碳酸锌反应制得。
(1)基态 的电子排布式为
的电子排布式为_______ ,元素铜和锌在周期表中相邻,元素第一电离能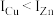 的原因是
的原因是_______ 。
(2)葡萄糖酸[ ]分子中元素的电负性由大到小的顺序为
]分子中元素的电负性由大到小的顺序为_______ ,C原子的杂化类型为_______ 。1mol该分子含有的手性碳原子(连有四个不同的原子或基团的碳原子)的个数为_______ NA。
(3)葡萄糖酸易溶于水,可能的原因是_______ 。
(4)葡萄糖酸和碳酸锌反应生成的 为
为_______ (填“极性”或“非极性”)分子; 分子中的σ键和π键个数之比为
分子中的σ键和π键个数之比为_______ 。
(5)加热碳酸锌可得到一种锌的氧化物,其晶胞如图所示,则该物质的化学式为_______ ,若晶胞棱长为apm,则晶体的密度为_______  (用字母表示,阿伏加德罗常数的值用NA表示)。
(用字母表示,阿伏加德罗常数的值用NA表示)。
 }用于治疗缺锌引起的营养不良、厌食症、异食癖、口腔溃疡、痤疮、儿童生长发育迟缓等,可用葡萄糖酸和碳酸锌反应制得。
}用于治疗缺锌引起的营养不良、厌食症、异食癖、口腔溃疡、痤疮、儿童生长发育迟缓等,可用葡萄糖酸和碳酸锌反应制得。(1)基态
 的电子排布式为
的电子排布式为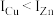 的原因是
的原因是(2)葡萄糖酸[
 ]分子中元素的电负性由大到小的顺序为
]分子中元素的电负性由大到小的顺序为(3)葡萄糖酸易溶于水,可能的原因是
(4)葡萄糖酸和碳酸锌反应生成的
 为
为 分子中的σ键和π键个数之比为
分子中的σ键和π键个数之比为(5)加热碳酸锌可得到一种锌的氧化物,其晶胞如图所示,则该物质的化学式为
 (用字母表示,阿伏加德罗常数的值用NA表示)。
(用字母表示,阿伏加德罗常数的值用NA表示)。
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐2】下表是元素周期表的一部分,表中所列的字母分别代表一种元素。
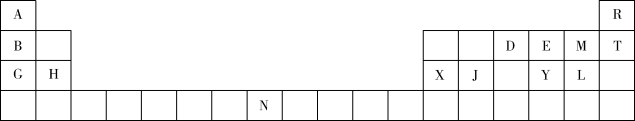
回答下列问题:
(1)D的简单气态氢化物的VSEPR模型为_______ 。
(2)第一电离能H_______ X(填“>”“<”或“=”),其原因是_______ 。
(3)电负性E_______ M(填“>”“<”或“=”)。
(4)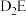 的沸点比
的沸点比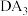 的沸点低,其原因是
的沸点低,其原因是_______ 。
(5)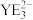 的键角比
的键角比 的键角小的原因是
的键角小的原因是_______ 。

回答下列问题:
(1)D的简单气态氢化物的VSEPR模型为
(2)第一电离能H
(3)电负性E
(4)
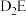 的沸点比
的沸点比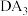 的沸点低,其原因是
的沸点低,其原因是(5)
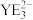 的键角比
的键角比 的键角小的原因是
的键角小的原因是
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐3】砷的一些化合物常用作半导体、除草剂、杀鼠药等。回答下列问题:
(1)基态As原子的核外电子排布式为[Ar]__________ ,有___________ 个未成对电子。
(2)镓氮砷合金材料的太阳能电池效率达40%。Ga、N、As电负性由大至小的顺序是_____________ 。
(3)As4O6的分子结构如图所示,其中As原子的杂化方式为____________ ,1mol 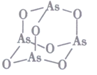 As4O6含有σ键的物质的量为
As4O6含有σ键的物质的量为________ mol。
(4)晶胞有两个基本要素:
①原子坐标参数,表示晶胞内部各原子的相对位置,LiZnAs基稀磁半导体的晶胞如图所示,其中原子
坐标参数A处Li为(0,0, );B处As为(
);B处As为( ,
, ,
, );C处Li的坐标参数为
);C处Li的坐标参数为_____________ 。
②晶胞参数,描述晶胞的大小和形状,已知LiZnAs单晶的晶胞参数α=594 pm,NA表示阿伏伽德罗常数的数值,其密度为____________ g·cm-3(列出计算式即可)。
(1)基态As原子的核外电子排布式为[Ar]
(2)镓氮砷合金材料的太阳能电池效率达40%。Ga、N、As电负性由大至小的顺序是
(3)As4O6的分子结构如图所示,其中As原子的杂化方式为
 As4O6含有σ键的物质的量为
As4O6含有σ键的物质的量为(4)晶胞有两个基本要素:
①原子坐标参数,表示晶胞内部各原子的相对位置,LiZnAs基稀磁半导体的晶胞如图所示,其中原子
坐标参数A处Li为(0,0,
 );B处As为(
);B处As为( ,
, ,
, );C处Li的坐标参数为
);C处Li的坐标参数为②晶胞参数,描述晶胞的大小和形状,已知LiZnAs单晶的晶胞参数α=594 pm,NA表示阿伏伽德罗常数的数值,其密度为
您最近一年使用:0次
【推荐1】Ⅰ.过渡区金属元素原子或离子易形成配合物,广泛用作催化剂。回答下列问题:
(1)硫酸铜溶液中滴入氨水可形成配离子 。
。 还可与其他微粒形成配离子,如与乙二胺形成
还可与其他微粒形成配离子,如与乙二胺形成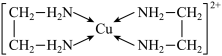 ,此配离子内部不含有的化学键类型是
,此配离子内部不含有的化学键类型是_______ 。
(2)在 的水溶液中,一定条件下存在组成为
的水溶液中,一定条件下存在组成为 (n为正整数)的配离子,提供孤电子对的是
(n为正整数)的配离子,提供孤电子对的是_______ (填序号)。
Ⅱ.晶体世界丰富多彩,复杂多样,各类晶体具有不同的结构特点,决定着他具有不同的性质和用途,回答下列问题:
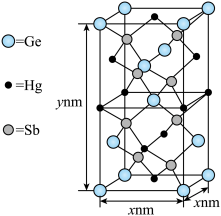
(3)由汞(Hg)、锗(Ge)、锑(Sb)形成的一种新物质X为潜在的拓扑绝缘体材料。X的晶体的晶胞如图所示,X晶体的化学式为:_______
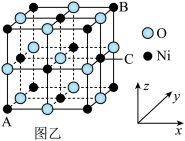
(4)NiO的晶胞结构如图乙所示,其中离子坐标参数A为(0,0,0),B为(1,1,1),则C的离子坐标参数为_______ 。 配位数是
配位数是_______ ,若晶胞边长为apm,则NiO晶体的密度为_______  (用含a、
(用含a、 的代数式表示,
的代数式表示, 表示阿伏伽德罗常数)。
表示阿伏伽德罗常数)。
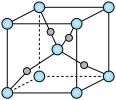
(5)已知 的立方晶胞结构如图所示,若晶体的密度为
的立方晶胞结构如图所示,若晶体的密度为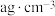 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则Cu与O之间最短距离为
,则Cu与O之间最短距离为_______ cm(用含a、 的代数式表示)。
的代数式表示)。
(1)硫酸铜溶液中滴入氨水可形成配离子
 。
。 还可与其他微粒形成配离子,如与乙二胺形成
还可与其他微粒形成配离子,如与乙二胺形成 ,此配离子内部不含有的化学键类型是
,此配离子内部不含有的化学键类型是| A.离子键 | B.非极性键 | C.配位键 | D.氢键 |
 的水溶液中,一定条件下存在组成为
的水溶液中,一定条件下存在组成为 (n为正整数)的配离子,提供孤电子对的是
(n为正整数)的配离子,提供孤电子对的是A. | B.H | C.O | D.Cr |
Ⅱ.晶体世界丰富多彩,复杂多样,各类晶体具有不同的结构特点,决定着他具有不同的性质和用途,回答下列问题:
(3)由汞(Hg)、锗(Ge)、锑(Sb)形成的一种新物质X为潜在的拓扑绝缘体材料。X的晶体的晶胞如图所示,X晶体的化学式为:

(4)NiO的晶胞结构如图乙所示,其中离子坐标参数A为(0,0,0),B为(1,1,1),则C的离子坐标参数为
 配位数是
配位数是 (用含a、
(用含a、 的代数式表示,
的代数式表示, 表示阿伏伽德罗常数)。
表示阿伏伽德罗常数)。
(5)已知
 的立方晶胞结构如图所示,若晶体的密度为
的立方晶胞结构如图所示,若晶体的密度为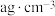 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则Cu与O之间最短距离为
,则Cu与O之间最短距离为 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
【推荐2】碱金属元素形成的单质及其化合物有广泛的应用。回答下列问题:
(1)K与Br2反应可形成离子晶体KBr,其离子键形成的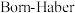 循环如图所示。可知,K原子的第一电离能为
循环如图所示。可知,K原子的第一电离能为_________  ,
,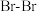 键键能为
键键能为_________  。
。

(2)Li及其周期表中相邻元素的第一电离能(I1)。
①I1(Li)> I1(Na),原因是_________ 。
②I1(Be)> I1(B)> I1(Li),原因是_________ 。
(3)K与Cr属于同一周期,且核外最外层电子构型相同,但单质K的熔点较低,其原因为_________ 。
(4)Na与Cl2在高压下可以形成组成和结构均不相同的晶体。判断晶体与非晶体最科学的方法是_________ ,上面图是其中一种晶体的晶胞。则该晶体的化学式为_________ 。

(1)K与Br2反应可形成离子晶体KBr,其离子键形成的
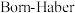 循环如图所示。可知,K原子的第一电离能为
循环如图所示。可知,K原子的第一电离能为 ,
,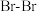 键键能为
键键能为 。
。
(2)Li及其周期表中相邻元素的第一电离能(I1)。
①I1(Li)> I1(Na),原因是
②I1(Be)> I1(B)> I1(Li),原因是
(3)K与Cr属于同一周期,且核外最外层电子构型相同,但单质K的熔点较低,其原因为
(4)Na与Cl2在高压下可以形成组成和结构均不相同的晶体。判断晶体与非晶体最科学的方法是

您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐3】氮及其化合物,在工农业生产中作用巨大。
(1)下列有关氮的化合物的说法,正确的是___________。
(2)氮和碳组成的一种新型材料,硬度超过金刚石,其部分结构如下图所示。它的化学式为___________ ,它的硬度超过金刚石的主要原因是___________ 。 ),则原子2和4的原子分数坐标为
),则原子2和4的原子分数坐标为___________ 、___________ 。___________ ,氮化钼晶胞边长为a pm,晶体的密度ρ=___________ g·cm-3(列出计算式,设NA为阿伏加德罗常数的值)。
(1)下列有关氮的化合物的说法,正确的是___________。
| A.肼(N2H4)的沸点低于乙烷(C2H6) |
| B.NH3极易溶于水,原因之一是NH3能够与水分子形成分子间氢键 |
| C.NF3和NH3空间构型均为三角锥形,分子中键角:NH3>NF3 |
D.尿素(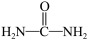 )中σ键与π键的比例为7:1 )中σ键与π键的比例为7:1 |
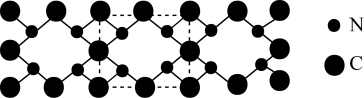
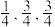 ),则原子2和4的原子分数坐标为
),则原子2和4的原子分数坐标为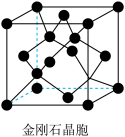
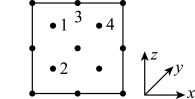
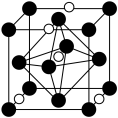
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐1】蛋氨酸铬(Ⅲ)配合物是一种治疗Ⅱ型糖尿病的药物,其结构简式如图所示。回答下列相关问题:
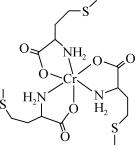
(1)基态Cr原子核外有___________ 种运动状态的电子,下列不同状态的Cr微粒中,电离最外层一个电子所需能量最大的是___________ (填标号)。
A.[Ar]3d54s1 B.[Ar]3d5 C.[Ar]3d44s14p1 D.[Ar]3d54p1
(2)蛋氨酸铬(Ⅲ)配合物的中心铬离子的配位数为___________ ;N的___________ 杂化轨道与Cr的空轨道形成配位键。
(3)哈勃-韦斯(Haber-Weiss)原理表明,某些金属离子可以催化双氧水分解的原因是:其次外层未排满的d轨道可以存取电子,降低活化能,使分解反应容易发生。Cr3+___________ (填“能”或“不能”)催化双氧水分解。
(4)化学式为CrCl3·6H2O的化合物有三种结构,一种呈紫罗兰色,一种呈暗绿色,一种呈亮绿色。在三种化合物中,Cr3+的配位数均为6,将它们配制成等体积等物质的量浓度的溶液,分别加入足量AgNO3溶液,依次所得AgCl沉淀的物质的量之比为3:2:l,则呈亮绿色的配合物,其内界离子的化学式为___________ 。
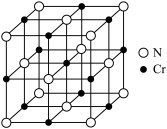
(5)氮化铬的晶胞结构如图所示。已知氮化铬的晶体密度为dg·cm-3,摩尔质量为M mol/L,NA为阿伏加德罗常数的值,则晶胞参数为___________ cm。

(1)基态Cr原子核外有
A.[Ar]3d54s1 B.[Ar]3d5 C.[Ar]3d44s14p1 D.[Ar]3d54p1
(2)蛋氨酸铬(Ⅲ)配合物的中心铬离子的配位数为
(3)哈勃-韦斯(Haber-Weiss)原理表明,某些金属离子可以催化双氧水分解的原因是:其次外层未排满的d轨道可以存取电子,降低活化能,使分解反应容易发生。Cr3+
(4)化学式为CrCl3·6H2O的化合物有三种结构,一种呈紫罗兰色,一种呈暗绿色,一种呈亮绿色。在三种化合物中,Cr3+的配位数均为6,将它们配制成等体积等物质的量浓度的溶液,分别加入足量AgNO3溶液,依次所得AgCl沉淀的物质的量之比为3:2:l,则呈亮绿色的配合物,其内界离子的化学式为
(5)氮化铬的晶胞结构如图所示。已知氮化铬的晶体密度为dg·cm-3,摩尔质量为M mol/L,NA为阿伏加德罗常数的值,则晶胞参数为

您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐2】我国科学家通过三(三苯基膦)溴化亚铜和BINAP在溶液中共晶生长得到两种单晶,其图示如下:
回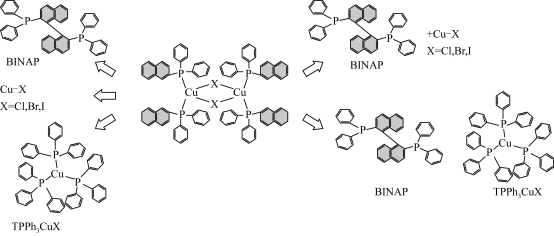 答下列问题:
答下列问题:
(1)基态Cu原子价层电子排布式为_______ 。
(2)BINAP中磷原子的杂化类型是_______ 。
(3)在 、
、 中一种分子是极性分子。另种是非极性分子。
中一种分子是极性分子。另种是非极性分子。 的空间构型是
的空间构型是_______ ;非极性分子是_______ (填化学式)。
(4)在周期表中磷相邻元素有氮、砷、硅、硫, 、
、 、
、 的沸点依次降低,其原因是
的沸点依次降低,其原因是_______ 。 、
、 、
、 分子的键角依次减小,其原因是
分子的键角依次减小,其原因是_______ 。
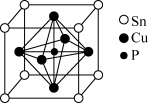
(5)磷青铜晶胞结构如图所示,已知磷青铜晶体密度为 ,
, 为阿伏加德罗常数的值。有
为阿伏加德罗常数的值。有_______ 个Cu与P相邻且等距离。Cu和Sn之间最近距离为_______ pm(只要求列出计算式即可)。
回
 答下列问题:
答下列问题:(1)基态Cu原子价层电子排布式为
(2)BINAP中磷原子的杂化类型是
(3)在
 、
、 中一种分子是极性分子。另种是非极性分子。
中一种分子是极性分子。另种是非极性分子。 的空间构型是
的空间构型是(4)在周期表中磷相邻元素有氮、砷、硅、硫,
 、
、 、
、 的沸点依次降低,其原因是
的沸点依次降低,其原因是 、
、 、
、 分子的键角依次减小,其原因是
分子的键角依次减小,其原因是(5)磷青铜晶胞结构如图所示,已知磷青铜晶体密度为
 ,
, 为阿伏加德罗常数的值。有
为阿伏加德罗常数的值。有
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐3】锰单质及其化合物应用十分广泛。回答下列问题:
(1)基态锰原子的核外电子排布式为_______
(2)MnO和MnS的熔点分别为1650℃和1610℃,前者熔点较高的原因是_______ 。
(3)锰的一种配合物的化学式为Mn(BH4)2(THF)3,THF的结构简式如图所示。

①THF中与Mn2+形成配位键的原子为_______ (填元素符号)。
②写出一种与BH 互为等电子体的分子
互为等电子体的分子_______ 。
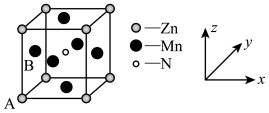
(4)某种含锰特殊材料的晶胞结构如图所示,该晶体的化学式为_______ ;其中原子坐标参数A为(0,0,0),B为(0, ,
, ),则晶胞中氮原子的坐标参数为
),则晶胞中氮原子的坐标参数为_______ 。
(5)金属锰有多种晶型,其中δ−Mn的结构为体心立方堆积,晶胞参数为apm,δ−Mn中锰的原子半径为_______ pm。已知阿伏加德罗常数的值为NA,δ−Mn的理论密度ρ=_______ g∙cm−3 (列出计算式)。
(1)基态锰原子的核外电子排布式为
(2)MnO和MnS的熔点分别为1650℃和1610℃,前者熔点较高的原因是
(3)锰的一种配合物的化学式为Mn(BH4)2(THF)3,THF的结构简式如图所示。

①THF中与Mn2+形成配位键的原子为
②写出一种与BH
 互为等电子体的分子
互为等电子体的分子(4)某种含锰特殊材料的晶胞结构如图所示,该晶体的化学式为
 ,
, ),则晶胞中氮原子的坐标参数为
),则晶胞中氮原子的坐标参数为
(5)金属锰有多种晶型,其中δ−Mn的结构为体心立方堆积,晶胞参数为apm,δ−Mn中锰的原子半径为
您最近一年使用:0次



