氮及其化合物,在工农业生产中作用巨大。
(1)下列有关氮的化合物的说法,正确的是___________。
(2)氮和碳组成的一种新型材料,硬度超过金刚石,其部分结构如下图所示。它的化学式为___________ ,它的硬度超过金刚石的主要原因是___________ 。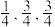 ),则原子2和4的原子分数坐标为
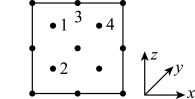
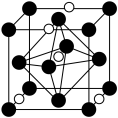
),则原子2和4的原子分数坐标为___________ 、___________ 。___________ ,氮化钼晶胞边长为a pm,晶体的密度ρ=___________ g·cm-3(列出计算式,设NA为阿伏加德罗常数的值)。
(1)下列有关氮的化合物的说法,正确的是___________。
| A.肼(N2H4)的沸点低于乙烷(C2H6) |
| B.NH3极易溶于水,原因之一是NH3能够与水分子形成分子间氢键 |
| C.NF3和NH3空间构型均为三角锥形,分子中键角:NH3>NF3 |
D.尿素(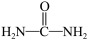 )中σ键与π键的比例为7:1 )中σ键与π键的比例为7:1 |
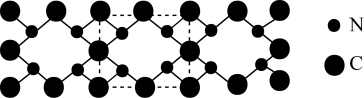
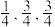 ),则原子2和4的原子分数坐标为
),则原子2和4的原子分数坐标为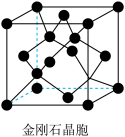
更新时间:2023-04-15 14:51:42
|
相似题推荐
解答题-原理综合题
|
较易
(0.85)
名校
解题方法
【推荐1】短周期非金属元素B、C、N、O、P、S、Cl,可形成各种单质、化合物的分子。
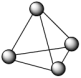
(1)意大利罗马大学的FulvioCacace等人获得了极具理论研究意义的气态N4分子,其分子结构如图。已知断裂1molN—N吸收167kJ热量,生成1molN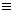 N放出942kJ热量,根据以上信息和数据,判断下列说法不正确的是
N放出942kJ热量,根据以上信息和数据,判断下列说法不正确的是___ 。
A.N4属于一种新型的化合物
B.N4分子中N—N键角为60°
C.N4分子中存在非极性键
D.1molN4转变成N2将吸收882kJ热量
(2)1919年,Langmuir提出等电子体的概念,由短周期元素组成的粒子,只要其原子数相同,各原子的最外层电子数之和相同,也可互称为等电子体。等电子体的结构相似、物理性质相似。与CO互为等电子体的分子和离子分别为___ 和___ (写1种,填化学式)。
(3)BF3和过量NaF作用可生成NaBF4,BF 的空间立体构型为
的空间立体构型为___ 。
(1)意大利罗马大学的FulvioCacace等人获得了极具理论研究意义的气态N4分子,其分子结构如图。已知断裂1molN—N吸收167kJ热量,生成1molN
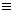 N放出942kJ热量,根据以上信息和数据,判断下列说法不正确的是
N放出942kJ热量,根据以上信息和数据,判断下列说法不正确的是
A.N4属于一种新型的化合物
B.N4分子中N—N键角为60°
C.N4分子中存在非极性键
D.1molN4转变成N2将吸收882kJ热量
(2)1919年,Langmuir提出等电子体的概念,由短周期元素组成的粒子,只要其原子数相同,各原子的最外层电子数之和相同,也可互称为等电子体。等电子体的结构相似、物理性质相似。与CO互为等电子体的分子和离子分别为
(3)BF3和过量NaF作用可生成NaBF4,BF
 的空间立体构型为
的空间立体构型为
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐2】Na2FeO4、Li4YiO12和LiFePO4均可用作电极材料。请回答下列问题:
⑴基态Fe3+的价层电子轨道表达式为________ ;同周期元素中,基态原子的未成对电子数与基态Fe3+相同的元素为________ 。
⑵PO43-的空间构型为________ ,其中P原子的杂化方式为________ ;写出一种与PO43-互为等电子体且中心原子与P不同主族的阴离子:________ (填离子符号)。
⑶[Ti(H2O)6]Cl3为紫色晶体,其中1mol阳离子中所含δ键的数目为________ ;配位键中提供孤电子对的原子为________ (填元素符号)。
⑷已知物质间的转化关系如图甲所示,其中a、c均大于0。
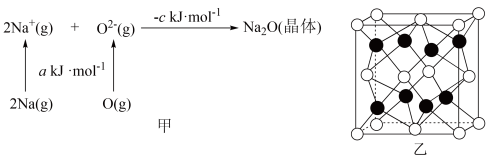
①基态Na原子的第一电离能可表示为________ 。
②相同条件下,Li2O的晶格能________ (填“>”“<”或“=”)ckJ∙mol-1,原因为________________________________ 。
③Na2O的立方晶胞结构如图乙所示。若紧邻的两个Na+之间的距离为d pm,阿伏加 德罗常数的值为NA,晶体的密度为ρ g∙cm-3,则Na的摩尔质量可表示为_______ g∙mol-1(用含有d、ρ、NA的代数式表示)。
⑴基态Fe3+的价层电子轨道表达式为
⑵PO43-的空间构型为
⑶[Ti(H2O)6]Cl3为紫色晶体,其中1mol阳离子中所含δ键的数目为
⑷已知物质间的转化关系如图甲所示,其中a、c均大于0。

①基态Na原子的第一电离能可表示为
②相同条件下,Li2O的晶格能
③Na2O的立方晶胞结构如图乙所示。若紧邻的两个Na+之间的距离为d pm,阿伏加 德罗常数的值为NA,晶体的密度为ρ g∙cm-3,则Na的摩尔质量可表示为
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐3】黄铜矿(主要成分为CuFeS2)是生产铜、铁和硫酸的原料。回答下列问题:
(1)基态Cu原子的价电子排布式为_______ 。
(2)血红素是吡咯(C4H5N)的重要衍生物,血红素(含Fe2+)可用于治疗缺铁性贫血。吡咯和血红素的结构如图所示:
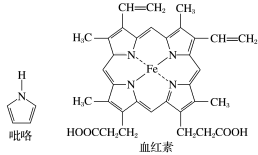
①已知吡咯中的各个原子均在同一平面内,则吡咯分子中N原子的杂化类型为_______ 。
②1mol吡咯分子中所含的σ键总数为_______ 个。
③C、N、O三种元素的简单氢化物中,沸点由低到高的顺序为_______ (填化学式)。
④血液中O2是由血红素在人体内形成的血红蛋白来输送的,则血红蛋白中的Fe2+与O2是通过_______ 键相结合的。
(3)黄铜矿冶炼铜时产生的SO2可经过SO2→SO3→H2SO4途径形成酸雨。SO2的立体构型为_______ 。H2SO4的酸性强于H2SO3的原因是_______ 。
(1)基态Cu原子的价电子排布式为
(2)血红素是吡咯(C4H5N)的重要衍生物,血红素(含Fe2+)可用于治疗缺铁性贫血。吡咯和血红素的结构如图所示:

①已知吡咯中的各个原子均在同一平面内,则吡咯分子中N原子的杂化类型为
②1mol吡咯分子中所含的σ键总数为
③C、N、O三种元素的简单氢化物中,沸点由低到高的顺序为
④血液中O2是由血红素在人体内形成的血红蛋白来输送的,则血红蛋白中的Fe2+与O2是通过
(3)黄铜矿冶炼铜时产生的SO2可经过SO2→SO3→H2SO4途径形成酸雨。SO2的立体构型为
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
【推荐1】回答下列问题
(1)在较低温度下CuFeS2与浓硫酸作用时,有少量臭鸡蛋气味的气体X产生。
①X分子的立体构型是___________ ,中心原子杂化类型为___________ ,属于___________ (填“极性”或“非极性”)分子。
②X的沸点比水低的主要原因是___________ 。
(2)CuFeS2与氧气反应生成SO2,SO2中心原子的价层电子对数为___________ ,共价键的类型有___________ 。
(1)在较低温度下CuFeS2与浓硫酸作用时,有少量臭鸡蛋气味的气体X产生。
①X分子的立体构型是
②X的沸点比水低的主要原因是
(2)CuFeS2与氧气反应生成SO2,SO2中心原子的价层电子对数为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐2】短周期元素A、D、E、F、W原子序数依次递增,已知:
①D元素的某种同位素通常用于地质年代的鉴定;
②F元素电负性在周期表所有元素中位列第二;
③W的各级电离能如图。
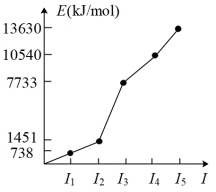
请回答:
(1)D、E、F三元素的第一电离能由大到小的顺序是___________ (用元素符号表示)。
(2)写出一种由上述元素形成氢键的表达式___________ 。
(3)元素W在周期表中的位置是___________ 。
①D元素的某种同位素通常用于地质年代的鉴定;
②F元素电负性在周期表所有元素中位列第二;
③W的各级电离能如图。

请回答:
(1)D、E、F三元素的第一电离能由大到小的顺序是
(2)写出一种由上述元素形成氢键的表达式
(3)元素W在周期表中的位置是
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐3】某抗失眠药物的结构简式为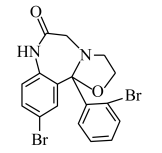 ,其分子式为
,其分子式为 。回答下列问题:
。回答下列问题:
(2)
 、
、 和
和 分子的价层电子对互斥模型是否相同
分子的价层电子对互斥模型是否相同(3)在由H元素与O元素形成的化合物中,含有非极性键的某极性分子的结构式为
(4)元素周期表中位于斜对角线的两种元素及其性质十分相似,称之为对角线规则。根据元素周期表对角线规则,金属铍Be与铝单质性质十分相似。写出金属铍Be与NaOH溶液反应的化学方程式
(5)用“*”标出下列化合物中的手性碳原子:

您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐1】镍的合金及其配合物用途非常广泛。回答下列问题:
(1)Ni与Ca均位于第四周期,最外层电子数也相同,但Ni的熔点和沸点均比Ca的高,这是因为_______ 。
(2)Ni2 MnGa晶体的立方晶胞结构如图a所示。

①已知Ni2MnGa的晶胞参数为0.5822nm,设NA为阿伏加德罗常数的数值,则Ni2MnGa晶体的密度为_______ (列出计算式)g· cm-3。
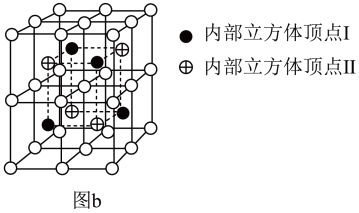
②Ni2MnGa晶体的晶胞结构还可以用图b表示,若●表示的是Mn,则 表示的是
表示的是_______ ,⊕表示的是_______ 。
(1)Ni与Ca均位于第四周期,最外层电子数也相同,但Ni的熔点和沸点均比Ca的高,这是因为
(2)Ni2 MnGa晶体的立方晶胞结构如图a所示。

①已知Ni2MnGa的晶胞参数为0.5822nm,设NA为阿伏加德罗常数的数值,则Ni2MnGa晶体的密度为
②Ni2MnGa晶体的晶胞结构还可以用图b表示,若●表示的是Mn,则
 表示的是
表示的是
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐2】含硅化合物在生活中的应用非常广泛。请回答下列问题:
(1)祖母绿宝石的主要成分化学式为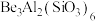 ,Be与Al的第一电离能大小关系为:
,Be与Al的第一电离能大小关系为: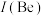
___________ 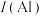 。
。
(2)硅酸盐的阴离子结构丰富多样,有些是有限数目的硅氧四面体构建的简单阴离子,如图所示,最简单的硅酸盐阴离子a的化学式为 ,则六元环状硅酸盐阴离子b的化学式是
,则六元环状硅酸盐阴离子b的化学式是___________ (不能用最简式表示)。___________ 。
(4)β-石英是晶质石英( )的一种变体,其晶胞结构如图所示,一个晶胞中含有的硅原子数为
)的一种变体,其晶胞结构如图所示,一个晶胞中含有的硅原子数为___________ ,请用价层电子对互斥模型解释图中键角。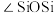 并不是180°的原因是
并不是180°的原因是___________ 。
(5)金刚砂的晶胞结构如图丙所示,在SiC中,每个C原子周围最近且等距的C原子数目为___________ ;若金刚砂的密度为ρ g⋅cm ,则晶体中最近的碳、硅原子之间的距离为
,则晶体中最近的碳、硅原子之间的距离为___________ pm(用代数式表示即可)。
(1)祖母绿宝石的主要成分化学式为
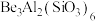 ,Be与Al的第一电离能大小关系为:
,Be与Al的第一电离能大小关系为: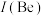
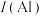 。
。(2)硅酸盐的阴离子结构丰富多样,有些是有限数目的硅氧四面体构建的简单阴离子,如图所示,最简单的硅酸盐阴离子a的化学式为
 ,则六元环状硅酸盐阴离子b的化学式是
,则六元环状硅酸盐阴离子b的化学式是
 |  |  |  | |
| 沸点/K | 187.2 | 330.8 | 427.2 | 560.7 |
(4)β-石英是晶质石英(
 )的一种变体,其晶胞结构如图所示,一个晶胞中含有的硅原子数为
)的一种变体,其晶胞结构如图所示,一个晶胞中含有的硅原子数为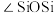 并不是180°的原因是
并不是180°的原因是(5)金刚砂的晶胞结构如图丙所示,在SiC中,每个C原子周围最近且等距的C原子数目为
 ,则晶体中最近的碳、硅原子之间的距离为
,则晶体中最近的碳、硅原子之间的距离为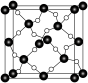

您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
【推荐3】碱金属元素形成的单质及其化合物有广泛的应用。回答下列问题:
(1)K与Br2反应可形成离子晶体KBr,其离子键形成的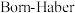 循环如图所示。可知,K原子的第一电离能为
循环如图所示。可知,K原子的第一电离能为_________  ,
,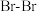 键键能为
键键能为_________  。
。

(2)Li及其周期表中相邻元素的第一电离能(I1)。
①I1(Li)> I1(Na),原因是_________ 。
②I1(Be)> I1(B)> I1(Li),原因是_________ 。
(3)K与Cr属于同一周期,且核外最外层电子构型相同,但单质K的熔点较低,其原因为_________ 。
(4)Na与Cl2在高压下可以形成组成和结构均不相同的晶体。判断晶体与非晶体最科学的方法是_________ ,上面图是其中一种晶体的晶胞。则该晶体的化学式为_________ 。

(1)K与Br2反应可形成离子晶体KBr,其离子键形成的
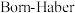 循环如图所示。可知,K原子的第一电离能为
循环如图所示。可知,K原子的第一电离能为 ,
,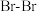 键键能为
键键能为 。
。
(2)Li及其周期表中相邻元素的第一电离能(I1)。
①I1(Li)> I1(Na),原因是
②I1(Be)> I1(B)> I1(Li),原因是
(3)K与Cr属于同一周期,且核外最外层电子构型相同,但单质K的熔点较低,其原因为
(4)Na与Cl2在高压下可以形成组成和结构均不相同的晶体。判断晶体与非晶体最科学的方法是

您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐1】晶体世界丰富多彩,复杂多样,各类晶体具有不同的结构特点,决定着它们具有不同的性质和用途,请回答下列问题:
 .立方砷化硼有潜力成为比硅更优良的半导体材料,其晶胞结构如下图所示,晶体中As填充在B围成的四面体空隙中。
.立方砷化硼有潜力成为比硅更优良的半导体材料,其晶胞结构如下图所示,晶体中As填充在B围成的四面体空隙中。___________ 。
(2)找出距离3号砷原子 最近的砷原子
最近的砷原子___________ (用分数坐标表示)。
(3)已知砷化硼的晶胞密度是a g⋅cm ,则As和B的最短距离是
,则As和B的最短距离是___________ nm。
 .氧化铈(
.氧化铈( )是一种重要的光催化材料,光催化过程中立方晶胞的组成变化如图所示。
)是一种重要的光催化材料,光催化过程中立方晶胞的组成变化如图所示。 晶胞中阳离子形成的八面体空隙有
晶胞中阳离子形成的八面体空隙有___________ 个,每个 晶胞中
晶胞中 个数为
个数为___________ 。
 .石墨晶体的结构及晶胞示意图如图所示。
.石墨晶体的结构及晶胞示意图如图所示。___________ ,已知石墨晶体的密度为ρ g⋅m ,则阿伏加德罗常数为
,则阿伏加德罗常数为___________ mol 。
。
 .立方砷化硼有潜力成为比硅更优良的半导体材料,其晶胞结构如下图所示,晶体中As填充在B围成的四面体空隙中。
.立方砷化硼有潜力成为比硅更优良的半导体材料,其晶胞结构如下图所示,晶体中As填充在B围成的四面体空隙中。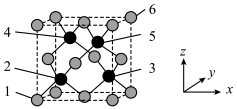
(2)找出距离3号砷原子
 最近的砷原子
最近的砷原子(3)已知砷化硼的晶胞密度是a g⋅cm
 ,则As和B的最短距离是
,则As和B的最短距离是 .氧化铈(
.氧化铈( )是一种重要的光催化材料,光催化过程中立方晶胞的组成变化如图所示。
)是一种重要的光催化材料,光催化过程中立方晶胞的组成变化如图所示。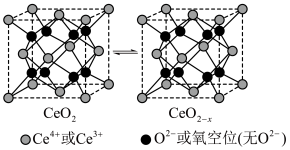
 晶胞中阳离子形成的八面体空隙有
晶胞中阳离子形成的八面体空隙有 晶胞中
晶胞中 个数为
个数为 .石墨晶体的结构及晶胞示意图如图所示。
.石墨晶体的结构及晶胞示意图如图所示。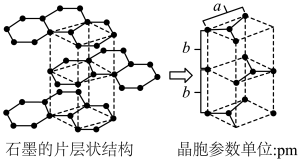
 ,则阿伏加德罗常数为
,则阿伏加德罗常数为 。
。
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐2】锡、铬、钴、铜等金属及其化合物在工业上有重要用途。
(1)锡合金具有优异的抗蚀性能,可以用来生产制作各种精美合金饰品。
①基态Sn原子价层电子排布为_______
②Co元素在元素周期表中的位置是_______
③Cu元素位于元素周期表的_______ 区
(2)制备CrO2Cl2的反应为K2Cr2O7 + 3CCl4 = 2KCl + 2CrO2Cl2 + 3COCl2↑
①上述方程式中非金属元素电负性由小到大的顺序为_______ (用元素符号表示)。
②COCl2分子中π键和σ键的个数比为_______ ,中心原子的杂化方式为_______ ,COCl2属于_______ 分子(填“极性”或“非极性”)。
(3)Cu−Mn−Al合金为磁性形状记忆合金材料之一,其晶胞结构如图所示:
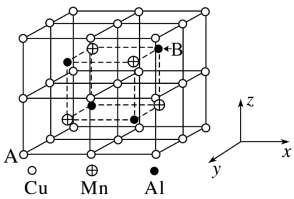
①合金的化学式为_______ 。
②A原子坐标参数为(0,1,0),则B原子坐标参数为_______ 。
③已知该合金晶体密度为ρg·cm-3,则两个Al原子间的最近距离为_______ nm (阿伏加德罗常数用NA表示,只列计算式)。
(1)锡合金具有优异的抗蚀性能,可以用来生产制作各种精美合金饰品。
①基态Sn原子价层电子排布为
②Co元素在元素周期表中的位置是
③Cu元素位于元素周期表的
(2)制备CrO2Cl2的反应为K2Cr2O7 + 3CCl4 = 2KCl + 2CrO2Cl2 + 3COCl2↑
①上述方程式中非金属元素电负性由小到大的顺序为
②COCl2分子中π键和σ键的个数比为
(3)Cu−Mn−Al合金为磁性形状记忆合金材料之一,其晶胞结构如图所示:

①合金的化学式为
②A原子坐标参数为(0,1,0),则B原子坐标参数为
③已知该合金晶体密度为ρg·cm-3,则两个Al原子间的最近距离为
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐3】教材插图具有简洁而又内涵丰富的特点。请回答以下问题:
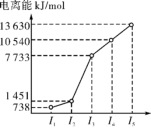
(1)第三周期的某主族元素,其第一至第五电离能数据如图所示,则该元素对应的原子有__________ 种不同空间运动状态的电子。
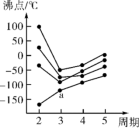
(2)如图所示,每条折线表示周期表ⅣA ~ⅦA 中的某一族元素氢化物的沸点变化。每个小黑点代表一种氢化物,其中 a 点代表的是___________ 。判断依据是_____________________ 。
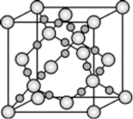
(3)CO2 在高温高压下所形成的晶体其晶胞如图所示。则该晶体的类型属于___________ 晶体。
(4)第一电离能介于 Al、P 之间的第三周期元素有___________ 种。 GaCl3 中中心原子的杂化方式为___________ ,写出与 GaCl3 结构相同的一种离子___________ 。
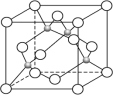
(5)下图是碳化硅的晶胞结构 。若碳化硅晶胞边长为 apm,阿伏加德罗常数为 NA ,则碳化硅晶体的密度为___________ g/cm3.(列出计算式即可)
(1)第三周期的某主族元素,其第一至第五电离能数据如图所示,则该元素对应的原子有

(2)如图所示,每条折线表示周期表ⅣA ~ⅦA 中的某一族元素氢化物的沸点变化。每个小黑点代表一种氢化物,其中 a 点代表的是

(3)CO2 在高温高压下所形成的晶体其晶胞如图所示。则该晶体的类型属于

(4)第一电离能介于 Al、P 之间的第三周期元素有
(5)下图是碳化硅的晶胞结构 。若碳化硅晶胞边长为 apm,阿伏加德罗常数为 NA ,则碳化硅晶体的密度为

您最近一年使用:0次



