含硅化合物在生活中的应用非常广泛。请回答下列问题:
(1)祖母绿宝石的主要成分化学式为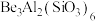 ,Be与Al的第一电离能大小关系为:
,Be与Al的第一电离能大小关系为: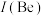
___________ 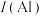 。
。
(2)硅酸盐的阴离子结构丰富多样,有些是有限数目的硅氧四面体构建的简单阴离子,如图所示,最简单的硅酸盐阴离子a的化学式为 ,则六元环状硅酸盐阴离子b的化学式是
,则六元环状硅酸盐阴离子b的化学式是___________ (不能用最简式表示)。___________ 。
(4)β-石英是晶质石英( )的一种变体,其晶胞结构如图所示,一个晶胞中含有的硅原子数为
)的一种变体,其晶胞结构如图所示,一个晶胞中含有的硅原子数为___________ ,请用价层电子对互斥模型解释图中键角。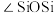 并不是180°的原因是
并不是180°的原因是___________ 。
(5)金刚砂的晶胞结构如图丙所示,在SiC中,每个C原子周围最近且等距的C原子数目为___________ ;若金刚砂的密度为ρ g⋅cm ,则晶体中最近的碳、硅原子之间的距离为
,则晶体中最近的碳、硅原子之间的距离为___________ pm(用代数式表示即可)。
(1)祖母绿宝石的主要成分化学式为
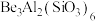 ,Be与Al的第一电离能大小关系为:
,Be与Al的第一电离能大小关系为: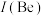
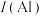 。
。(2)硅酸盐的阴离子结构丰富多样,有些是有限数目的硅氧四面体构建的简单阴离子,如图所示,最简单的硅酸盐阴离子a的化学式为
 ,则六元环状硅酸盐阴离子b的化学式是
,则六元环状硅酸盐阴离子b的化学式是
 |  |  |  | |
| 沸点/K | 187.2 | 330.8 | 427.2 | 560.7 |
(4)β-石英是晶质石英(
 )的一种变体,其晶胞结构如图所示,一个晶胞中含有的硅原子数为
)的一种变体,其晶胞结构如图所示,一个晶胞中含有的硅原子数为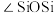 并不是180°的原因是
并不是180°的原因是(5)金刚砂的晶胞结构如图丙所示,在SiC中,每个C原子周围最近且等距的C原子数目为
 ,则晶体中最近的碳、硅原子之间的距离为
,则晶体中最近的碳、硅原子之间的距离为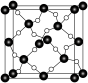

更新时间:2024-04-12 12:34:57
|
相似题推荐
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐1】X是第四周期元素,最外层只有1个电子,次外层的所有原子轨道均充满电子。元素Y的负一价离子的最外层电子数与次外层的相同。回答下列问题:
(1)单质X的晶体类型为___________ ,其中X原子的配位数为___________ 。
(2)元素Y基态原子的核外电子排布式为_____________ ,同周期元素中,第一电离能最大的是___________ (写元素符号)。
(3)X与Y形成的一种化合物的立方晶胞如图所示。
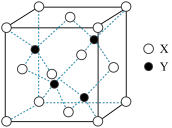
①该化合物的化学式为____________________ ,已知晶胞参数a=0.542nm,此晶体的密度为____________ g·cm-3。(写出计算式,不要求计算结果。阿伏加 德罗常数为NA)
②该化合物难溶于水但易溶于氨水,其原因是________ 。
(1)单质X的晶体类型为
(2)元素Y基态原子的核外电子排布式为
(3)X与Y形成的一种化合物的立方晶胞如图所示。

①该化合物的化学式为
②该化合物难溶于水但易溶于氨水,其原因是
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐2】根据所学知识回答问题
(1)基态Ge原子的核外电子排布式为[Ar]___________ ,有___________ 个未成对电子。光催化还原CO2制备CH4反应中,带状纳米Zn2GeO4是该反应的良好催化剂。Zn、Ge、O电负性由大至小的顺序是___________ 。
(2)镍元素基态原子的电子排布式为___________ ,3d能级上的未成对电子数为___________ 。元素铜与镍的第二电离能分别为:ICu=1 958 kJ·mol-1、INi=1 753 kJ·mol-1,ICu>INi的原因是___________ 。
(3)写出基态As原子的核外电子排布式___________ 。根据元素周期律,原子半径Ga___________ As,第一电离能Ga___________ As(填“大于”或“小于”)。
(1)基态Ge原子的核外电子排布式为[Ar]
(2)镍元素基态原子的电子排布式为
(3)写出基态As原子的核外电子排布式
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐3】砷化镓(GaAs)是当前最重要、技术成熟度最高的半导体材料之一,我国“玉兔二号”月球车就是通过砷化镓太阳能电池提供能量。
(1)GaAs、GaN结构相似,晶体类型都为共价晶体,沸点GaAs___________ GaN(填“>”或“<”,下同),第一电离能Ga___________ As。
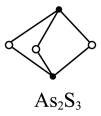
(2)成语“信口雌黄”中雌黄的分子式为As2S3,分子结构如图,As原子的杂化方式为___________ 。
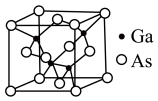
(3)GaAs的晶胞结构如图,在GaAs晶体中,与As原子最近且等距离的As原子数为______ 。
(4)若砷化镓晶胞边长为apm,则Ga与最近As的核间距为___________ cm。
(1)GaAs、GaN结构相似,晶体类型都为共价晶体,沸点GaAs
(2)成语“信口雌黄”中雌黄的分子式为As2S3,分子结构如图,As原子的杂化方式为

(3)GaAs的晶胞结构如图,在GaAs晶体中,与As原子最近且等距离的As原子数为

(4)若砷化镓晶胞边长为apm,则Ga与最近As的核间距为
您最近一年使用:0次
【推荐1】Q、R、X、M、Y、Z是元素周期表前四周期的六种元素,原子序数依次递增。已知:
①Z位于 区,最外层没有单电子,其余的均为短周期主族元素;
区,最外层没有单电子,其余的均为短周期主族元素;
②基态Y原子的价电子排布式为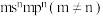 ;
;
③基态Q、X原子p轨道的未成对电子数都是2;
④基态M原子的 能级有1个单电子。
能级有1个单电子。
请回答下列问题:
(1)Z在周期表中的位置为______ 。
(2)Q、R、X、M四种元素第一电离能由大到小的顺序为______ (用对应元素的符号填写)。
(3)分析下表中两种物质的键能数据(单位: )。
)。
结合数据说明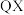 比
比 活泼的原因:
活泼的原因:__________________ 。
①Z位于
 区,最外层没有单电子,其余的均为短周期主族元素;
区,最外层没有单电子,其余的均为短周期主族元素;②基态Y原子的价电子排布式为
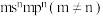 ;
;③基态Q、X原子p轨道的未成对电子数都是2;
④基态M原子的
 能级有1个单电子。
能级有1个单电子。请回答下列问题:
(1)Z在周期表中的位置为
(2)Q、R、X、M四种元素第一电离能由大到小的顺序为
(3)分析下表中两种物质的键能数据(单位:
 )。
)。 |  |  | |
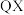 | 351 | 745 | 1076 |
 | 196 | 418 | 945 |
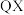 比
比 活泼的原因:
活泼的原因:
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
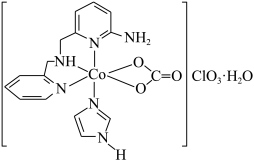
【推荐2】一种具有光催化作用的配合物A结构简式如图所示: 的空间构型为
的空间构型为___________ ,比较键角大小:
___________ ClO 。
。
(2)咪唑(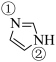 )具有类似苯环的芳香性,其中的大π键可以表示为
)具有类似苯环的芳香性,其中的大π键可以表示为___________ ,___________ 更易与钴形成配位键(填“①号N”、“②号N”)。___________ 更易溶于水(填“咪唑”或“苯”),原因:___________ 。
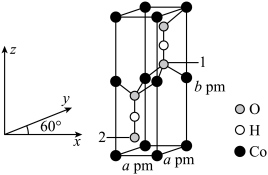
(3)Co的一种化合物为六方晶系晶体,晶胞结构如图所示。___________ 。 为阿伏加德罗常数的值,该晶体的密度为
为阿伏加德罗常数的值,该晶体的密度为___________  (用计算式表示)。
(用计算式表示)。
 的空间构型为
的空间构型为
 。
。(2)咪唑(
 )具有类似苯环的芳香性,其中的大π键可以表示为
)具有类似苯环的芳香性,其中的大π键可以表示为(3)Co的一种化合物为六方晶系晶体,晶胞结构如图所示。
 为阿伏加德罗常数的值,该晶体的密度为
为阿伏加德罗常数的值,该晶体的密度为 (用计算式表示)。
(用计算式表示)。
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐3】硅烷广泛应用在现代高科技领域。制备硅烷的反应为:SiF4+NaAlH4=SiH4+NaAlF4.
(1)①基态硅原子的价层电子轨道表示式为_____ ,基态硅原子的电子有_____ 种空间运动状态。
②SiF4中,硅的化合价为+4价。硅显正化合价的原因是_____ 。
③下列说法正确的是_____ (填字母)。
a.SiH4的稳定性比CH4的差
b.SiH4中4个Si-H的键长相同,H-Si-H的键角为90°
c.SiH4中硅原子以4个sp3杂化轨道分别与4个氢原子的1s轨道重叠,形成4个Si-Hσ键
④SiF4的沸点(-86℃)高于SiH4的沸点(-112℃),原因是_____ 。
⑤键角:SiF4_____ SiH4,原因_____ 。
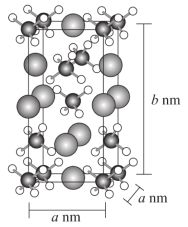
(2)NaAlH4的晶胞结构如图所示,晶胞的体积为a2b×10-21cm3。
① 的VSEPR模型名称为
的VSEPR模型名称为_____ 。
②用NA表示阿伏加德罗常数的值。NaAlH4晶体密度为_____ g•cm-3(用含a、b、NA的代数式表示)。
③NaAlH4是一种具有应用潜能的储氢材料,其释氢过程可用化学方程式表示为:3NaAlH4═Na3AlH6+2Al+3H2↑。掺杂22Ti替换晶体中部分Al,更利于NaAlH4中H的解离,使体系更容易释放氢。从结构的角度推测其可能的原因:_____ 。
(1)①基态硅原子的价层电子轨道表示式为
②SiF4中,硅的化合价为+4价。硅显正化合价的原因是
③下列说法正确的是
a.SiH4的稳定性比CH4的差
b.SiH4中4个Si-H的键长相同,H-Si-H的键角为90°
c.SiH4中硅原子以4个sp3杂化轨道分别与4个氢原子的1s轨道重叠,形成4个Si-Hσ键
④SiF4的沸点(-86℃)高于SiH4的沸点(-112℃),原因是
⑤键角:SiF4
(2)NaAlH4的晶胞结构如图所示,晶胞的体积为a2b×10-21cm3。

①
 的VSEPR模型名称为
的VSEPR模型名称为②用NA表示阿伏加德罗常数的值。NaAlH4晶体密度为
③NaAlH4是一种具有应用潜能的储氢材料,其释氢过程可用化学方程式表示为:3NaAlH4═Na3AlH6+2Al+3H2↑。掺杂22Ti替换晶体中部分Al,更利于NaAlH4中H的解离,使体系更容易释放氢。从结构的角度推测其可能的原因:
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
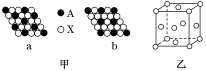
【推荐1】下面是一些晶体的结构示意图。
(1)下列关于晶体的说法正确的是___________(填字母)。
(2)图甲表示的是晶体的二维平面示意图,a、b中可表示化学式为AX3的化合物的是___________ (填“a”或“b”)。
(3)图乙表示的是金属铜的晶胞。
①该晶胞“实际”拥有的铜原子数是___________ ,铜原子的配位数为___________ 。
②该晶胞称为___________ (填字母)。
A.六方晶胞 B.体心立方晶胞 C.面心立方晶胞
(4)NiO、FeO的晶体结构相同,且r(Fe2+)>r(Ni2+),NiO的熔点为1 960 ℃,则FeO的熔点___________ (填“>”或“<”)1 960 ℃,判断的依据是___________ 。

(1)下列关于晶体的说法正确的是___________(填字母)。
| A.晶体的形成与晶体的自范性有关 |
| B.可以用X射线衍射仪区分晶体和非晶体 |
| C.石蜡是非晶体,但有固定的熔点 |
| D.晶胞就是晶体 |
(3)图乙表示的是金属铜的晶胞。
①该晶胞“实际”拥有的铜原子数是
②该晶胞称为
A.六方晶胞 B.体心立方晶胞 C.面心立方晶胞
(4)NiO、FeO的晶体结构相同,且r(Fe2+)>r(Ni2+),NiO的熔点为1 960 ℃,则FeO的熔点
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐2】完成下列问题
(1)As2Se3是一种非晶态半导体,也称玻璃半导体。区分晶体与非晶体的最可靠的科学方法是_______ 。
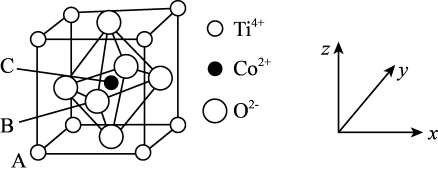
(2)钴的一种化合物的立方晶胞结构如图所示,已知A点的原子坐标参数为(0,0,0),B点为( ,0,
,0, ),则C点的原子坐标参数为
),则C点的原子坐标参数为_______ ,钴周围等距离且最近的O2-数目为 _______ ,该物质的化学式为_______ 。
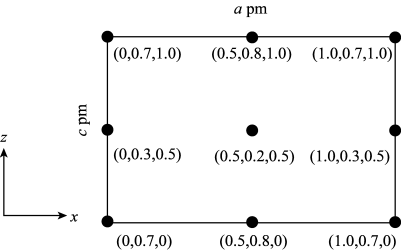
(3)以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标。CsSiB3O7属正交晶系(长方体形)。晶胞参数为a pm、b pm、c pm。如图为沿y轴投影的晶胞中所有Cs原子的分布图和原子分数坐标。据此推断该晶胞中Cs原子的数目为_______ 。CsSiB3O7的摩尔质量为M g∙mol−1,设NA为阿伏加德罗常数的值,则CsSiB3O7晶体的密度为_______ g·cm−3(用代数式表示)。为点(0.5,0.8,0)与点(1.0,0.7,1.0)之间的距离为_______ pm。
(1)As2Se3是一种非晶态半导体,也称玻璃半导体。区分晶体与非晶体的最可靠的科学方法是
(2)钴的一种化合物的立方晶胞结构如图所示,已知A点的原子坐标参数为(0,0,0),B点为(
 ,0,
,0, ),则C点的原子坐标参数为
),则C点的原子坐标参数为
(3)以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标。CsSiB3O7属正交晶系(长方体形)。晶胞参数为a pm、b pm、c pm。如图为沿y轴投影的晶胞中所有Cs原子的分布图和原子分数坐标。据此推断该晶胞中Cs原子的数目为

您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐3】材料是人类文明进步的阶梯,第ⅢA族、ⅣA族、VA族及Ⅷ族元素是组成特殊材料的重要元素。回答下列问题:
(1)某元素位于第四周期Ⅷ族,其基态原子的未成对电子数与基态氮原子的未成对电子数相同,则其基态原子的核外电子数为___________ 。
(2)经测定发现,N2O5固体由NO 和NO
和NO 两种离子组成,该固体中N原子杂化类型有
两种离子组成,该固体中N原子杂化类型有___________ 。
(3)K4[Fe(CN)6]溶液可以检验铁陨石中铁元素的价态。1mol K4[Fe(CN)6]含σ键的物质的量为___________ ,化合物K4[Fe(CN)6]中存在的作用力有___________ (填字母)。
a.离子键 b.极性键 c.非极性键 d.配位键 e.氢键
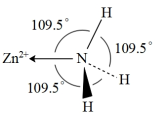
(4)NH3分子在独立存在时H−N−H键角为107°。如图是[Zn(NH3)6]2+离子的部分结构以及H−N−H键角的测量值。解释NH3形成如图配合物后H−N−H键角变大的原因:___________ 。
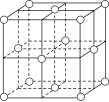
(5)某种金属锂的硼氢化物是优质固体电解质,并具有高储氢密度。阳离子为Li+,每个阴离子是由12个硼原子和12个氢原子所构成的原子团。阴离子在晶胞中位置如图所示,其堆积方式为___________ (填“简单立方”、“体心立方”、“六方最密”或“面心立方最密”)Li+占据阴离子组成的所有正四面体中心,该化合物的化学式为___________ (用最简整数比表示)。假设晶胞边长为anm,NA代表阿伏加德罗常数的值,则该晶胞的密度为___________ g/cm3。
(1)某元素位于第四周期Ⅷ族,其基态原子的未成对电子数与基态氮原子的未成对电子数相同,则其基态原子的核外电子数为
(2)经测定发现,N2O5固体由NO
 和NO
和NO 两种离子组成,该固体中N原子杂化类型有
两种离子组成,该固体中N原子杂化类型有(3)K4[Fe(CN)6]溶液可以检验铁陨石中铁元素的价态。1mol K4[Fe(CN)6]含σ键的物质的量为
a.离子键 b.极性键 c.非极性键 d.配位键 e.氢键
(4)NH3分子在独立存在时H−N−H键角为107°。如图是[Zn(NH3)6]2+离子的部分结构以及H−N−H键角的测量值。解释NH3形成如图配合物后H−N−H键角变大的原因:

(5)某种金属锂的硼氢化物是优质固体电解质,并具有高储氢密度。阳离子为Li+,每个阴离子是由12个硼原子和12个氢原子所构成的原子团。阴离子在晶胞中位置如图所示,其堆积方式为

您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
【推荐1】铁在史前就为人们所用。在人类文明发展过程中,铁所起的作用是其他任何元素都不能比拟的。请回答下列问题:
(1)基态铁原子中,价电子电子云的伸展方向有_______ 种。
(2)五羰基合铁[Fe(CO)5]分解制铁晶体,反应过程中断裂和形成的化学键有_________ ( 填序号);
A.离子键 B.极性键 C.非极性键 D.配位键 E.金属键 F.范德华力
Fe(CO)5中各元素电负性的大小顺序是___________________ 。
(3)绿矾(FeSO4·7H2O)结构如图。

①H2O分别与Fe2+、 的相互作用分别为
的相互作用分别为_______________ 、_____________ 。
②比较 中的键角∠O−S−O
中的键角∠O−S−O________ H2O中的键角∠H−O−H。 (填“<” “>”或“=”)
(4)铁的化合物种类众多,其中FeF3的熔点高于1000°C,而FeBr3的熔点只有200°C,原因是___________ 。
(5)铁的一种配位化合物(普鲁士蓝)中铁氰骨架结构如图(a)所所示,骨架为正六面体,K+位于骨架的正六面体的空穴中,以平衡铁氰骨架的负电荷,则该钾盐的化学式为_____________________ 。

(6)一种锂电池的正极材料磷酸铁锂(LiFePO4) 的晶胞结构如上图(b)所示。其中Li+分别位于顶角、棱心、面心,O围绕Fe和P分别形成正八面体和正四面体,它们通过共顶点、共棱形成空间链结构。磷酸铁锂晶体的晶胞参数分别为anm、bnm,则磷酸铁锂晶体的摩尔体积Vm=____________ cm3·mol−1 (已知阿伏加德罗常数为NA,晶体的摩尔体积是指单位物质的量晶体所占的体积)。
(1)基态铁原子中,价电子电子云的伸展方向有
(2)五羰基合铁[Fe(CO)5]分解制铁晶体,反应过程中断裂和形成的化学键有
A.离子键 B.极性键 C.非极性键 D.配位键 E.金属键 F.范德华力
Fe(CO)5中各元素电负性的大小顺序是
(3)绿矾(FeSO4·7H2O)结构如图。

①H2O分别与Fe2+、
 的相互作用分别为
的相互作用分别为②比较
 中的键角∠O−S−O
中的键角∠O−S−O(4)铁的化合物种类众多,其中FeF3的熔点高于1000°C,而FeBr3的熔点只有200°C,原因是
(5)铁的一种配位化合物(普鲁士蓝)中铁氰骨架结构如图(a)所所示,骨架为正六面体,K+位于骨架的正六面体的空穴中,以平衡铁氰骨架的负电荷,则该钾盐的化学式为

(6)一种锂电池的正极材料磷酸铁锂(LiFePO4) 的晶胞结构如上图(b)所示。其中Li+分别位于顶角、棱心、面心,O围绕Fe和P分别形成正八面体和正四面体,它们通过共顶点、共棱形成空间链结构。磷酸铁锂晶体的晶胞参数分别为anm、bnm,则磷酸铁锂晶体的摩尔体积Vm=
您最近一年使用:0次
【推荐2】锗(Ge)是典型的半导体元素,在电子、材料等领域应用广泛。回答下列问题:
(1)基态Ge原子的核外电子排布式为_______ ,最高能级电子的电子云轮廓形状为_______ 。
(2)比较下列锗卤化物的熔点和沸点,分析其变化的原因_______ 。
(3)光催化还原CO2制备CH4反应中,带状纳米Zn2GeO4是该反应的良好催化剂。Zn、Ge、O电负性由大至小的顺序是_______ 。
(4)Ge单晶具有金刚石型结构,其中Ge原子的杂化方式为_______ ,微粒之间存在的作用力是_______ 。
(5)晶胞有两个基本要素:
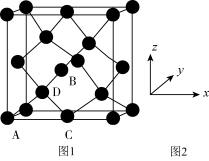
①原子坐标参数,表示晶胞内部各原子的相对位置,下图为Ge单晶的晶胞,其中原子坐标参数A为(0,0,0);B为( ,0,
,0, );C为(
);C为(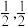 ,0)。则D原子的坐标参数为
,0)。则D原子的坐标参数为_______ 。
②晶胞参数,描述晶胞的大小和形状。已知Ge单晶的晶胞参数a=565.76pm,其密度为_______ g·cm-3(列出计算式即可)。
(1)基态Ge原子的核外电子排布式为
(2)比较下列锗卤化物的熔点和沸点,分析其变化的原因
| GeCl4 | GeBr4 | GeI4 | |
| 熔点/℃ | −49.5 | 26 | 146 |
| 沸点/℃ | 83.1 | 186 | 约400 |
(4)Ge单晶具有金刚石型结构,其中Ge原子的杂化方式为
(5)晶胞有两个基本要素:
①原子坐标参数,表示晶胞内部各原子的相对位置,下图为Ge单晶的晶胞,其中原子坐标参数A为(0,0,0);B为(
 ,0,
,0, );C为(
);C为(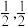 ,0)。则D原子的坐标参数为
,0)。则D原子的坐标参数为
②晶胞参数,描述晶胞的大小和形状。已知Ge单晶的晶胞参数a=565.76pm,其密度为
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐3】KZnF3被认为是良好的光学基质材料,可由K2CO3、ZnF2、NH4HF2制备。回答下列问题;
(1)基态F原子的价电子轨道表达式为__ ;基态Zn原子核外占据最高能层电子的电子云轮廓图形状为___ 。
(2)O的第一电离能____ (填"大于"或"小于")N的第一电离能,原因为___ 。
(3)K2CO3中阴离子的立体构型为____ 。
(4)NH4HF2的组成元素的电负性由大到小的顺序为____ 。(用元素符号表示);其中N原子的杂化方式为___ ;HF能形成分子缔合体(HF)n的原因为____ 。
(5)ZnF2具有金红石型四方结构,KZnF3具有钙钛矿型立方结构,两种晶体的晶胞结构如图所示∶
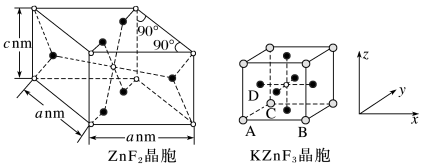
①ZnF2和KZnF3晶体(晶胞顶点为K+)中,Zn的配位数之比为____ 。
②若NA表示阿伏加德罗常数的值,则ZnF2晶体的密度为____ g·cm-3(用含a、c、NA的代数式表示)。
③KZnF3晶胞中原子坐标参数A为(0,0,0),B为(1,0,0),C为(0,1,0),则D的原子坐标参数为___ 。
(1)基态F原子的价电子轨道表达式为
(2)O的第一电离能
(3)K2CO3中阴离子的立体构型为
(4)NH4HF2的组成元素的电负性由大到小的顺序为
(5)ZnF2具有金红石型四方结构,KZnF3具有钙钛矿型立方结构,两种晶体的晶胞结构如图所示∶

①ZnF2和KZnF3晶体(晶胞顶点为K+)中,Zn的配位数之比为
②若NA表示阿伏加德罗常数的值,则ZnF2晶体的密度为
③KZnF3晶胞中原子坐标参数A为(0,0,0),B为(1,0,0),C为(0,1,0),则D的原子坐标参数为
您最近一年使用:0次



